文档内容
2025-2026 学年高一化学上学期第一次月考卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第1章~第2章第1节(人教版2019必修第一册)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.下列关于氧化还原反应的说法正确的是
A.失去电子的物质是氧化剂
B.氧化剂发生氧化反应
C.氧化还原反应的本质是电子的转移
D.反应前后元素化合价不变的反应一定是氧化还原反应
2.下列有关电解质、非电解质、强电解质、弱电解质的分类正确的是
选项 A B C D
电解质
非电解质 乙醇 葡萄糖
强电解质 HClO
4
弱电解质 氨水
A.A B.B C.C D.D
3.下列物质属于电解质且状态不同导电性不同的是
A.氯化钠晶体与氯化钠溶液
B.铜与硫酸铜溶液
C.乙醇与蔗糖溶液
D.二氧化碳与碳酸溶液
4.下列各组离子在指定溶液中能大量共存的是
1 / 6
学科网(北京)股份有限公司A.无色透明溶液中:Cu2+、K+、 、
B.酸性溶液中:Na+、 、Cl-、
C.碱性溶液中:K+、Ba2+、Cl-、
D.含Fe3+的溶液中:Na+、SCN-、Cl-、OH-
5.下列反应的离子方程式书写正确的是
A.氯气溶于水:Cl+HO=2H++Cl-+ClO-
2 2
B.碳酸钙加入盐酸中: +2H+=CO ↑+HO
2 2
C.氢氧化钠溶液与氯化铜溶液混合:2OH-+Cu2+=Cu(OH) ↓
2
D.硫酸溶液与氢氧化钡溶液混合: +Ba2+=BaSO ↓
4
6.有三瓶失去标签的无色溶液,已知它们分别是HCl溶液、KNO 溶液、NaOH溶液中的一种。下列四种
3
试剂中,能将上述三种无色溶液一次鉴别出来的是
A.稀硫酸 B.(NH )CO 溶液 C.KCO 溶液 D.无色酚酞试液
4 2 3 2 3
7.下列说法错误的是
A.胶体粒子的直径大小在1~100nm之间
B.当光束通过NaCl溶液时会产生丁达尔效应
C.氢氧化铝胶体粒子具有较强的吸附能力,可作净水剂
D.向沸水中逐滴加入少量饱和FeCl 溶液,可制得Fe(OH) 胶体
3 3
8.ClO 是一种高效水处理剂,实验室通过以下反应制得ClO :2KClO+H C O+H SO
2 2 3 2 2 4 2 4
2ClO ↑+K SO +2CO ↑+2H O,关于此反应的说法正确的是
2 2 4 2 2
A.KClO 中氯元素化合价升高,失电子 B.HC O 被氧化
3 2 2 4
C.反应中HSO 发生还原反应 D.反应中CO 是还原产物
2 4 2
9.已知SO 是酸性氧化物。由单质到盐的转化关系可表示为:
2
下列转化关系正确的是
A.Cu CuO Cu(OH) CuCl
2 2
B.Mg MgO MgCl MgSO
2 4
C.C CO HCO CaCO
2 2 3 3
D.S SO HSO NaSO
2 2 4 2 4
2 / 6
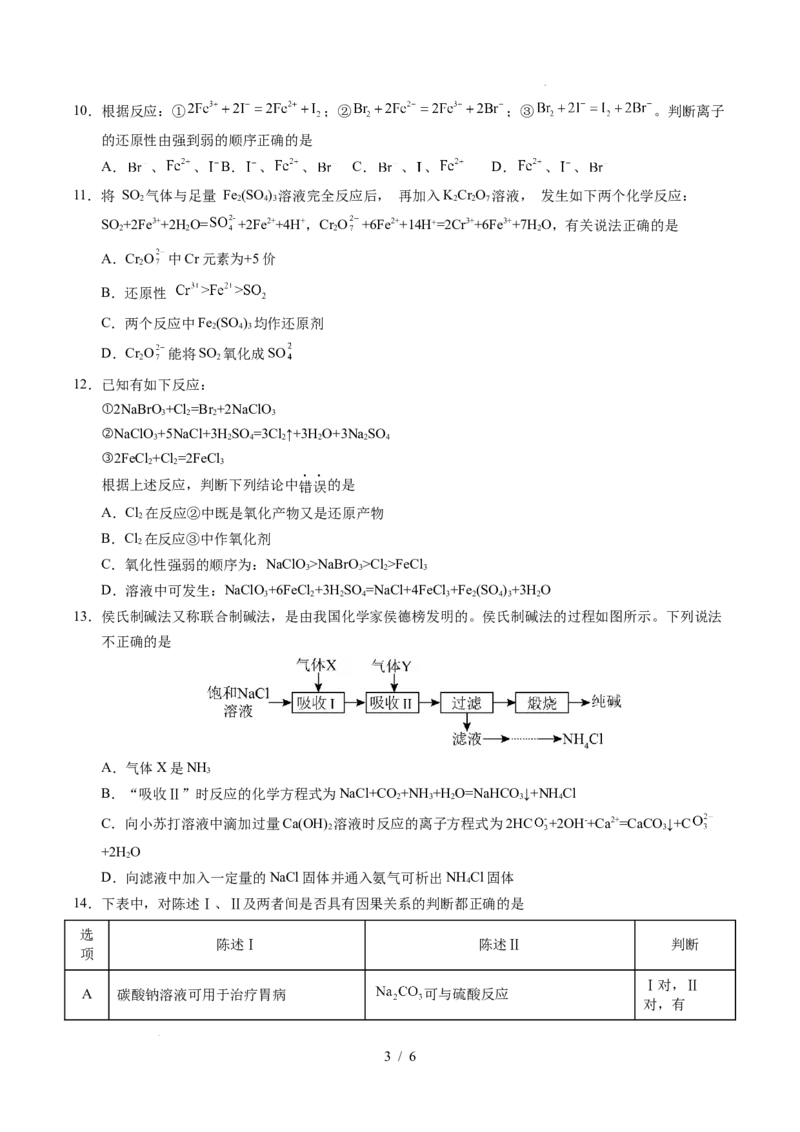
学科网(北京)股份有限公司10.根据反应:① ;② ;③ 。判断离子
的还原性由强到弱的顺序正确的是
A. 、 、 B. 、 、 C. 、 、 D. 、 、
11.将 SO 气体与足量 Fe (SO ) 溶液完全反应后, 再加入KCr O 溶液, 发生如下两个化学反应:
2 2 4 3 2 2 7
SO +2Fe3++2H O= +2Fe2++4H+,Cr O +6Fe2++14H⁺=2Cr3++6Fe3++7H O,有关说法正确的是
2 2 2 2
A.Cr O 中Cr元素为+5价
2
B.还原性
C.两个反应中Fe (SO ) 均作还原剂
2 4 3
D.Cr O 能将SO 氧化成SO
2 2
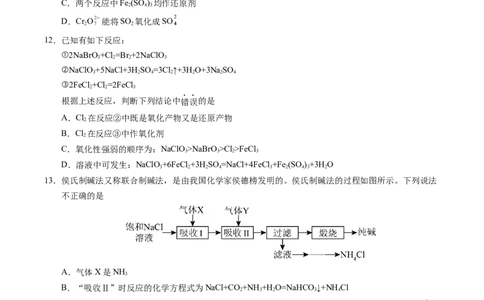
12.已知有如下反应:
①2NaBrO+Cl=Br +2NaClO
3 2 2 3
②NaClO+5NaCl+3HSO =3Cl↑+3H O+3Na SO
3 2 4 2 2 2 4
③2FeCl +Cl=2FeCl
2 2 3
根据上述反应,判断下列结论中错误的是
A.Cl 在反应②中既是氧化产物又是还原产物
2
B.Cl 在反应③中作氧化剂
2
C.氧化性强弱的顺序为:NaClO>NaBrO>Cl>FeCl
3 3 2 3
D.溶液中可发生:NaClO+6FeCl +3H SO =NaCl+4FeCl +Fe (SO )+3H O
3 2 2 4 3 2 4 3 2
13.侯氏制碱法又称联合制碱法,是由我国化学家侯德榜发明的。侯氏制碱法的过程如图所示。下列说法
不正确的是
A.气体X是NH
3
B.“吸收Ⅱ”时反应的化学方程式为NaCl+CO +NH+H O=NaHCO ↓+NHCl
2 3 2 3 4
C.向小苏打溶液中滴加过量Ca(OH) 溶液时反应的离子方程式为2HC +2OH-+Ca2+=CaCO ↓+C
2 3
+2H O
2
D.向滤液中加入一定量的NaCl固体并通入氨气可析出NH Cl固体
4
14.下表中,对陈述Ⅰ、Ⅱ及两者间是否具有因果关系的判断都正确的是
选
陈述Ⅰ 陈述Ⅱ 判断
项
Ⅰ对,Ⅱ
A 碳酸钠溶液可用于治疗胃病 可与硫酸反应
对,有
3 / 6
学科网(北京)股份有限公司向 加入酚酞试液中,酚酞变红 Ⅰ对,Ⅱ
B 与水反应生成氢氧化钠
色 错,无
常温下,金属钠在空气中会生成过氧化 Ⅰ对,Ⅱ
C 金属钠保存在煤油中,以隔绝空气
钠 对,有
Ⅰ对,Ⅱ
D 可用作航天员的供氧剂 能与 反应生成
对,有
A.A B.B C.C D.D
第 II 卷(非选择题 共 58 分)
二、非选择题:本题共4小题,共58分。
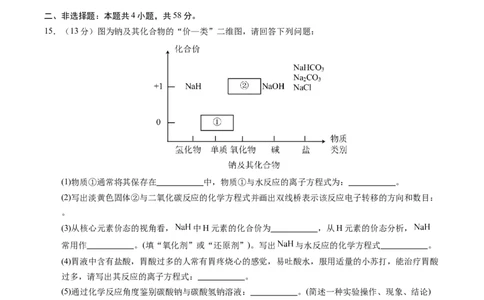
15.(13分)图为钠及其化合物的“价—类”二维图,请回答下列问题:
(1)物质①通常将其保存在 中,物质①与水反应的离子方程式为: 。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并画出双线桥表示该反应电子转移的方向和数目:
。
(3)从核心元素价态的视角看, 中H元素的化合价为 ,从H元素的价态分析,
常用作 。(填“氧化剂”或“还原剂”)。写出 与水反应的化学方程式 。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打,能治疗胃酸
过多,请写出其反应的离子方程式: 。
(5)通过化学反应角度鉴别碳酸钠与碳酸氢钠溶液: 。(简述一种实验操作、现象、结论)
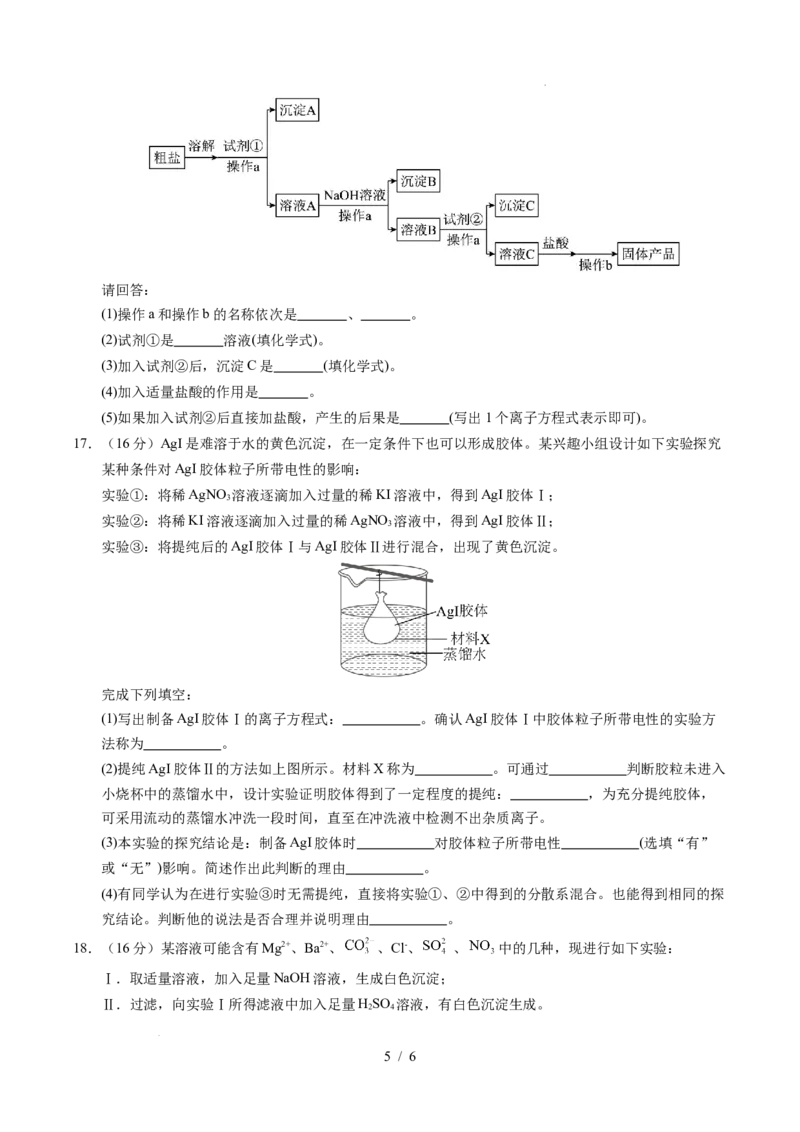
16.(13分)通过海水晾晒可得粗盐,粗盐中除 外,还含有 以及泥沙等杂
质,需要提纯后才能综合利用。某同学利用给定试剂 溶液、 溶液、 溶液和盐酸,
设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
4 / 6
学科网(北京)股份有限公司请回答:
(1)操作a和操作b的名称依次是 、 。
(2)试剂①是 溶液(填化学式)。
(3)加入试剂②后,沉淀C是 (填化学式)。
(4)加入适量盐酸的作用是 。
(5)如果加入试剂②后直接加盐酸,产生的后果是 (写出1个离子方程式表示即可)。
17.(16分)AgI是难溶于水的黄色沉淀,在一定条件下也可以形成胶体。某兴趣小组设计如下实验探究
某种条件对AgI胶体粒子所带电性的影响:
实验①:将稀AgNO 溶液逐滴加入过量的稀KI溶液中,得到AgI胶体Ⅰ;
3
实验②:将稀KI溶液逐滴加入过量的稀AgNO 溶液中,得到AgI胶体Ⅱ;
3
实验③:将提纯后的AgI胶体Ⅰ与AgI胶体Ⅱ进行混合,出现了黄色沉淀。
完成下列填空:
(1)写出制备AgI胶体Ⅰ的离子方程式: 。确认AgI胶体Ⅰ中胶体粒子所带电性的实验方
法称为 。
(2)提纯AgI胶体Ⅱ的方法如上图所示。材料X称为 。可通过 判断胶粒未进入
小烧杯中的蒸馏水中,设计实验证明胶体得到了一定程度的提纯: ,为充分提纯胶体,
可采用流动的蒸馏水冲洗一段时间,直至在冲洗液中检测不出杂质离子。
(3)本实验的探究结论是:制备AgI胶体时 对胶体粒子所带电性 (选填“有”
或“无”)影响。简述作出此判断的理由 。
(4)有同学认为在进行实验③时无需提纯,直接将实验①、②中得到的分散系混合。也能得到相同的探
究结论。判断他的说法是否合理并说明理由 。
18.(16分)某溶液可能含有Mg2+、Ba2+、 、Cl-、 、 中的几种,现进行如下实验:
Ⅰ.取适量溶液,加入足量NaOH溶液,生成白色沉淀;
Ⅱ.过滤,向实验Ⅰ所得滤液中加入足量HSO 溶液,有白色沉淀生成。
2 4
5 / 6
学科网(北京)股份有限公司根据上述实验回答下列问题。
(1)溶液中一定不存在的离子是 。
(2)写出Ⅰ和Ⅱ中所发生反应的离子方程式: ; 。
(3)为了验证溶液中是否存在Cl-、 ,某同学提出下列假设:
①只存在Cl-;②Cl-、 同时存在;③只存在 。
已知实验提供的试剂只有稀盐酸、AgNO 溶液、稀硝酸、NaOH溶液和蒸馏水。
3
验证溶液中是否存在Cl-的实验方法: 。
(4)某化工厂排出的废液中含有Ag+、Ba2+、Cu2+三种金属阳离子,欲用分别含 、OH-、Cl-三种不
同的阴离子的物质将上述金属阳离子逐一形成沉淀除去。正确加入阴离子的先后顺序是
。
6 / 6
学科网(北京)股份有限公司