文档内容
2025-2026 学年高一化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干
净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.测试范围:必修第一册第一章、第二章第一节。
4.难度系数:0.65
5.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求
的。
1.下列离子方程式书写正确的是
A.FeCl 溶液腐蚀印刷电路铜板:Cu+Fe3+=Cu2++Fe2+
3
B.醋酸溶解鸡蛋壳:2H++CaCO
3
=Ca2++CO
2
+H
2
O
C.在 NaHSO
4
溶液中滴入 Ba(OH)
2
溶液至溶液呈中性:Ba2++2OH +2H++ =BaSO
4
+2H
2
O
D.向 NaHCO 溶液中加入 NaOH: +OH =CO +H O
3 2 2
2. 表示阿伏加德罗常数的值,下列叙述正确的是
A.等物质的量的 和 CO 所含分子数均为
B.1.7 g 中含有的电子数为
C.1 mol 固体中含离子总数为
D.标准状况下,2.24 L 乙醇所含分子数为
3.铬被广泛应用于电镀、颜料等化工生产中,但生产过程中排放出的铬渣中含有铬酸钙等致癌物,会持久
损害地下水和农田。因此,我国采取了一系列措施控制铬污染。铬酸钙(CaCrO)中铬元素的化合价为
4
A.0 B.+3 C.+4 D.+6
4.有甲、乙、丙三种金属,将甲、乙两种金属分别投入硫酸铜溶液中,甲的表面有红色物质析出,乙的表
面没有明显变化,将丙投入甲的硫酸盐溶液中时有甲析出,则甲、乙、丙三种金属的活动性顺序排列正
确的是
A.甲>乙>丙 B.甲>丙>乙 C.乙>丙>甲 D.丙>甲>乙
5.向含 Fe(NO )、Mg(NO) 和 Cu(NO ) 的混合溶液中加入一定量的锌粉,充分反应后过滤。下列关于得
3 2 3 2 3 2
到的溶液或滤渣的叙述正确的是(不考虑溶液中存在的微量 H+和 OH-)
A.若滤液中含 Fe2+,则滤渣中一定不含 Fe
B.若滤渣中含 Cu,则滤液中一定含 Fe2+
C.若滤渣中含 Zn,则滤液中含 2 种离子
D.若滤渣中不含 Zn,则滤液中至少含 3 种离子
/6.下列分散系不能产生丁达尔效应的是
A. 胶体 B.云、雾 C.NaCl 溶液 D.有色玻璃
7.通过分门别类的研究可以发现物质及其变化的规律。下列有关物质的分类正确的是
选项 混合物 碱 碱性氧化物 酸性氧化物 电解质
A 液氯 NaOH NaO CO CHCOOH
2 3
B 胆矾 Ba(OH) CaO CO NH
2 2 3
C 氯水 烧碱 MgO SO HClO
3
D 盐酸 纯碱 NaO SO NaHSO
2 2 2 4
A.A B.B C.C D.D
8.下列物质的电离方程式书写正确的是
A. B.
C. D.
9. 在固体、熔融状态、溶于水三种状态下导电实验如图所示,下列说法正确的是
A.固体 中不存在离子,不能导电
B. 熔融状态下不能导电
C. 表示水合氯离子
D. 溶液能导电,是电解质
10.同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应称为歧化反应。下列反应中是歧
化反应的是
A.2NaNO =2NaNO +O ↑ B.SO +2H S=3S+2H O
3 2 2 2 2 2
C.3Cl+6KOH=5KCl+KClO +3H O D.NH NO =N O↑+2H O
2 3 2 4 3 2 2
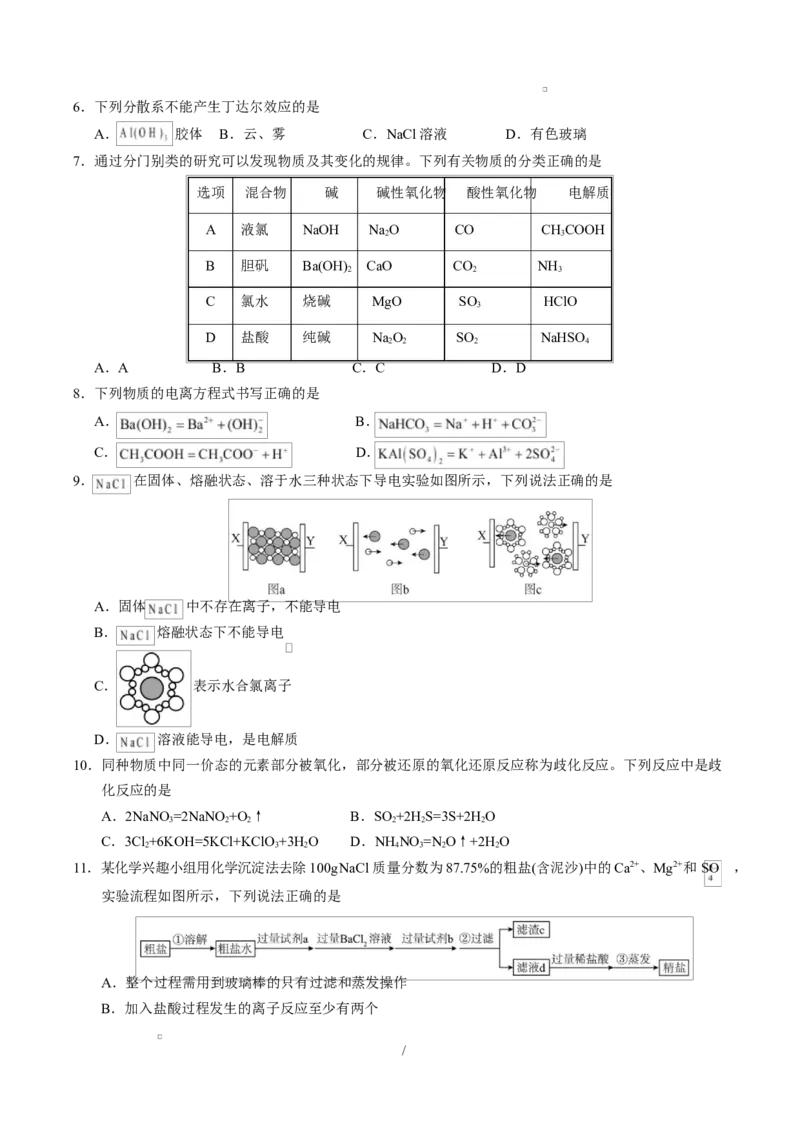
11.某化学兴趣小组用化学沉淀法去除100gNaCl质量分数为87.75%的粗盐(含泥沙)中的Ca2+、Mg2+和 SO ,
实验流程如图所示,下列说法正确的是
A.整个过程需用到玻璃棒的只有过滤和蒸发操作
B.加入盐酸过程发生的离子反应至少有两个
/C.滤渣 c 的主要成分为泥沙和 Mg OH 、BaSO 和 CaCO
2 4 3
D.从成本和除杂效果考虑,工业生产中常用 Ba OH 溶液代替 BaCl 溶液
2 2
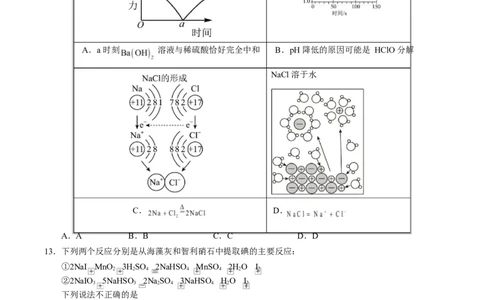
12.下列对图示的解释不正确的是
向 溶液中加入稀硫酸,溶液导电能力变
化 光照过程中氯水的 pH 变化
A.a 时刻 溶液与稀硫酸恰好完全中和 B.pH 降低的原因可能是 HClO 分解
NaCl 溶于水
C. D.
A.A B.B C.C D.D
13.下列两个反应分别是从海藻灰和智利硝石中提取碘的主要反应:
①2NaI MnO 3HSO 2NaHSO MnSO 2HO I
2 2 4 4 4 2 2
②2NaIO 5NaHSO 2NaSO 3NaHSO HO I
3 3 2 4 4 2 2
下列说法不正确的是
A.反应①②中生成等量 I 时转移电子数为 2:5
2
B.反应②中 NaSO 和 NaHSO 均为氧化产物
2 4 4
C.还原性:I- Mn2+,氧化性:IO SO
D.碘元素在反应①中被氧化,在反应②中被还原
14.一瓶不纯的 粉末,所含杂质可能是 、 、KCl、 、 中的一种或几种,
为确定其成分,进行如下流程:
/下列推断正确的是
A.无色溶液 2 中一定含有的阳离子为 、 、 、 、
B.生成无色溶液 3 的离子方程式为
C.白色沉淀 1 为
D.上述过程涉及的反应有复分解反应,也有氧化还原反应
二、非选择题:本题共 4 小题,共 58 分。
15.(14 分)以下为中学化学中常见的几种物质:① ②二氧化碳 ③ ④ ⑤ ⑥饱
和 溶液 ⑦ 。
(1)其中属于非电解质的有(填序号) 。
(2)俗名为苏打的是(填序号) 。
(3)④中阴阳离子的比值为 。
(4)用⑦可以治疗胃酸( 的盐酸)过多,写出有关离子反应方程式 。
(5)侯氏制碱法利用②⑤⑥反应先制取 ,然后加热 制取纯碱 ,有关的加热反应
方程式为: , ,实
验室模拟侯氏制碱法制取少量 ,下列有关制取的操作不正确的是___________。
A.利用 A 装置可以加热 制取纯碱
B.利用 B 装置可以干燥 ,但是不能干燥
C.利用 C 装置分离出
D.利用 D 装置可以制取
(6)下列实验方案中,不能测定出①和⑦的混合物中①质量分数的是_______。
A.取 ag 混合物充分加热,质量减少 bg
B.取 ag 混合物与足量的稀盐酸充分反应,加热、蒸干、灼烧,得到 bg 固体
C.取 ag 混合物与足量的稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加 bg
/D.取 ag 混合物与足量的 NaOH 溶液充分反应,得到 bg 溶液
(7)一定质量的②与足量的 充分反应后固体质量增加了 28g,则生成 的物质的量是
mol。
16.(16 分)回答下列问题:
(1)已知 CuO 具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下 CuO 和 反应的化
学方程式: 。
(2)氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1 价。NaH 用作生氢剂时的化学反应原理为:
。
该反应中 NaH 中的氢元素被 , 中的氢元素被 (填“氧化”或“还原”)。
(3)高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,
其中一种方法的化学原理可用离子方程式表示为:
请用单线桥表示该反应的电子转移方向与数目 。上述反应中氧化剂是 ,还原
剂是 。
(4)查阅资料知: 在一定条件下可以转化为 , 易溶于水且溶解时吸热,有咸味,遇
酸易放出气体,人误食会中毒。请回答下列问题:
①已知 能发生如下反应:
上述反应中氧化剂是 ,氧化产物是 。
②根据上述反应鉴别 和 NaCl,可选择以下物质中的 进行实验(填序号)。
A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.酒精
③某厂废液中含有 3%~6%的 ,直接排放会造成污染,下列试剂能使 转化为不引起二次
污染的 的是 (填序号)。
A.浓硫酸 B. C. D.
17.(14 分)研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题。
I.按如图所示操作,充分反应后:
(1)i 中铁丝表面有红色固体生成,ⅱ中铜丝上观察到的现象是 。
(2)结合 i、ii 实验现象可知,Fe2+、Cu2+、Ag+ 的氧化性由强到弱的顺序为 。
/Ⅱ.焊接铜器时,可先用 NH Cl 溶液除去表面的 CuO 再进行焊接,该反应是 CuO
4
NH Cl Cu CuCl N HO。
4 2 2 2
(3)配平该反应方程式: 。
□CuO □NH Cl □Cu □CuCl □N □H O
4 2 2 2
(4)每生成 2 个 N 分子,转移电子数为 个。
2
Ⅲ.氮氧化物(NOx)储存还原的工作原理(NSR)如下图所示,柴油发动机工作时在稀燃(O 充足、柴油较
2
少)和富燃(O 不足、柴油较多)条件下交替进行,通过 BaO 和 Ba(NO ) 的相互转化实现 NOx 的储存和
2 3 2
还原。
(5)BaO 吸收 NO 的反应中氧化剂与还原剂的粒子个数之比为 。
2
(6)富燃条件下 Pt 表面反应的化学方程式是 。
(7)一定范围内,BaO 对氮氧化物的吸收率随气体中 CO 的体积分数的增大而下降的原因可能
2
是 。
18.(14 分)如图是某课外活动小组的同学设计的实验室制取 CO 并检验其性质的装置示意图,请回答问
2
题:
(1)代号 a 所指仪器的名称是 ,A 装置中发生反应的化学方程式为 。
(2)将 A 中产生的气体通入到 B 中一会儿,未见澄清石灰水变浑浊。李祥同学认为这是浓盐酸挥发出的
HCl 气体干扰所致。他用化学方程式表示为:
Ca(OH) +CO=CaCO ↓+HO
2 2 3 2
CaCO +2HCl=CaCl +HO+CO↑
3 2 2 2
你的解释还可更简捷,请用一个化学方程式表示: 。
(3)张华同学用烧瓶收集 A 中产生的气体后,向其中加入过员无色透明的 M 溶液组成 C 装置,振荡,
发现烧瓶中的气球逐渐变大,且溶液始终无色透明,则 M 可能是 (填一种物质的化学式)。
(4)请设计一个方案,验证 C 装置中反应的生成物中含有 。简述实验过程: 。
(5)将 A 中药品换成过氧化氢溶液和二氧化锰,则反应的化学方程式为: 。
/