文档内容
遵义市2015年初中毕业升学统一考试
化学部分
一、选择题(本大题包括10个小题,每小题2分,共20分。每小题只有一个正确答案,请在答
题卡选择题栏内用2B铅笔将对应题目答案的标号涂黑。)
1.材料是人类发展中的重要物质,陶瓷属于( )
A.合成材料 B.无机非金属材料
C.复合材料 D.金属材料
2.(2分)(2015•遵义)下列净化水的方法中,净化程度最高的是( )
A.静置 B.吸附 C.过滤 D.蒸馏
3.(2分)(2015•遵义)物质的性质决定用途,下列说法不正确的是( )
A.用甲醛溶液浸泡食品保鲜 B.用熟石灰改良酸性土壤
C.干冰用于人工降雨 D.一氧化碳可用作燃料
4.(2分)(2015•遵义)分类是学习和研究化学的常用方法,下列分类正确的是( )
A.有机物:甲烷、碳酸钡 B.化石燃料:石油、天然气
C.混合物:氮气、空气 D.复合肥料:硝酸钾、氯化铵
5.(2分)(2015•遵义)某反应的围观示意图如图,有关说法错误的是( )
A.甲的化学式为NH
3
B.该反应是置换反应
C.丙、丁属于氧化物
D.化学反应前后分子种类发生了变化
6.(2分)(2015•遵义)根据 这4种微粒结构示意图,判断
下列说法中正确的是( )
A.它们都带有电荷 B.它们表示同一种元素
C.它们核外电子排布相同 D.它们都具有相对稳定结构
7.(2分)(2015•遵义)下列离子在水溶液中无色且能大量共存的一组是( )
A.
Ca2+,K+,Cl﹣,NO
B.
Na+,Cu2+,NO ,SO
C.
Fe3+,Na+,OH﹣,NO
D.
K+,H+,SO ,CO
18.(2分)(2015•遵义)质量守恒定律是帮助我们学习认识化学反应实质的重要理论,在化学
反应aA+bB═cC+dD中,下列说法正确的是( )
A.化学计量数a与b之和一定等于c与d之和
B.若A和C都是盐,则该反应一定是复分解反应
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取xgA和xgB反应,生成C和D的质量总和不一定是2xg
9.(2分)(2015•遵义)酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于
盐酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊试液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
10.(2分)(2015•遵义)下列各项实验(括号内为相应的操作或方法),能达到实验目的是(
)
A.除去CO 中的少量CO(点燃)
2
B.验证硫酸铵溶液(取样,加氢氧化钠溶液)
C.检验CaO中混有的CaCO 溶液(滴加稀盐酸)
3
D.鉴别氢氧化钠和碳酸钠(取样,溶解,滴加酚酞)
二、非选择题(11-17小题每空1分,18小题4分,共40分)
11.(4分)(2015•遵义)用化学用于填空:
(1)氢原子 H
(2)2个二氧化硫分子 2S O
2
(3)3个铵根离子 3N H+
4
(4)氧化铁中铁元素的化合价 O .
2 3
12.(4分)(2015•遵义)根据图示完成相关问题:
(1)写出标号为①的仪器名称 铁架台 .
(2)制取气体前图C的操作是 检查装置的气密性 .
(3)实验室用图A装置制取二氧化碳的化学方程式为 CaC O+2HCl═CaCl+HO+CO ↑ ,将
3 2 2 2
产生的气体通入图B装置中,无明显现象,可能的原因是 二氧化碳中混有氯化氢气体 .
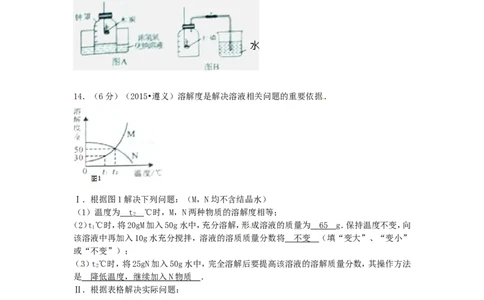
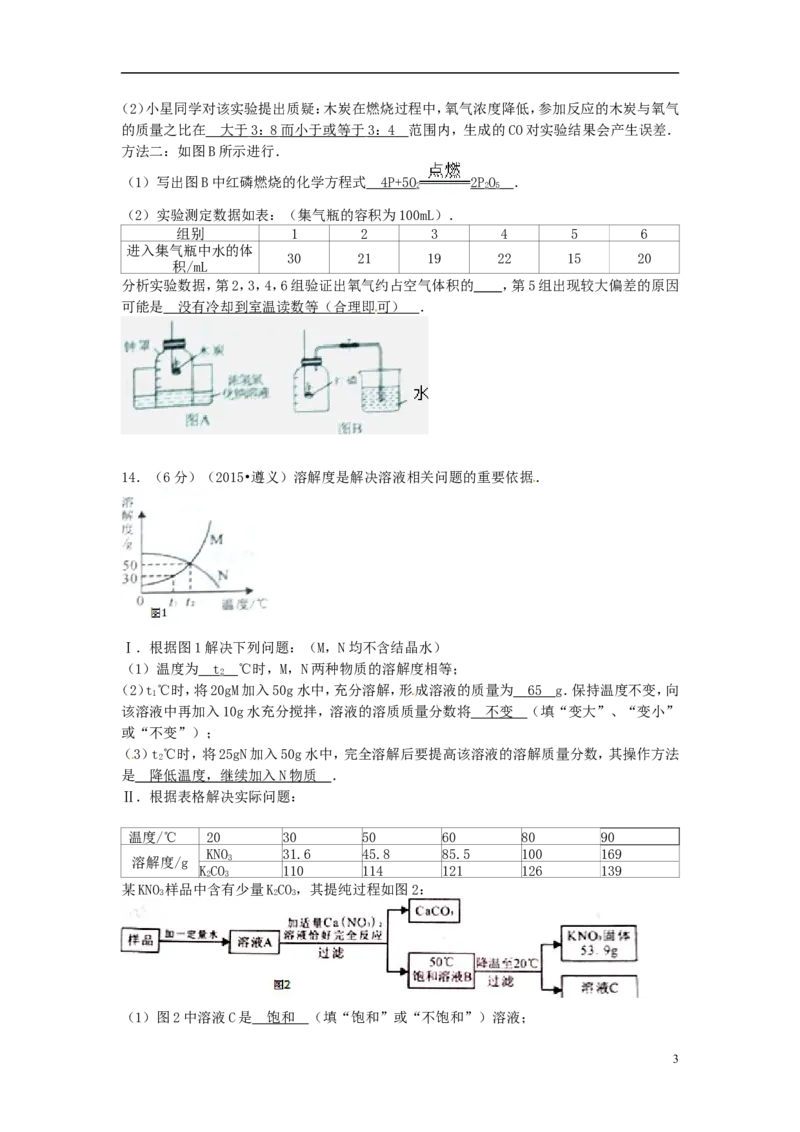
13.(6分)(2015•遵义)某化学实验小组用两种方法验证空气中的氧气含量.
方法一:如图A所示进行.
(1)写出图A中二氧化碳与氢氧化钠溶液反应的化学方程式 C O+2NaOH=NaCO+H O .
2 2 3 2
2(2)小星同学对该实验提出质疑:木炭在燃烧过程中,氧气浓度降低,参加反应的木炭与氧气
的质量之比在 大于 3 : 8 而小于或等于 3 : 4 范围内,生成的CO对实验结果会产生误差.
方法二:如图B所示进行.
(1)写出图B中红磷燃烧的化学方程式 4P+5 O 2PO .
2 2 5
(2)实验测定数据如表:(集气瓶的容积为100mL).
组别 1 2 3 4 5 6
进入集气瓶中水的体
30 21 19 22 15 20
积/mL
分析实验数据,第2,3,4,6组验证出氧气约占空气体积的 ,第5组出现较大偏差的原因
可能是 没有冷却到室温读数等(合理即可) .
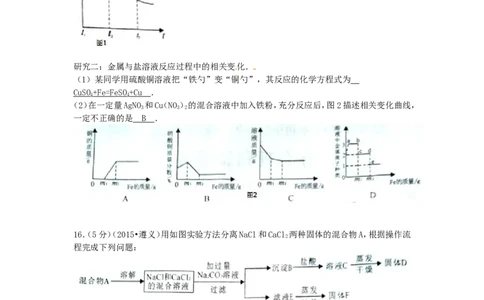
14.(6分)(2015•遵义)溶解度是解决溶液相关问题的重要依据.
Ⅰ.根据图1解决下列问题:(M,N均不含结晶水)
(1)温度为 t ℃时,M,N两种物质的溶解度相等;
2
(2)t℃时,将20gM加入50g水中,充分溶解,形成溶液的质量为 6 5 g.保持温度不变,向
1
该溶液中再加入10g水充分搅拌,溶液的溶质质量分数将 不变 (填“变大”、“变小”
或“不变”);
(3)t℃时,将25gN加入50g水中,完全溶解后要提高该溶液的溶解质量分数,其操作方法
2
是 降低温度,继续加入 N 物质 .
Ⅱ.根据表格解决实际问题:
温度/℃ 20 30 50 60 80 90
KNO 31.6 45.8 85.5 100 169
溶解度/g 3
KCO 110 114 121 126 139
2 3
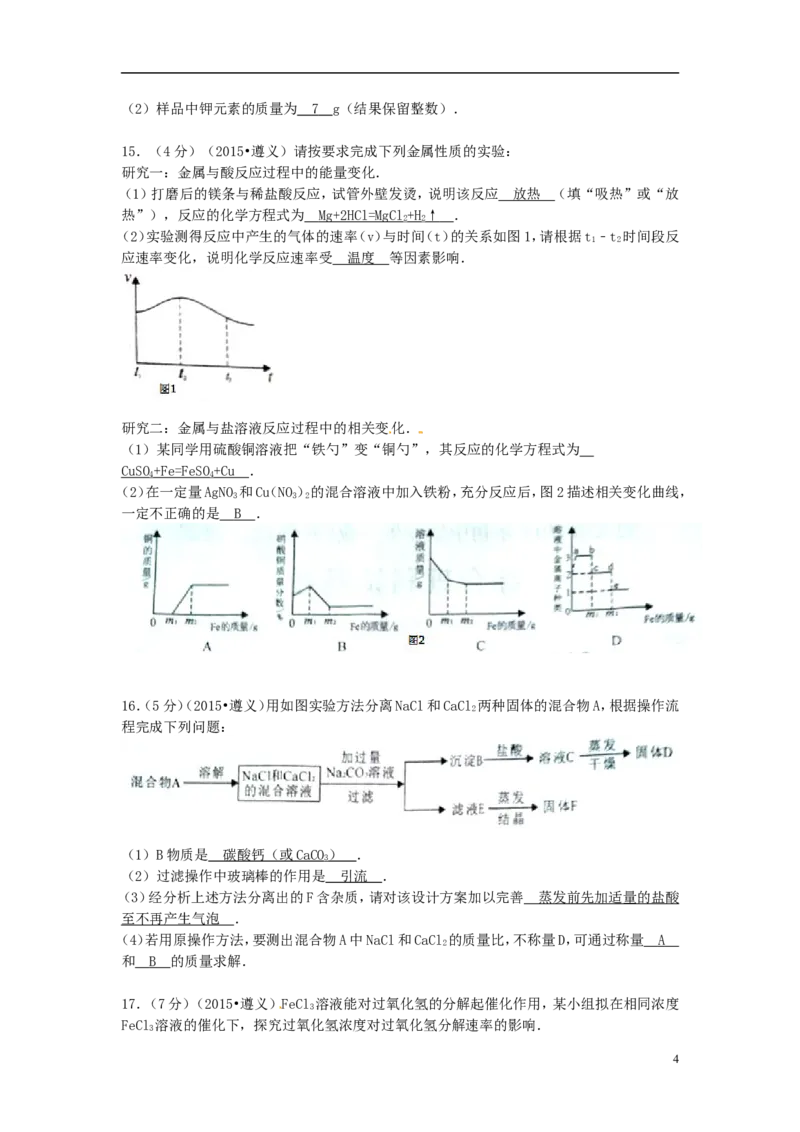
某KNO 样品中含有少量KCO,其提纯过程如图2:
3 2 3
(1)图2中溶液C是 饱和 (填“饱和”或“不饱和”)溶液;
3(2)样品中钾元素的质量为 7 g(结果保留整数).
15.(4分)(2015•遵义)请按要求完成下列金属性质的实验:
研究一:金属与酸反应过程中的能量变化.
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应 放热 (填“吸热”或“放
热”),反应的化学方程式为 Mg+2HCl=MgC l+H ↑ .
2 2
(2)实验测得反应中产生的气体的速率(v)与时间(t)的关系如图1,请根据t﹣t 时间段反
1 2
应速率变化,说明化学反应速率受 温度 等因素影响.
研究二:金属与盐溶液反应过程中的相关变化.
(1)某同学用硫酸铜溶液把“铁勺”变“铜勺”,其反应的化学方程式为
CuSO+Fe=FeSO +C u .
4 4
(2)在一定量AgNO 和Cu(NO)的混合溶液中加入铁粉,充分反应后,图2描述相关变化曲线,
3 3 2
一定不正确的是 B .
16.(5分)(2015•遵义)用如图实验方法分离NaCl和CaCl 两种固体的混合物A,根据操作流
2
程完成下列问题:
(1)B物质是 碳酸钙(或 CaC O) .
3
(2)过滤操作中玻璃棒的作用是 引流 .
(3)经分析上述方法分离出的F含杂质,请对该设计方案加以完善 蒸发前先加适量的盐酸
至不再产生气泡 .
(4)若用原操作方法,要测出混合物A中NaCl和CaCl 的质量比,不称量D,可通过称量 A
2
和 B 的质量求解.
17.(7分)(2015•遵义)FeCl 溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度
3
FeCl 溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
3
4写出本实验发生反应的化学方程式 2 HO 2HO+O ↑ .
2 2 2 2
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的
FeCl 溶液,如图观察到 反应速率 ,就可以粗略判断,得出实验结果.
3
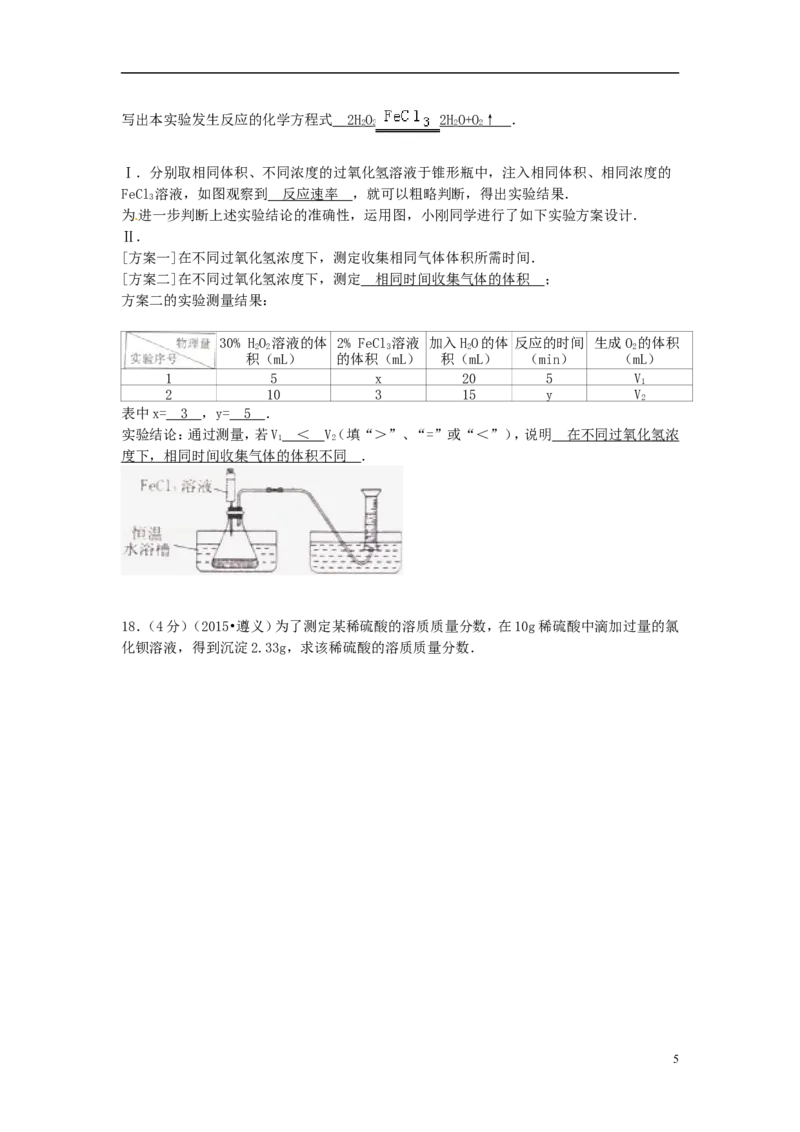
为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设计.
Ⅱ.
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
[方案二]在不同过氧化氢浓度下,测定 相同时间收集气体的体积 ;
方案二的实验测量结果:
30% HO 溶液的体 2% FeCl 溶液 加入HO的体 反应的时间 生成O 的体积
2 2 3 2 2
积(mL) 的体积(mL) 积(mL) (min) (mL)
1 5 x 20 5 V
1
2 10 3 15 y V
2
表中x= 3 ,y= 5 .
实验结论:通过测量,若V < V(填“>”、“=”或“<”),说明 在不同过氧化氢浓
1 2
度下,相同时间收集气体的体积不同 .
18.(4分)(2015•遵义)为了测定某稀硫酸的溶质质量分数,在10g稀硫酸中滴加过量的氯
化钡溶液,得到沉淀2.33g,求该稀硫酸的溶质质量分数.
567