文档内容
2025年湖北省七市州高三年级3月联合统一调研考试
化学参考答案
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
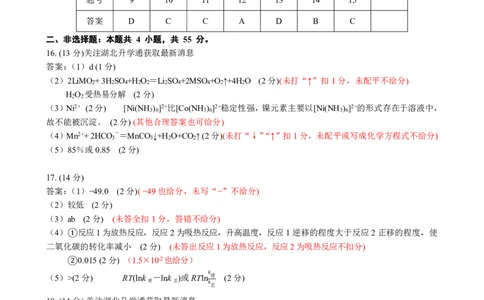
题号 1 2 3 4 5 6 7 8
答案 B D A B C B D A
题号 9 10 11 12 13 14 15
答案 D C C A D B C
二、非选择题:本题共 4 小题,共 55 分。
16.(13分)关注湖北升学通获取最新消息
答案:(1)d(1分)
(2)2LiMO +3HSO +H O =Li SO +2MSO +O ↑+4HO (2分)(未打“↑”扣1分,未配平不给分)
2 2 4 2 2 2 4 4 2 2
H O 受热易分解 (2分)
2 2
(3)Ni2+ (2分) [Ni(NH ) ]2+比[Co(NH ) ]2+稳定性强,镍元素主要以[Ni(NH ) ]2+的形式存在于溶液中,
3 6 3 6 3 6
故不能被沉淀。 (2分)(其他合理答案也可给分)
(4)Mn2++2HCO -=MnCO↓+H O+CO↑(2分)(未打“↓”“↑”扣1分,未配平或写成化学方程式不给分)
3 3 2 2
(5)85%或0.85 (2分)
17.(14分)
答案:(1)−49.0 (2分)(−49也给分,未写“−”不给分)
(2)较低 (2分)
(3)ab (2分) (未答全扣1分,答错不给分)
(4) 反应1为放热反应,反应2为吸热反应,升高温度,反应1逆移的程度大于反应2正移的程度,使
二氧化碳的转化率减小 (2分) (未答出反应1为放热反应,反应2为吸热反应不扣分)
①
0.015(2分) (1.5×10-2也给分)
(5)②>(2分) RT(lnk
逆
-lnk
正
)或RTln 逆 (2分)
正
18.(14分) 关注湖北升学通获取最新消息
答案:(1)bcd(2分)(未答全扣1分,答错不给分)
(2)Fe (SO ) +Cu=2FeSO +CuSO (2分)(未配平或写成离子方程式不给分)
2 4 3 4 4
(3)Fe(OH) 或氢氧化铁(2分)
3
(4) (2分) SCN- Fe2+(共2分,对1个给1分)
(5)Fe2++Cu2++4SCN-=CuSCN↓+Fe(SCN) 或Fe2++Cu2++SCN-=CuSCN↓+Fe3+(2分)(未打“↓”扣1分,
② 3
未配平或写成化学方程式不给分)
(6)当存在SCN-时,生成了难溶的CuSCN,增强了Cu2+的氧化性(2分)
(或当存在SCN-时,生成了难电离的Fe(SCN) ,增强了Fe2+的还原性也可给分)
3
119.(14分) 关注湖北升学通获取最新消息
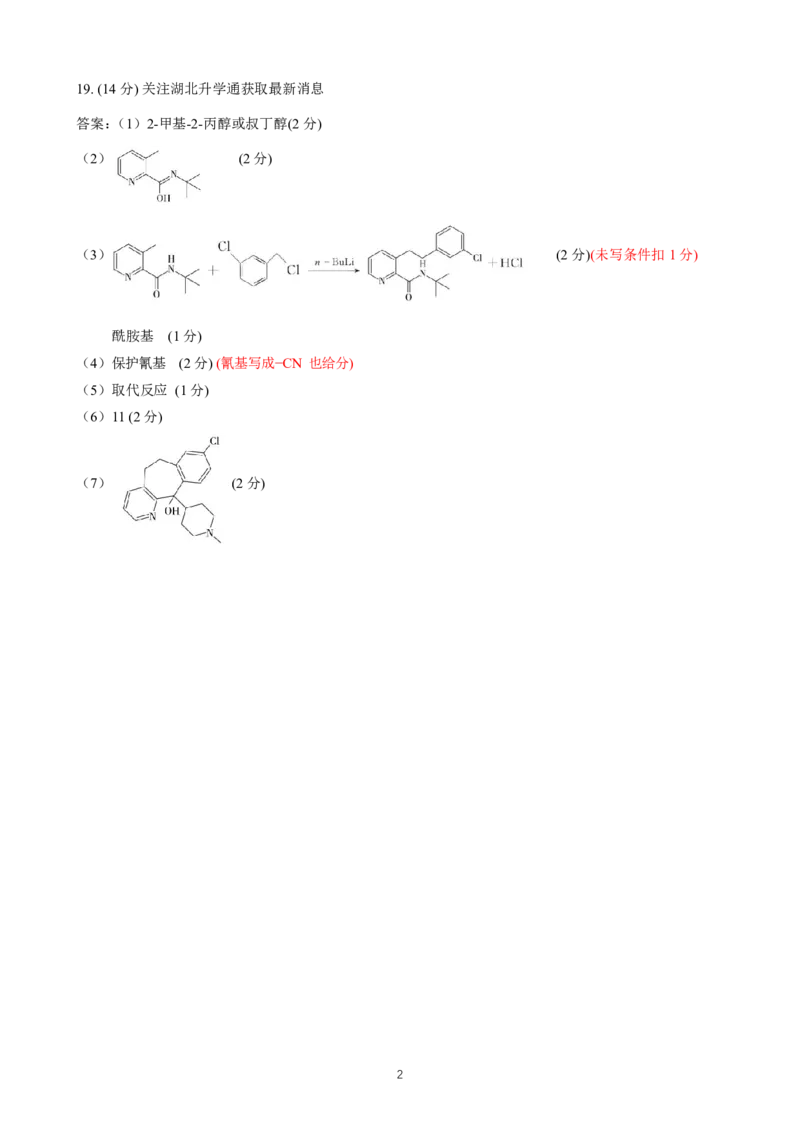
答案:(1)2-甲基-2-丙醇或叔丁醇(2分)
(2) (2分)
(3) (2分)(未写条件扣1分)
酰胺基 (1分)
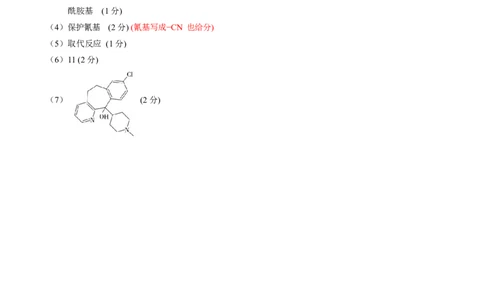
(4)保护氰基 (2分)(氰基写成−CN 也给分)
(5)取代反应 (1分)
(6)11(2分)
(7) (2分)
2试题解析
1.答案:B
解析:蚕丝属于天然纤维,不属于化学纤维,B错误。
2.答案:D
解析:稀土元素包括镧系元素以及钪和钇,D错误。
3.答案:A
解析:灼烧碎海带应在坩埚中进行,B错误;C装置不能检验二氧化硫的漂白性,C错误;氨气应用Ca(OH)
2
和NH Cl固体加热制取,D错误。
4
4.答案:B
解析:基态As原子的核外电子排布式应为[Ar]3d104s24p3,A错误;基态镁原子价层电子的电子云轮廓图为球
形,而不是哑铃形,C错误;CO 的电子式书写错误,D错误。
2
5.答案:C
解析:SiH 中硅为+4价,A错误;BF 为平面三角形,B错误;F-F的键能小于Cl-Cl,D错误。
4 3
6.答案:B
解析:布洛芬的核磁共振氢谱显示应为8组峰,B错误。
7.答案:D
解析:向含3molFeI
2
的溶液中通入4molCl
2
,离子方程式应为:2Fe2++6I-+4Cl 2=2Fe3++3I
2
+8Cl-,D错误。
8.答案:A
解析:O 的极性较弱,在CCl 中的溶解度高于在水中的溶解度,A错误。
3 4
9.答案:D
解析:X、Y、Z、W、Q分别为H、C、N、P、Cl。第一电离能:PNCl ,C错误。
3 3
10.答案:C
解析:装置A硫酸浓度太大,难以电离出离子,反应速率减慢,A错误;装置C中悬浊液变澄清只表明装置
C反应完成,装置D不一定反应完成,B错误;装置D热水浴中MnS O 受热分解形成MnSO ,C正确;装置D
2 6 4
热水浴温度太高,降低了SO 在溶液中的溶解度,不利于反应进行,D错误。
2
11.答案:C
解析:距离Ca最近的B有24个,A错误;依据晶胞结构推出,硼化钙的化学式为CaB ,Ca与B个数比为
6
106
1:6,B错误;该晶体的密度为 ·g·cm3,D错误。
N (a107)3
A
12.答案:A
解析:1mol甘氨酸合铜含有σ键20mol,A错误。
13.答案:D
解析:M极C H O 转化为CO ,碳元素化合价升高,M极为原电池负极,负极电势低于正极电势,A错误;
6 12 6 2
升高温度微生物容易失去活性,影响电池工作效率,B错误;未指明CO 所处的温度和压强,C错误。
2
14.答案:B
c(H A) c(HA2)
解析:曲线Ⅰ表示lg 2 随pH变化曲线,A错误;当pH=6时,lg =-1.2,B正确;当V(NaOH)=20.00
c(H A) c(H A)
3 2
mL时,生成NaHA,依据图像判断溶液显酸性,HA-的电离程度大于水解程度,则c(HA−)>c(HA2−)>c(HA),C
2 2 2 3
错误;当V(NaOH)=40.00mL时, 生成NaHA,溶液显碱性,依据电荷守恒:c(Na+)+c(H+)=c(HA−)+2c(HA2−)+3c(A3−)
2 2
+c(OH−),物料守恒:c(Na+)=2c(HA)+2c(HA−)+2c(HA2−)+2c(A3−),得到2c(HA)+c(HA−)>c(A3−),D错误。
3 2 3 2
315.答案:C
解析:分子B只能与直径适合的碱金属离子发生作用形成超分子,不能与所有碱金属离子发生相互作用,C错误。
16.解析:
(1)Co位于元素周期表第四周期第Ⅷ族,属于d区。
(2)LiMO“酸浸”时将HO 氧化,Ni、Co、Mn元素被还原为+2价,离子方程式为:2LiMO +3H SO +H O
2 2 2 2 2 4 2 2
=LiSO +2MSO +O ↑+4HO;H O 受热易分解,温度过高浸出率反而降低。
2 4 4 2 2 2 2
(3)25℃时,K (CoC O )=6.3×10−8,K (NiC O )=4.0×10−10,浸出液中c(Co2+)=0.11mol/L ,c(Ni2+)
sp 2 4 sp 2 4
=0.03mol/L, Ni2+开始沉淀需要c(C O 2−)=1.3×10−8mol/L,Co2+开始沉淀需要c(C O 2−)=5.7×10−7mol/L,
2 4 2 4
故Ni2+先沉淀。[Ni(NH) ]2+比[Co(NH ) ]2+稳定性强,镍元素主要以[Ni(NH ) ]2+的形式存在于溶液中,故不
3 6 3 6 3 6
能被沉淀。
(4)“沉锰”过程产生气体X,故发生反应的离子方程式为Mn2++2HCO -=MnCO ↓+H O+CO ↑。
3 3 2 2
(5)10L浸出液中n(Li+)=10L×0.14mol/L=1.4mol,n(Li CO )=44.03g÷74g/mol=0.595mol,回收得
2 3
到n(Li+)=1.19mol,Li+的回收率为1.19÷1.4=85%。
17.解析:
(1)ΔH =-200.7kJ·mol−1-241.8kJ·mol−1+393.5kJ·mol−1=−49kJ·mol−1
1
(2)反应3的ΔS<0,ΔH <0,据ΔG=ΔH−TΔS<0反应才能自发,推出反应3在较低温度下能自发进行。
3
(3)其他条件相同,反应1是气体体积减小的反应,反应在恒压条件下进行,容器体积减小,相当于恒容条
件下的加压,反应1平衡正向移动,CO 的平衡转化率更高,a正确;反应1和反应3是气体体积减小的
2
反应,反应2是气体体积不变的反应,容器内气体的压强不再改变,说明体系达到平衡状态,b正确;
增加催化剂的表面积,可加快反应速率,但不能引起平衡的移动,也不能影响CH OH的平衡产率,c
3
错误;其他条件相同,增大投料比[n(CO/n(H))],CO 的平衡转化率变小,d错误。
2 2 2
(4) 反应1为放热反应,反应2为吸热反应,升高温度,反应1逆移的程度大于反应2正移的程度,使
二氧化碳的转化率减小。
①
270℃时,体积固定的密闭容器中,按照n(CO
2
):n(H
2
)=1:3投料,容器内发生反应1和反应2,
平衡时α(CO)=24%,CO和CH OH在含碳产物中的物质的量分数相等,得出平衡时n(CO )=
2 3 2
②
0.76mol,n(CO)=0.12mol,n(H O)=0.24mol,n(H )=2.52mol,反应2为反应前后气体体积不变的反应,
2 2
则K= =0.015
p
0.12×0.24
E
(5)据0阿.7伦6×尼2.5乌2斯公式:lnk= a +C,结合图像,反应2的倾斜程度大于反应3,斜率等于−E ,
a
RT
即|E |越大,直线倾斜程度越大,则E :反应2>反应3;
a a
ΔH =E −E =(C−lnk )RT−(C−lnk )RT=RT(lnk -lnk )或RTln 逆。
2 a正 a逆 正 逆 逆 正
正
18.解析:
(1)配置250mL0.05mol/LFe(SO) 溶液,需要用到250mL容量瓶、烧杯、胶头滴管。
2 4 3
(2)实验1盛有Fe (SO ) 溶液的试管中加入过量铜粉,溶液颜色变蓝,发生反应的化学方程式为
2 4 3
Fe (SO ) +Cu=2FeSO +CuSO
2 4 3 4 4
(3)FeSO 溶液于试管中长时间放置,观察到少量红褐色沉淀,依据此特征颜色推断出红褐色沉淀为
4
Fe(OH) 。
3
4(4)取CuSO 溶液于试管中,滴加KSCN溶液,放置2小时,未见白色沉淀,不可能发生反应
4
2Cu2++4SCN- ===2CuSCN↓+(SCN)
2
,故假设②不合理。实验1反应后生成了Cu2+、Fe2+,滴加了KSCN
溶液,溶液变红并产生少量白色沉淀,实验2观察到的现象有可能是Cu2+、SCN-、Fe2+共同反应的结果。
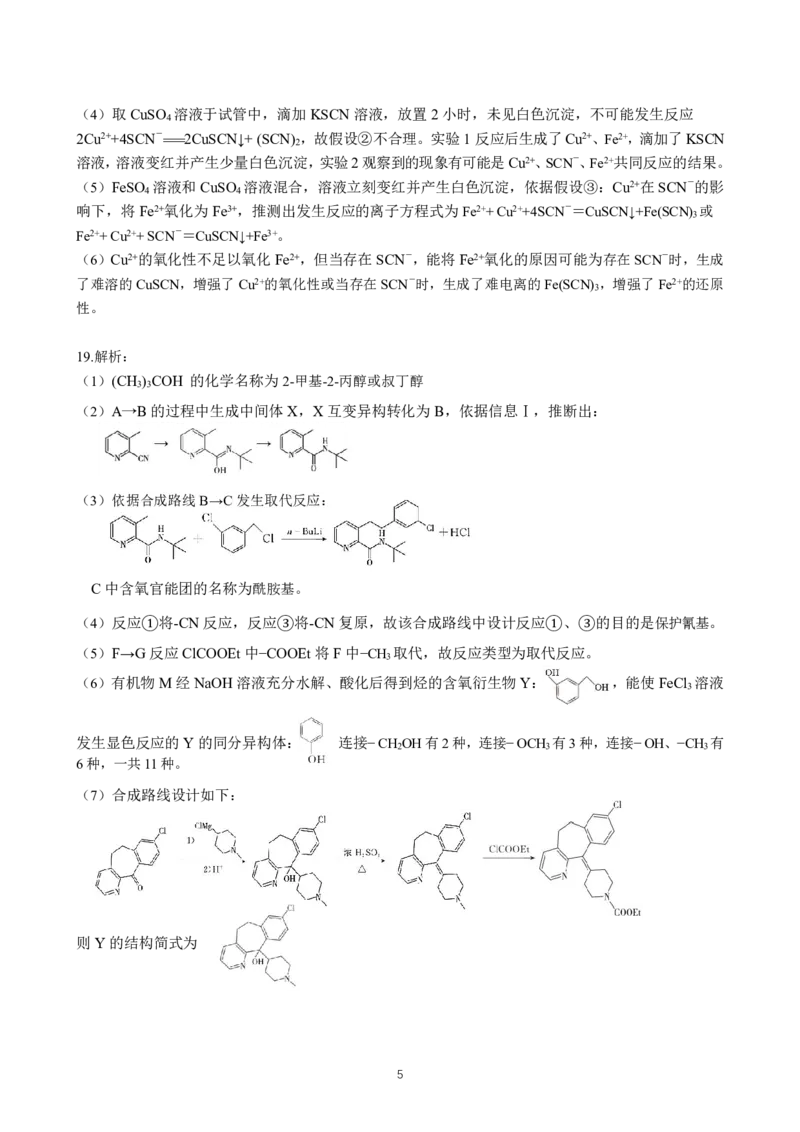
(5)FeSO 溶液和CuSO 溶液混合,溶液立刻变红并产生白色沉淀,依据假设③:Cu2+在SCN-的影
4 4
响下,将Fe2+氧化为Fe3+,推测出发生反应的离子方程式为Fe2++Cu2++4SCN-=CuSCN↓+Fe(SCN) 或
3
Fe2++Cu2++SCN-=CuSCN↓+Fe3+。
(6)Cu2+的氧化性不足以氧化Fe2+,但当存在SCN-,能将Fe2+氧化的原因可能为存在SCN-时,生成
了难溶的CuSCN,增强了Cu2+的氧化性或当存在SCN-时,生成了难电离的Fe(SCN) ,增强了Fe2+的还原
3
性。
19.解析:
(1)(CH ) COH 的化学名称为2-甲基-2-丙醇或叔丁醇
3 3
(2)A→B的过程中生成中间体X,X互变异构转化为B,依据信息Ⅰ,推断出:
(3)依据合成路线B→C发生取代反应:
C中含氧官能团的名称为酰胺基。
(4)反应 将-CN反应,反应 将-CN复原,故该合成路线中设计反应 、 的目的是保护氰基。
(5)F→G①反应ClCOOEt中−CO③OEt将F中−CH
3
取代,故反应类型为取代①反应③。
(6)有机物M经NaOH溶液充分水解、酸化后得到烃的含氧衍生物Y: ,能使FeCl 溶液
3
发生显色反应的Y的同分异构体: 连接−CH OH有2种,连接−OCH 有3种,连接−OH、−CH 有
2 3 3
6种,一共11种。
(7)合成路线设计如下:
则Y的结构简式为
5