文档内容
2024-2025 学年高二化学上学期期中模拟卷
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准
考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修1(不含电化学部分)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷(选择题 共 40 分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.合理利用某些盐能水解的性质,可以解决许多生产、生活中的问题。下列叙述的事实与盐水解的性质
无关的是
A.配制FeSO 溶液时,加入一定量 Fe粉
4
B.沸水中加入饱和的氯化铁溶液制备Fe(OH) 胶体
3
C.长期施用铵态氮肥会使土壤酸化
D.热碱水清洗厨房里的油污
2.下列事实一定能说明HF是弱酸的是
A.用HF溶液做导电性实验,灯泡很暗
B.1mol/L的HF水溶液能使紫色石蕊试液变红
C.常温下0.1mol/L的HF溶液的pH为2.3
D.HF能与NaCO 溶液反应,产生CO 气体
2 3 2
3.工业上由CO 和H 合成气态甲醇的热化学方程式为CO(g)+3H(g)=CH OH(g)+HO(g) ΔH<0。已知
2 2 2 2 3 2
该反应是放热反应。下列表示合成甲醇的反应的能量变化示意图正确的是
A. B.
C. D.
4.已知: ; ; ;
1
学学科科网网((北北京京))股股份份有有限限公公司司。
下列叙述正确的是
A. B.
C. D. 代表 的燃烧热
5.下列说法正确的是
A.凡是放热反应都是自发的,因为吸热反应都是非自发的
B.非自发反应在任何情况下都不会发生反应
C.常温下,反应 不能自发进行,则该反应的
D.标准状况下,熵值:1mol <1mol CO
6.某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列说法正确的是
2 2 2 3 2
A.恒容下,再充入一定量的HO(g),平衡向正反应方向移动,v 加快、v 减慢
2 正 逆
B.缩小容器的体积,v >v
正 逆
C.恒容下,再充入一定量的Ar气,平衡向正反应方向移动
D.恒容下,再充入一定量的CH=CH (g),CH=CH (g)的平衡转化率增大
2 2 2 2
7.已知反应① 和反应② 在T℃时的
平衡常数分别为 和 ,该温度下反应③ 的平衡常数为 ,则
下列说法正确的是
A.反应①的平衡常数
B.反应②中,增大氢气浓度,平衡正移, 增大
C.对于反应②,T℃时,
D.对于反应②,恒容时,温度升高,K值减小,则该反应为放热反应
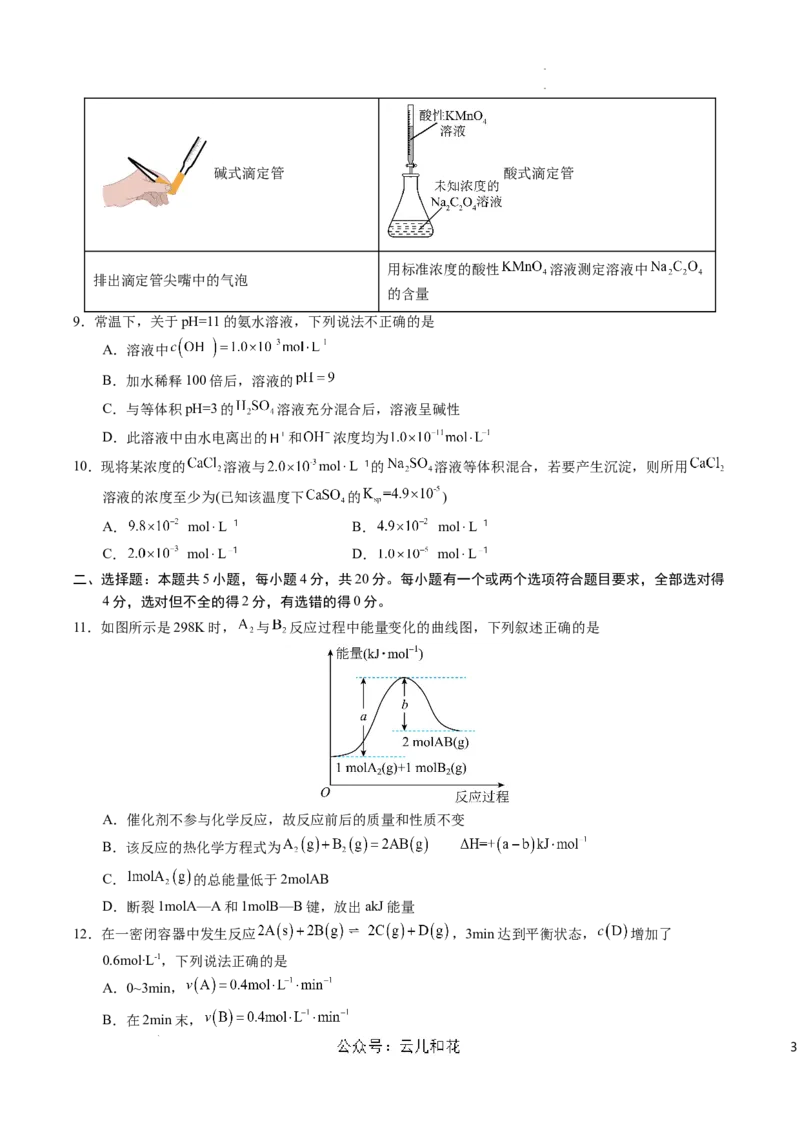
8.酸碱中和滴定是一种重要的实验方法,需要用到酸式滴定管和碱式滴定管,下列有关滴定管的判断、
使用或操作有误的是
A B
酸式滴定管 酸式/碱式滴定管
涂抹凡士林在图中旋塞的a端和旋塞套内的c
正确读取滴定管的读数为
端,防止漏水
C D
2
学学科科网网((北北京京))股股份份有有限限公公司司碱式滴定管 酸式滴定管
用标准浓度的酸性 溶液测定溶液中
排出滴定管尖嘴中的气泡
的含量
9.常温下,关于pH=11的氨水溶液,下列说法不正确的是
A.溶液中
B.加水稀释100倍后,溶液的
C.与等体积pH=3的 溶液充分混合后,溶液呈碱性
D.此溶液中由水电离出的 和 浓度均为
10.现将某浓度的 溶液与 mol⋅L 的 溶液等体积混合,若要产生沉淀,则所用
溶液的浓度至少为(已知该温度下 的 )
A. mol⋅L B. mol⋅L
C. mol⋅L D. mol⋅L
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
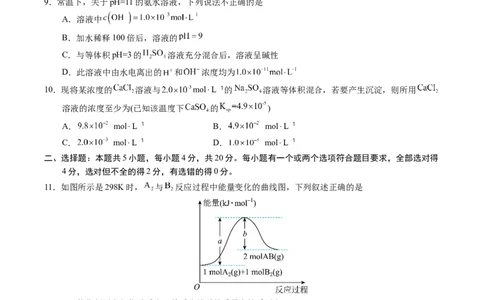
11.如图所示是298K时, 与 反应过程中能量变化的曲线图,下列叙述正确的是
A.催化剂不参与化学反应,故反应前后的质量和性质不变
B.该反应的热化学方程式为
C. 的总能量低于2molAB
D.断裂1molA—A和1molB—B键,放出akJ能量
12.在一密闭容器中发生反应 ,3min达到平衡状态, 增加了
0.6mol∙L-1,下列说法正确的是
A.0~3min,
B.在2min末,
3
学学科科网网((北北京京))股股份份有有限限公公司司C.第4min时, 和 表示的反应速率的值相等
D.若相同时间内, ,则这两段时间内反应速率相等
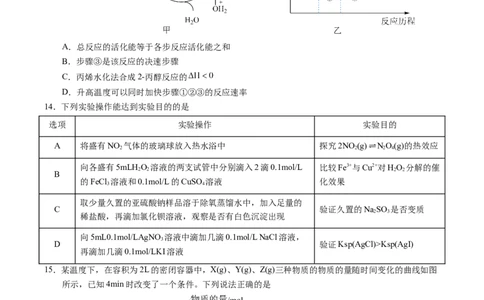
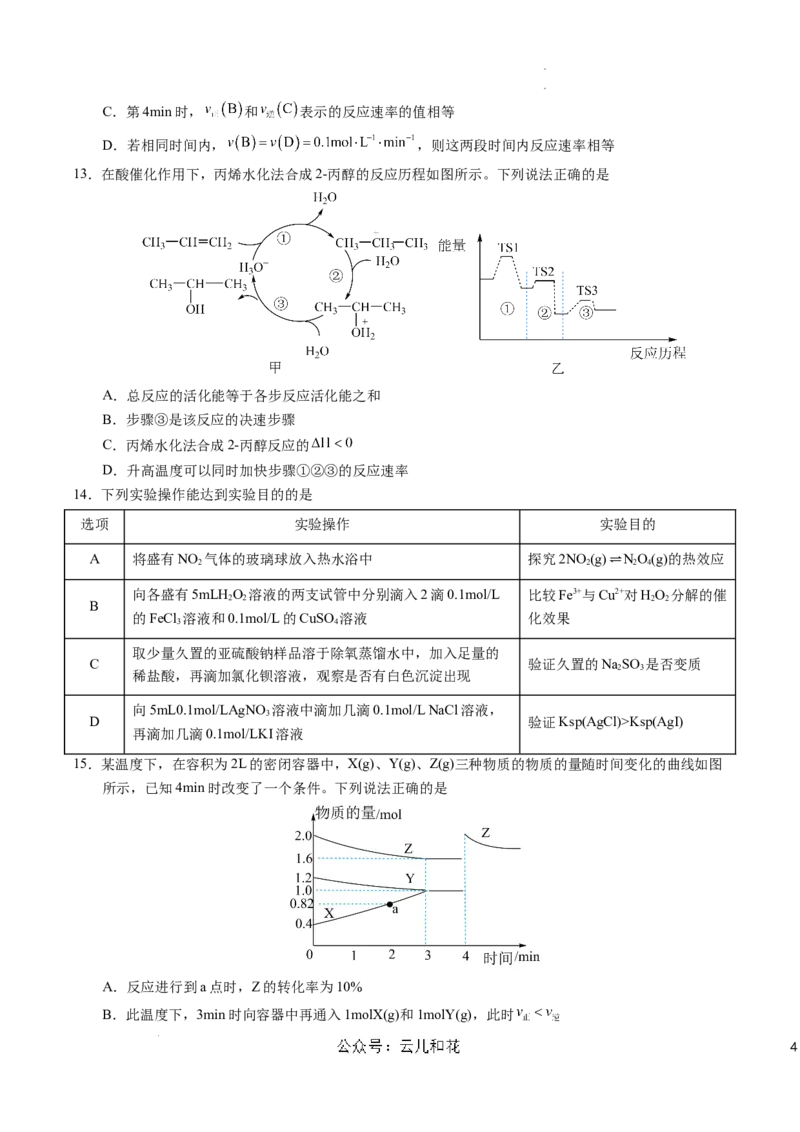
13.在酸催化作用下,丙烯水化法合成2-丙醇的反应历程如图所示。下列说法正确的是
A.总反应的活化能等于各步反应活化能之和
B.步骤③是该反应的决速步骤
C.丙烯水化法合成2-丙醇反应的
D.升高温度可以同时加快步骤①②③的反应速率
14.下列实验操作能达到实验目的的是
选项 实验操作 实验目的
A 将盛有NO
2
气体的玻璃球放入热水浴中 探究2NO
2
(g)⇌N
2
O
4
(g)的热效应
向各盛有5mLH O 溶液的两支试管中分别滴入2滴0.1mol/L 比较Fe3+与Cu2+对HO 分解的催
2 2 2 2
B
的FeCl 溶液和0.1mol/L的CuSO 溶液 化效果
3 4
取少量久置的亚硫酸钠样品溶于除氧蒸馏水中,加入足量的
C 验证久置的NaSO 是否变质
2 3
稀盐酸,再滴加氯化钡溶液,观察是否有白色沉淀出现
向5mL0.1mol/LAgNO 溶液中滴加几滴0.1mol/L NaCl溶液,
3
D 验证Ksp(AgCl)>Ksp(AgI)
再滴加几滴0.1mol/LKI溶液
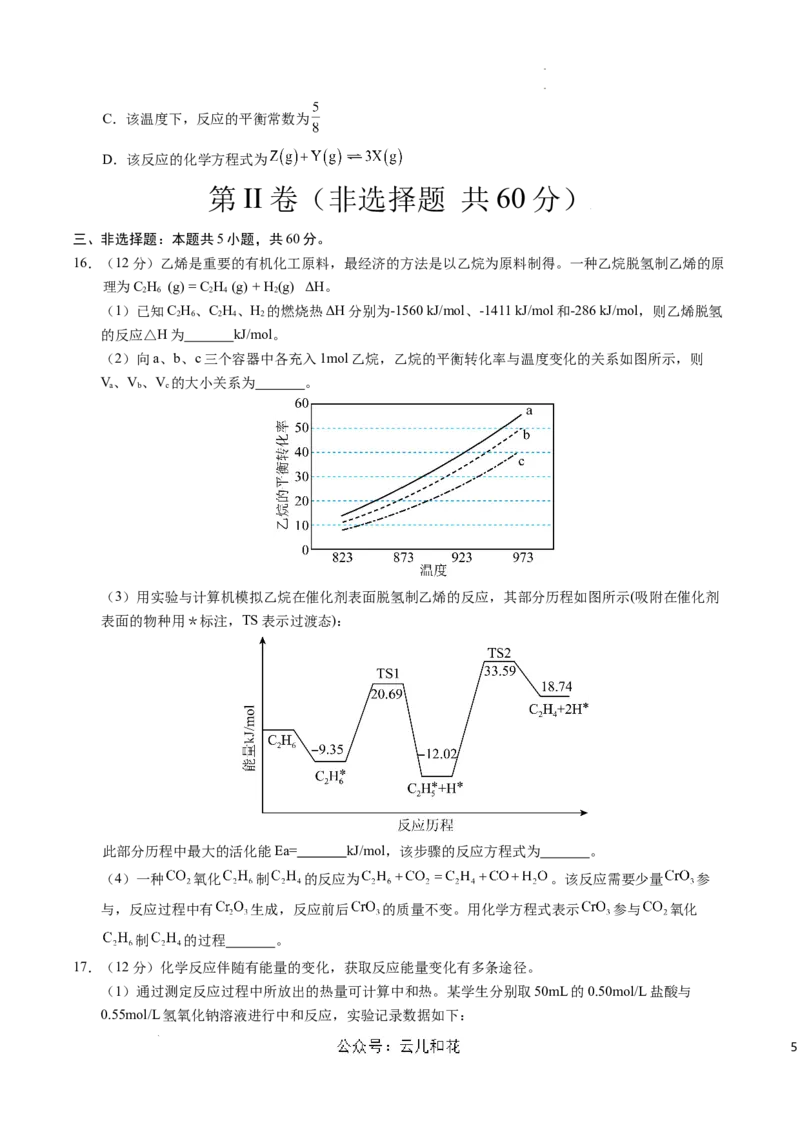
15.某温度下,在容积为2L的密闭容器中,X(g)、Y(g)、Z(g)三种物质的物质的量随时间变化的曲线如图
所示,已知4min时改变了一个条件。下列说法正确的是
A.反应进行到a点时,Z的转化率为10%
B.此温度下,3min时向容器中再通入1molX(g)和1molY(g),此时
4
学学科科网网((北北京京))股股份份有有限限公公司司C.该温度下,反应的平衡常数为
D.该反应的化学方程式为
第 II 卷(非选择题 共 60 分)
三、非选择题:本题共5小题,共60分。
16.(12分)乙烯是重要的有机化工原料,最经济的方法是以乙烷为原料制得。一种乙烷脱氢制乙烯的原
理为C H (g) = C H (g)+H(g) ΔH。
2 6 2 4 2
(1)已知C H、C H、H 的燃烧热ΔH分别为-1560 kJ/mol、-1411 kJ/mol和-286 kJ/mol,则乙烯脱氢
2 6 2 4 2
的反应△H为 kJ/mol。
(2)向a、b、c三个容器中各充入1mol乙烷,乙烷的平衡转化率与温度变化的关系如图所示,则
V、V、V 的大小关系为 。
a b c
(3)用实验与计算机模拟乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如图所示(吸附在催化剂
表面的物种用*标注,TS表示过渡态):
此部分历程中最大的活化能Ea= kJ/mol,该步骤的反应方程式为 。
(4)一种 氧化 制 的反应为 。该反应需要少量 参
与,反应过程中有 生成,反应前后 的质量不变。用化学方程式表示 参与 氧化
制 的过程 。
17.(12分)化学反应伴随有能量的变化,获取反应能量变化有多条途径。
(1)通过测定反应过程中所放出的热量可计算中和热。某学生分别取50mL的0.50mol/L盐酸与
0.55mol/L氢氧化钠溶液进行中和反应,实验记录数据如下:
5
学学科科网网((北北京京))股股份份有有限限公公司司起始温度 ℃ 终止温度 ℃
实验序
号
盐酸 氢氧化钠 混合溶液
1 20.0 20.2 23.3
2 20.2 20.4 23.5
3 20.6 20.6 25.6
①已知热量计算 ,盐酸和氢氧化钠溶液的密度都是 ,又知中和后生成溶液的比热容
c=4.180J/(g・℃),依据该学生的实验数据计算,该实验测得的 ℃, J;该实
验数据测出的中和热 (保留1位有效数字)。
②上述实验得出的 大于-57.3 ,产生偏差的原因不可能是 (填字母)。
a.实验装置保温、隔热效果差
b.量取HCl溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
③若改用60mL 0.25 和50mL 0.55 NaOH溶液进行反应与上述实验相比,所放
出的热量 (填“相等”或“不相等”),若实验操作均正确,则是否影响中和热的计算结果
(填“偏大”、“偏小”或“不影响”)。
④若改用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热 会 (填“偏
大”、“偏小”或“不影响”)。
(2)通过化学键的键能计算。已知:
化学键种类
键能/ 436 496 463.4
计算可得: 。
(3)通过盖斯定律计算。氧化亚铜()常用于制船底防污漆,已知反应:
则 的 (用 和 表达)。
18.(12分)合成氨工艺是人工固氮最重要的途径。回答下列问题:
(1)工业合成氨的反应为 。在容积为2L的密闭容器中,通入amolN 和
2
6
学学科科网网((北北京京))股股份份有有限限公公司司bmolH ,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN 。
2 2
①达到平衡时,H 的转化率为 。
2
②在t min内以NH 的浓度变化表示的化学反应速率为 。
3
③若把容器的容积缩小一半,则正反应速率 (填“增大”、“减小”或“不变”,下
同),N 的转化率 。
2
(2)在合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前需经过铜氨液处
2 2 3
理,目的是除去其中的CO,其反应为: 。铜氨
液吸收CO适宜的生产条件是 。
(3)合成氨工业中采用循环操作,主要是为了 (填序号)。
a.增大化学反应速率 b.提高平衡混合物中氨的含量
c.降低氨的沸点 d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为 ,该反应自发的条件是
(填“低温自发”、“高温自发”或“任意温度自发”)。
②为提高CH 的平衡转化率,可采用的措施是 (填序号)。
4
a.使用合适的催化剂 b.采用较高的温度
c.采用较高的压强 d.延长反应时间
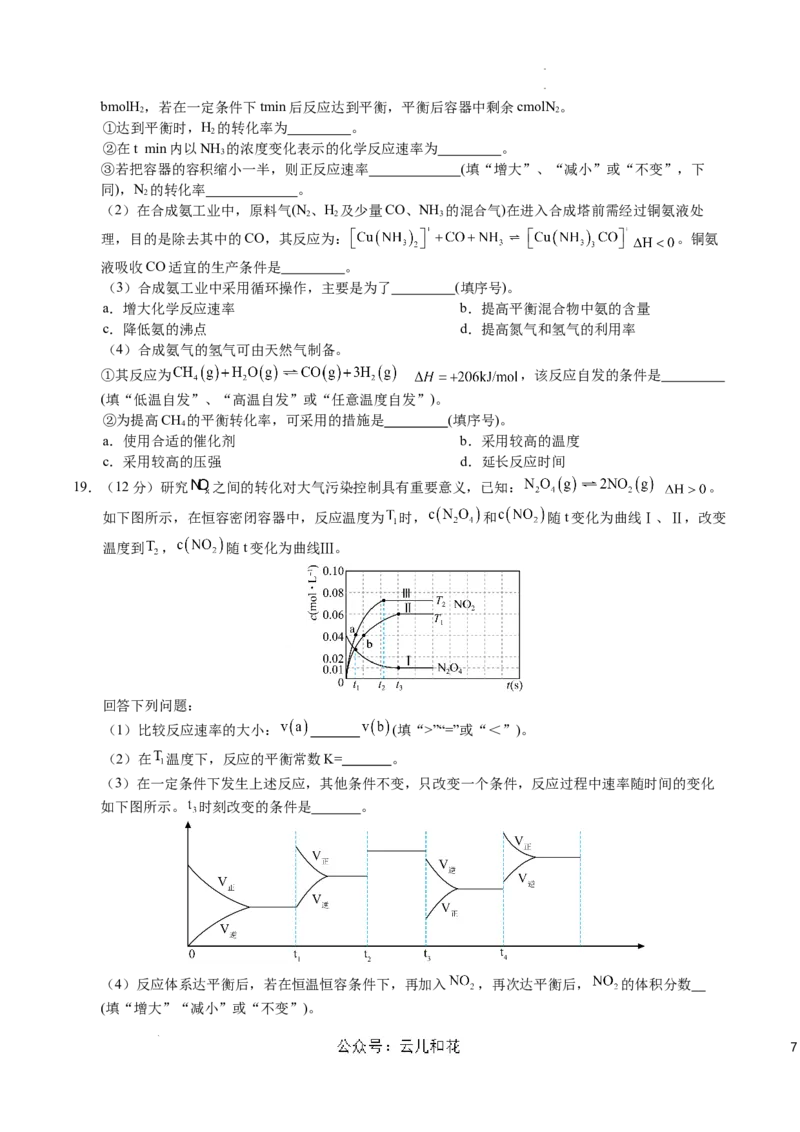
19.(12分)研究 之间的转化对大气污染控制具有重要意义,已知: 。
如下图所示,在恒容密闭容器中,反应温度为 时, 和 随t变化为曲线Ⅰ、Ⅱ,改变
温度到 , 随t变化为曲线Ⅲ。
回答下列问题:
(1)比较反应速率的大小: (填“>”“=”或“<”)。
(2)在 温度下,反应的平衡常数K= 。
(3)在一定条件下发生上述反应,其他条件不变,只改变一个条件,反应过程中速率随时间的变化
如下图所示。 时刻改变的条件是 。
(4)反应体系达平衡后,若在恒温恒容条件下,再加入 ,再次达平衡后, 的体积分数
(填“增大”“减小”或“不变”)。
7
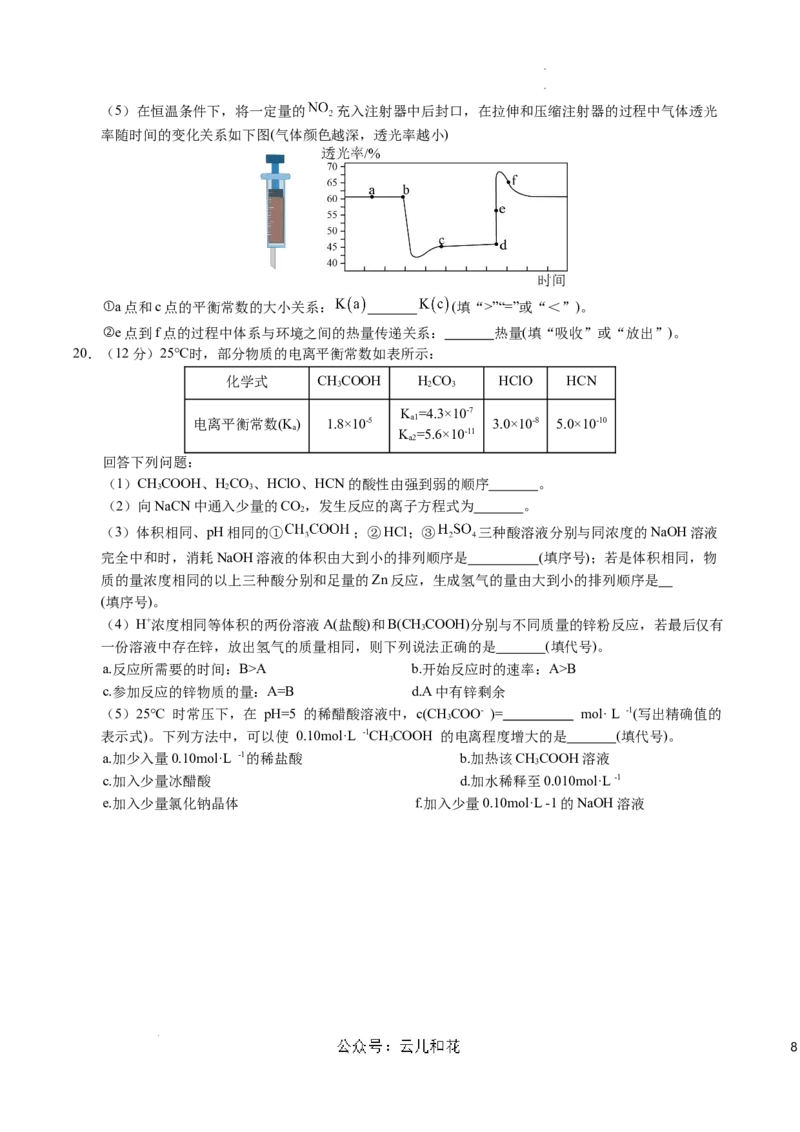
学学科科网网((北北京京))股股份份有有限限公公司司(5)在恒温条件下,将一定量的 充入注射器中后封口,在拉伸和压缩注射器的过程中气体透光
率随时间的变化关系如下图(气体颜色越深,透光率越小)
①a点和c点的平衡常数的大小关系: (填“>”“=”或“<”)。
②e点到f点的过程中体系与环境之间的热量传递关系: 热量(填“吸收”或“放出”)。
20.(12分)25℃时,部分物质的电离平衡常数如表所示:
化学式 CHCOOH HCO HClO HCN
3 2 3
K =4.3×10-7
电离平衡常数(K) 1.8×10-5 a1 3.0×10-8 5.0×10-10
a K =5.6×10-11
a2
回答下列问题:
(1)CHCOOH、HCO、HClO、HCN的酸性由强到弱的顺序 。
3 2 3
(2)向NaCN中通入少量的CO,发生反应的离子方程式为 。
2
(3)体积相同、pH相同的① ;②HCl;③ 三种酸溶液分别与同浓度的NaOH溶液
完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是 (填序号);若是体积相同,物
质的量浓度相同的以上三种酸分别和足量的Zn反应,生成氢气的量由大到小的排列顺序是
(填序号)。
(4)H+浓度相同等体积的两份溶液A(盐酸)和B(CHCOOH)分别与不同质量的锌粉反应,若最后仅有
3
一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是 (填代号)。
a.反应所需要的时间:B>A b.开始反应时的速率:A>B
c.参加反应的锌物质的量:A=B d.A中有锌剩余
(5)25°C 时常压下,在 pH=5 的稀醋酸溶液中,c(CHCOO- )= mol· L -1(写出精确值的
3
表示式)。下列方法中,可以使 0.10mol·L -1CHCOOH 的电离程度增大的是 (填代号)。
3
a.加少入量0.10mol·L -1的稀盐酸 b.加热该CHCOOH溶液
3
c.加入少量冰醋酸 d.加水稀释至0.010mol·L -1
e.加入少量氯化钠晶体 f.加入少量0.10mol·L -1的NaOH溶液
8
学学科科网网((北北京京))股股份份有有限限公公司司