文档内容
2024-2025 学年高二化学上学期第一次月考卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修1第1-2章(人教版2019)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 O 16 C 12 N 14 S 32
第Ⅰ卷(选择题 共 40 分)
一、选择题:本题共16个小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.“自热”火锅的发热包主要成分有:生石灰、铁粉、焦炭粉、氯化钙……等。下列说法错误的是
A.生石灰与水反应放热
B.使用时须向发热包中加入沸水
C.铁粉发生缓慢氧化,辅助放热
D.氯化钙可以吸收微量的水,减缓发热包失效
【答案】B
【解析】A.生石灰与水发生反应生成氢氧化钙,会放出大量的热,故A正确;B.反应本身放热,无
需加入沸水,故B错误;C.铁粉缓慢氧化 的过程也是放热反应,故C正确;D.生石灰吸水会使发热
包失效,氯化钙有吸水干燥作用,减缓发热包失效,故D正确;故选B。
2.S(单斜)和S(正交)是硫的两种同素异形体。
已知:①S(单斜,s)+O(g)=SO(g)△H=-297.16kJ·mol-1
2 2 1
②S(正交,s)+O(g)=SO(g)△H=-296.83kJ·mol-1
2 2 2
③S(单斜,s)=S(正交,s)△H
3
学科网(北京)股份有限公司 学科网(北京)股份有限公司下列说法正确的是
A.△H=+0.33kJ·mol-1
3
B.单斜硫转化为正交硫的反应是吸热反应
C.S(单斜,s)=S(正交,s)△H <0,正交硫比单斜硫稳定
3
D.S(单斜,s)=S(正交,s)△H >0,单斜硫比正交硫稳定
3
【答案】C
【解析】A.由盖斯定律可知,反应①-②=③,所以
,A错误;B.S(单斜,s)=S(正
交,s) ,反应为放热反应,B错误;C.S(单斜,s)=S(正交,s)
,△H<0,正交硫能量低,比单斜硫稳定,C正确;D.S(单斜,s)=S(正交,s)
3
,△H<0,D错误;故选C。
3
3.化学反应中不仅伴随着物质的变化还伴随能量的变化,下列说法正确的是
A.热化学方程式和化学方程式中的化学计量数的意义不完全相同
B.常温常压下, 完全燃烧比 完全燃烧时的焓变大
C.已知甲烷的燃烧热为 ,则甲烷燃烧热的热化学方程式可表示为
D.已知C(石墨,s)= C(金刚石,s) ,则金刚石比石墨稳定
【答案】A
【解析】A.热化学方程式的计量数表示物质的量,化学方程式中的化学计量数可以是物质的量或者是
分子数,意义不完全相同,故A正确;B.常温常压下, 完全燃烧放出的热量比
完全燃烧时多,因为 变成 还需要吸收一部分能力,故 完全燃烧比
完全燃烧时的焓变小,故B错误;C.1mol可燃物完全燃烧生成指定产物放出的热量叫燃烧
热,甲烷的燃烧热为 ,则甲烷燃烧热的热化学方程式可表示为
,故C错误;D.已知C(石墨,s)=
C(金刚石,s) ,说明金刚石能量高于石墨,则石墨比金刚石稳定,故D错误;故答案为A。
4.下列事实中,能用勒夏特列原理解释的个数为
①夏天,打开啤酒瓶时会从瓶口逸出大量气体
②浓氨水中加入氢氧化钠固体时产生较多有刺激性气味的气体
③实验室可用排饱和食盐水的方法收集氯气
④将盛有 和 混合气体的密闭容器置于冷水中,混合气体的颜色变浅
⑤合成氨时,将氨液化分离,可提高原料利用率
学科网(北京)股份有限公司 学科网(北京)股份有限公司A.2 B.5 C.4 D.3
【答案】B
【解析】①啤酒中存在二氧化碳的溶解平衡,夏天,打开啤酒瓶时,气体压强减小,平衡向生成气体
的方向移动,会从瓶口逸出气体,则打开啤酒瓶时会从瓶口逸出大量气体能用勒夏特列原理解释,故
符合题意;
②浓氨水中存在氨气的溶解平衡和氨水的电离平衡,加入氢氧化钠固体时,溶解放出大量的热,溶液
中氢氧根离子浓度变大,氨水电离平衡和溶解平衡均逆向移动,氨气的溶解度减小,溶解放出的热量
有利于氨气逸出,则产生较多的刺激性气味的气体,能用勒夏特列原理解释,故符合题意;③氯气与
水反应生成盐酸和次氯酸的反应为可逆反应,饱和实验水中氯离子浓度较大,使平衡向逆反应方向移
动,有利于降低氯气的溶解度,所以实验室可用排饱和食盐水的方法收集氯气能用勒夏特列原理解
释,故符合题意;④二氧化氮转化为四氧化二氮的反应为放热反应,将盛有二氧化氮和四氧化二氮混
合气体的密闭容器置于冷水中,温度降低,平衡向生成四氧化氮的方向移动,气体颜色变浅,则混合
气体的颜色变浅能用勒夏特列原理解释,故符合题意;⑤合成氨时,将氨液化分离,生成物浓度减
小,平衡向正反应方向移动,原料的利用率提高,则将氨液化分离可提高原料利用率能用勒夏特列原
理解释,故符合题意;能用勒夏特列原理解释的有5个,故选B。
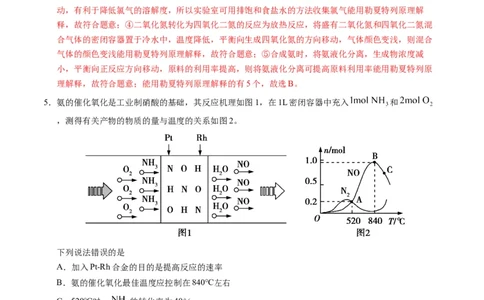
5.氨的催化氧化是工业制硝酸的基础,其反应机理如图1,在1L密闭容器中充入 和
,测得有关产物的物质的量与温度的关系如图2。
下列说法错误的是
A.加入Pt-Rh合金的目的是提高反应的速率
B.氨的催化氧化最佳温度应控制在840℃左右
C.520℃时, 的转化率为40%
D.840℃以上,可能发生了反应:2NO = O (g) + N
2 2
【答案】C
【解析】A.催化剂可加快反应速率,不影响平衡移动,则Pt-Rh合金的作用是提高反应速率,故A正
确;B.由图可知,840℃时NO的物质的量最大,则氨的催化氧化最佳温度应控制在840℃左右,故B
正确;C.520℃时NO、N 的物质的量均为0.2mol,由N原子守恒可知, 的转化率为
2
,故C错误;D.840℃以上NO的物质的量减小,N 的物质的量增加,则
2
学科网(北京)股份有限公司 学科网(北京)股份有限公司可能发生反应:2NO = O (g) + N ,故D正确;故答案为C。
2 2
6.已知可逆反应aA(g)+ bB(g) cC(g) + dD(g),在其他条件不变时,C的物质的量
分数随温度(T)或压强(P)的变化如下图所示,下列说法正确的是
A.反应达到平衡后,添加合适的催化剂,D的百分含量增加
B.e、f点对应的化学反应速率:
C.平衡常数K: ,
D. ,
【答案】C
【解析】先拐先平衡的原理可知 , ,温度升高C平衡时的物质的量分数减少,平衡逆向移
动,说明该反应是放热反应,压强增大C平衡时的物质的量分数减少,平衡逆向移动,说明该反应是
分子数增大的反应。A.催化剂只能增大速率,不能改变转化率,反应达到平衡后,添加合适的催化
剂,D的百分含量不变,故A错误;B.温度高速率快,e对应温度低,f点对应的温度高,故对应的化
学反应速率: ,故B错误;C.温度不变平衡常数不变,根据分析可知该反应是放热反
应, 升温平衡逆向移动, ,压强不影响平衡, ,故C正确;
D.根据分析可知 ,压强增大C平衡时的物质的量分数减少,平衡逆向移动,说明该反应是分子
数增大的反应 ,故D错误;故答案为C。
7.某学习小组为了探究 +5Br-+6H+=3Br +3H O反应速率(v)与反应物浓度的关系,在20℃进行实验,
2 2
所得的数据如下表:
实验编号相关
① ② ③ ④ ⑤
数据
c(H+)/mol/L 0.008 0.008 0.004 0.008 0.004
0.001 0.001 0.001 0.002 0.002
c( )/mol/L
c(Br-)/mol/L 0.10 0.20 0.20 0.10 0.40
2.4×10-8 4.8×10-8 1.2×10-8 4.8×10- v
v/mol/(L·s) 1
8
下列结论不正确的是
学科网(北京)股份有限公司 学科网(北京)股份有限公司A.若温度升高到40℃,则反应速率增大
B.实验②④,探究的是c( )对反应速率的影响
C.若该反应速率方程 为v=k c( )·c(Br-)·c(H+)(k为常数),则c=2
D.实验⑤中,v=4.8×10-8
1
【答案】B
【解析】实验②中,Br‾的浓度是实验①的2倍,速率也是实验①的2倍,由此可得a=1,实验②H+浓
度为③的2倍,其他条件都相同,速率②是③的4倍,带入公式求出c=2。A.温度升高到40℃,活化
分子百分数增大,有效碰撞次数增多,化学反应速率增大,A正确;B.②和④对比, 和Br-浓
度都不一样,变量不单一,因此无法探究c( )对反应速率的影响,B错误;C.实验②H+浓度为③
的2倍,其他条件都相同,速率②是③的4倍,带入公式求出c=2,C正确;D.实验②中,Br-的浓度
是实验①的2倍,速率也是实验①的2倍,由此可得a=1,实验⑤中H+的浓度是④中H+浓度的 ,实
验⑤中Br‾浓度是实验④中Br-浓度的4倍,则速率④=⑤,v=4.8×10-8,D正确;答案为B。
1
8. 与 在 作用下发生反应的能量变化及反应历程如图所示。下列说法中,不正确的是
A.该反应的
B. 使反应的活化能减小
C.催化剂通过参与反应改变了反应历程
D.上述过程在 作用下,提高了 与 的平衡转化率
【答案】D
【解析】A.由图示可知,该反应的反应物NO和CO的总能量高于生成物N 和CO 的总能量,反应为
2 2 2
放热反应,故 ,A正确;B.由图示可知, 是该反应的催化剂,故其能使反应的活化能减
小,从而加快反应速率,B正确;C.由图示可知,Fe+参与了反应,即催化剂通过参与反应改变了反应
历程,C正确;D.由B项分析可知,反应中Fe+是催化剂,催化剂只能影响反应速率不能使化学平衡
发生移动,故上述过程在 作用下,不能提高 与 的平衡转化率,D错误;故答案为:D。
学科网(北京)股份有限公司 学科网(北京)股份有限公司9.在容积不变的密闭容器中进行反应:A(g)+ 3B(g) 2C(g) 。下列各图表示当
其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示 时刻使用催化剂对反应速率的影响
C.图Ⅲ表示 时刻增大A的浓度对反应速率的影响
D.图Ⅳa、b、c三点,只有b点达到平衡状态
【答案】B
【解析】A.根据“先拐先平数值大”,乙先拐先达到平衡,用的时间短,速率快,对应的温度高,A
错误;B.使用催化剂能同等程度 的加快反应速率不影响平衡的移动,B正确;C.增大A的浓度正反
应速率增大,此时逆反应速率不变,C错误;D.b点代表正逆反应的平衡常数相等,平衡曲线上的点
都是平衡状态,D错误;答案选B。
10.用50 mL0.50 mol•L-1盐酸和50 mL0.55 mol•L-1NaOH溶液测定H+(aq)+OH-(aq)=H O(l)的反应热(ΔH)的
2
实验时,下列说法不正确的是
A.酸碱混合时,量筒中NaOH溶液应缓缓倒入量热计内筒中,不断用玻璃搅拌器搅拌
B.装置中的大小烧杯之间填满碎泡沫塑料的作用是保温隔热,减少热量损失
C.用量筒量取NaOH溶液时,仰视取液,测得的反应热ΔH不变
D.改用25 mL0.50 mol•L-1盐酸跟25 mL0.55 mol•L-1NaOH溶液进行测定,ΔH数值不变
【答案】A
【解析】A.酸碱混合时为了减少实验过程中的热量损失,要将量筒中NaOH溶液迅速倒入量热计内
筒中,并且迅速盖上盖板,防止热量的散失,而不能用玻璃棒搅拌,A错误;B.中和反应反应热测
定实验成败的关键是做好保温工作,为减少热量损失,装置中的大小烧杯之间填满碎泡沫塑料的作用
是保温隔热,B正确;C.用量筒量取NaOH溶液时,仰视取液,氢氧化钠溶液体积高于所需量的体
积,但由于碱过量,反应产生水的量以不足量的HCl为标准,故产生的水的量不变,则放出的热量不
变,测得的中和反应反应热ΔH不变,C正确;D.反应放出的热量与所用酸和碱的量有关,但生成1
mol水时中和反应反应热的大小与参加反应的酸碱用量无关,D正确;故合理选项是A。
11.一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO (s) + CO(g) MgO(s) + CO (g)
4 2
+SO(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡
2
后,纵坐标y随x变化趋势合理的是
学科网(北京)股份有限公司 学科网(北京)股份有限公司选项 x y
A 温度 容器内混合气体的密度
B CO的物质的量 CO 与CO的物质的量之比
2
C SO 的浓度 平衡常数K
2
D MgSO 的质量(忽略体积) CO的转化率
4
【答案】A
【解析】A、△H>0,升高温度,平衡正向移动,二氧化碳浓度增大,混合气体的密度增大,故A正
确;B、 ,平衡常数只与温度有关,温度不变常数不变,增加CO的物质的量,平
衡正向移动,SO 浓度增大,CO 与CO的物质的量之比减小,故B错误;C、平衡常数只与温度有
2 2
关,温度不变常数不变,故C错误;D、MgSO 是固体,增加固体质量,平衡不移动, CO的转化率
4
不变,故D错误;答案选A。
12.一定条件下存在反应:2SO (g)+O(g) 2SO (g) ΔH<0。现有三个体积相同 的密闭容器Ⅰ、Ⅱ、Ⅲ,
2 2 3
按如图所示投料,并在条件下开始反应。达到平衡时,下列说法正确的是
A.容器I、Ⅲ中平衡常数相同
B.容器Ⅱ、Ⅲ中正反应速率始终相同
C.容器Ⅱ、Ⅲ中的反应达平衡时,SO 的体积分数:Ⅱ>Ⅲ
3
D.容器I中SO 的转化率与容器Ⅱ中的转化率之和等于1
2
【答案】C
【解析】A.A 装置向正反应方向进行, ,Ⅲ装置向逆反应方向进行,
,因此两者的平衡常数不同,故错误;B.Ⅱ是恒温恒容状态,Ⅲ是恒压状
态,反应向逆反应方向进行,反应中气体物质的量增大,则Ⅱ的压强大于Ⅲ,Ⅱ的化学反应速率大于
学科网(北京)股份有限公司 学科网(北京)股份有限公司Ⅲ,故错误;C.结合选项B可知,Ⅱ平衡等效与Ⅲ增压平衡右移,因此SO 的体积分数:Ⅱ>Ⅲ,故
3
正确;D.如果I是恒容恒温状态,和Ⅱ是等效平衡,SO 的转化率之和等于1,但I是绝热容器,正
2
反应是放热反应,SO 转化率降低,两者转化率之和小于1,故错误。选C。
2
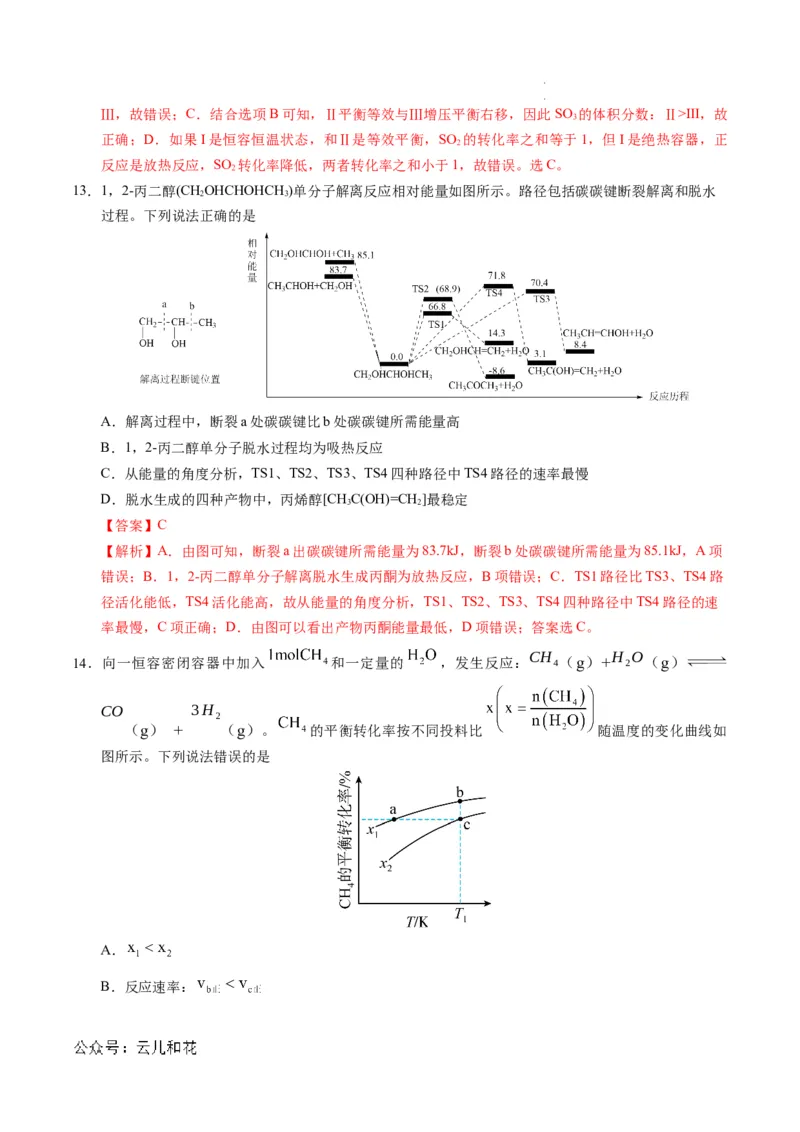
13.1,2-丙二醇(CHOHCHOHCH )单分子解离反应相对能量如图所示。路径包括碳碳键断裂解离和脱水
2 3
过程。下列说法正确的是
A.解离过程中,断裂a处碳碳键比b处碳碳键所需能量高
B.1,2-丙二醇单分子脱水过程均为吸热反应
C.从能量的角度分析,TS1、TS2、TS3、TS4四种路径中TS4路径的速率最慢
D.脱水生成的四种产物中,丙烯醇[CHC(OH)=CH ]最稳定
3 2
【答案】C
【解析】A.由图可知,断裂a出碳碳键所需能量为83.7kJ,断裂b处碳碳键所需能量为85.1kJ,A项
错误;B.1,2-丙二醇单分子解离脱水生成丙酮为放热反应,B项错误;C.TS1路径比TS3、TS4路
径活化能低,TS4活化能高,故从能量的角度分析,TS1、TS2、TS3、TS4四种路径中TS4路径的速
率最慢,C项正确;D.由图可以看出产物丙酮能量最低,D项错误;答案选C。
CH H O
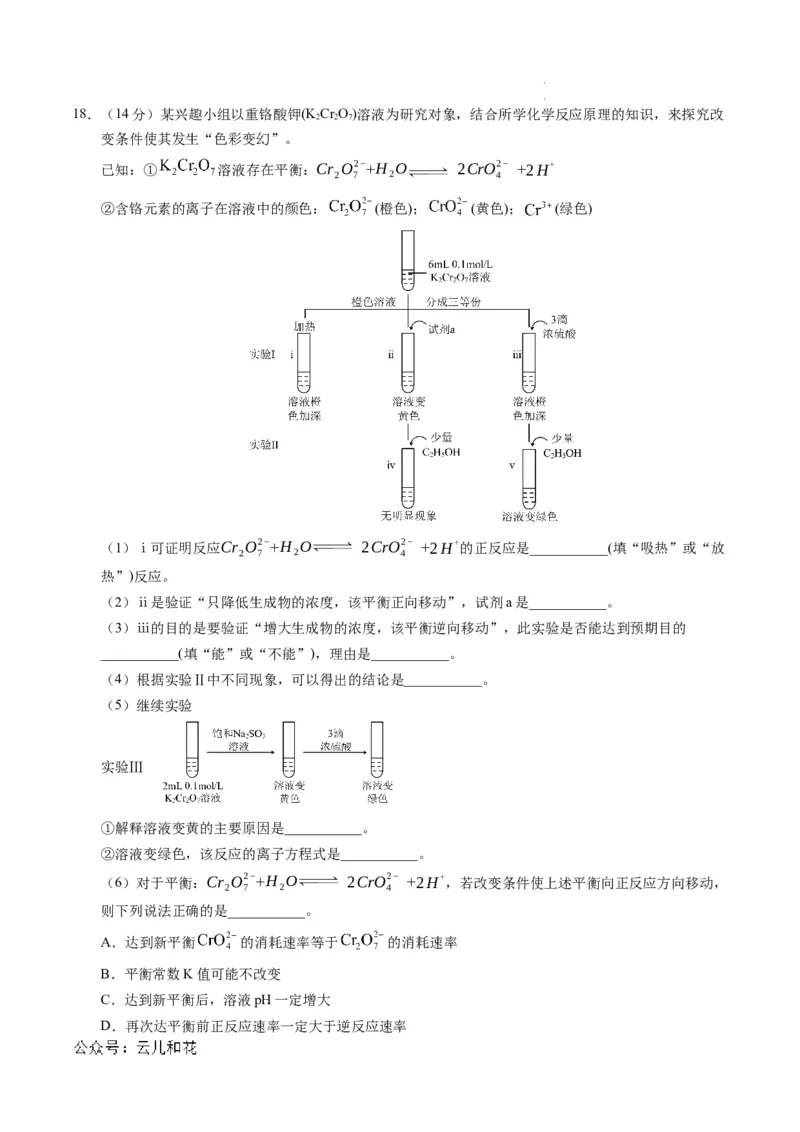
14.向一恒容密闭容器中加入 和一定量的 ,发生反应: 4 (g)+ 2 (g)
CO 3H
2
(g) + (g)。 的平衡转化率按不同投料比 随温度的变化曲线如
图所示。下列说法错误的是
A.
B.反应速率:
学科网(北京)股份有限公司 学科网(北京)股份有限公司C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
【答案】B
【解析】A.一定条件下,增大水的浓度,能提高CH 的转化率,即x值越小,CH 的转化率越大,则
4 4
,故A正确;B.b点和c点温度相同,CH 的起始物质的量都为1mol,b点x值小于c点,则
4
b点加水多,反应物浓度大,平衡正向移动,甲烷的转化率增大,生成物的浓度增大,则在相同温度
下反应速率: ,故B错误;C.由图像可知,x一定时,温度升高CH 的平衡转化率增大,
4
说明正反应为吸热反应,温度升高平衡正向移动,K增大;温度相同,K不变,则点a、b、c对应的
平衡常数: ,故C正确;D.该反应为气体分子数增大的反应,反应进行时压强发生改
变,所以温度一定时,当容器内压强不变时,反应达到平衡状态,故D正确;答案选B。
15.在一定条件下,取一定量的X和Y在恒容密闭容器中发生反应:aX(g)+ bY(g) cM
(g) + dN(g) ,达到平衡时,M的浓度与温度和容器容积的关系如图所
示。下列判断正确的是
A. B.
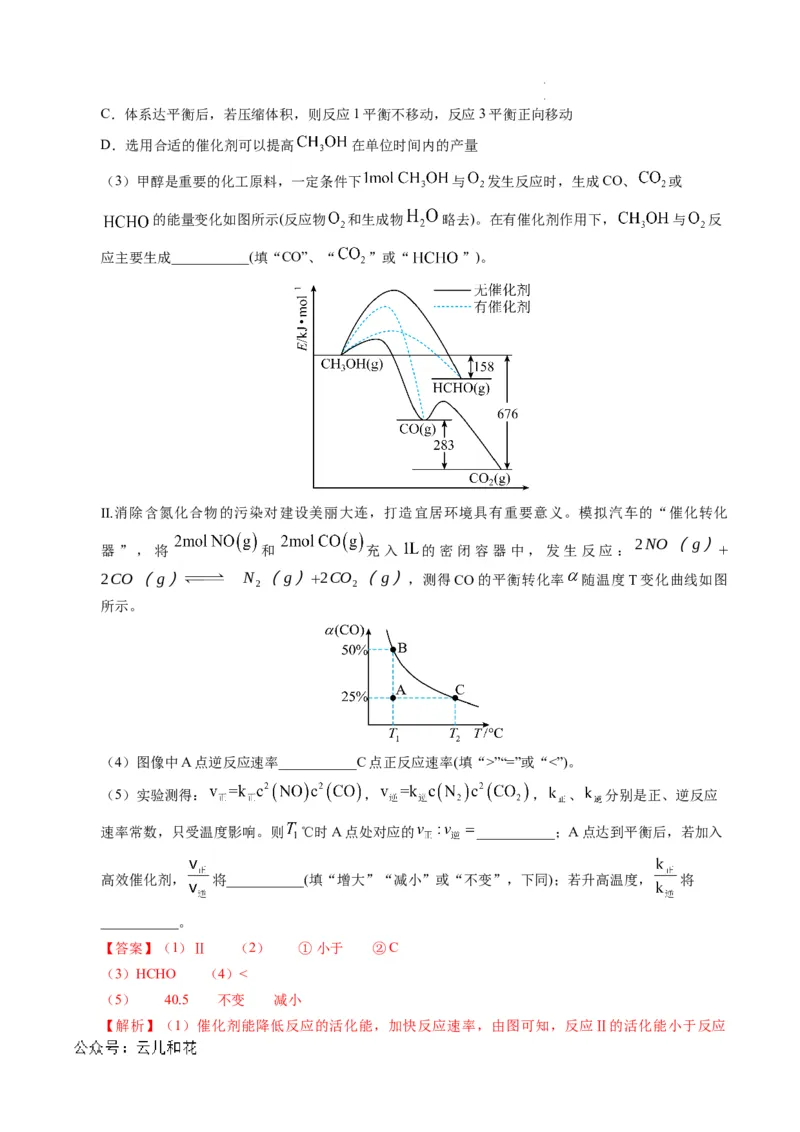
C.X的转化率:E点>F点 D.平衡常数:E点Fe2+,实验b中I—”“=”或“<”)。
(5)实验测得: , , 、 分别是正、逆反应
速率常数,只受温度影响。则 ℃时A点处对应的 ___________;A点达到平衡后,若加入
高效催化剂, 将___________(填“增大”“减小”或“不变”,下同);若升高温度, 将
___________。
.
【答案】(1)Ⅱ (2) ①小于 ②C
(3)HCHO (4)<
(5) 40.5 不变 减小
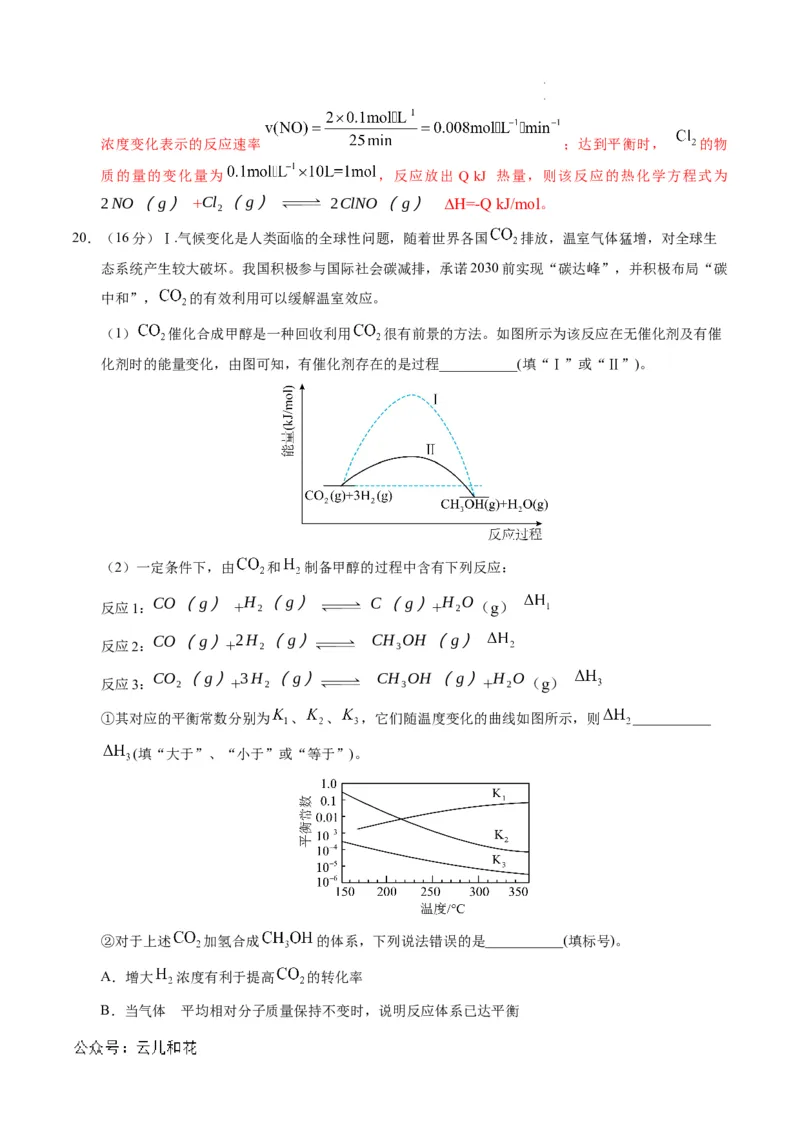
【解析】(1)催化剂能降低反应的活化能,加快反应速率,由图可知,反应Ⅱ的活化能小于反应
学科网(北京)股份有限公司 学科网(北京)股份有限公司Ⅰ,则有催化剂存在的是过程Ⅱ,故答案为:Ⅱ;
(2)①由盖斯定律可知,反应1+2得到反应3,则ΔH=ΔH+ΔH,由图可知,升高温度,平衡常数
3 1 2
K 增大,说明平衡向正反应方向移动,反应1的焓变ΔH>0,则ΔH<ΔH,故答案为:小于;
1 1 2 3
②A.增大反应物氢气浓度,平衡向正反应方向移动,二氧化碳的转化率增大,则增大氢气浓度有利
于提高二氧化碳的转化率,故正确;
B.由质量守恒定律可知,反应前后气体的质量相等,反应3为气体体积减小的反应,反应中平均相
对分子质量增大,则气体的平均相对分子质量保持不变说明正逆反应速率相等,反应已达到平衡,故
正确;
C.反应1为气体体积减小的反应,体系达平衡后,若压缩体积,气体压强增大,反应1平衡向正反
应方向移动,故错误;
D.选用合适的催化剂,可以降低反应的活化能,加快反应速率,提高甲醇在单位时间内的产量,故
正确;
故选C;
(3)选用合适的催化剂,可以降低反应的活化能,由图可知,在有催化剂作用下,甲醇与氧气反应
生成一氧化碳的活化能增大,生成甲醛的活化能减小,所以在有催化剂作用下,甲醇与氧气反应生成
甲醛,故答案为:HCHO;
(4)由图可知,A点T℃时反应未达到平衡,正反应速率大于逆反应速率,B点T℃时反应达到平
1 2
衡,正逆反应速率相等,升高温度,反应速率加快,所以A点逆反应速率小于C点正反应速率,故答
案为:<;
(5)由图可知,T℃反应达到平衡时,一氧化碳转化率为50%,则体积为1L的容器中一氧化氮、一
1
氧 化 碳 、 氮 气 、 二 氧 化 碳 的 浓 度 分 别 为 2mol/L—2mol/L×50%=1mol/L 、 2mol/L—2mol/
L×50%=1mol/L、2mol/L×50%× =0.5mol/L、2mol/L×50%=1mol/L,反应的平衡常数K= =0.5,
由反应达到平衡时正逆反应速率相等可得: = ,整理可得
= = K=0.5;A点反应未达到平衡,一氧化碳转化率为25%,容器中一氧化氮、
一氧化碳、氮气、二氧化碳的浓度分别为 2mol/L—2mol/L×25%=1.5mol/L、2mol/L—2mol/
L×25%=1.5mol/L、2mol/L×25%× =0.25mol/L、2mol/L×25%=0.5mol/L,则 A 点处对应的 =
=0.5× =40.5;A点达到平衡后,若加入高效催化剂,反应速率加快,
化学平衡不移动,正逆反应速率相等,则 不变;该反应为放热反应,升高温度,平衡向逆反应方
学科网(北京)股份有限公司 学科网(北京)股份有限公司向移动,平衡转化率减小,则 减小。
学科网(北京)股份有限公司 学科网(北京)股份有限公司