文档内容
2025-2026 学年高二化学上学期第一次月考卷 3.甲醇的用途非常广泛。科学家通过 合成甲醇的反应为:
。
(考试时间:75 分钟 试卷满分:100 分)
注意事项: 已知:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
若合成甲醇的反应中正反应的活化能为 ,逆反应的活化能为 ,则 一定等于
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。写在本试卷上无效。 A. B.
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
C. D.
4.测试范围:第 1 章~第 2 章第 2 节(人教版 2019 选择性必修 1)。
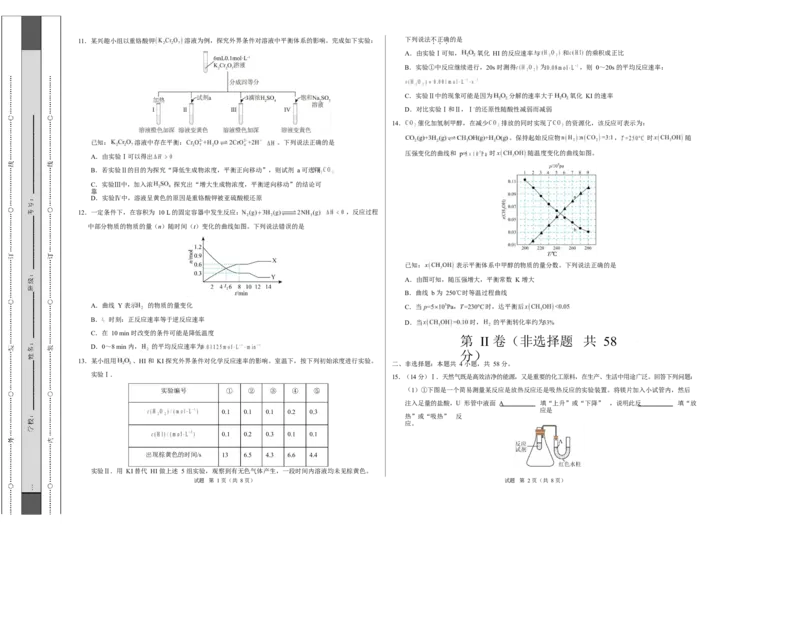
4.碳(C)与氧气反应的焓变如图所示,已知 键能为 akJ/mol, 键能为 bkJ/mol,则 中碳氧键
5.难度系数:0.65
键能(单位:kJ/mol)为
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.下列科技成果中蕴含的化学知识叙述正确的是
A.高效光解水催化剂能降低化学反应的焓变
B.二氧化碳作制冷剂与断裂碳氧键需要吸收热量有关 A. B. C. D.
C.运载火箭所采用的“液氢液氧”推进剂可把化学能全部转化为热能
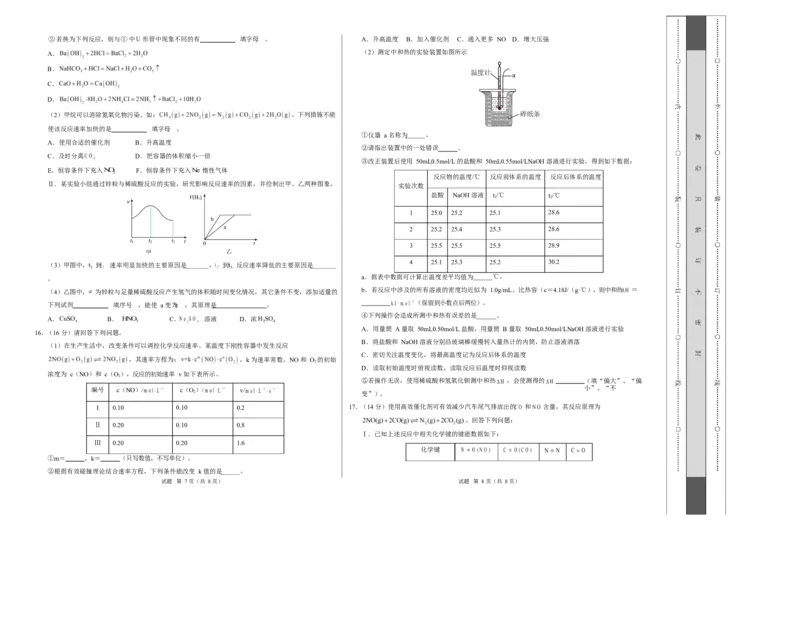
5.下列关于反应过程中能量变化的说法正确的是
D.小麦保存时常常采用低温冷冻技术,原因之一是温度低,腐烂速率会减慢
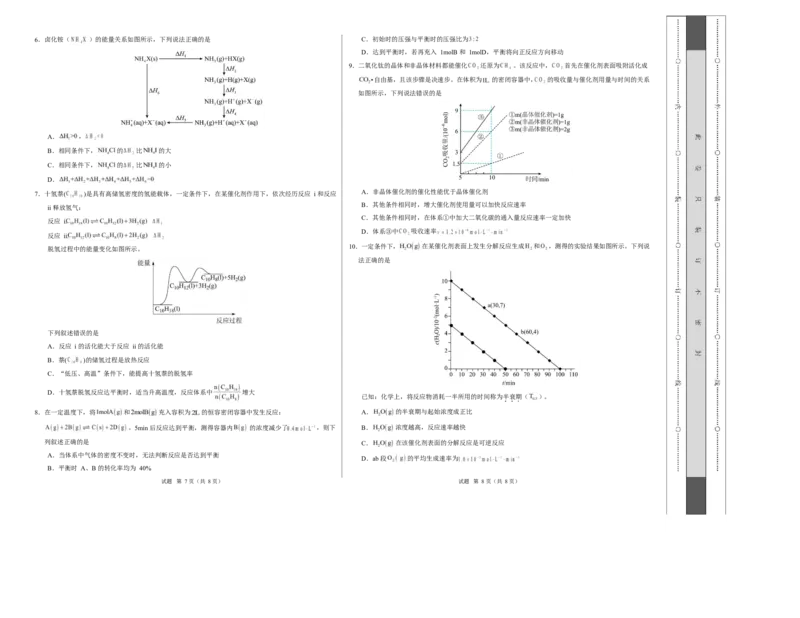
2.碰撞理论是我们理解化学反应速率的重要工具,下图为 HI 分解反应中分子碰撞示意图。
A.如图表示的反应为吸热反应
下面说法正确的是
B.能量变化如图所示,则
A.图 1 中分子取向合适,发生有效碰撞
C.化学反应过程中一定有化学键的变化,这是反应过程中能量变化的本质原因
B.活化分子具有的能量与反应物分子具有的能量之差,是反应的活化能
D.活化能越大代表化学反应需要吸收或放出的能量越大
C.用光辐照的方法,也可以增大活化分子数目,加快反应速率
D.由图知, 是基元反应
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)6.卤化铵( )的能量关系如图所示,下列说法正确的是 C.初始时的压强与平衡时的压强比为
D.达到平衡时,若再充入 1molB 和 1molD,平衡将向正反应方向移动
9.二氧化钛的晶体和非晶体材料都能催化 还原为 。该反应中, 首先在催化剂表面吸附活化成
自由基,且该步骤是决速步。在体积为 的密闭容器中, 的吸收量与催化剂用量与时间的关系
如图所示,下列说法错误的是
A. ,
B.相同条件下, 的 比 的大
C.相同条件下, 的 比 的小
D.
7.十氢萘( )是具有高储氢密度的氢能载体,一定条件下,在某催化剂作用下,依次经历反应 i 和反应
A.非晶体催化剂的催化性能优于晶体催化剂
B.其他条件相同时,增大催化剂使用量可以加快反应速率
ii 释放氢气:
C.其他条件相同时,在体系①中加大二氧化碳的通入量反应速率一定加快
反应 i.
D.体系③中 吸收速率
反应 ii.
10.一定条件下, 在某催化剂表面上发生分解反应生成 和 ,测得的实验结果如图所示。下列说
脱氢过程中的能量变化如图所示。
法正确的是
下列叙述错误的是
A.反应 i 的活化能大于反应 ii 的活化能
B.萘( )的储氢过程是放热反应
C.“低压、高温”条件下,能提高十氢萘的脱氢率
D.十氢萘脱氢反应达平衡时,适当升高温度,反应体系中 增大
已知:化学上,将反应物消耗一半所用的时间称为半衰期( )。
8.在一定温度下,将 和 充入容积为 的恒容密闭容器中发生反应: A. 的半衰期与起始浓度成正比
。5min 后反应达到平衡,测得容器内 的浓度减少了 ,则下 B. 浓度越高,反应速率越快
列叙述正确的是 C. 在该催化剂表面的分解反应是可逆反应
A.当体系中气体的密度不变时,无法判断反应是否达到平衡
D.ab 段 的平均生成速率为
B.平衡时 A、B 的转化率均为 40%
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)11.某兴趣小组以重铬酸钾 溶液为例,探究外界条件对溶液中平衡体系的影响。完成如下实验: 下列说法不正确的是
A.由实验Ⅰ可知, 氧化 HI 的反应速率与 和 的乘积成正比
B.实验①中反应继续进行,20s 时测得 为 ,则 0~20s 的平均反应速率:
C.实验Ⅱ中的现象可能是因为 分解的速率大于 氧化 KI 的速率
D.对比实验Ⅰ和Ⅱ,Ⅰ-的还原性随酸性减弱而减弱
14. 催化加氢制甲醇,在减少 排放的同时实现了 的资源化,该反应可表示为:
。保持起始反应物 , 时 随
已知: 溶液中存在平衡: 。下列说法正确的是
压强变化的曲线和 p= 时 随温度变化的曲线如图。
A.由实验Ⅰ可以得出
B.若实验Ⅱ的目的为探究“降低生成物浓度,平衡正向移动”,则试剂 a 可选用
C.实验Ⅲ中,加入浓 探究出“增大生成物浓度,平衡逆向移动”的结论可
靠
D.实验Ⅳ中,溶液呈黄色的原因是重铬酸钾被亚硫酸根还原
12.一定条件下,在容积为 10 L 的固定容器中发生反应: ,反应过程
中部分物质的物质的量(n)随时间(t)变化的曲线如图。下列说法错误的是
已知: 表示平衡体系中甲醇的物质的量分数。下列说法正确的是
A.由图可知,随压强增大,平衡常数 K 增大
B.曲线 b 为 250℃时等温过程曲线
A.曲线 Y 表示 的物质的量变化 C.当 时,达平衡后
B. 时刻:正反应速率等于逆反应速率
D.当 时, 的平衡转化率约为
C.在 10 min 时改变的条件可能是降低温度
第 II 卷(非选择题 共 58
D.0~8 min 内, 的平均反应速率为
分)
13.某小组用 、HI 和 KI 探究外界条件对化学反应速率的影响。室温下,按下列初始浓度进行实验。
二、非选择题:本题共 4 小题,共 58 分。
实验Ⅰ.
15.(14 分)Ⅰ.天然气既是高效洁净的能源,又是重要的化工原料,在生产、生活中用途广泛。回答下列问题:
实验编号 ① ② ③ ④ ⑤ (1)①下图是一个简易测量某反应是放热反应还是吸热反应的实验装置。将镁片加入小试管内,然后
注入足量的盐酸, 形管中液面 A 填“上升”或“下降” ,说明此反 填“放
应是
0.1 0.1 0.1 0.2 0.3
热”或“吸热” 反
应。
0.1 0.2 0.3 0.1 0.1
出现棕黄色的时间/s 13 6.5 4.3 6.6 4.4
实验Ⅱ.用 KI 替代 HI 做上述 5 组实验,观察到有无色气体产生,一段时间内溶液均未见棕黄色。
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)若换为下列反应,则与 中 形管中现象不同的有 填字母 。 A.升高温度 B.加入催化剂 C.通入更多 NO D.增大压强
A. (2)测定中和热的实验装置如图所示
B.
C.
D.
(2)甲烷可以消除氮氧化物污染。如: 。下列措施不能
使该反应速率加快的是 填字母 。
①仪器 a 名称为 。
A.使用合适的催化剂 B.升高温度
②请指出装置中的一处错误 。
C.及时分离 D.把容器的体积缩小一倍
③改正装置后使用 50mL0.5mol/L 的盐酸和 50mL0.55mol/LNaOH 溶液进行实验,得到如下数据:
E.恒容条件下充入 F.恒容条件下充入 惰性气体
反应物的温度/℃ 反应前体系的温度 反应后体系的温度
Ⅱ.某实验小组通过锌粒与稀硫酸反应的实验,研究影响反应速率的因素,并绘制出甲、乙两种图象。
实验次数
盐酸 NaOH 溶液 t/℃ t/℃
1 2
1 25.0 25.2 25.1 28.6
2 25.2 25.4 25.3 28.6
3 25.5 25.5 25.5 28.9
4 25.1 25.3 25.2 30.2
(3)甲图中, 到 速率明显加快的主要原因是 , 到 反应速率降低的主要原因是
。
a.据表中数据可计算出温度差平均值为 ℃。
(4)乙图中, 为锌粒与足量稀硫酸反应产生氢气的体积随时间变化情况,其它条件不变,添加适量的 b.若反应中涉及的所有溶液的密度均近似为 1.0g/mL、比热容(c=4.18J/(g·℃),则中和热 =
(保留到小数点后两位)。
下列试剂 填序号 ,能使 a 变为 ,其原理是 。
④下列操作会造成所测中和热有误差的是 。
A. B. C. 溶液 D.浓
A.用量筒 A 量取 50mL0.50mol/L 盐酸,用量筒 B 量取 50mL0.50mol/LNaOH 溶液进行实验
16.(16 分)请回答下列问题。
B.将盐酸和 NaOH 溶液分别沿玻璃棒缓慢转入量热计的内筒,防止溶液洒落
(1)在生产生活中,改变条件可以调控化学反应速率。某温度下刚性容器中发生反应
C.密切关注温度变化,将最高温度记为反应后体系的温度
,其速率方程为: ,k 为速率常数。NO 和 O 的初始
2
D.读取初始温度时俯视读数,读取反应后温度时仰视读数
浓度为 c(NO)和 c(O),反应的初始速率 v 如下表所示。
2
⑤若操作无误,使用稀硫酸和氢氧化钡测中和热 ,会使测得的 (填“偏大”、“偏
编号 c(NO)/ c(O)/ v/ 小”、“不
2 变”)。
I 0.10 0.10 0.2 17.(14 分)使用高效催化剂可有效减少汽车尾气排放出的 和 含量,其反应原理为
。回答下列问题:
Ⅱ 0.20 0.10 0.8
Ⅰ.已知上述反应中相关化学键的键能数据如下:
Ⅲ 0.20 0.20 1.6
化学键
①m= ,k= (只写数值,不写单位)。
②根据有效碰撞理论结合速率方程,下列条件能改变 k 值的是 。
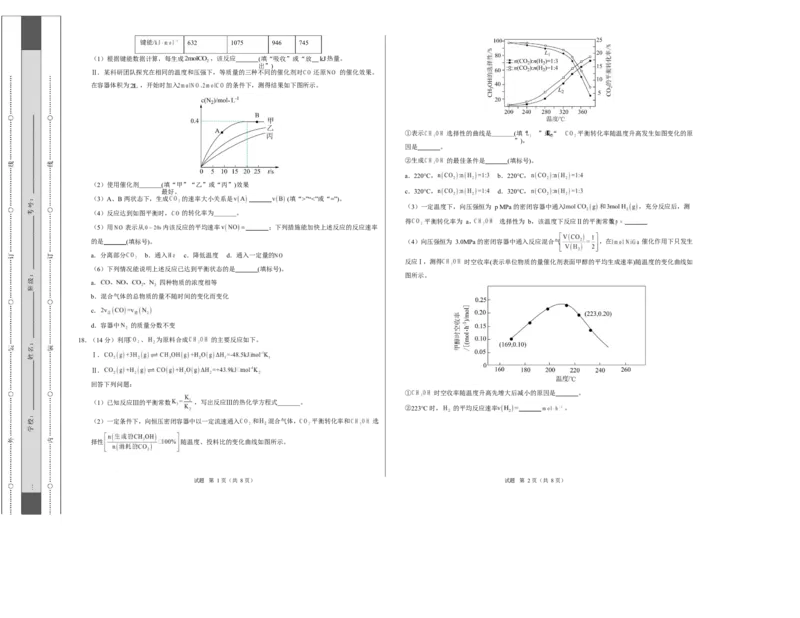
试题 第 7 页(共 8 页) 试题 第 8 页(共 8 页)键能/ 632 1075 946 745
(1)根据键能数据计算,每生成 ,该反应 (填“吸收”或“放 热量。
出”)
Ⅱ.某科研团队探究在相同的温度和压强下,等质量的三种不同的催化剂对 还原 的催化效果。
在容器体积为 ,开始时加入 的条件下,测得结果如下图所示。
①表示 选择性的曲线是 (填“ ”或“ 平衡转化率随温度升高发生如图变化的原
”),
因是 。
②生成 的最佳条件是 (填标号)。
a.220°C, b.220°C,
(2)使用催化剂 (填“甲”“乙”或“丙”)效果
最好。 c.320°C, d.320°C,
(3)A、B 两状态下,生成 的速率大小关系是 (填“>”“<”或“=”)。
(3)一定温度下,向压强恒为 p MPa 的密闭容器中通入 和 ,充分反应后,测
(4)反应达到如图平衡时, 的转化率为 。
得 平衡转化率为 a, 选择性为 b,该温度下反应Ⅱ的平衡常数
(5)用 表示从 内该反应的平均速率 ;下列措施能加快上述反应的反应速率
的是 (填标号)。 (4)向压强恒为 3.0MPa 的密闭容器中通入反应混合气 ,在 催化作用下只发生
a.分离部分 b.通入 c.降低温度 d.通入一定量的
反应Ⅰ,测得 时空收率(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度的变化曲线如
(6)下列情况能说明上述反应已达到平衡状态的是 (填标号)。
图所示。
a. 四种物质的浓度相等
b.混合气体的总物质的量不随时间的变化而变化
c.
d.容器中 的质量分数不变
18.(14 分)利用 、 为原料合成 的主要反应如下。
Ⅰ.
Ⅱ.
回答下列问题:
① 时空收率随温度升高先增大后减小的原因是 。
(1)已知反应Ⅲ的平衡常数 ,写出反应Ⅲ的热化学方程式 。
②223°C 时, 的平均反应速率 。
(2)一定条件下,向恒压密闭容器中以一定流速通入 和 混合气体, 平衡转化率和 选
择性 随温度、投料比的变化曲线如图所示。
试题 第 1 页(共 8 页) 试题 第 2 页(共 8 页)