文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【安徽版】
可能用到的相对原子质量:O—16、Ti—48、Ga—70、As—75
一、单项选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.下列颜色变化与氧化还原反应无关的是( )
A.将SO 通入滴有酚酞的NaOH溶液中,溶液红色褪去
2
B.将新制氯水滴入紫色石蕊溶液中,溶液先变红后褪色
C.久置的氯水,颜色逐渐变浅
D.久置的浓硝酸显黄色,通入空气后颜色变浅
2.化学与人类生活息息相关,正确预防、处理事故,可以大大减少生命危险和财产损失。下
列做法错误的是( )
A.煤气中毒后首先将中毒者移至通风处
B.报警器装在炉灶下方探测天然气泄漏
C.冬天取菜时先打开菜窖通风一段时间
D.火灾逃生时用湿毛巾捂住口鼻沿墙壁低姿势跑离
3.类比推理是化学中常用的思维方法,下列说法正确的是( )
A.S 是非极性分子,则O 是非极性分子
8 3
B.NH 有还原性,则PH 也有还原性
3 3
C.Na CO 易溶于水,则Li CO 也易溶于水
2 3 2 3
D.CH CH OH被足量酸性KMnO 溶液氧化为CH COOH,则HOCH CH OH被足量酸性
3 2 4 3 2 2
KMnO 溶液氧化为HOOCCOOH
4
4.抗抑郁药米那普伦中间体的合成路线如图所示。下列说法正确的是( )
A.化合物甲中最多有8个碳原子共平面
B.化合物乙不能发生消去反应
C.化合物丙转化为化合物丁发生了加成反应
D.化合物丁与苯乙酸互为同系物
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
5.化学反应中有颜色变化之美。下列相关离子方程式表示不正确的是( )
A.向Na S O 溶液中滴加稀硫酸出现黄色沉淀:S O2 2H SSO H O
2 2 3 2 3 2 2
B.向FeSO 溶液中加入H O 出现红褐色沉淀:2Fe2 H O 4OH 2Fe(OH)
4 2 2 2 2 3
C,向酸性KMnO 溶液中通入SO 后溶液紫色褪去:
4 2
2MnO 5SO 2H O 2Mn2 5SO2 4H
4 2 2 4
D.向HI溶液中加入H O 后溶液变为黄色:2I 2H H O I 2H O
2 2 2 2 2 2
6.X、Y、Z、R、M、Q为六种短周期元素,其原子半径和最外层电子数之 间的关系如图所
示,下列判断正确的是( )
A. Y的原子的轨道表示式为
B.MQ2的中心原子采取sp2杂化
3
C.R Q 中含有离子键和极性共价键
2 2
D.ZX 比YX 在水中的溶解度大的原因之一是ZX 与水之间能形成氢键
3 4 3
7.用如图所示的装置进行实验(夹持及尾气处理仪器略去),能达到实验目的的是( )
选项 a中试剂 b中试剂 c中试剂 实验目的 装置
A 浓盐酸 MnO 无 制取并收集Cl
2 2
B 浓氨水 碱石灰 浓硫酸 制备纯净的NH
3
C 稀硫酸 NaHCO 硅酸钠溶液 比较非金属性强弱:S>C>Si
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
D 浓硫酸 Cu 品红溶液 验证SO 具有漂白性
2
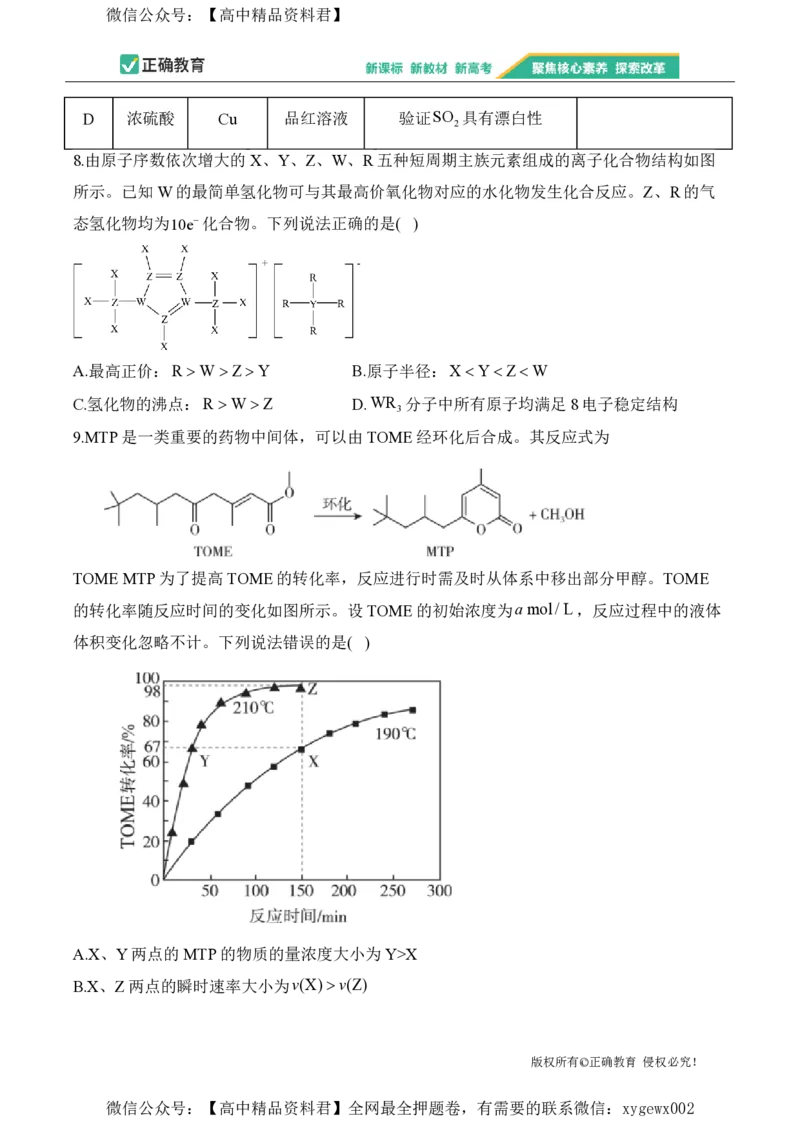
8.由原子序数依次增大的X、Y、Z、W、R五种短周期主族元素组成的离子化合物结构如图
所示。已知W的最简单氢化物可与其最高价氧化物对应的水化物发生化合反应。Z、R的气
态氢化物均为10e化合物。下列说法正确的是( )
A.最高正价:R W ZY B.原子半径:XYZW
C.氢化物的沸点:R W Z D.WR 分子中所有原子均满足8电子稳定结构
3
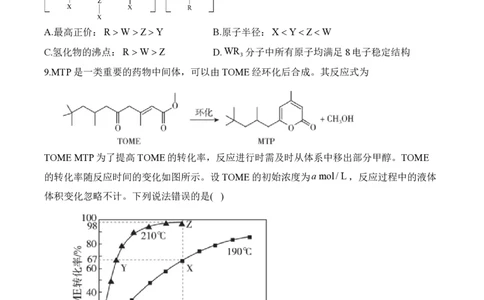
9.MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为
TOME MTP为了提高TOME的转化率,反应进行时需及时从体系中移出部分甲醇。TOME
的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体
体积变化忽略不计。下列说法错误的是( )
A.X、Y两点的MTP的物质的量浓度大小为Y>X
B.X、Z两点的瞬时速率大小为v(X)v(Z)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
0.98a0.98a
C.若Z点处于化学平衡状态,则210 ℃时反应的平衡常数K
0.02a
0.67a
D.190 ℃时,0~150 min MTP的平均反应速率为 mol(Lmin)
150
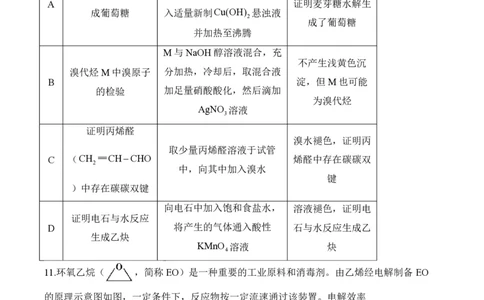
10.下列实验方案设计、现象和结论都正确的是( )
目的 实验方案设计 现象和结论
在麦芽糖溶液中加入麦芽糖
产生砖红色沉淀,
证明麦芽糖水解生 酶,反应一段时间后,再加
A 证明麦芽糖水解生
成葡萄糖 入适量新制Cu(OH) 悬浊液
2
成了葡萄糖
并加热至沸腾
M与 NaOH醇溶液混合,充
不产生浅黄色沉
溴代烃 M中溴原子 分加热,冷却后,取混合液
B 淀,但M也可能
的检验 加足量硝酸酸化,然后滴加
为溴代烃
AgNO 溶液
3
证明丙烯醛
溴水褪色,证明丙
取少量丙烯醛溶液于试管
C (CH CHCHO 烯醛中存在碳碳双
2
中,向其中加入溴水
键
)中存在碳碳双键
向电石中加入饱和食盐水, 溶液褪色,证明电
证明电石与水反应
D 将产生的气体通入酸性 石与水反应生成乙
生成乙炔
KMnO 溶液 炔
4
11.环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO
的原理示意图如图,一定条件下,反应物按一定流速通过该装置。电解效率
n(生成 B 所用的电子)
(B) 100%。下列说法不正确的是( )
n(通过电极的电子)
A.电极B为阴极,应与电源负极相连
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
B.溶液 a为KCl和KOH的混合溶液
C.若(EO)100%,则溶液 b的溶质为KCl
D.电极A的电极反应式:CH CH 2e Cl H OHOCH CH ClH
2 2 2 2 2
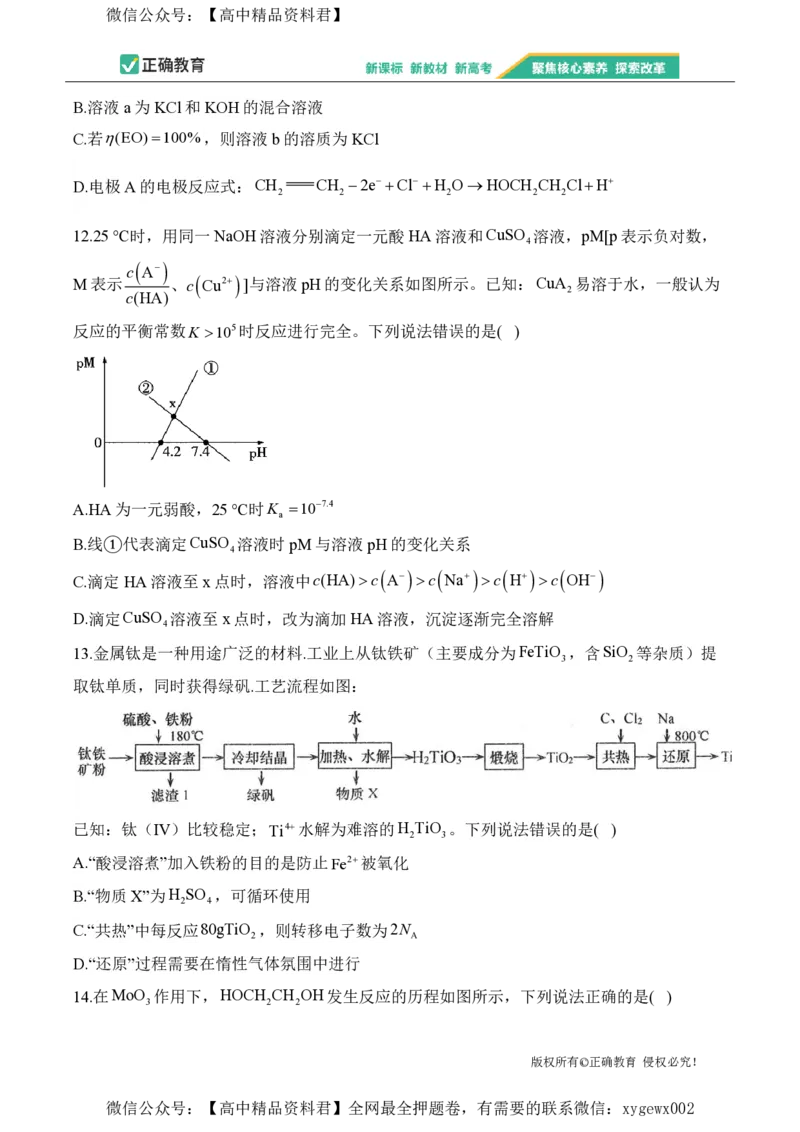
12.25 ℃时,用同一 NaOH溶液分别滴定一元酸HA溶液和CuSO 溶液,pM[p表示负对数,
4
c
A
M表示 、c Cu2 ]与溶液pH的变化关系如图所示。已知:CuA 易溶于水,一般认为
2
c(HA)
反应的平衡常数K 105时反应进行完全。下列说法错误的是( )
A.HA为一元弱酸,25 ℃时K 107.4
a
B.线①代表滴定CuSO 溶液时 pM与溶液pH的变化关系
4
C.滴定 HA溶液至x点时,溶液中c(HA)c
A
c
Na
c
H
c
OH
D.滴定CuSO 溶液至 x点时,改为滴加HA溶液,沉淀逐渐完全溶解
4
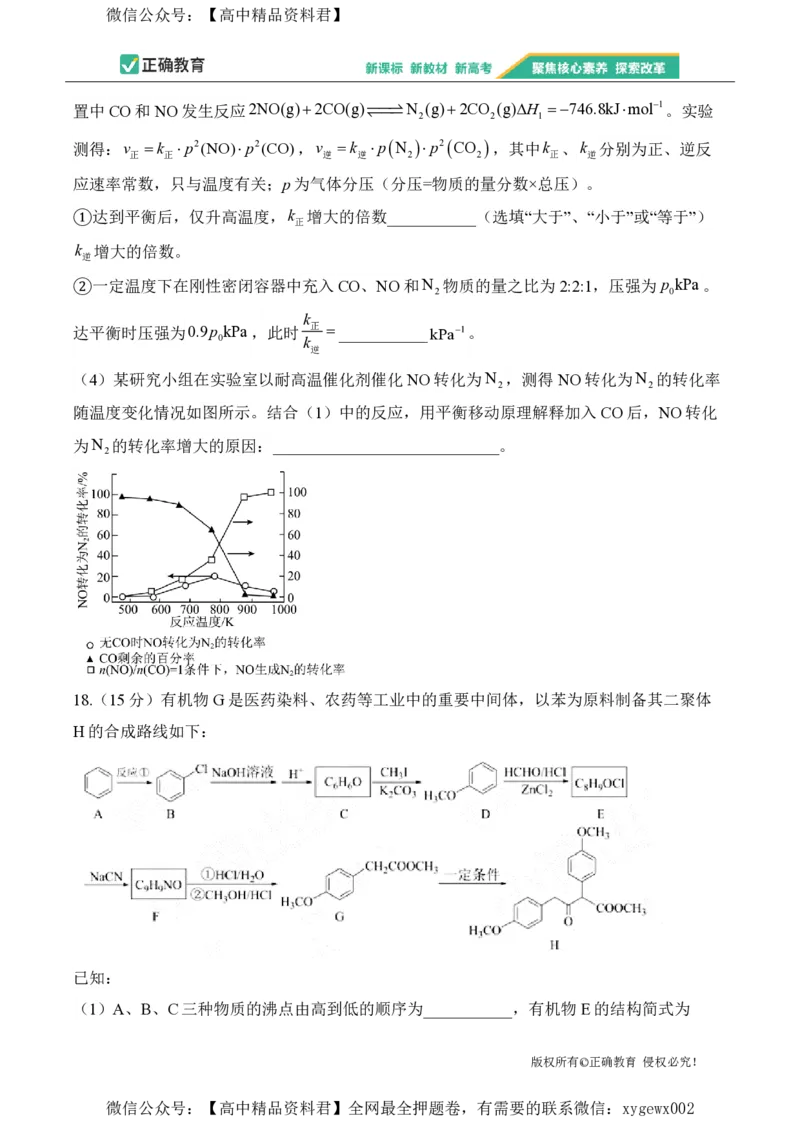
13.金属钛是一种用途广泛的材料.工业上从钛铁矿(主要成分为FeTiO ,含SiO 等杂质)提
3 2
取钛单质,同时获得绿矾.工艺流程如图:
已知:钛(Ⅳ)比较稳定;Ti4水解为难溶的H TiO 。下列说法错误的是( )
2 3
A.“酸浸溶煮”加入铁粉的目的是防止Fe2被氧化
B.“物质 X”为H SO ,可循环使用
2 4
C.“共热”中每反应80gTiO ,则转移电子数为2N
2 A
D.“还原”过程需要在惰性气体氛围中进行
14.在MoO 作用下,HOCH CH OH发生反应的历程如图所示,下列说法正确的是( )
3 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.MoO 能提高HOCH CH OH的平衡转化率
3 2 2
B.该反应历程中C-C、C-H键均发生断裂
C.HOCH CH OH滴入过量酸性高锰酸钾溶液中生成CO
2 2 2
D.若将原料换为HOCHCH CH(OH)CH ,则生成物为乙醛和丙烯
3 3
二、非选择题:共 58 分
15.(14分)钛是一种稀有金属,钛及钛系化合物作为精细化工产品,有着很高的附加价值,
前景十分广阔。某中学对此开展了相应的研究性学习。
Ⅰ.甲小组同学以TiO 、TiCl 、H 为原料,用如下装置制备Ti O 。
2 4 2 2 3
B为直形管式电阻炉,880℃时,该装置内先后发生以下反应:
①3TiO TiCl 2H 2Ti O 4HCl②2TiCl H 2TiCl 2HCl
2 4 2 2 3 4 2 3
已知:①TiCl 易挥发,高温时能与O 反应,不与HCl反应,易水解,能溶于有机溶剂。
4 2
②TiO 、Ti O 熔沸点较高,在反应装置内为固态。
2 2 3
(1)C装置的作用是____________,D装置中浓硫酸的作用是____________。
(2)TiCl 过多,易引发副反应②,可通过调节____________控制TiCl 通入量。
4 4
Ⅱ.乙小组同学利用如下装置在实验室制备TiCl (夹持装置略去)。
4
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(3)装置C中除生成TiCl 外,还生成一种气态不成盐氧化物,该反应的化学方程式为
4
____________。
(4)制得的TiCl 中常含有少量CCl ,已知TiCl 与CCl 分子结构相似。TiCl 属于
4 4 4 4 4
____________分子(“极性”或者“非极性”),通过减压蒸馏提纯,先馏出的物质为
____________。
(5)利用如图装置测定所得TiCl 的纯度:取1.0g产品加入烧瓶,向安全漏斗中加入适量蒸
4
馏水,待TiCl 充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴
4
0.10molL1K CrO 溶液作指示剂,用0.5000molL1AgNO 标准溶液滴定至终点,消耗标准
2 4 3
溶液40.00mL。
已知:常温下,K (AgCl)1.81010、K Ag CrO 1.11012,Ag CrO 呈砖红色,
sp sp 2 4 2 4
TiCl 2nH O TiO nH O4HCl。
4 2 2 2
①滴定终点的判断方法是____________;
②产品的纯度为____________%(保留一位小数)。
16.(14分)2023年7月3日,商务部与海关总署发布公告,宣布对镓、锗相关物项实施出口
管制。金属镓被称为“电子工业脊梁”,氮化镓是5G技术中广泛应用的新型半导体材料。利用
粉煤灰(主要成分为Ga O、Al O、SiO 还有少量Fe O 等杂质)制备镓和氮化镓的流程如
2 3 2 3 2 2 3
下:
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:①镓与铝同族,其化合物性质相似。
②“碱浸”后溶液的主要成分为NaGa(OH) 、NaAl(OH) 、Na SiO 。
4 4 2 3
③常温下,相关元素可溶性组分的物质的量浓度的对数与pH的关系如下图所示,当溶液中
可溶性组分浓度c105mol/L时,可认为已除尽。
回答下列问题:
(1)基态Ga原子的核外电子排布式为______,Br在元素周期表中的位置为______。
(2)已知“焙烧”后铝、镓、硅元素均转化为可溶性钠盐,写出Ga O 所发生反应的化学方程
2 3
式为______。
(3)“沉淀”步骤中加入过量稀硫酸至生成的沉淀不再溶解,则滤渣 2的主要成分是______
(写化学式)。
(4)步骤①和②中通入过量气体A发生反应的离子方程式为______。
(5)常温下,反应Al(OH) (aq)Al(OH) (s)OH(aq)的平衡常数K ______。
4 3
(6)以纯镓为原料可制得另一种半导体材料GaAs,其晶体结构如下图所示,已知晶胞密度
为g/cm3,阿伏加德罗常数值为N ,晶胞边长a为______pm(列出计算式即可)。
A
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
17.(15分)研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。回答下列
问题:
(1)己知:2NO(g)O (g)2NO (g)H 114kJmol1;
2 2 1
C(s)O (g)CO (g)H 393.5kJmol1;
2 2 2
2NO(g)N (g)O (g)H 181kJmol1
2 2 3
C(s)与NO (g)反应生成N (g)和CO (g)的热化学方程式为___________。
2 2 2
(2)NO 的排放主要来自于汽车尾气,包含NO 和NO,有人提出用活性炭对NO 进行吸
x 2 x
收。对于反应:C(s)2NO(g)N (g)CO (g)H 34.0kJmol1,T℃时,借助传感器
2 2 1
测得反应在不同时间点上各物质的浓度如下:
0 10 20 30 40 50
NO 1.00 0.58 0.40 0.40 0.48 0.48
N 0 0.21 0.30 0.30 0.36 0.36
2
①0~10min内,NO的平均反应速率vNO___________,当升高反应温度,该反应的平衡
常数K___________(选填“增大”“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能
是___________(填字母)。
A.加入一定量的活性炭 B.通入一定量的NO
C.适当缩小容器的体积 D.加入合适的催化剂
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
置中CO和NO发生反应2NO(g)2CO(g)N (g)2CO (g)H 746.8kJmol1。实验
2 2 1
测得:v k p2(NO) p2(CO),v k pN p2CO ,其中k 、k 分别为正、逆反
正 正 逆 逆 2 2 正 逆
应速率常数,只与温度有关;p为气体分压(分压=物质的量分数×总压)。
①达到平衡后,仅升高温度,k 增大的倍数___________(选填“大于”、“小于”或“等于”)
正
k 增大的倍数。
逆
②一定温度下在刚性密闭容器中充入 CO、NO和N 物质的量之比为2:2:1,压强为 p kPa。
2 0
k
达平衡时压强为0.9p kPa,此时 正 ___________kPa1。
0 k
逆
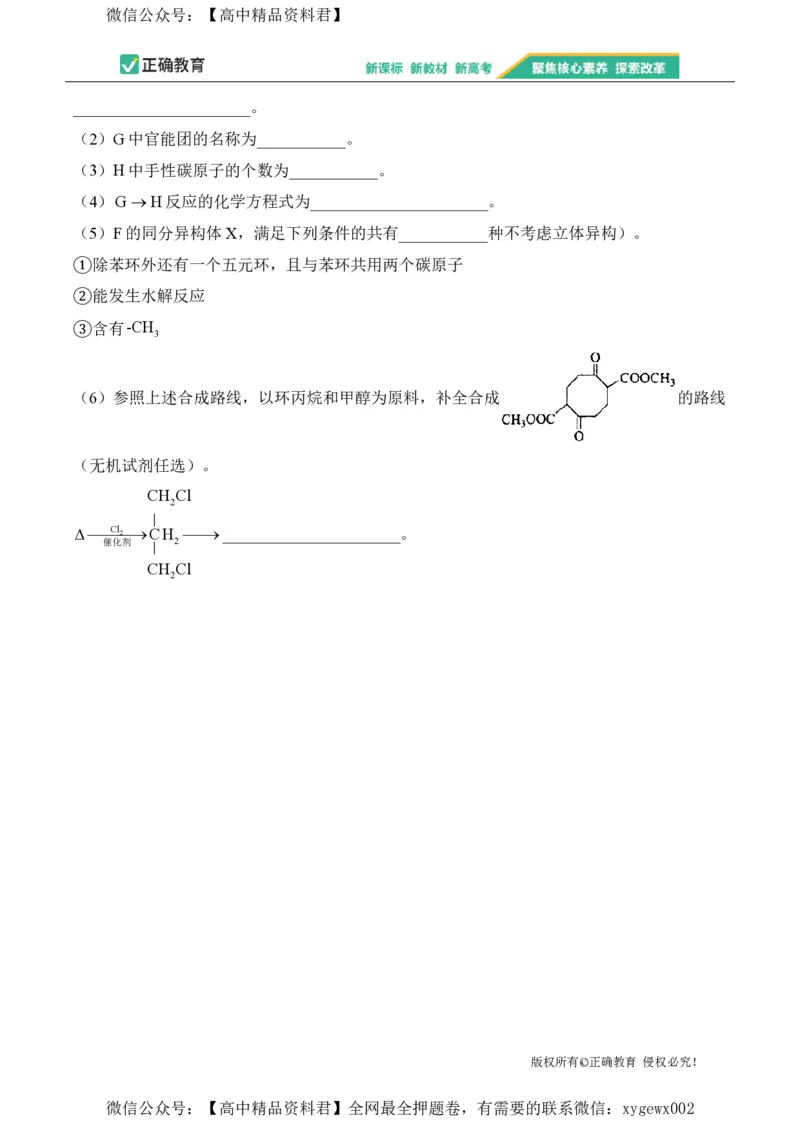
(4)某研究小组在实验室以耐高温催化剂催化NO转化为N ,测得NO转化为N 的转化率
2 2
随温度变化情况如图所示。结合(1)中的反应,用平衡移动原理解释加入CO后,NO转化
为N 的转化率增大的原因:____________________________。
2
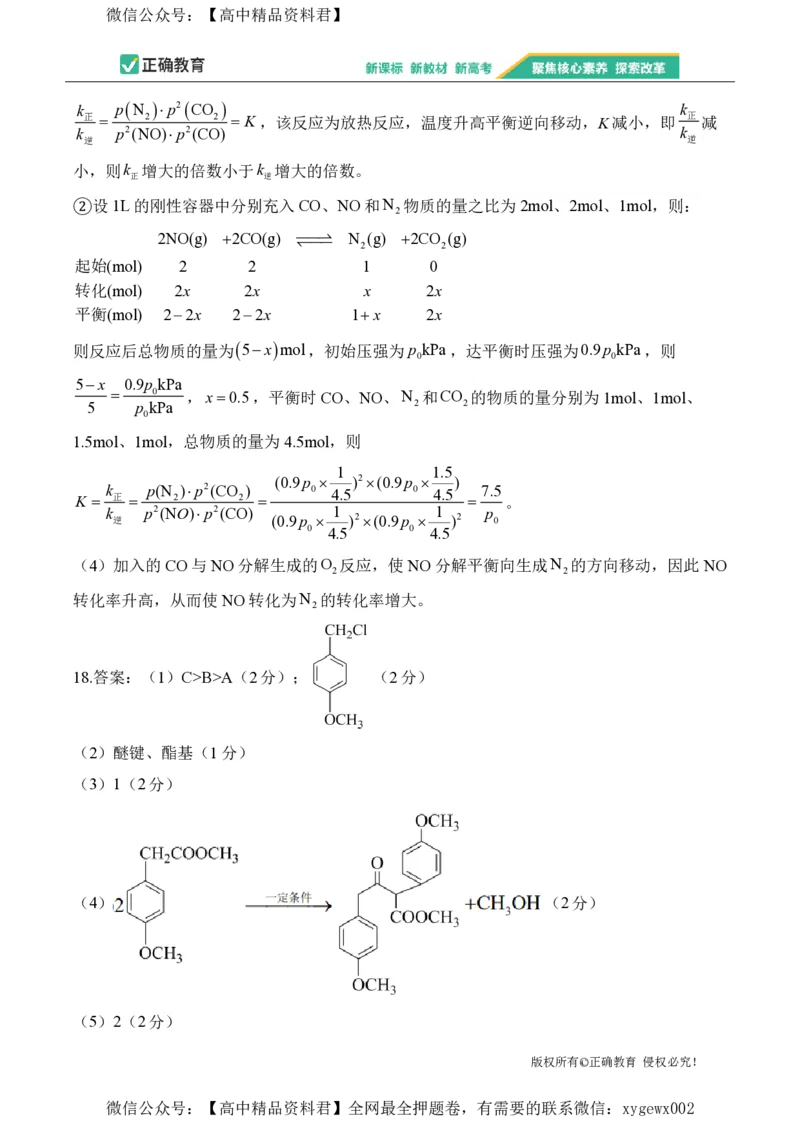
18.(15分)有机物G是医药染料、农药等工业中的重要中间体,以苯为原料制备其二聚体
H的合成路线如下:
已知:
(1)A、B、C三种物质的沸点由高到低的顺序为___________,有机物E的结构简式为
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
______________________。
(2)G中官能团的名称为___________。
(3)H中手性碳原子的个数为___________。
(4)GH反应的化学方程式为______________________。
(5)F的同分异构体 X,满足下列条件的共有___________种不考虑立体异构)。
①除苯环外还有一个五元环,且与苯环共用两个碳原子
②能发生水解反应
③含有-CH
3
(6)参照上述合成路线,以环丙烷和甲醇为原料,补全合成 的路线
(无机试剂任选)。
CH Cl
2
|
Cl 2CH ______________________。
催化剂 | 2
CH Cl
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:A
解析:A.将SO 通入滴有酚酞的NaOH溶液中,二者反应产生Na SO 和H O,使溶液中
2 2 3 2
NaOH浓度降低,溶液碱性减弱,因此溶液红色褪去,与氧化还原反应无关,A正确;
B.将新制氯水滴入紫色石蕊溶液中,Cl 与H O反应产生HCl、HClO,酸使紫色石蕊溶液变
2 2
红色,由于溶液中含有HClO,该物质具有强氧化性,会将红色物质氧化变为无色,因此后
来看到溶液的红色又褪色,与氧化还原反应有关,B不符合题意;
C.Cl 溶于水,反应产生HCl、HClO,该反应是可逆反应,反应产生的 HClO不稳定,受热
2
分解产生HCl、O ,导致氯气与水反应的可逆反应正向移动,最终完全转化为稀盐酸,故久
2
置的氯水,颜色逐渐变浅,与氧化还原反应有关,C不符合题意;
D.浓硝酸不稳定,光照分解产生的NO 溶解在硝酸中,使硝酸溶液显黄色。当向其中通入空
2
气后会发生反应:4NO O 2H O 4HNO ,cNO 减小,因此溶液变浅,溶液颜色变
2 2 2 3 2
化与氧化还原反应有关,D不符合题意;
故选A。
2.答案:B
解析:A、煤气中毒后首先将中毒者移至通风处,让其呼吸新鲜的空气,故A正确;B、天然
气的密度比空气小,所以报警器装在炉灶上方探测天然气泄漏,故B错误;C、菜窖中二氧
化碳的浓度可能较高,而二氧化碳不能供给呼吸,为防止人发生窒息,所以冬天取菜时先打
开菜窖通风一段时间,故C正确;D、湿毛巾有类似防毒面具作用,用湿毛巾捂住口鼻能防
止吸入燃烧时生成的烟尘;气体受热密度变小,有毒气体上升聚集在高处,故要尽量贴近地
面逃离,故D正确。故选B。
3.答案:B
解析:O 是由极性键构成的极性分子,A错误;NH 中N为3价,PH 中P为3价,最低
3 3 3
价表现还原性,B正确;Li与Mg处于对角线,化合物性质相似,MgCO 难溶于水,Li CO
3 2 3
微溶于水,C错误;乙二醇被氧化为乙二酸,乙二酸可以被酸性高锰酸钾氧化为CO ,D错
2
误。
4.答案:A
解析:单键可旋转,故化合物甲中最多有8个碳原子共平面,A正确;化合物乙中与羟基相
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
连的碳原子的邻位碳原子上有氢原子,可以发生消去反应,B错误;化合物丙转化为化合物
丁断开的是环,而不是双键或三键,不属于加成反应,C错误;化合物丁与苯乙酸虽然均含
羧基,但丁中还含有环和Br原子,二者不互为同系物,D错误。
5.答案:B
解析:B.H O 具有较强氧化性,FeSO 溶液中加入H O 产生沉淀的离子方程式为
2 2 4 2 2
2Fe2 H O 4H O 3Fe(OH) 4H,故B错误。
2 2 2 3
6.答案:D
解析:X、Y、Z、R、MQ为六种短周期元素,X、R元素原子核外最外层电子数为1,为第
ⅠA族元素;Y元素原子核外最外层电子数为4,为第ⅣA族元素;Z元素原子核外最外层电
子数为5,为第ⅤA族元素;M、Q元素原子核外最外层电子数为6,为第ⅥA族元素。由于
原子半径:M>Q,故M为S,Q为O,R的原子半径比核外最外层电子数为2的两种元素原
子的半径大,故R为Na,X的原子半径最小,则X为H,由于原子半径:Y>S>Z>O,故Z
为N,Y为Si。Si原子的轨道表示式为 ,A项错
6223
误;SO2-中 S原子的价层电子对数3 4,采取sp3杂化,B项错误;Na O 中含有
3 2 2 2
离子键和非极性共价键,C项错误;NH 在水中溶解度大的原因之一是NH 与水之间能形成
3 3
氢键,D项正确。
7.答案:C
解析:A.浓盐酸与MnO 在常温下不发生反应,不能制得氯气,A不正确;
2
B.NH 显碱性,而浓硫酸显酸性,所以不能用浓硫酸干燥NH ,B不正确;
3 3
C.浓硫酸滴入NaHCO 固体中,发生反应生成CO 气体,二氧化碳溶于水生成的碳酸能与硅
3 2
酸钠反应,生成硅酸等,从而得出酸性:H SO H CO H SiO ,单质的非金属性:
2 4 2 3 2 3
S>C>Si,C正确;
D.Cu与浓硫酸常温下不能发生反应,D不正确;
故选C。
8.答案:D
解析:A.F元素非金属性强,没有最高正价,故A错误;
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
C.HF分子间、NH 分子间均存在氢键,导致二者沸点较高,但C、B的氢化物种类多,有的
3
是固体,如聚乙烯的沸点较高,则不能进行比较,故C错误;
D.NF 分子中含有NF键,N原子还含有1对孤电子对,则NF 分子中所有原子均满足8电
3 3
子稳定结构,故D正确;
故选:D。
9.答案:C
解析:A.由题图可知,X、Y两点反应物的转化率相等,则 MTP的物质的量浓度相等,故A
错误;
B.由题图可知,X点曲线斜率大于Z点,则X、Z两点的瞬时速率大小为v(X)v(Z),故B
正确;
C.由题意可知,反应过程中甲醇不断从体系中移走,若Z点处于化学平衡状态,则210 ℃时
0.98a0.98a
甲醇的浓度不等于0.98amol/L,则反应的平衡常数K ,故C错误;
0.02a
D.190 ℃时,0~150 min MTP的浓度增加了0.67a mol/L,则其平均反应速率为
0.67a
mol/(Lmin),故D正确;
150
故选AC。
10.答案:B
解析:麦芽糖为还原性糖,本身会与新制氢氧化铜反应,A项错误;溴代烃不一定能与
NaOH醇溶液发生消去反应,B项正确;丙稀醛中的醛基可使溴水褪色,故不能证明是否存
在碳碳双键,C项错误;电石与水反应除了生成乙炔,还有H S、PH 等杂质,需要先除杂,
2 3
再通入酸性高锰酸钾溶液,D项错误。
11.答案:D
解析:分析图示可知,电极A上Cl Cl ,发生氧化反应,为阳极,则电极 B为阴极,应
2
与电源负极相连,A项正确;阴极的电极反应式为2H O2e 2OH H ,阳极Cl放
2 2
电后,K通过阳离子膜进入阴极区,生成KOH,故得到的溶液a为KCl和KOH的混合溶
液,B项正确;若(EO)100%,则说明在阳极区最终只有碳元素的化合价发生变化,其他
元素化合价没有变化,故所得溶液b的溶质为KCl,C项正确;电极A为阳极,其电极反应
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
式为2Cl 2e Cl ,生成的Cl 与水反应生成HClO,HClO再发生反应
2 2
HClOCH CH HOCH CH Cl,D项错误。
2 2 2 2
12.答案:D
解析:根据NaOH溶液与 HA溶液、CuSO 溶液的反应可知,随着 NaOH溶液的滴加,pH增
4
大,c
Cu2
逐渐减小,lgc
Cu2
变大,所以线①代表滴定CuSO 溶液时pM与溶液pH
4
的变化关系,线②代表滴定一元酸 HA溶液时pM与pH的变化关系,从线②与横坐标轴的
c
H
c
A
交点可知c A /c(HA)1时,c H 107.4 molL1,K c H 107.4,A
a
c(HA)
正确、B正确;x点溶液呈酸性,则c
H
c
OH
,根据电荷守恒得
c
H
c
Na
c
OH
c
A
,所以c
A
c
Na
c
H
c
OH
,再根据x点的
pM>0,即c
A
c(HA),可得c(HA)c
A
c
Na
c
H
c
OH
,C正确;若发生
反应Cu(OH) (s)2HA(aq) Cu2(aq)2A(aq)2H O(l),则该反应的
2 2
c Cu2 c2 A K Cu(OH) K2
K sp 2 a ,根据线①与横坐标轴的交点可知pM=0,即
c2(HA) K2
W
c Cu2 1.0 molL1时,c OH
1014
molL1 109.8 molL1,所以
104.2
K Cu(OH) 1019.6,K 1019.6 107.42 / 10142 106.4 105,故沉淀不能完全溶解,D错
sp 2
误。
13.答案:C
解析:C.“共热”二氧化钛与碳、氯气共热得到四氯化钛和一氧化碳,反应的化学方程式为:
加热
TiO 2C2Cl TiCl 2CO,每反应80gTiO ,其物质的量为1mol,则转移电子数为
2 2 4 2
4N ,故C错误。
A
14.答案:C
解析:从该反应历程图可以看出反应物为乙二醇,催化剂为MoO ,生成物为水、乙烯、甲
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
醛, 为反应的中间体。
A.催化剂不能提高反应物的平衡转化率,A错误;
B.该过程中没有CH键断裂,B错误;
C.HOCH CH OH滴入过量酸性高锰酸钾溶液,生成的乙二酸会被过量酸性高锰酸钾氧化成
2 2
CO ,C正确;
2
D.由图中反应③可知,连接两个醇羟基的碳原子之间CC键断裂分别生成甲醛,由反应①
② ④ 可知相邻的两个醇羟基生成水分子的同时还生成碳碳双键,如果原料为
HOOHCH CH(OH)CH ,则生成的有机物为乙醛和2一丁烯,D错误。
3 3
15.答案:(1)收集冷凝的四氯化钛并防止倒吸(1分);防止空气中氧气、水进入装置(1
分)
(2)A中水浴的温度(2分)
△
(3)TiO 2C2Cl TiCl 2CO(2分)
2 2 4
(4)非极性(2分);CCl (2分)
4
(5)①当加入最后半滴AgNO 标准溶液时,溶液恰好出现砖红色沉淀,且半分钟不消失
3
(2分)
②95.0%(2分)
解析:(1)TiCl 在C装置中被液化从而使气压变小,起到安全瓶的作用,故C装置的作用
4
是收集冷凝的四氯化钛并防止倒吸;浓硫酸具有吸水性,D装置中浓硫酸的作用是防止空气
中水进入装置BC中,干扰实验的进行;
(2)TiCl 与H 的比例过大,容易引发副反应②,可通过调节装置A中水浴的温度,控制
4 2
TiCl 的气化量,达到调整TiCl 的通入量;
4 4
(3)根据元素守恒可知一种气态不成盐氧化物为CO,则该反应的化学方程式为
△
TiO 2C2Cl TiCl 2CO;
2 2 4
(4)根据TiCl 与CCl 分子结构相似,则都是正四面体结构,所以TiCl 属于非极性分子;
4 4 4
CCl 的相对分子量小,则熔沸点比TiCl 低,所以CCl 先蒸馏出来。
4 4 4
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
16.答案:(1)[Ar]3d104s24p1(2分);第四周期,ⅦA族(2分)
焙烧
(2)Ga O Na CO 2NaGaO CO (2分)
2 3 2 3 2 2
(3)H SiO (2分)
2 3
(4)Ga(OH) CO Ga(OH) HCO(2分)
4 2 3 3
(5)100.8(2分)
3 580
(6) 1010(2分)
N
A
解析:(1)基态Ga原子的核外电子排布式为[Ar]3d104s24p1;Br在元素周期表中的位置为第
四周期,ⅦA族;
(2)“焙烧”后镓元素均转化为可溶性钠盐NaGaO ,则反应方程式为
2
焙烧
Ga O Na CO 2NaGaO CO ;
2 3 2 3 2 2
(3)依据上述分析,滤渣2为H SiO ;
2 3
(4)步骤①和②中通入过量气体A生成Ga(OH) 沉淀和NaHCO 发生反应的离子方程式为
3 3
Ga(OH) CO Ga(OH) HCO。
4 2 3 3
c(OH)
(5)反应Al(OH) 4 (aq) Al(OH) 3 (s)OH(aq)的平衡常数K c Al(OH) ,当
4
K 1014
pH=9.8时,c(OH) w 104.2mol/L,c Al(OH) 105mol/L,则
c H 109.8 4
c(OH) 104.2
K 100.8。
c Al(OH) 105
4
1 1
(6)砷化镓晶胞中Ga原子数目为4,As原子数目为 8 64,晶胞的质量
8 2
470475 580
m g g,晶胞的体积V a3pm3,晶胞密度为gcm3,则晶胞边长a为
N N
A A
m 580 580
a
3
1010pm
3
1010pm,故答案为
3
1010。
N N
A A
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
17.答案:(1)2C(s)2NO (g) N (g)2CO (g)H 854kJmol1(2分)
2 2 2
(2)①0.042molL1min1(2分);减小(2分);②BC(2分)
7.5
(3)①小于(2分);② (2分)
p
0
(4)加入的CO与NO分解生成的O 反应,使NO分解平衡向生成N 的方向移动,因此NO
2 2
转化率升高(3分)
解析:(1)①2NO(g)O (g)2NO (g)H 114kJmol1;
2 2 1
②C(s)O (g)CO (g)H 393.5kJmol1;
2 2 2
③2NO(g)N (g)O (g)H 181kJmol1
2 2 3
C(s)与NO (g)反应生成N (g)和CO (g)的反应为:2C(s)2NO (g) N (g)2CO (g)。
2 2 2 2 2 2
根据盖斯定律可知该反应可由2×②+③-①得到,则该反应H 2H H H
2 3 1
2(393.5kJmol1)(181kJmol1)(114kJmol1)854kJmol1,反应热化学方程式
为:2C(s)2NO (g) N (g)2CO (g)H 854kJmol1;
2 2 2
(2)①0~10min内,NO的平均反应速率
c (1.000.58)molL1
vNO 0.042molL1min1;该反应为放热反应,温度升高,平
t 10min
衡逆向移动,平衡常数K减小;
②30min后,只改变某一条件,反应重新达到平衡,新平衡时NO和N 的浓度均大于原平衡
2
浓度,加入一定量的活性炭,碳是固体对反应速率和化学平衡均无影响,故A错误;
通入一定量的NO,可增大NO浓度,同时使平衡正向移动,从而使N 的浓度增大,故B正
2
确;
适当缩小容器的体积,反应前后体积不变,平衡状态物质浓度增大,故C正确;
加入合适催化剂,催化剂只改变化学反应速率,不改变化学平衡,故D错误;
故选BC;
(3)①平衡时v v ,则k p2(NO) p2(CO)k pN p2CO ,可得
正 逆 正 逆 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
k pN p2CO k
正 2 2 K,该反应为放热反应,温度升高平衡逆向移动,K减小,即 正 减
k p2(NO)p2(CO) k
逆 逆
小,则k 增大的倍数小于k 增大的倍数。
正 逆
②设 1L的刚性容器中分别充入 CO、NO和N 物质的量之比为2mol、2mol、1mol,则:
2
2NO(g) 2CO(g) N (g) 2CO (g)
2 2
起始(mol) 2 2 1 0
转化(mol) 2x 2x x 2x
平衡(mol) 22x 22x 1x 2x
则反应后总物质的量为5xmol,初始压强为 p kPa,达平衡时压强为0.9p kPa,则
0 0
5x 0.9p kPa
0 ,x0.5,平衡时CO、NO、N 和CO 的物质的量分别为1mol、1mol、
5 p kPa 2 2
0
1.5mol、1mol,总物质的量为4.5mol,则
1 1.5
(0.9p )2(0.9p )
k p(N )p2(CO ) 0 4.5 0 4.5 7.5
K 正 2 2 。
k p2(NO)p2(CO) 1 1 p
逆 (0.9p )2(0.9p )2 0
0 4.5 0 4.5
(4)加入的CO与NO分解生成的O 反应,使NO分解平衡向生成N 的方向移动,因此NO
2 2
转化率升高,从而使NO转化为N 的转化率增大。
2
18.答案:(1)C>B>A(2分); (2分)
(2)醚键、酯基(1分)
(3)1(2分)
(4) (2分)
(5)2(2分)
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(6) (4分)
解析:由有机物的转化关系可知,氯化铁做催化剂作用下,苯与氯气发生取代反应生成氯
苯,氯苯在氢氧化钠溶液发生水解反应后,酸化得到苯酚,则C为 ;碳酸钾作用下
与一碘甲烷发生取代反应生成 ,结合G的结构简式可知,
一定条件下与甲醛和氯化氢反应转化为E,则E为 ; 与氰化钠发
生取代反应生成F,则F为 ; 酸性条件下发生水解反应所得产物与甲醇在氯化
氢作用下发生酯化反应生成G( ),G在一定条件下发生分子间取代反应生成
。
(1)A、B、C三种物质分别为苯、氯苯和苯酚,含 相同碳原子的烃沸点低于卤代烃的沸
点,苯酚分子 能形成分子间存在氢键,沸点高于卤代烃,则三种 物质的沸点由高到低的顺序
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
为C>B>A;由分析可知,E的结构简式为 。
(2)由结构简式可知, 的官能团为醚键、酯基;
(3)由结构简式可知,H分子中含有如图*所示的 1个手性碳原子: ;
(4)由分析可知,G→H的反应为 ,一定条件下发生分子间取代反应生成
和甲醇,反应的化学方程式为 ;
(5)F的同分异构体 X含有甲基,除苯环外还有一个五元环,且与苯环共用两个碳原子,能
发生水解反应说明X分子中含有酰胺基,则符合条件的结构简式为
,共有2种;
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(6)由题给有机物的转化关系可知,以环丙烷和甲醇为原料合成 的合
成步骤为催化剂作用下环丙烷与氯气发生环加成反应生成1,2-二氯丙烷,1,2-二氯丙烷与
氰化钠发生取代反应生成 , 酸性条件下发生水解反应所得产物与甲醇在氯化氢
作用下发生酯化反应生成 , 一定条件下发生分子间取代反应生成
,合成路线为
。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002