文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【贵州版】
可能用到的相对原子质量:H—1、C—12、O—16、Na—23、Ni—59、Ba—137
一、单项选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.三星堆遗址出土了黄金面具残片、铜神坛、铜神像、泥塑陶猪、丝绸、象牙制品、龟背形
网格状器等大量文物,三星堆文化惊艳世界。下列相关说法错误的是( )
A.铜神坛由青铜制成,其硬度大于各组分金属的硬度
B.泥塑陶猪主要是由硅酸盐材料高温烧结而成的
C.金和铜的活泼性不同,两种元素在自然界中的主要存在形式也不同
D.丝绸的主要成分为纤维素,性质稳定,不易被水解
通电
2.工业上通常利用反应2Al O (熔融) 4Al3O 来获得单质铝,该反应还需要添加
2 3 2
Na AlF (冰晶石)以降低氧化铝的熔化温度。下列表示相关微粒的化学用语错误的是( )
3 6
A.质子数与中子数相等的氟原子:18F
9
B.Al3的结构示意图:
C.基态钠原子外围电子排布式:3s1
D.基态氧原子的轨道表示式:
3.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.2L1molL1CuSO 溶液中,Cu2的数目为2N
4 A
B.1.68g熔融的NaHCO 中含有0.04N 个阳离子
3 A
C.1mol冰醋酸中含有 键的数目为6N
A
D.标准状况下,44.8mL15NO中含有的中子数为0.032N
A
4.下列仪器在实验中使用合理的是( )
A B C D
梨形分液漏斗 容量瓶 酸式滴定管 玻璃塞细口瓶
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
利用饱和Na CO 检漏洗涤后注入
2 3 代替平底烧瓶用
溶液除去乙酸乙 标准溶液至“0”刻 实验室长期储存
于KMnO 和浓盐
4
酯中混有的少量 度下,记录读 NaOH溶液
酸反应制Cl
2
乙酸 数,开始滴定
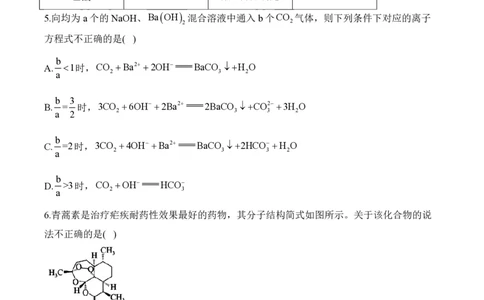
5.向均为a个的 NaOH、BaOH 混合溶液中通入b个CO 气体,则下列条件下对应的离子
2 2
方程式不正确的是( )
b
A. 1时,CO Ba2 2OH BaCO H O
a 2 3 2
b 3
B. = 时,3CO 6OH 2Ba2 2BaCO CO2 3H O
a 2 2 3 3 2
b
C. =2时,3CO 4OH Ba2 BaCO 2HCO H O
a 2 3 3 2
b
D. >3时,CO OH HCO
a 2 3
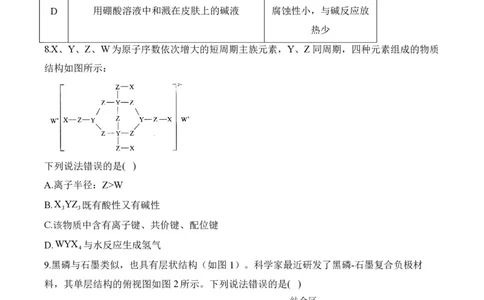
6.青蒿素是治疗疟疾耐药性效果最好的药物,其分子结构简式如图所示。关于该化合物的说
法不正确的是( )
A.能与NaOH溶液反应
B.受热易分解
C.该分子中含有4个手性碳原子
D.从植物中提取青蒿素的方法是研磨、浸泡、过滤、萃取、结晶
7.生活中处处有化学。下列有关化学在日常生活中的应用与所给化学原理无关的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
选项 项目 化学原理
A 用电渗析法由海水制淡水 水在通电条件下能分解
NH水解使溶液显酸
4
B 用浓氯化铵溶液除去镁条表面的氧化膜
性,能溶解MgO
防止钠与空气中的氧气
C 少量钠保存在石蜡油中
和水蒸气反应
硼酸为弱酸,对皮肤的
D 用硼酸溶液中和溅在皮肤上的碱液 腐蚀性小,与碱反应放
热少
8.X、Y、Z、W为原子序数依次增大的短周期主族元素,Y、Z同周期,四种元素组成的物质
结构如图所示:
下列说法错误的是( )
A.离子半径:Z>W
B.X YZ 既有酸性又有碱性
3 3
C.该物质中含有离子键、共价键、配位键
D.WYX 与水反应生成氢气
4
9.黑磷与石墨类似,也具有层状结构(如图1)。科学家最近研发了黑磷-石墨复合负极材
料,其单层结构的俯视图如图2所示。下列说法错误的是( )
A.黑磷区中P—P的键能不完全相同
B.单层复合材料中C和P间的作用力为共价键
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
C.基态磷原子核外电子中,两种自旋状态的电子数之比为3:2
D.黑磷中P原子的杂化方式和石墨中C原子的杂化方式相同
10.下列实验推论不合理的是( )
选项 实验操作或现象 实验推论
反应原理
将 Na投入到含CuBr 的丙酮溶液中,产生
2
A
紫红色固体 Cu2 2Na 2Na Cu
向银镜中滴加少量FeCl 溶液,银镜逐渐溶
3 反应原理
B 解,溶液颜色变浅;向溶解液中继续滴加
Fe3 Ag‡ˆ ˆˆ†ˆ Fe2 Ag
KSCN溶液,溶液变成红色
向盛有少量Mg(OH) 沉淀的试管中加入适 NH Cl促进Mg(OH) 沉
2 4 2
C
量饱和NH Cl溶液,振荡后沉淀溶解 淀溶解平衡正向移动
4
将铜丝分别插入稀硫酸和浓硫酸中,二者均 稀硫酸与浓硫酸均无法氧
D
未出现明显现象 化铜
11.NiC O 可用于制备镍粉和镍催化剂等。以废镍渣(含少量铁、钙单质)为原料制备草酸
2 4
镍的流程如图所示。已知:CaF、NiC O 均不溶于水。下列说法不正确的是( )
2 2 4
A.滤渣Ⅰ回收处理后可用作净水剂
B.“操作 X”“操作 Y”“操作Z”的目的分别为除铁、除钙、沉淀草酸镍
C.NiC O 中Ni的化合价为+1价
2 4
D.若试剂a、试剂b分别为稀硫酸、烧碱,则滤液Ⅲ中含有H、Na、F、SO2、NH
4 4
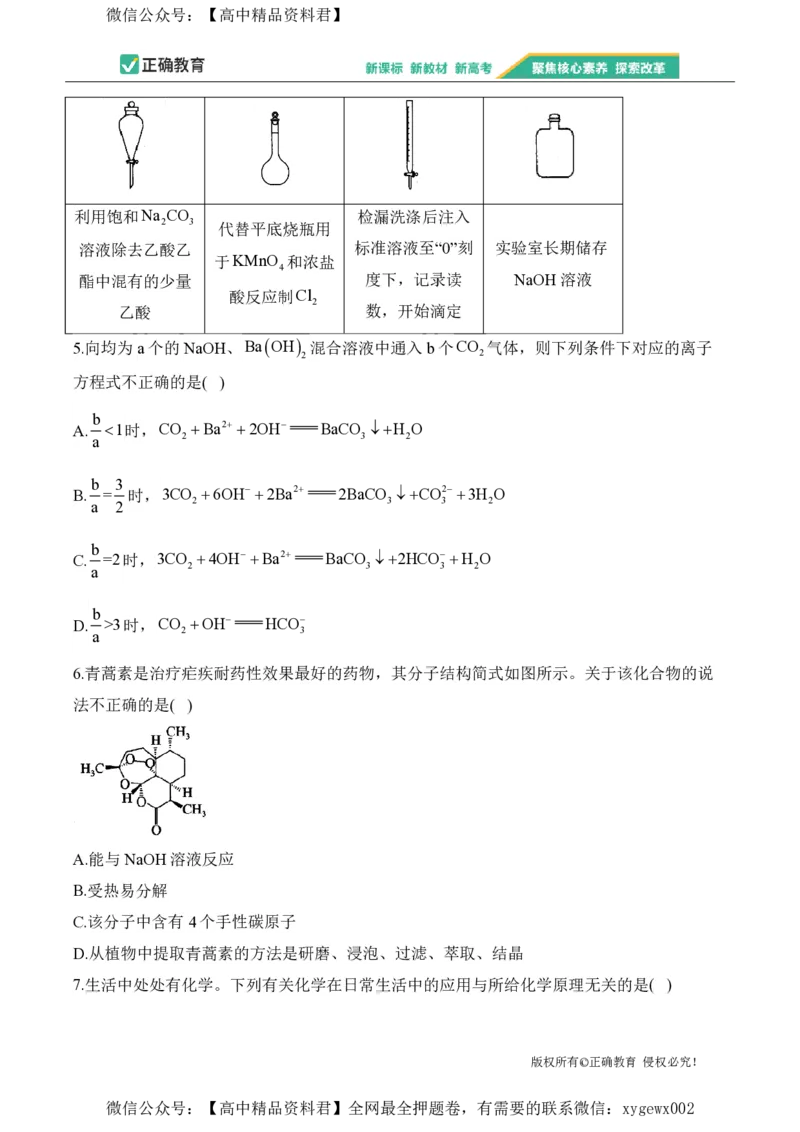
12.探究一元弱酸HA在苯-水体系中的溶解状况。常温下,HA在水(W)和苯(B)两相中
c (HA)
的变化如图所示,HA在两相间的分配系数K B 1.00,HA在水中的电离平衡常数
D c (HA)
W
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
K (HA)1.00104。下列说法不正确的是( )
a
A.水中,c(HA)c
H
c
A
c
OH
B.水中,c(HA)103molL1
C.实验测得苯中,c(HA) 104molL1,二聚反应的平衡常数K=100
2
D.向水中滴入少量浓盐酸,则苯中c(HA) 增大
2
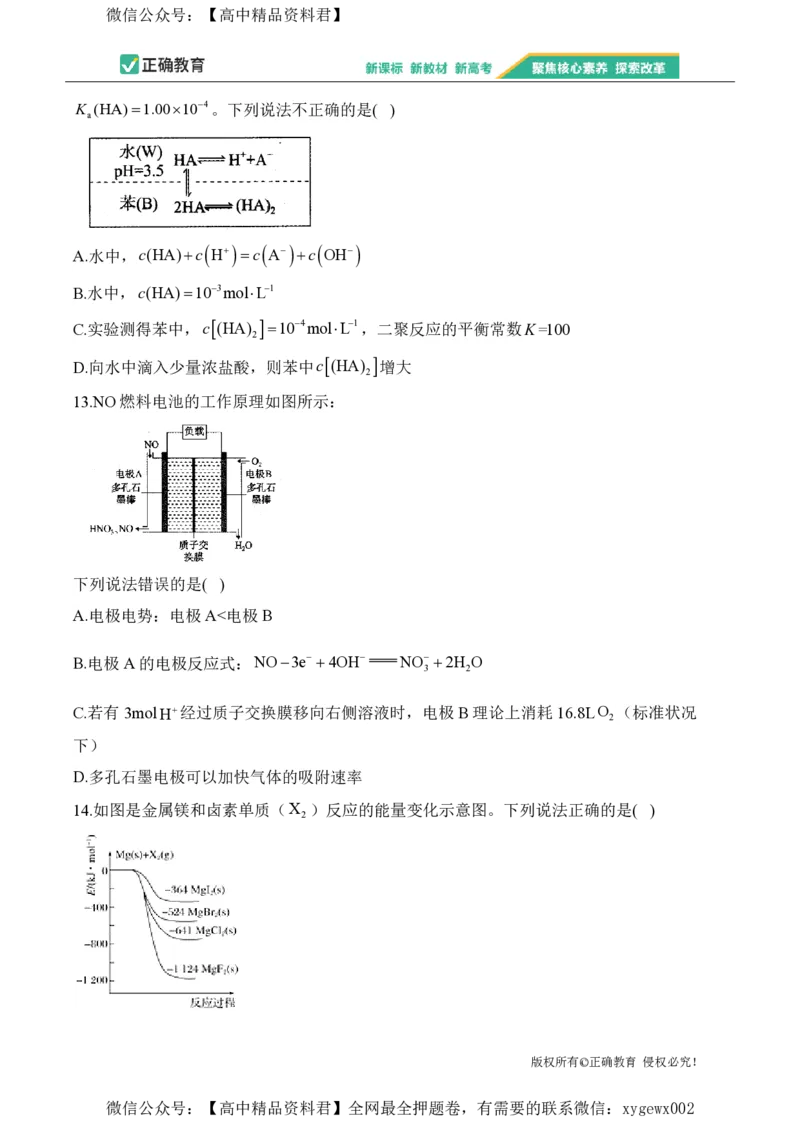
13.NO燃料电池的工作原理如图所示:
下列说法错误的是( )
A.电极电势:电极A<电极 B
B.电极 A的电极反应式:NO3e 4OH NO 2H O
3 2
C.若有 3molH经过质子交换膜移向右侧溶液时,电极B理论上消耗16.8LO (标准状况
2
下)
D.多孔石墨电极可以加快气体的吸附速率
14.如图是金属镁和卤素单质(X )反应的能量变化示意图。下列说法正确的是( )
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.热稳定性:MgF MgCl MgBr MgI
2 2 2 2
B.22.4LF g与足量的Mg充分反应,放热1124kJ
2
C.工业上可由电解MgCl 溶液冶炼金属Mg,该过程需要吸收热量
2
D.由图可知:MgBr s分解吸收的能量比MgCl s大
2 2
二、非选择题:共 58 分
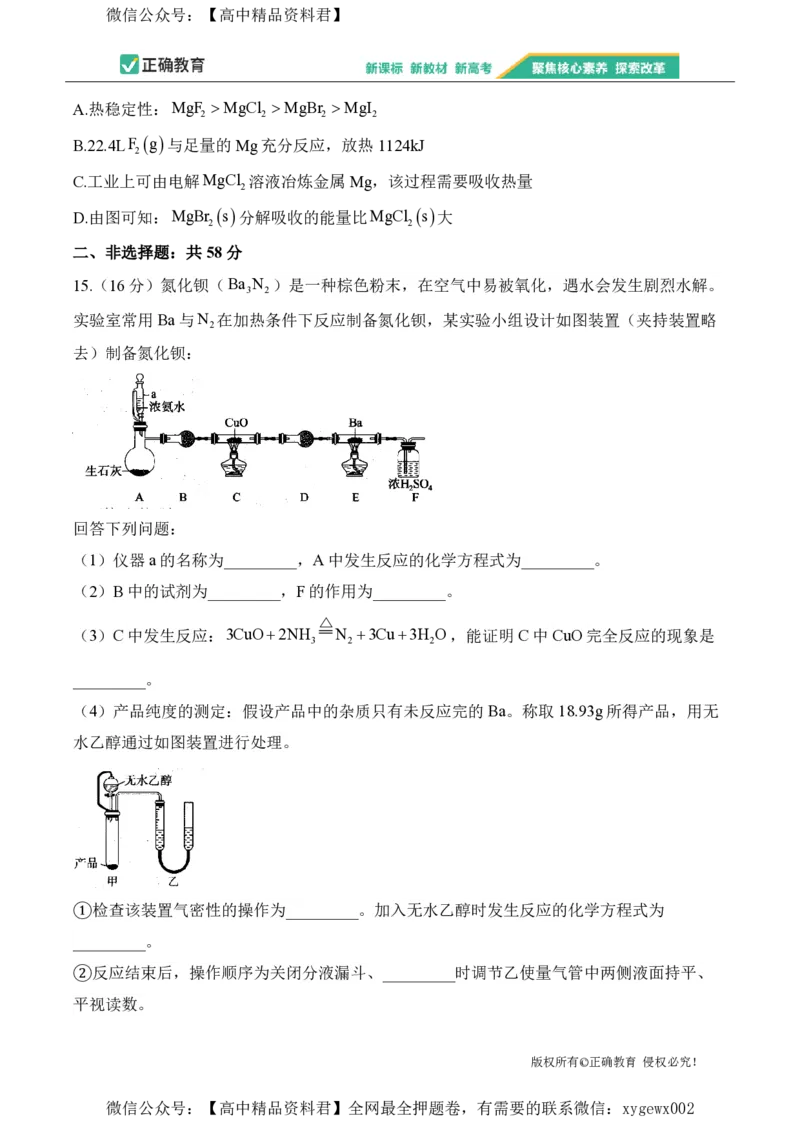
15.(16分)氮化钡(Ba N )是一种棕色粉末,在空气中易被氧化,遇水会发生剧烈水解。
3 2
实验室常用Ba与N 在加热条件下反应制备氮化钡,某实验小组设计如图装置(夹持装置略
2
去)制备氮化钡:
回答下列问题:
(1)仪器a的名称为_________,A中发生反应的化学方程式为_________。
(2)B中的试剂为_________,F的作用为_________。
△
(3)C中发生反应:3CuO2NH N 3Cu3H O,能证明C中CuO完全反应的现象是
3 2 2
_________。
(4)产品纯度的测定:假设产品中的杂质只有未反应完的Ba。称取18.93g所得产品,用无
水乙醇通过如图装置进行处理。
①检查该装置气密性的操作为_________。加入无水乙醇时发生反应的化学方程式为
_________。
②反应结束后,操作顺序为关闭分液漏斗、_________时调节乙使量气管中两侧液面持平、
平视读数。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
③若测量的气体体积换算成标准状况下为 224mL,则产品的纯度为_________%(结果保留
4位有效数字)。若读数时乙中右侧液面高于左侧,测定结果将_________(填“偏高”“偏低”
或“不变”)。
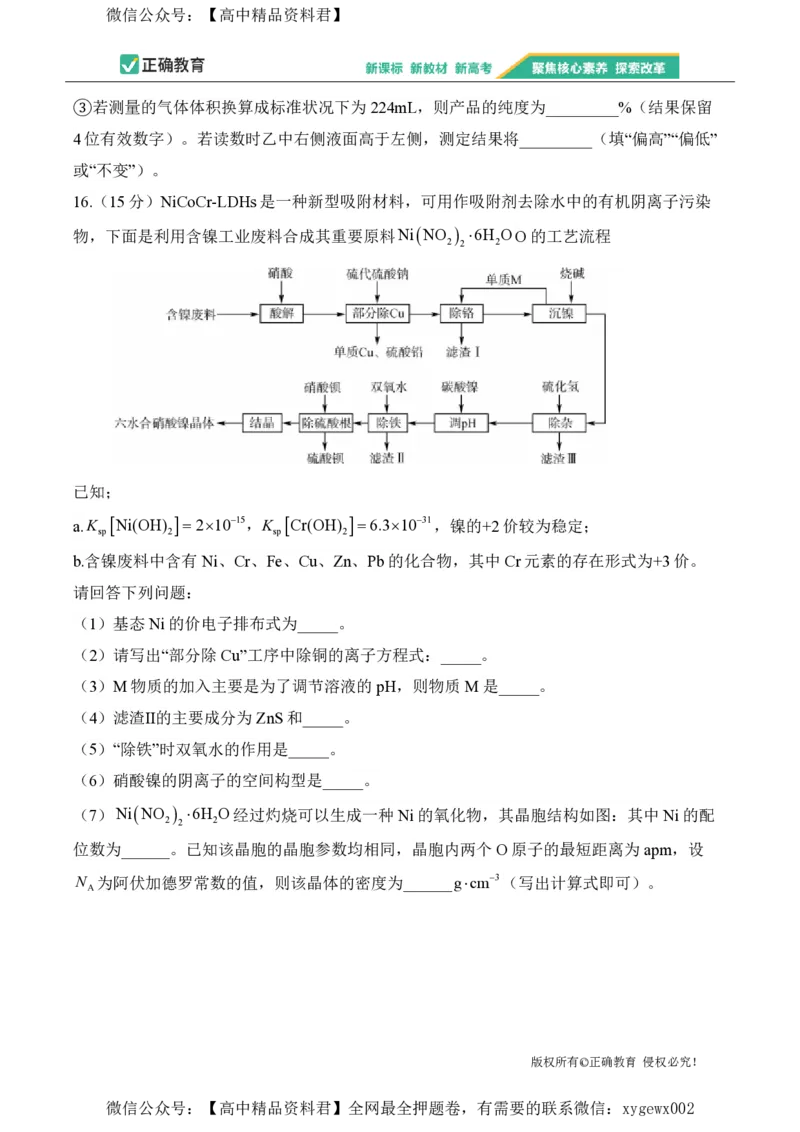
16.(15分)NiCoCr-LDHs是一种新型吸附材料,可用作吸附剂去除水中的有机阴离子污染
物,下面是利用含镍工业废料合成其重要原料NiNO 6H OO的工艺流程
2 2 2
已知;
a.K Ni(OH) 21015,K Cr(OH) 6.31031,镍的+2价较为稳定;
sp 2 sp 2
b.含镍废料中含有Ni、Cr、Fe、Cu、Zn、Pb的化合物,其中Cr元素的存在形式为+3价。
请回答下列问题:
(1)基态Ni的价电子排布式为_____。
(2)请写出“部分除Cu”工序中除铜的离子方程式:_____。
(3)M物质的加入主要是为了调节溶液的pH,则物质M是_____。
(4)滤渣Ⅱ的主要成分为ZnS和_____。
(5)“除铁”时双氧水的作用是_____。
(6)硝酸镍的阴离子的空间构型是_____。
(7)NiNO 6H O经过灼烧可以生成一种Ni的氧化物,其晶胞结构如图:其中Ni的配
2 2 2
位数为______。已知该晶胞的晶胞参数均相同,晶胞内两个O原子的最短距离为apm,设
N 为阿伏加德罗常数的值,则该晶体的密度为______gcm3(写出计算式即可)。
A
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
17.(12分)碱法合成CH ONa 的反应原理是
3
CH OH(aq)NaOH(aq)‡ˆ ˆˆ†ˆ CH ONa(aq)H O(l),反应平衡常数和 t 时刻H O的物质的量
3 3 2 2
分数随温度的变化如表所示。
温度/℃ 平衡常数 K 液相x
H O
2
60 0.0316 0.0635
80 0.0242 0.0571
100 0.0191 0.0518
120 0.0154 0.0473
140 0.0127 0.0436
(1)CH ONa 比NaOH的碱性强,原因是_____。
3
(2)下列措施中可以提高平衡体系中CH ONa 含量的是_____(填字母)。
3
A.不断补充CH OH
3
B.将H O汽化移出
2
C.升高温度
(3)当起始投料nCH OH:n(NaOH)5:1,温度为100℃时, t 时刻CH OH的转化率为
3 3
_____%(结果保留 3位有效数字)。
(4)相比钠法(2Na2CH OH2CH ONaH ),碱法合成CH OH的优势是
3 3 2 3
_____。结合工业生产实际分析,反应温度设定为100~120℃的原因是_____(写出一种)。
(5)已知:CH OH(l)NaOH(aq)‡ˆ ˆˆ†ˆ CH ONa(s)H O(l) H 54.62kJmol1
3 3 2 1
CH ONa(s)CH ONa(sln) H 76.84kJmol1
3 3 2
NaOH(aq)NaOH(sln) H 12.13kJmol1
3
H O(l)H O(sln) H 3kJmol1
2 2 4
反应CH OH(1)NaOH(sln)‡ˆ ˆˆ†ˆ CH ONa(sln)H O(sln)的H ______kJmol1。
3 3 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
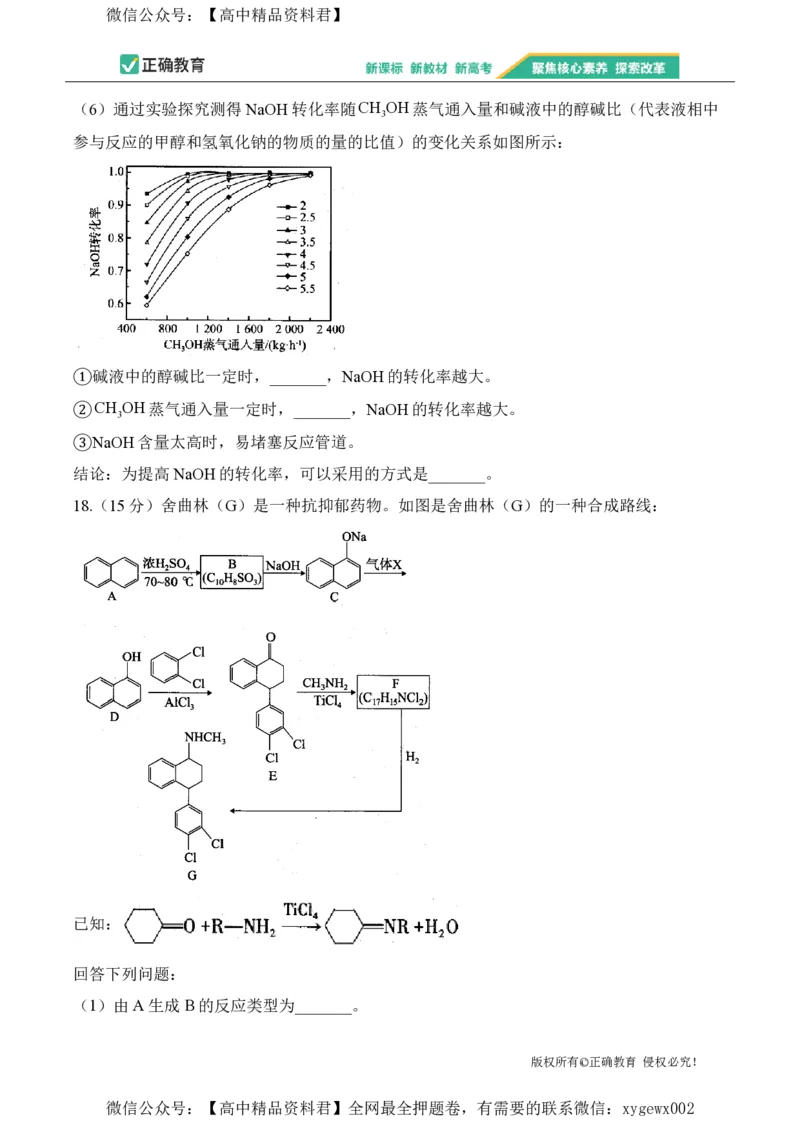
(6)通过实验探究测得NaOH转化率随CH OH蒸气通入量和碱液中的醇碱比(代表液相中
3
参与反应的甲醇和氢氧化钠的物质的量的比值)的变化关系如图所示:
①碱液中的醇碱比一定时,_______,NaOH的转化率越大。
②CH OH蒸气通入量一定时,_______,NaOH的转化率越大。
3
③NaOH含量太高时,易堵塞反应管道。
结论:为提高NaOH的转化率,可以采用的方式是_______。
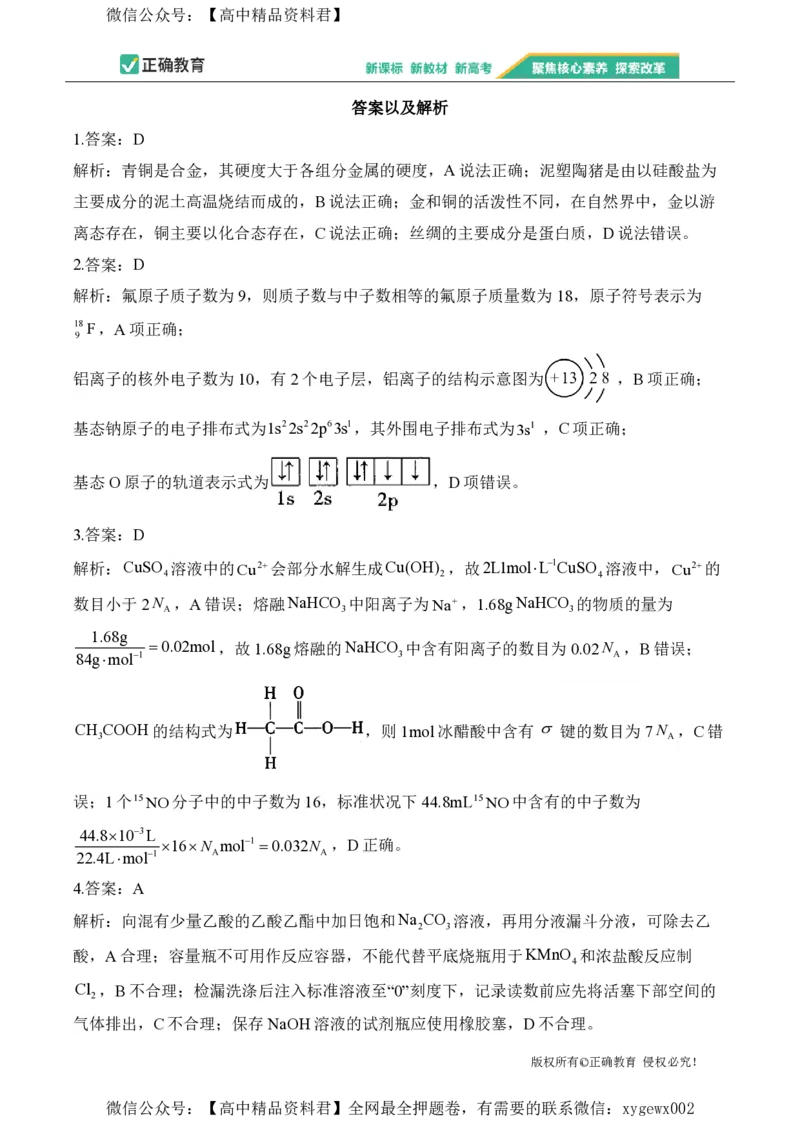
18.(15分)舍曲林(G)是一种抗抑郁药物。如图是舍曲林(G)的一种合成路线:
已知:
回答下列问题:
(1)由A生成B的反应类型为_______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2)气体X为_______(写分子式),D中含氧官能团的名称为_______。
(3) 的化学名称是_______。
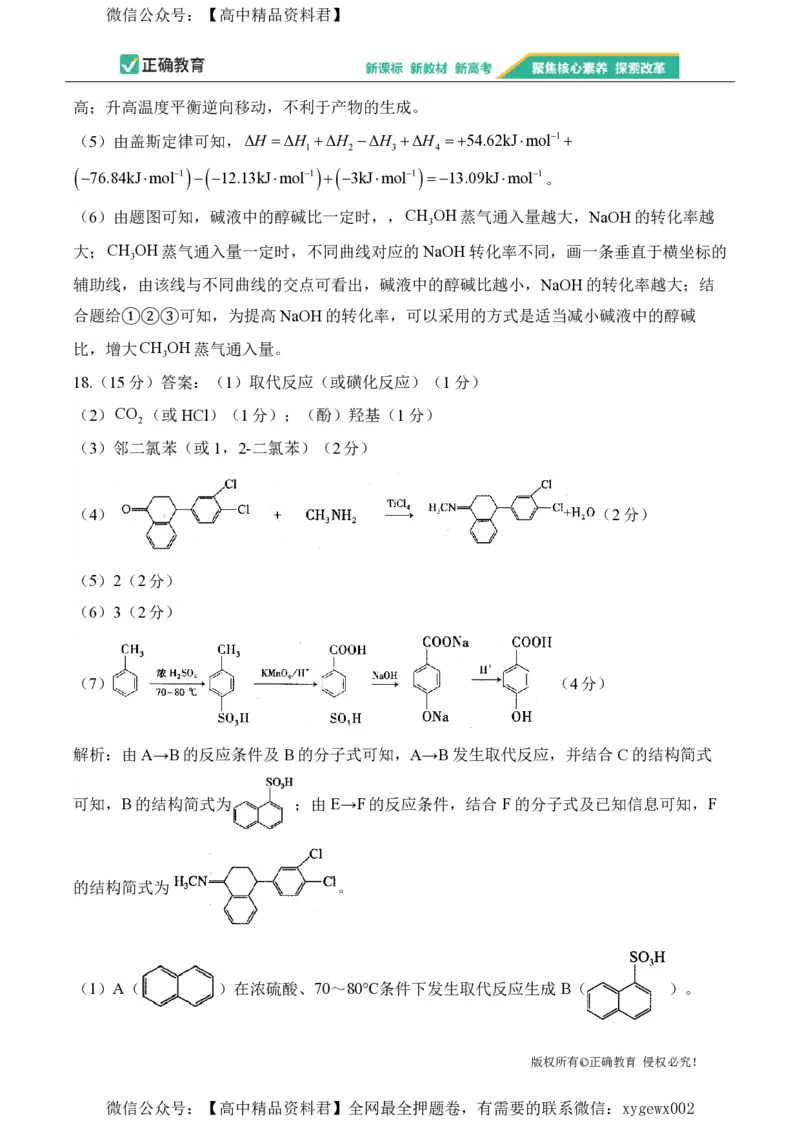
(4)由E生成F的化学方程式为_______。
(5)G中手性碳原子(注:与四个各不相同的原子或原子团相连的碳原子)的个数为
_______。
(6)化合物A的同分异构体中同时满足下列条件的有_______种。
①苯环上只有1个取代基
②不含 C C C结构
③不能被氧化为苯甲酸
④存在 2个环状结构
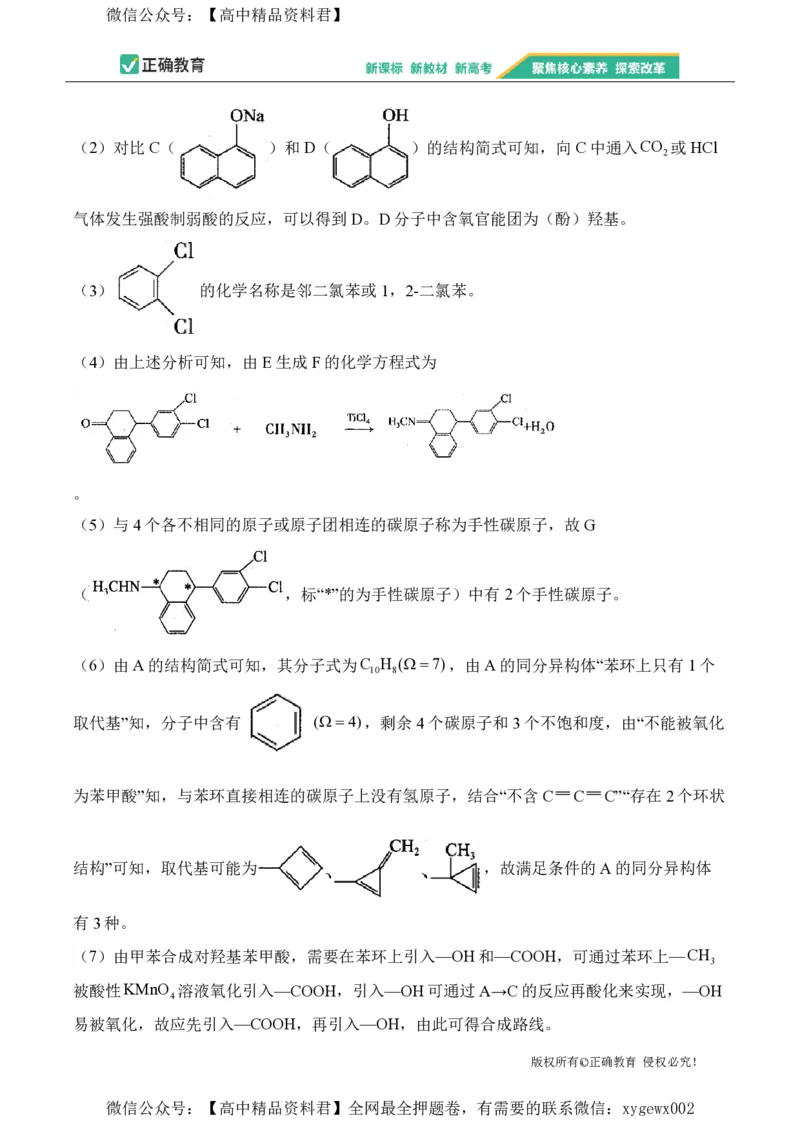
(7)根据上述路线中的相关知识,以甲苯为主要原料用不超过四步的反应设计合成对羟基苯
甲酸的路线(其他无机试剂任选):_______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:D
解析:青铜是合金,其硬度大于各组分金属的硬度,A说法正确;泥塑陶猪是由以硅酸盐为
主要成分的泥土高温烧结而成的,B说法正确;金和铜的活泼性不同,在自然界中,金以游
离态存在,铜主要以化合态存在,C说法正确;丝绸的主要成分是蛋白质,D说法错误。
2.答案:D
解析:氟原子质子数为9,则质子数与中子数相等的氟原子质量数为18,原子符号表示为
18F,A项正确;
9
铝离子的核外电子数为10,有2个电子层,铝离子的结构示意图为 ,B项正确;
基态钠原子的电子排布式为1s22s22p63s1,其外围电子排布式为3s1 ,C项正确;
基态O原子的轨道表示式为 ,D项错误。
3.答案:D
解析:CuSO 溶液中的Cu2会部分水解生成Cu(OH) ,故2L1molL1CuSO 溶液中,Cu2的
4 2 4
数目小于2N ,A错误;熔融NaHCO 中阳离子为Na,1.68gNaHCO 的物质的量为
A 3 3
1.68g
0.02mol,故1.68g熔融的NaHCO 中含有阳离子的数目为0.02N ,B错误;
84gmol1 3 A
CH COOH的结构式为 ,则1mol冰醋酸中含有 键的数目为7N ,C错
3 A
误;1个15NO分子中的中子数为16,标准状况下44.8mL15NO中含有的中子数为
44.8103L
16N mol1 0.032N ,D正确。
22.4Lmol1 A A
4.答案:A
解析:向混有少量乙酸的乙酸乙酯中加日饱和Na CO 溶液,再用分液漏斗分液,可除去乙
2 3
酸,A合理;容量瓶不可用作反应容器,不能代替平底烧瓶用于KMnO 和浓盐酸反应制
4
Cl ,B不合理;检漏洗涤后注入标准溶液至“0”刻度下,记录读数前应先将活塞下部空间的
2
气体排出,C不合理;保存NaOH溶液的试剂瓶应使用橡胶塞,D不合理。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
5.答案:C
b
解析:A. 1时,二氧化碳不足,反应生成碳酸钡沉淀,离子方程式
a
CO Ba2 2OH BaCO H O,故A正确;
2 3 2
b 3
B. = 时,假设2个氢氧化钠和2个氢氧化钡通 3个二氧化碳,先是2个氢氧化钡与2个二
a 2
氧化碳反应,再是1个二氧化碳与2个氢氧化钠反应,其离子方程式为
3CO 6OH 2Ba2 2BaCO CO2 3H O,故B正确;
2 3 3 2
b
C. =2时,假设2个氢氧化钠和2个氢氧化钡通4个二氧化碳,先是2个氢氧化钡与2个二
a
氧化碳反应,再是1个二氧化碳与2个氢氧化钠反应生成1个碳酸钠,再是1个碳酸钠与1
个二氧化碳、水反应生成2个碳酸氢钠,其离子方程式为
2CO 3OH Ba2 BaCO HCO H O,故C错误;
2 3 3 2
b
D. =3时,假设 2个氢氧化钠和2个氢氧化钡通6个二氧化碳,先是2个氢氧化钡与2个二
a
氧化碳反应生成2个碳酸钡,再是1个二氧化碳与2个氢氧化钠反应生成1个碳酸钠,再是
1个碳酸钠与1个二氧化碳、水反应生成2个碳酸氢钠,最后是 2个二氧化碳和2个碳酸钡、
b
水反应生成1个碳酸氢钡,故最后所得为碳酸氢钠和碳酸氢钡溶液,若 >3,二氧化碳还有
a
过量,则其离子方程式为CO OH HCO,故D正确。
2 3
综上所述,答案为C。
6.答案:C
解析:该化合物分子中含有酯基,可与NaOH溶液发生水解反应,A说法正确;该化合物分
子中含有过氧键,根据H O 受热分解会断开过氧键可推测青蒿素的热稳定性较差,B说法正
2 2
确;由该化合物的结构简式可知,其分子中含有7个手性碳原子,C说法错误;从植物中提
取有机化合物的一般方法是用有机溶剂浸泡已研磨过的固体原料,过滤获得提取液,再进行
萃取得到浓溶液,最后冷却结晶,D说法正确。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
7.答案:A
解析:海水中的离子在通电条件下能定向移动,从而使海水淡化,与水在通电条件下能分解
无关,A符合题意;NH水解使溶液显酸性,所以浓氯化铵溶液能溶解镁条表面的氧化膜
4
MgO,B不符合题意;钠的密度比石蜡油的大,且与石蜡油不反应,故为了防止钠与空气中
的氧气和水蒸气反应而变质,可将少量钠保存在石蜡油中,C不符合题意;硼酸为弱酸,对
皮肤的腐蚀性小,与碱反应放热少,故可用硼酸溶液中和溅在皮肤上的碱液,D不符合题
意。
8.答案:B
解析:X、Y、Z、W为原子序数依次增大的短周期主族元素,Y、Z同周期,结合题给物质
结构中各元素原子的价键情况得出X为H,Y为B,Z为O,W为Na。简单离子的电子层结
构相同时,原子序数越大,半径越小,故离子半径:O2 Na,A说法正确;H BO 只显弱
3 3
酸性,B说法错误;该物质中阳离子和阴离子间存在离子键,阴离子中存在共价键和配位
键,C说法正确;NaBH 中-1价的氢元素与水中+1价的氢元素可发生氧化还原反应生成
4
H ,反应的化学方程式为NaBH 2H O NaBO 4H ,D说法正确。
2 4 2 2 2
9.答案:D
解析:A.根据黑磷中p-p键的键长不相同可知,黑磷区中p-p键的键能不完全相同,A项正
确;B.黑磷与石墨以共价键相连,B项正确;C.基态磷原子核外电子排布式为
1s22s22p63s23p3,两种自旋状态的电子数之比为3:2,C项正确;D.黑磷中每个p原子与周
围3个p原子成键,还有一对孤对电子,为sp3染化,石墨中C原子为sp2染化,D项错误。
故答案选D。
10.答案:D
解析:无水环境下,Cu2可以氧化Na生成Na和紫红色的铜单质,A不符合题意;向银镜
中加入少量的FeCl 溶液,银镜逐渐溶解,溶液颜色变浅,则还原产物为Fe2,但向溶解液中
3
滴加KSCN溶液后,溶液变红,则溶液中仍有Fe3剩余,说明该反应为可逆反应,B不符合
题意;Mg(OH) 在溶液中存在沉淀溶解平衡Mg(OH) (s)‡ˆ ˆˆ†ˆ Mg2(aq)2OH(aq),加入适
2 2
量饱和NH Cl溶液时,NH Cl溶液中的NH会与OH反应,使Mg(OH) 的沉淀溶解平衡正
4 4 4 2
向移动,促进Mg(OH) 溶解,C不符合题意;稀硫酸与Cu不反应,但在加热条件下,浓硫
2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
酸与Cu能发生反应,D符合题意。
11.答案:C
解析:结合信息分析可知,“粉碎”“酸浸”使金属转化为阳离子(Ni2、Fe2、Ca2),随后经
“氧化”将Fe2氧化为Fe3,再调节pH使Fe3沉淀,加入NH F沉淀Ca2,最后加入H C O
4 2 2 4
沉淀Ni2得到NiC O 。滤渣I中含有Fe(OH) 沉淀,经处理后可用作净水剂,A、B说法正
2 4 3
确;NiC O 中Ni的化合价为+2价,C说法错误;若试剂a、试剂b分别为稀硫酸、烧碱,
2 4
则滤液Ⅲ中含有H、Na(来自烧碱)、F(来自NH F)、SO2(来自硫酸)、NH(来
4 4 4
自NH F),D说法正确。
4
12.答案:A
解析:水中存在电荷守恒,即c
H
c
A
c
OH
,A说法错误;
c
H
c
A
K (HA) 1.00104,水中pH=3.5,则c A c H 103.5molL1,
a c(HA)
c (HA)
c(HA)103molL1,B说法正确;HA在两相间的分配系数K B 1.00,则苯中
D c (HA)
W
c(HA) 104
c(HA)103molL1,c(HA) 104molL1, K 2 100 ,C说法正确;
2 c2(HA) 1032
向水中滴入少量浓盐酸,HA的电离平衡逆向移动,使c (HA)增大,促使更多的HA进入苯
W
层,即HA(W)‡ˆ ˆˆ†ˆ HA(B)正向移动,c (HA)增大,则苯中二聚反应的平衡正向移动,使苯
B
中c(HA) 增大,D说法正确。
2
13.答案:B
解析:根据题给NO燃料电池的工作原理图可知,电极A上NO失去电子发生氧化反应,则
电极A为负极,电极B上O 得到电子发生还原反应,则电极 B为正极。原电池中,正极的
2
电极电势高于负极,即电极电势:电极A<电极B,A说法正确;电解质溶液为酸性溶液,所
以电极A的电极反应式为NO3e 2H O NO 4H,B说法错误;有3molH经过质子
2 3
交换膜移向右侧溶液时,说明反应中转移了3mol电子,根据电极B的电极反应式
O 4e 4H 2H O可知,每转移3mol电子时,消耗0.75molO ,即在标准状况下消耗
2 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
氧气的体积为0.75mol22.4Lmol1 16.8L,C说法正确;多孔石墨的表面积较大,可以加快
气体的吸附速率,D说法正确。
14.答案:A
解析:A项,物质的能量越低越稳定,根据图象数据分析,化合物的热稳定性由强到弱的顺
序为MgF MgCl MgBr MgI ,正确;
2 2 2 2
B项,没有说明是否在标准状况下,22.4LF (g)不一定为1mol,错误;
2
C项,工业上用电解熔融MgCl 的方法冶炼金属Mg,而不是电解MgCl 溶液,错误。
2 2
15.(16分)答案:(1)恒压滴液漏斗(1分);CaONH H O NH Ca(OH) (2
3 2 3 2
分)
(2)碱石灰(1分);防止空气中的水蒸气和氧气进入装置中(1分)
(3)C中黑色固体完全变为红色(1分)
(4)①连接好装置,关闭分液漏斗活塞,向乙中量气管右侧加入水至两侧液面有明显的高
度差,停止加水,若高度差长时间不变,则证明气密性良好;(2分)
2CH CH OHBaCH CH O BaH (2分);②待装置恢复至室温(1分);
3 2 3 2 2 2
③92.76(2分);偏高(2分)
解析:(1)根据题给实验装置图可知,仪器a为恒压滴液漏斗;A中浓氨水与CaO反应生成
NH 和Ca(OH) ,故反应的化学方程式为CaONH H O NH Ca(OH) 。
3 2 3 2 3 2
(2)根据题给实验装置图可知,B的作用主要是除去氨气中的水蒸气,故B中的试剂应为碱
石灰,F的作用主要是防止空气中的水蒸气和氧气进入装置中。
(3)由题意可知,若C中CuO完全反应时,C中黑色固体会完全变为红色。
(4)①根据题给装置图可知,该装置的气密性检查应通过向装置中注入水,使里面气体与
大气形成压强差,从而产生液面高度差且高度差在长时间内不变化的现象,进行检验;根据
乙醇与钠反应可类比得到无水乙醇与Ba反应的化学方程式为
2CH CH OHBaCH CH O BaH 。②由于温度和压强均会对气体体积产生影
3 2 3 2 2 2
响,所以反应结束后,应先关闭分液漏斗的活塞,待装置恢复至室温后再调节量气管使其两
侧液面持平,最后平视读数。③若测量的气体体积换算成标准状况下为224mL,则生成H
2
的物质的量为0.01 mol,消耗Ba的物质的量为0.01mol,质量为1.37g,故产品的纯度为
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
18.93g1.37g
100%92.76%。若读数时题图乙中右侧液面高于左侧,则装置中氢气压强高
18.93g
于实验条件下的大气压,故测出的氢气体积偏小,则测定结果偏高。
16.(15分)答案:(1)3d84s2(2分)
(2)4Cu2 S O2 H O 4Cu2SO2 10H(2分)
2 3 2 4
(3)Ni(OH) (2分)
2
(4)CuS(2分)
(5)将Fe2氧化为Fe3,使其转化为Fe(OH) 沉淀除去(2分)
3
(6)平面三角形(2分)
4(5916)
(7) (3分)
N ( 2a)31030
A
解析:(1)Ni为28号元素,价电子排布式为3d84s2。故答案为:3d84s2。
(2)“部分除铜”工序中,硫代硫酸钠与铜离子反应生成铜单质,根据生成了硫酸铅以及之后
的“除硫酸根”流程可以推测该步氧化产物为硫酸根。故答案为:
4Cu2 S O2 H O 4Cu2SO2 10H。
2 3 2 4
(3)M物质作用为调节pH,故M物质显碱性,但 M物质不是烧碱,因为烧碱碱性太强,
无法准确控制Cr3与Ni2分解沉淀。结合流程箭头方向和给出的K Ni(OH) 和
sp 2
K Cr(OH) 大小可以推测,M物质为沉镍流程的产物Ni(OH) 。故答案为:Ni(OH) 。
sp 3 2 2
(4)由“部分除铜”可以推测铜离子未被除尽,而铅离子已在之前的步骤中与SO2反应生成
4
了PbSO 被除去,故滤渣Ⅱ中除ZnS外,应当还有CuS。故答案为:CuS。
4
(5)“酸解”步骤中Fe元素转化为Fe3,而后在“部分除铜”步骤中,硫代硫酸钠将Fe3还原
为Fe2,导致Fe元素难以沉淀,故“沉铁”步骤中需要用双氧水将Fe2氧化为Fe3。由于上一
步“调pH”中已经用NiCO 将溶液pH调高,故Fe3会生成沉淀而被除去。故答案为:将Fe2
3
氧化为Fe3,使其转化为Fe(OH) 沉淀除去。
3
(6)硝酸镍的阴离子为硝酸根,其空间构型为平面三角形,故答案为:平面三角形。
(7)由晶胞结构图可知,Ni的配位数为6,故第一空填:6;由几何关系知,晶胞参数为
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
m M 4(5916) 4(5916)
2a,由 ,m 解得晶胞密度为 。故答案为 。
v N N ( 2a)31030 N ( 2a)31030
A A A
17.(12分)答案:(1)CH O结合H的能力比OH强(2分)
3
(2)AB(2分)
(3)6.22(2分)
(4)操作安全,原料便宜易得水的沸点是100℃,温度高于100℃时,有利于水的汽化,提
高CH ONa 的平衡产率(或温度太高会使设备内压强增大,对设备要求更高,成本更高或升
3
高温度平衡逆向移动,不利于产物的生成)(2分)
(5)-13.09(2分)
(6)CH OH蒸气通入量越大碱液中的醇碱比越小适当减小碱液中的醇碱比,增大CH OH蒸
3 3
气通入量(2分)
解析:(1)CH OH是非电解质,H O是弱电解质,CH OH比H O更易以分子形式存在于
3 2 3 2
水中,所以CH O结合H的能力比OH强,CH ONa 的碱性比NaOH的碱性强。
3 3
(2)不断补充CH OH,平衡正向移动,有利于提高CH ONa 的含量,A符合题意;将H O
3 3 2
汽化移出,会使平衡正向移动,有利于提高CH ONa 的含量,B符合题意;由题表中数据可
3
知,升高温度,K减小,说明平衡逆向移动,CH ONa 的含量降低,C不符合题意。
3
(3)100℃时,设起始时CH OH与NaOH的物质的量分别为5 x mol、 x mol, t 时刻
3
CH OH转化的物质的量为 y mol,则可列“三段式”:
3
CH OH(aq)NaOH(aq)‡ˆ ˆˆ†ˆ CH ONa(aq)H O(l)
3 3 2
起始量/mol 5x x 0 0
转化量/mol y y y y
t时刻/mol 5x y x y y y
y
由题表可知,100℃时H O的物质的量分数为0.0518,则有 0.0518,故CH OH的转化率
2 6x 3
y
为 100%6.22%。
5x
(4)钠法合成CH ONa 的同时产生H ,且金属Na较活泼,反应剧烈,不如碱法合成
3 2
CH ONa 安全;原料NaOH便宜易得。水的沸点是 100℃,温度高于100℃时有利于水的汽
3
化,提高CH ONa 的平衡产率;温度太高会使设备内压强增大,对设备要求更高,成本更
3
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
高;升高温度平衡逆向移动,不利于产物的生成。
(5)由盖斯定律可知,H H H H H 54.62kJmol1
1 2 3 4
76.84kJmol1 12.13kJmol1 3kJmol1 13.09kJmol1。
(6)由题图可知,碱液中的醇碱比一定时,,CH OH蒸气通入量越大,NaOH的转化率越
3
大;CH OH蒸气通入量一定时,不同曲线对应的NaOH转化率不同,画一条垂直于横坐标的
3
辅助线,由该线与不同曲线的交点可看出,碱液中的醇碱比越小,NaOH的转化率越大;结
合题给①②③可知,为提高 NaOH的转化率,可以采用的方式是适当减小碱液中的醇碱
比,增大CH OH蒸气通入量。
3
18.(15分)答案:(1)取代反应(或磺化反应)(1分)
(2)CO (或HCl)(1分);(酚)羟基(1分)
2
(3)邻二氯苯(或1,2-二氯苯)(2分)
(4) (2分)
(5)2(2分)
(6)3(2分)
(7) (4分)
解析:由A→B的反应条件及B的分子式可知,A→B发生取代反应,并结合C的结构简式
可知,B的结构简式为 ;由E→F的反应条件,结合F的分子式及已知信息可知,F
的结构简式为 。
(1)A( )在浓硫酸、70~80℃条件下发生取代反应生成B( )。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(2)对比C( )和D( )的结构简式可知,向 C中通入CO 或HCl
2
气体发生强酸制弱酸的反应,可以得到D。D分子中含氧官能团为(酚)羟基。
(3) 的化学名称是邻二氯苯或1,2-二氯苯。
(4)由上述分析可知,由E生成F的化学方程式为
。
(5)与4个各不相同的原子或原子团相连的碳原子称为手性碳原子,故G
( ,标“*”的为手性碳原子)中有 2个手性碳原子。
(6)由A的结构简式可知,其分子式为C H (7),由A的同分异构体“苯环上只有1个
10 8
取代基”知,分子中含有 (4),剩余4个碳原子和3个不饱和度,由“不能被氧化
为苯甲酸”知,与苯环直接相连的碳原子上没有氢原子,结合“不含C C C”“存在2个环状
结构”可知,取代基可能为 ,故满足条件的A的同分异构体
有3种。
(7)由甲苯合成对羟基苯甲酸,需要在苯环上引入—OH和—COOH,可通过苯环上—CH
3
被酸性KMnO 溶液氧化引入—COOH,引入—OH可通过A→C的反应再酸化来实现,—OH
4
易被氧化,故应先引入—COOH,再引入—OH,由此可得合成路线。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002