文档内容
高三化学参考答案
【答案】
1. C
【解析】 肥皂水 弱碱性 可与酸性物质反应 可减轻蚊虫叮咬引起的痛痒症状
A. ( ) , ,A
正确
;
食品中添加适量的二氧化硫可以起到漂白 防腐和抗氧化等作用 但要在合理范围
B. 、 ,
内 正确
,B ;
燃煤中加入生石灰或石灰石可以减少二氧化硫的量 但是不能吸收二氧化碳 故不能
C. , ,
减少温室效应 错误
,C ;
铝比铁活泼 海水浸泡区的铝基为负极发生氧化反应 铁为正极被保护 可保障船体
D. , 、 ,
不易腐蚀 利用了牺牲阳极的保护法 正确
, ,D 。
【答案】
2. C
【解析】 与稀硫酸反应生成氢气可排出空气 但无法使硫酸亚铁溶液与 接
A.Fe , NaOH
触 则不能制备氢氧化亚铁 错误
, ,A ;
氨气极易溶于水 所以通氨气的导管不能插入液面下 二氧化碳溶解度小 所以应插
B. , , ,
入液面下 错误
,B ;
乙醇易挥发 挥发出来的乙醇可以使酸性高锰酸钾溶液褪色 正确
C. , ,C ;
制备 晶体应通入 错误
D. FeCl3•6H2O HCl,D 。
【答案】
3. A
【解析】 缺角的明矾晶体在其饱和溶液中慢慢变为完整的规则晶体 是由于晶体在
A. ,
饱和溶液中存在溶解和结晶平衡 最终使晶体形成规则的几何外形 从内部结构上讲是
, ,
由于晶体微粒有规则的排列 即晶体具有自范性 正确
, ,A ;
石墨能导电而金刚石不导电 是由于在石墨中 原子采用 杂化 在层内 原子之
2
B. , C sp , C
间以 键形成平面正六边形结构 每个 有一个未参与杂化的 电子可在整个
C-C , C 2p C
原子平面中运动 而金刚石中 原子采用 杂化 形成了立体网状结构 没有自由移动
3
; C sp , ,
的电子 因此石墨导电而金刚石不导电 错误
, ,B ;
酸性 不是因为 的非金属性强于 而是因为 中非羟基氧
C. :H3PO4>HClO, P Cl, H3PO4
原子数比 多 使 中 键极性更强 更易电离出 实际上 的非
+
HClO , H3PO4 O - H , H , Cl
金属性强于 错误
P,C ;
能与水形成氢键 而 与水不能形成氢键 所以水溶性
D.C2H5OH , CH3OCH3 , C2H5OH
错误
> CH3OCH3,D 。
【答案】
4. D
【解析】 醋酸为弱电解质 工人用食醋除铁锈的离子方程式为 x
A. , :Fe2O3· H2O+
3+ x - 错误
6CH3COOH2Fe + +3 H2O+6CH3COO ,A ;
泡沫灭火器原料是硫酸铝和碳酸氢钠 发生反应生成氢氧化铝和二氧化碳 灭火的原
B. , ,
理 错误
3+ -
:Al +3HCO3 Al OH 3↓+3CO2↑,B ;
高三化学参考答案 第 页(共 页)
1 10惰性电极电解氯化镁溶液 阴极生成的氢氧根离子会结合 生成 沉
2+
C. , Mg Mg(OH)2
通电
淀 正确的离子方程式为
- 2+
, :2Cl +2H2O+Mg Cl2↑+H2↑+Mg(OH)2↓,C
错误
;
溶液与少量 反应 氯气被还原为氯离子 部分亚硫酸根被氧化为硫酸根
D.Na2SO3 Cl2 , , ,
同时生成的氢离子与亚硫酸根结合成 反应离子方程式为
- 2-
HSO3 , :3SO3 +Cl2+
正确
- - 2-
H2O2HSO3 +2Cl +SO4 ,D 。
【答案】
5. C
【分析】 为原子序数依次增大的元素 原子中分别有 个运动状
X、Y、Z、W、R 。X、Z 1、7
态完全不同的电子 则 为 元素 为 元素 原子最外层电子数等于其电子层
, X H 、Z N ;Y
数 符合条件的元素是铍 原子最外层电子数是内层的 倍 则 的电子排布为
, (Be);W 3 , W
为 元素 为第四周期金属元素 基态原子无未成对电子且内层电子全满 则
2、6,W O ;R , ,
为 元素 从而得出 分别为
R Zn 。 X、Y、Z、W、R H、Be、N、O、Zn。
【解析】 是 是 的简单氢化物 中 原子价层电子对数
A.Z N,Y Be,Z(N) NH3 ,N =3+
5-3×1 采取 3 杂化 为 其氯化物 中 原子价层电子对数
=4, sp ;Y Be, BeCl2 ,Be =2+
2
2-2×1 采取 杂化 二者杂化方式不同 错误
=2, sp , ,A ;
2
分别为 三者属于同周期元素 的 轨道半充满 第一电离能反
B.Y、Z、W Be、N、O, ,N 2p ,
常 则第一电离能 错误
, :II(N)>I1(O)>I1(Be),B ;
根据元素周期律 同周期从左到右元素非金属性增强 非金属性越强 气态氢化物越
C. , , ,
稳定 所以稳定性 又因为 分子间都存在氢键 且 分子间氢
, H2O>NH3; H2O、NH3 , H2O
键数目更多 所以沸点也是 正确
, H2O>NH3,C ;
一个 离子中 共价键 配位键都属于 键 则 键数为
2+ 2+
D. Zn NH3 4 ,N-H 、N-Zn σ , σ
错误
4×4=16,D 。
【答案】
6. D
【解析】 分子中含有 键 易溶于水的原因可能是 能与水分
A.N2H4 N-H ,N2H4 N2H4
子形成分子间氢键 正确
,A ;
中心 原子有 对孤电子对 中心 原子有 对孤电子对 孤电子对数
B.N2H4 N 1 ,H2O O 2 ,
越多 孤电子对与成键电子对之间的斥力越大 所以 中 键角大于
, , N2H4 H-N-H H2O
中 键角 正确
H-O-H ,B ;
个 中含有 个氮氮键 的物质的量为 50g
C.1 N2H4·H2O 1 ,50gN2H4·H2O =1
50g/mol
含有氮氮键的数目为N 正确
mol, A,C ;
肼中存在 极性键 也有 非极性键 错误
D. N-H , N-N ,D 。
【答案】
7. B
高三化学参考答案 第 页(共 页)
2 10【解析】 根据盖斯定律可知 反应 反应 得
A. , I+ II :2NH3(l)+CO2(g)H2O(l)+
H 错误
CO(NH2)2(1)Δ =(a+b)kJ/mol,A ;
氯气与烧碱溶液的反应是放热反应 温度升高发生副反应生成 所以步骤
B. , NaClO3, Ⅰ
中为避免温度过高发生副反应 可采用冰水浴 正确
, ,B ;
将尿素滴到 溶液中或过快滴加 都会使过量的 溶液氧化水合肼 降低
C. NaClO , NaClO ,
产率 故实验中应将次氯酸钠溶液逐滴加入定量的尿素溶液中制备水合肼 滴加顺序不
, ,
能颠倒 且滴加速度不能过快 错误
, ,C ;
已知 酸性与醋酸相当 其酸性大于碳酸 无法制取 错误
D. HN3 , , ,D 。
【答案】
8. C
【解析】 由结构知 分子中的所有碳原子可能共平面 正确
A. , ,A ;
该分子中含有碳碳双键可发生加聚 正确
B. ,B ;
该分子与足量的氢气加成后生成 没有手性碳原子
C. , ,C
错误
;
醛基具有还原性 则该有机物可以做保鲜剂可能是因为它具有较强的还原性
D. , ,D
正确
。
【答案】
9. B
【解析】 加热 气体颜色加深 说明平衡逆向移动 正反应为
A. 2NO2 g N2O4 g , , ,
放热反应 即 H 正反应活化能 逆反应活化能 所以活化能 正反应 逆反应
, Δ = - <0, : < ,A
错误
;
溶液为蓝色是因为水与铜离子形成配合物 加入少量氯化钠固体 振
2+
B. [Cu(H2O)4] , ,
荡 溶液变为黄绿色 是因为生成 反应原理为
2- 2+ -
, , [CuCl4] , : Cu H2O 4 +4Cl
说明配位键的稳定性 正确
2- 2- 2+
CuCl4 +4H2O, : CuCl4 > Cu H2O 4 ,B ;
若变质 反应后溶液中生成的铁离子能与过量铁反应生成亚铁离子 则滴加硫氰化钾
C. , ,
溶液 溶液也不能变红 故不能说明铁粉样品未变质 错误
, , ,C ;
中 水 解 会 消 耗
+ + +
D.CH3COONH4 NH4 ,NH4 + H2O NH3 · H2 O+H ,
水解生成的 测定相同浓度的 和 溶液的
- -
CH3COO OH , NaHCO3 CH3COONH4 pH,
前者大于后者 不能说明K - K - 错误
, h HCO3 > h CH3COO ,D 。
【答案】
10. C
【分析】 废锌催化剂 主要成分为 及少量 酸浸时
( ZnO Fe2O3、FeO、MnO、PbO、SiO2) ,
二氧化硅不反应 金属氧化物与酸反应 只有硫酸铅沉淀 其他形成盐溶液 加入过二
, , , ,
硫酸钾发生氧化还原反应 生成二氧化锰沉淀 加氧化锌调 沉淀出铁元素 滤液为
, , pH, ,
硫酸锌 电解得到锌
, 。
【解析】 废锌催化剂研磨成粉末可以增大固体的表面积 有利于增大反应物的接触
A. ,
面积 加快浸取速率 正确
, ,A ;
根据分析 滤渣的主要成分为未反应的二氧化硅和反应生成的硫酸铅 正确
B. , ,B ;
高三化学参考答案 第 页(共 页)
3 10生成 的反应中 过二硫酸钾作氧化剂 二价锰离子被氧化 体系内有酸 所以
C. MnO2 , , , ,
离子方程式为 错误
2- 2+ 2- +
:S2O8 +Mn +2H2OMnO2↓+2SO4 +4H ,C ;
电解积液中含有硫酸等物质可在酸浸步骤循环利用 正确
D. ,D 。
【答案】
11. A
【解析】 容器 中达到平衡时 消耗的氢气的物质的量为36.88×3 因此
A. ① , =1.2mol,
92.2
反应的化学反应速率为v 1.2 容器体积V 所以v
(H2)=Vt mol/(L·min), =1L, (H2)
1
1.2 正确
=t mol/(L·min),A ;
1
由题意可知 中反应温度相同 故平衡常数K 的数值相同 错误
B. ,①② , ,B ;
容器 中恒温恒压 容器 中恒温恒容 容器 相当于在 的基础上加压 加压达到
C. ② , ① , ② ① ,
平衡所需时间缩短 平衡右移 反应放出的热量增多 故t t 错误
, , , 2< 1,Q>36.88kJ,C ;
容器 中达到平衡时 消耗的氢气的物质的量为 列三段式
D. ① , 1.2mol, :
N2 g +3H2 g 2NH3 g
起始
/mol 1 4 0
变化量
/mol 0.4 1.2 0.8
平衡时
/mol 0.6 2.8 0.8
平衡时n 总
( )=0.6+2.8+0.8=4.2mol
P
平
4.2
P 始= =0.84,
5
v 逆 v 正 错误
( )= ( ),D 。
【答案】
12. C
【分析】 太阳光照射 电极上 敏化后的 失去电子为原电池的负极 电极
TiO2 , TiO2 ,Pt
为正极
。
【解析】 由题可知 在特定光线照射下产生电流 所以电池工作时涉及光能转化为
A. , ,
电能 并非仅光能向化学能转化 错误
, ,A ;
太阳光照下 敏化后的 产生电子 和空穴 即敏化 电极失电子为
- +
B. , TiO2 e h , TiO2
负极 外电路中 电子从负极 敏化 电极 流向正极 电极 错误
, , ( TiO2 ) (Pt ),B ;
电极为正极 发生得电子还原反应 电极电极反应为
- - -
C.Pt , ,Pt :I3 +2e 3I ,C
正确
;
在元素周期表中的位置为第五周期第 族 其所在周期中 电负性最强的元素
D.44Ru Ⅷ , ,
是 的价层电子排布式为 错误
2 5
I,I 5s5p,D 。
【答案】
13. B
【解析】 中 2- 为 个 3+ 为 个 2+ 为 1 1 中 2- 为 个 2+ 为
A.B O 4 ,Fe 4 ,Fe 4× = ,A O 4 ,Fe
8 2
高三化学参考答案 第 页(共 页)
4 101 3 晶胞中含有 个 和 个 则晶胞中 2- 为 个 3+
1+4× = , 4 A 4 B, O 4×(4+4)=32 ,Fe
8 2
为 个 2+ 为 1 3 与 个数比为 正确
4×4=16 ,Fe 4×( + )=8,Fe O 24∶32=3∶4,A ;
2 2
放电时正极上得电子同时嵌入 的脱嵌过程为该电池的充电过程 错误
+ +
B. Li ,Li ,B ;
由 正方体单元的图可知 体心处的 位于 形成的正四面体空隙中
2+ 2-
C. A , Fe O ,C
正确
;
当 嵌入晶胞体心和所有棱心 一个晶胞中含有 为 个 为 个 为
+ + 2-
D. Li , :Li 4 ,Fe 24 ,O
个 则该锂电池正极材料的化学式为 正确
32 , LiFe6O8,D 。
【答案】
14. C
K
【解析】 由K c 2+ c2 - 可得c 2+ sp M(OH)2
A. sp M(OH)2 = M · OH M = c2 - =
OH
K
sp M(OH)2
-14
1×10
c +
H
高三化学参考答案 第 页(共 页)
5 10
c2 + K
H · sp M(OH)2 则 2+
2 = -28 , pM = -lgc M = 2pH -
1×10
K 故曲线 表示难溶物 的溶解平衡曲线 曲线 表示难
lg sp M(OH)2 -28, Ⅱ M(OH)2 , Ⅰ
溶物 的溶解平衡曲线 正确
MA ,A ;
由图可知 点溶液中c 2- -1c + -10.2 -1 常
B. ,M (A )≈0.05mol•L ,(H )≈10 mol•L ,
温下K -14 所以c - -3.8 -1 故c 2- c -
W=1×10 , (OH )=10 mol•L , (A )> (OH ),B
正确
;
根据元素质量守恒 从c + c 2- c - c
C. , (Na )=2×[(A )+ (HA )+ (H2A)],pH=10.5
时c - c 2- c + c - c 所以c + c -
, HA = A ,(Na )=4 (HA )+2 (H2A), Na >3 HA ,C
错误
;
由图 可知 溶液的 接近 溶液的
1 -1
D. 2 ,0.1mol•L NaHA pH 8,0.1mol•L Na2A
接近 时 优先于 生成沉淀 故选 溶
-1
pH 12,pH=10 ,MA M(OH)2 , 0.1mol•L NaHA
液效果好 正确
,D 。
分
15.(14 )
【答案】 分
(1)9(2 )
提供 与 形成稳定的配离子 促进金溶解 分
- 3+ -
(2) Cl Au [AuCl4] , (2 )
或 分
3
8×10 8000(2 )
分
2- - -
(3)①4NO2+O2+4CO3 +2H2O4NO3 +4HCO3 (2 )
催化剂
分
②2NH3+NO +NO22N2+3H2O(2 )
抑制氢离子在阴极放电 减少电镀过程中氢气的产生 合理即可 分
(4) , ( ,2 )
分
(5)131.3(2 )
【解析】 基态 中最高能层为 能层有 能级 共 个轨道
2+
(1) Cu M,M 3s3p3d , 9 。金与硝酸反应生成 与 形成配离子 使 浓度降低 促进金与硝
3+ - 3+ 3+
(2) Au ,Cl Au , Au ,
酸反应的平衡正向移动 反应 为反应 反应 则K K K -8
。 ③ 1+ 2, 3= 1× 2=2×10 ×4×
11 K 值越大 反应进行程度越大 故答案为
10 =8000, , ; :8000。
利用 溶液吸收 并通入空气使之全部转化为 利用碳酸钠
(3)① Na2CO3 NO2, NaNO3,
溶液吸收 碳酸钠溶液过量 所以生成碳酸氢钠 离子方程式为
2-
, , , :4NO2+O2+4CO3 +
由图可知 生成 的反应的离子方程式为
- -
2H2O4NO3 +4HCO3 ;② , X [(NH4)2
由电荷守恒和原子守恒可知 为
2+ + +
(NO2)] +NO[(NH4)(HNO2)] +H +X, ,X
催化剂
和 总反应的化学方程式为
N2 H2O, 2NH3+NO +NO22N2+3H2O;
为减少电镀时产生气体并提高镀层的质量 电镀液中常会加入醋酸钠 醋酸钠可结
(4) , ,
合溶液中的氢离子 降低氢离子浓度 从而抑制氢离子在阴极放电 减少电镀过程中氢
, , ,
气的产生
;
草酸和 反应时的关系 理论上消耗 草酸
(5) HAuCl4 2HAuCl4~3H2C2O4, 1mol
可得到 的物质的量为2 质量为2 故答
(H2C2O4) Au mol, mol×197g/mol≈131.3g,
3 3
案为
:131.3。
分
16.(15 )
【答案】 试纸由蓝色变为黑色 答出 黑色 即可得分 分
(1)CuSO4 ( “ ” ,2 )
分
NaHCO3、NaHS(2 )
浓 分
(2)Na2SO3+H2SO4( )Na2SO4+SO2↑+H2O(2 )
若浓度高于 溶液中氢离子浓度小 反应速率慢 不利于二氧化硫的生成 若浓度
70%, , , ;
低于 易溶于水的二氧化硫气体溶于水 不利于二氧化硫的逸出 合理即可 分
70%, , ( ,2 )
分
(3)d(1 )
滴入最后半滴硫代硫酸钠样品溶液时 溶液蓝色褪去 且 不恢复原色 分
(4)① , , 30s (2 )
cV
1500 分 漏选得 分 分
② m %(2 ) ③BC( 1 ,2 )
【解析】 当观察 试纸由蓝色变为黑色 可知此时有 气体逸出 据此判
(1) CuSO4 , H2S ,
断高炉煤气过量 可关闭 停止通入高炉煤气 根据 大小可知酸性
, K3, ; Ka :H2CO3>
则 与碳酸钠溶液反应可生成 因此三颈烧
- -
H2S>HCO3 >HS ; H2S NaHCO3、NaHS,
瓶中溶质的化学成分为
NaHCO3、NaHS;
若浓度高于 溶液中氢离子浓度小 反应速率慢 不利于二氧化硫的生成 若
(2) 70%, , , ;
浓度低于 易溶于水的二氧化硫气体溶于水 不利于二氧化硫的逸出
70%, ,
难溶于乙醇 洗涤时为尽可能避免产品溶解导致损失 则可用乙醇洗涤
(3)Na2S2O3 , , ,
选
d;
碘单质遇淀粉变蓝 所以滴定终点是滴入最后半滴硫代硫酸钠样品溶液时 溶液
(4)① , ,
蓝色褪去 且 不恢复原色
, 30s 。
高三化学参考答案 第 页(共 页)
6 10由测定数据可知 第 次实验所测数据误差较大 应删去 则反应消耗硫代硫酸钠溶
② , 2 , ,
液的体积为24.79mL+24.81mL 由方程式可得如下关系
2-
=24.80mL, :Cr2O7 ~3I2
2
2- 则m 该产品中含有的 的质量为 c V
~6S2O3 , g Na2S2O3·5H2O 6× mol/L× ×
cV cV
-3 250 cV 则样品纯度为15 1500
10 L× ×248g/mol=15 g, m ×100%= m %;
24.80
配制硫代硫酸钠样品溶液溶液时 仰视容量瓶的刻度线 溶液体积偏大 使配制溶
③A. , , ,
液的浓度偏低 溶液中 的质量偏小 所以
,250mL Na2S2O3·5H2O , Na2S2O3·5H2O
的纯度偏低 错误
,A ;
装 标准液的酸式滴定管洗涤后若未润洗 则 标准液的浓度偏低
B. K2Cr2O7 , K2Cr2O7 ,
根据关系 可知消耗 溶液体积偏小 所以
2- 2-
:Cr2O7 ~3I2~6S2O3 Na2S2O3 , Na2S2O3·
的纯度偏高 故 正确
5H2O , B ;
量取 标准液时 开始有气泡 终点无气泡 使量取 体积偏小 消耗
C. K2Cr2O7 , , , K2Cr2O7 ,
溶液体积偏小 所以 的纯度偏高 故 正确
Na2S2O3 , Na2S2O3·5H2O , C ;
容量瓶洗涤干净后 瓶内壁有少量水滴 对溶液配制过程中溶质的物质的量和溶液
D. , ,
体积都没有影响 所配溶液浓度不变 对测定结果无影响 错误
, , ,D 。
分
17.(14 )
【答案】 漏选得 分 分
(1)BC( 1 ,2 )
分
(2)①L1(2 )
反应 为吸热反应 升高温度 平衡正向移动 的物质的量增大 反应 为放热反
Ⅱ , , ,CO , Ⅰ
应 升高温度 平衡逆向移动 的物质的量减小 根据 的选择性公式 升高温
, , ,C2H2 , CO ,
度 选择性增大 合理即可 分
,CO ( ,2 )
1 分
② (2 )
3
分 分
- - 2-
(3)CH2=CH2-12e +16OH 2CO3 +10H2O(2 ) 6.72(2 )
分
(4)<(2 )
【解析】 v v 正逆反应速率不相等 反应未达平衡状态 故
(1)A. 逆 CO2 =3 正 H2 , , , A
错误
;
反应前后气体分子数不同 当体系内压强保持不变 反应达平衡状态 故 正确
B. , , , B ;
的体积分数保持不变 说明 的浓度不再变化 正逆反应速率相等 反应达
C.CO2 , CO2 , ,
到平衡状态 故 正确
, C ;
断裂 键即消耗 氢气 同时断裂 即消耗 水 正
D. 3molH-H 3mol , 4molH-O 2mol ,
逆反应速率相等 反应达到平衡状态 故 错误
, , D 。
反应 为放热反应 反应 为吸热反应 达到平衡时 随温度升高 反应 平衡逆向
(2) Ⅰ , Ⅱ , , , Ⅰ
移动n 减少 反应 的平衡正向移动 n 增大 根据 选择性定义可知
,(C2H4) , Ⅱ ,(CO) , CO ,
随着温度的升高 的选择性增大 推出 代表平衡时 的选择性随温度变化
,CO , L1 CO ,L2
高三化学参考答案 第 页(共 页)
7 10代表 平衡转化率随温度变化
CO2 ;
根据图像可知 随着温度升高 先减小后增大 其原因是温度较低时 以反应 为
① ,L2 , , , Ⅰ
主 反应 放热 温度升高 的平衡转化率下降 温度较高时 以反应 为主 反应
, Ⅰ , ,CO2 ; , Ⅱ ,
吸热 温度升高 的平衡转化率增大
Ⅱ , ,CO2 ;
根据图像可知 合成乙烯的适宜温度为 的理由是温度过低 反应速率太慢 温
② , 500K , ;
度过高 的选择性过大 乙烯的选择性较小 时 的平衡转化率为
,CO , ;500K ,CO2 50%,
则消耗n 令生成乙烯的物质的量为x 反应 中
(CO2)=3mol×50%=1.5mol, mol, Ⅰ
消耗 氢气物质的量分别为 x x 生成水蒸气物质的量为 x 反应
CO2、 2 mol、6 mol, 4 mol,
中消耗 物质的量为 x 消耗氢气物质的量为 x 生成
Ⅱ CO2 (1.5-2 )mol, (1.5-2 )mol,
x
物质的量均为 x 则有 1.5-2 解得x
CO、H2O (1.5-2 )mol, x x×100%=50%, =0.5
1.5-2 +
因此n n n n
mol, (CO2)=1.5mol, (C2H4)=0.5mol, (CO)=0.5mol, (H2O)=2.5
n 反应 中各组分系数为 用物质的量可以代替物质的量分数
mol,(H2)=2.5mol; Ⅱ 1, ,
因此该反应的平衡常数K 2.5×0.5 1
x = = ;
2.5×1.5 3
燃料电池 通入燃料的一极为负极 乙烯在负极失电子 由于介质为碱性 故乙烯在
(3) , , , ,
负极失电子后生成碳酸根和水 电极方程式为
- - 2-
, CH2=CH2-12e +16OH 2CO3
分子 在正极得 个电子生成 故当电路中通过 电子时
-
+10H2O;1 O2 4 OH , 1.2mol ,
消耗氧气物质的量为 标准状况下的体积为
0.3mol, 6.72L;
(4) 当反应达到平衡时 , v = k 正· p2 (CO2)· p6 (H2)- k 逆· p4 (H2O)· p (C2H4)=0,
即有 k 正 p4 (H2O)· p (C2H4) K 将数值代入 得出T 的平衡常数为 T
k 逆=p2 p6 = , , 1℃ 1.2, 2℃
(CO2)· (H2)
的平衡常数为 该反应为放热反应 升高温度平衡逆向进行 平衡常数减小 得到
0.8, , , ,
T T 故答案为
1℃< 2℃, <。
分
18.(15 )
【答案】 二羟基苯甲醛 分 羟基 酮 羰基 分
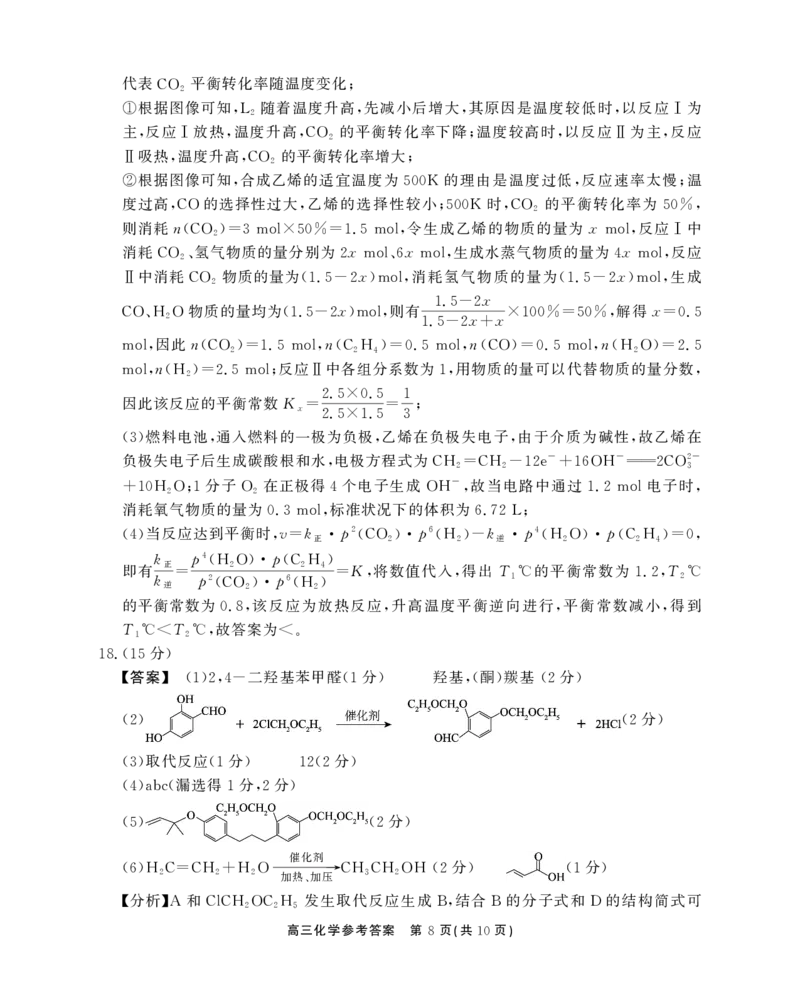
(1)2,4- (1 ) ,( ) (2 )
分
(2) (2 )
取代反应 分 分
(3) (1 ) 12(2 )
漏选得 分 分
(4)abc( 1 ,2 )
分
(5) (2 )
催化剂
分 分
(6)H2C=CH2+H2O 加热 加压→CH3CH2OH (2 ) (1 )
、
分析 和 发生取代反应生成 结合 的分子式和 的结构简式可
【 】A ClCH2OC2H5 B, B D
高三化学参考答案 第 页(共 页)
8 10以推知 的结构简式为 和 发生已知信息 的反应原理生
B ,B C i
成 由 的结构简式可知 的结构简式为 发生还原反应生成 由
D, D C ,D E,
的结构简式可知 的结构简式为 和
BroussoninC ,E ,F G
发生取代反应生成 由 的结构简式和 的分子式 可以推知 的结构简
H, H G C5H10O G
式 为 将 转 化 为 生 成 则 为
,J - OCH2OC2H5 - OH Broussonin C, J
发 生 已 知 信 息 的 反 应 原 理 生 成 则 为
,I ii J, I
以此解答
, 。
【解析】 由 的结构简式可知 名称是 二羟基苯甲醛 由分析可知 和
(1) A ,A 2,4- 。 ,B
发生已知信息 的反应原理生成 由 的结构简式可知 的结构简式为
C i D, D C
所以 中官能团的名称是羟基 羰基
, C , 。
由分析可知 反应方程式是
(2) ,A→B
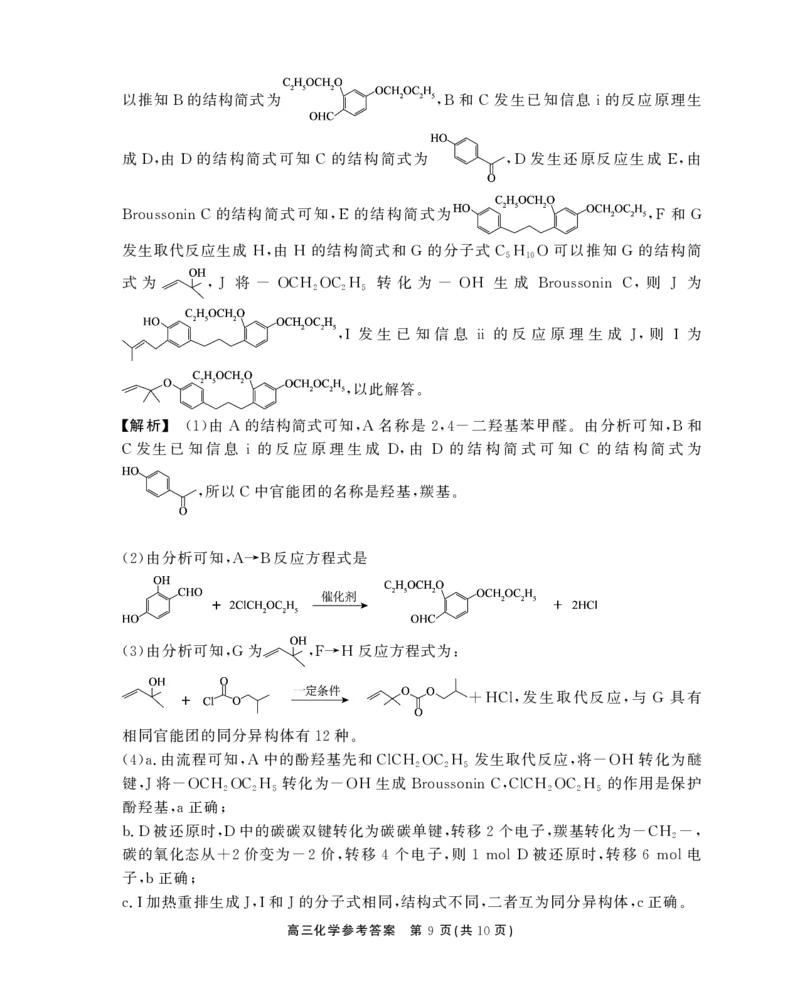
由分析可知 为 反应方程式为
(3) ,G ,F→H :
发生取代反应 与 具有
+HCl, , G
相同官能团的同分异构体有 种
12 。
由流程可知 中的酚羟基先和 发生取代反应 将 转化为醚
(4)a. ,A ClCH2OC2H5 , -OH
键 将 转化为 生成 的作用是保护
,J -OCH2OC2H5 -OH BroussoninC,ClCH2OC2H5
酚羟基 正确
,a ;
被还原时 中的碳碳双键转化为碳碳单键 转移 个电子 羰基转化为
b.D ,D , 2 , -CH2-,
碳的氧化态从 价变为 价 转移 个电子 则 被还原时 转移 电
+2 -2 , 4 , 1molD , 6mol
子 正确
,b ;
加热重排生成 和 的分子式相同 结构式不同 二者互为同分异构体 正确
c.I J,I J , , ,c 。
高三化学参考答案 第 页(共 页)
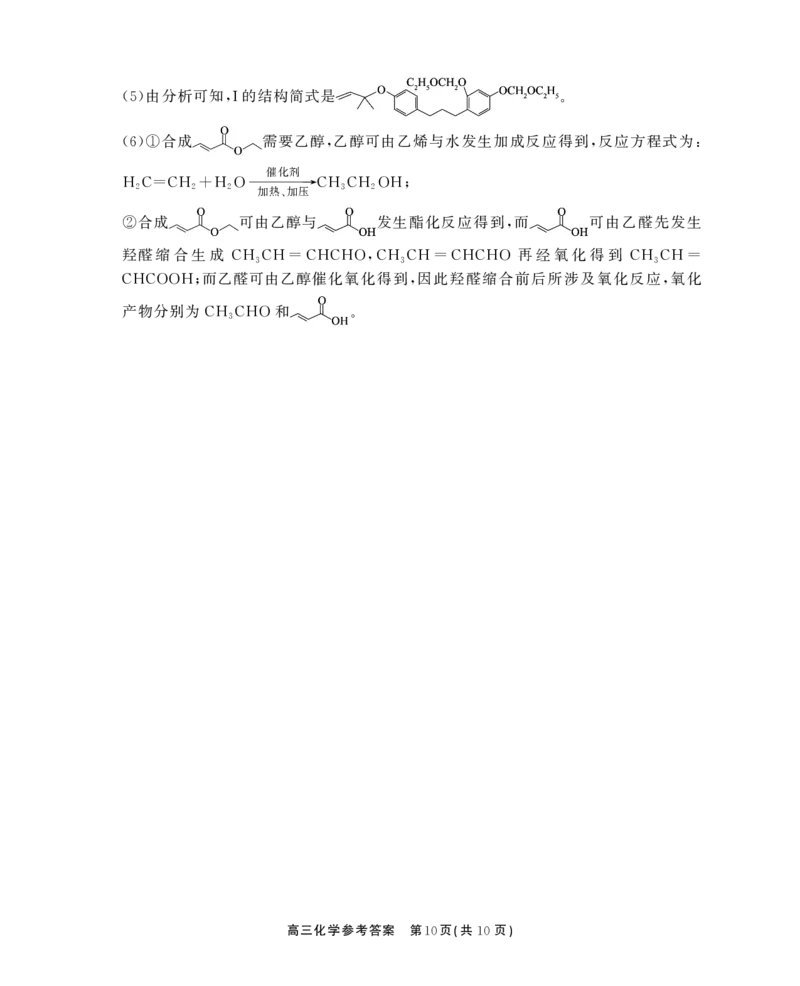
9 10由分析可知 的结构简式是
(5) ,I 。
合成 需要乙醇 乙醇可由乙烯与水发生加成反应得到 反应方程式为
(6)① , , :
催化剂
H2C=CH2+H2O 加热 加压→CH3CH2OH;
、
合成 可由乙醇与 发生酯化反应得到 而 可由乙醛先发生
② ,
羟醛缩合生成 再经氧化得到
CH3CH=CHCHO,CH3CH=CHCHO CH3CH=
而乙醛可由乙醇催化氧化得到 因此羟醛缩合前后所涉及氧化反应 氧化
CHCOOH; , ,
产物分别为 和
CH3CHO 。
高三化学参考答案 第 页(共 页)
1 0 10