文档内容
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 B C D B C A C
题号 8 9 10 11 12 13 14
答案 D C B B D B D
【解析】
1.亚硝酸钠能防腐且能使肉类呈现新鲜的红色,生产加工腊肉、香肠等肉制品时添加亚硝
酸钠,可用作防腐剂和护色剂,A正确。补铁酱油在酱油中加入一种新型铁强化剂乙二胺
四乙酸铁钠,使普通酱油在添加了这种铁强化剂之后具有补充铁元素的功效,属于营养
强化剂,B 错误。包装上有“OTC”标识是非处方药,无需凭医生处方购买和使用,C 正
确。抗坏血酸(即维生素 C)具有还原性,某些食品中添加的微量抗坏血酸(即维生素
C)是一种抗氧化剂,D正确。
2.二氧化硫与碘水反应生成硫酸和氢碘酸,反应的离子方程式为SO I 2H O=
2 2 2
4H+ SO2 2I,故C错误。
4
3.SiO 为共价晶体,和二氧化碳不同,每个 Si原子周围有 4个 O原子,每个 O原子周围有
2
2个 Si原子,Si原子与 O原子之间以单键相连,键角为 109°28′,上述电子式表达错误,
A 错误。2−丁烯的键线式应该为 ,B 错误。H O 的中心原子价层电子对数为
2
621
2 4,价层电子对互斥(VSEPR)模型为四面体结构: ,C 错误。
2
Cl 分子中σ键的形成为p轨道电子云“头碰头”重叠,D正确。
2
4.用石灰沉淀富镁海水中的 Mg2+,生成氢氧化镁,A 错误。将 SO 通入氯化钡溶液至饱
2
和,再加入氯水,亚硫酸被氧化为硫酸,生成硫酸钡沉淀。加入苛性钠溶液,生成亚硫
化学参考答案·第1页(共7页)酸钡沉淀,B 正确。配制氯化铁溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释
到所需要的浓度,C错误。AlCl 溶液与CO 不反应,D错误。
3 2
5.K S O 中,8 个 O 原子中有 6 个显−2 价,2 个显−1 价,发生反应后,O 元素全部显−2
2 2 8
价,则 1个“K S O ”得到 2e−,MnSO 转化为 KMnO ,Mn元素由+2价升高到+7价,失
2 2 8 4 4
去 5e−,依据得失电子守恒,可建立关系式:5K S O ~2MnSO ,再依据质量守恒,便可得
2 2 8 4
到配平的化学方程式为5K S O 2MnSO 8H O=2KMnO 4K SO 8H SO ,据
2 2 8 4 2 4 2 4 2 4
此回答。1 个“K S O ”得到 2e−,1mol 过二硫酸根发生反应,转移电子数为 2N ,A 正
2 2 8 A
确。反应 1mol时,转移 10mol电子,产物中 12mol硫酸根只有 10mol是还原产物,所以
转移 10mol 电子生成还原产物 10N ,B 正确。Mn2中M层电子排布为3s23p63d5,电子
A
数为26513,1molMn2中M层电子数为13N ,C 错误。SO2中硫原子的价层电
A 4
1
子对数为4 (6224)4,故1molSO2中硫原子的价层电子对数为4N ,D正确。
2 4 A
6.冲洗锥形瓶内壁,可保证充分反应,图中操作合理,A正确。实验室用水和电石为原料制
备乙炔,生成的氢氧化钙是糊状物,易导致分液漏斗堵塞,使水面难以升降,无法控制
反应速率,B错误。SO 溶于水,反应产生 H SO ,H SO 电离产生 H+使溶液表现酸性,
2 2 3 2 3
因此将 SO 通入显蓝色的石蕊试液中,能看到溶液变为红色,但 SO 不能使变为红色的溶
2 2
液变为无色,因此只能验证 SO 水溶液的酸性,而不能验证其漂白性,C错误。氨气极易
2
溶于水,导管口在液面下易发生倒吸,D错误。
7.合成过程是羟醛缩合反应,含有活性 α−氢原子的醛在催化剂的作用下与羰基化合物发生
加成,得到 β−羟基醛,并进一步脱水得到 α,β−不饱和醛。A、B正确。先加银氨溶液,
微热,产生银镜现象,说明有醛基;银氨溶液呈碱性,与溴水反应,也能使溴水褪色,
不能证明含有碳碳双键。应该先加盐酸酸化后向滤液中加入溴水,C 错误。1mol 醛基可
以与足量的银氨溶液反应生成2mol单质银,D正确。
8.醋酸易挥发,醋酸与苯酚钠溶液反应也能产生白色浑浊,所以不能比较碳酸、苯酚的酸
性强弱,A错误。NaOH溶液过量,不能证明红褐色 Fe(OH) 沉淀源自 Mg(OH) 沉淀的转
3 2
化学参考答案·第2页(共7页)化,B 错误。葡萄糖与新制氢氧化铜悬浊液反应,NaOH 需要过量,题中所给氢氧化钠量
不足,C 错误。将 SO 通入 FeCl 溶液中,溶液先变为红棕色,一段时间后又变成浅绿
2 3
色,说明 Fe3+与 SO 络合反应速率比氧化还原反应速率快,最终显浅绿色,说明氧化还原
2
反应的平衡常数更大,D正确。
9.短周期元素中,W 的基态原子 s 能级上的电子总数和 p 能级上的电子总数相等,W 可能
为O,也可能为Mg,根据化合物的化学式,W只能为O,W和Z同主族,且属于短周期
元素,则Z为S,Y是同周期离子半径最小的元素,则Y为Al,根据化合价代数为0,则
X 在该化合物中显+1 价,即 X 为 Na,据此分析;O 没有最高正化合价,A 错误。Z、W
简单氢化物的沸点为 H S、H O,常温下水为液体,H S 为气体,沸点:H O>H S,B 错
2 2 2 2 2
622
误。W 为 O ,ZW 为 SO ,价层电子对数为2 3,空间构型为 V 形,SO 、
3 3 2 2 2
2
O 互为等电子体,空间构型相同,均为 V 形,C 正确。Na 和 O 形成 Na O ,含有共价
3 2 2
键,D错误。
10.卤化铵的分解为吸热反应,则H 0,H 对应的为 HX 化学键断裂过程,断裂化学
1 2
键吸收热量,则H 0,A 错误。HCl 的键能大于 HI,故 NH Cl 的H 大于 NH I 的
2 4 2 4
H ,B 正确。H 为 NH 与 H+反应,与 X−无关,C 错误。途径 6 与途径 1、2、3、
2 5 3
4、5 之和的起点和终点相同,结合盖斯定律可知H H H H H H ,
1 2 3 4 5 6
D错误。
11.配合物中心离子 Co2+有 6个 NH 配体,A正确。该晶体由阳离子和阴离子相互作用而形
3
成,属于离子晶体,B 错误。由于孤对电子对成键电子对的排斥力较大,氨气分子中氮
原子含有一对孤对电子,所以配体中 H—N—H 键角>NH 分子,C 正确。氯离子全部在
3
晶胞中,共计是 8 个,该立方晶胞的边长为 a cm,[Co(NH ) ]Cl 的相对分子质量是
3 6 2
4232
232,则该晶体的密度为 g/cm3,D正确。
N a3
A
化学参考答案·第3页(共7页)12.由图可知,a 电极为电解池的阴极,水分子作用下硝酸根离子在阴极得到电子发生还原
反应生成氨和氢氧根离子,b 电极为阳极,氢氧根离子在阳极失去电子发生氧化反应生
成氧气和水,双极膜中水解离出的氢氧根离子移向阳极、氢离子移向阴极。由分析可
知,电解过程中,b 电极为阳极、连接电源正极,电极电势更高,A 错误。由分析可
知,OH移向 b 电极,B 错误。得失电子数守恒,若电极上每有 8mol 电子转移,则只
有 8mol氢离子移向阴极、不可能有 9mol氢离子移向阴极,结合分析可知 a电极为电解
池的阴极,电极反应式为 NO 8e 6H O=NH 9OH,C错误。阳极产生 11.2L
3 2 3
气体(标准状况)即0.5mol氧气时,因为FE(O )为50%,故通过电极的电子的物质的量
2
1
为2 mol50%4 mol,已知 FE(NH )可达 90%,则阴极有4mol 90%0.45mol氨气
3
8
生成,D正确。
13.甘氨酸中含有氨基和羧基,氨基显碱性,羧基显酸性,在酸性条件下,存在的形式为
H NCH COOH ,随着 pH 增大,逐步转化成 H NCH COO ,最终转化成
3 2 3 2
NH CH COO−,从而确定曲线 a 代表H NCH COOH,曲线 b 代表为H NCH COO,
2 2 3 2 3 2
曲线 c代表 NH CH COO−,据上述分析曲线 c代表 NH CH COO−,A正确。等电点是甘
2 2 2 2
氨酸所带正负电荷正好相等,因此 R+=R−,甘氨酸等电点为 5.97,根据图像可知,
R+ −>R+=R− , B 错 误 。 取 M 点 坐 标 ( 2.35 , 0.50 ), 此 时
K 1014
c(H NCH COO)c(H NCH COOH) ,因此有K c(OH) w 1011.65 ,
3 2 3 2 c(H) 102.35
C 正确。pH>9.78 对应溶液是向甘氨酸溶液中加入了 NaOH 溶液,溶液中存在电荷守
恒:c(R+)+c(H+)+c(Na+)=c(R−)+c(OH−),D正确。
14.图中在较高流速下,反应物分子进入反应体系时间较短,反应未达平衡,HCl 转化率主
要由化学反应速率控制,A 正确。由于在流速较低时的转化率视为平衡转化率,
化学参考答案·第4页(共7页)H 0,所以在流速低的时候,温度越高,HCl的转化率越小,故 T 代表的温度为 440
1
℃,T 为 360℃,B 正确。使用高效催化剂,可以增加该温度下的反应速率,使单位时
3
间内 HCl的转化率增加,C正确。由图像可知,N点 HCl的平衡转化率为 80%,设起始
n(HCl)n(O )4mol,可列出三段式
2
1
2HCl(g)+ O (g) Cl (g)+H O(g)
2 2 2 2
起始量/mol 4 4 0 0
变化量/mol 3.2 0.8 1.6 1.6
平衡量/mol 0.8 3.2 1.6 1.6
1.6 1.6
7.2 7.2
则K 6,D错误。
x 1
0.8 2 3.22
7.2 7.2
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共14分)
(1) (1分)
(2)适当升温、搅拌、适当增加盐酸浓度等(合理即可)
(3)SiO (1分)
2
(4)8.01022
(5)2AsCl 3NaH PO 3H O=2As↓3H PO 3NaCl3HCl
3 2 2 2 3 3
(6)2Cl−+4Sb3++5H O=Sb O Cl ↓+10H+
2 4 5 2
Sb O 是一种两性氧化物,溶于氢氧化钠溶液,造成产率降低
2 3
(7)Sb O
4 9
化学参考答案·第5页(共7页)16.(除特殊标注外,每空2分,共15分)
(1)无水CaCl (合理即可)
2
(2)分液漏斗
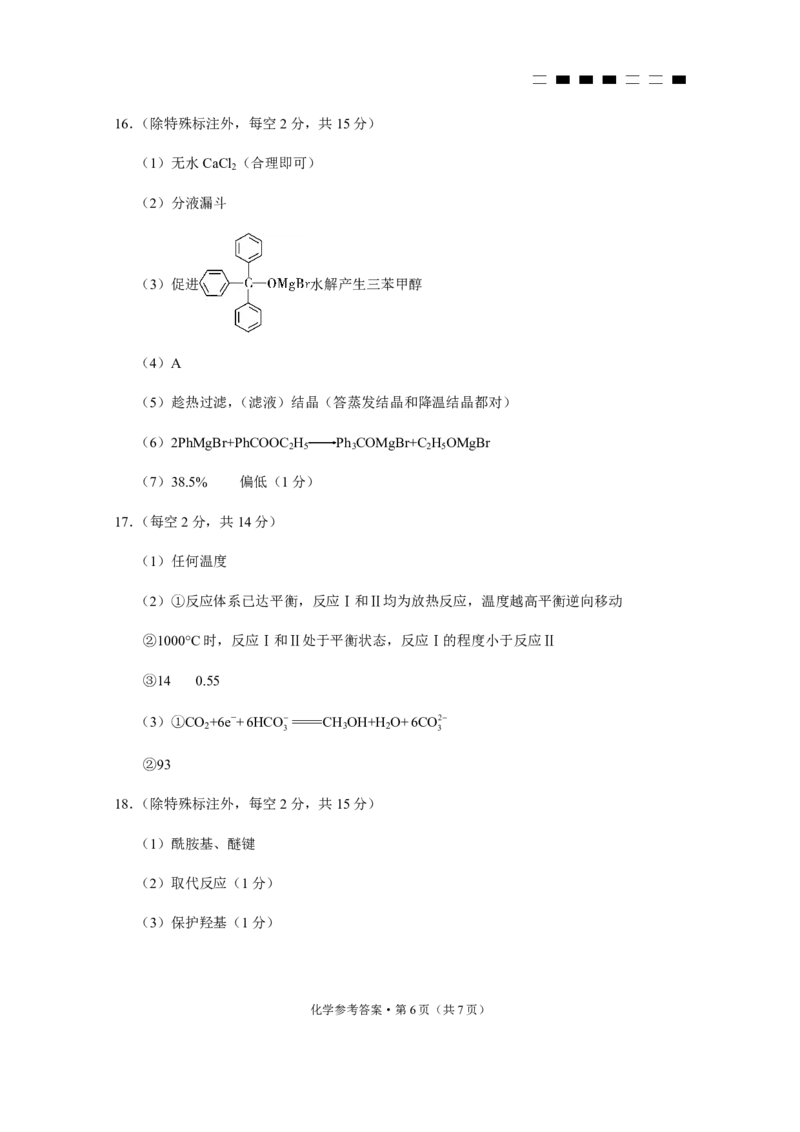
(3)促进 水解产生三苯甲醇
(4)A
(5)趁热过滤,(滤液)结晶(答蒸发结晶和降温结晶都对)
(6)2PhMgBr+PhCOOC H Ph COMgBr+C H OMgBr
2 5 3 2 5
(7)38.5% 偏低(1分)
17.(每空2分,共14分)
(1)任何温度
(2)①反应体系已达平衡,反应Ⅰ和Ⅱ均为放热反应,温度越高平衡逆向移动
②1000°C时,反应Ⅰ和Ⅱ处于平衡状态,反应Ⅰ的程度小于反应Ⅱ
③14 0.55
(3)①CO +6e−+6HCO=CH OH+H O+6CO2
2 3 3 2 3
②93
18.(除特殊标注外,每空2分,共15分)
(1)酰胺基、醚键
(2)取代反应(1分)
(3)保护羟基(1分)
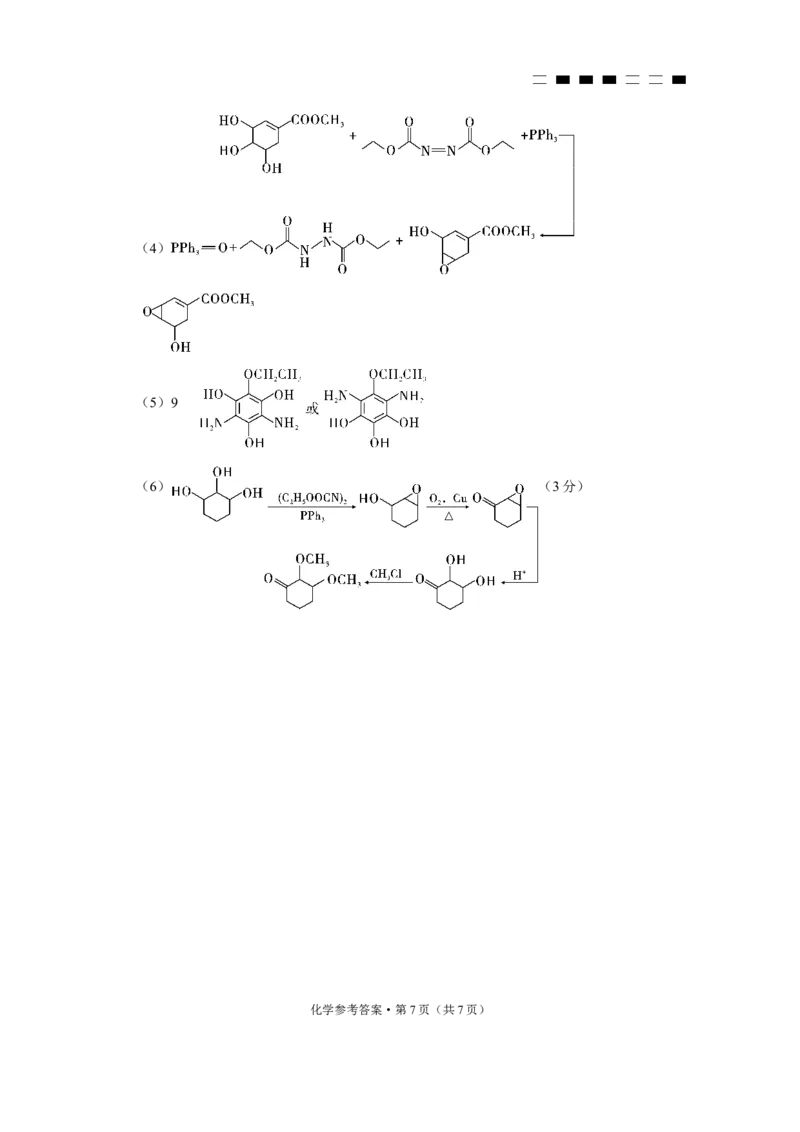
化学参考答案·第6页(共7页)(4)
(5)9
(6) (3分)
化学参考答案·第7页(共7页)