文档内容
2025 年湖北省“新八校”协作体高三 2 月联考
高三化学试卷
命题学校:恩施高中 命题教师:王维 审题学校:龙泉中学 武汉三中
考试时间:2025年2月7日下午14:30-17:05 试卷满分:100分
注意事项:
1. 答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并将准考
证号条形码粘贴在答题卡上的指定位置。
2. 选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写
在试卷、草稿纸和答题卡上的非答题区域均无效。
3. 非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷、草稿
纸和答题卡上的非答题区域均无效。
可能用到的相对原子质量:H:1 O:16 S:32 Fe:56
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1. 下列化学用语或图示表达正确的是
A. 不能表示四氯化碳分子 B.SiO 的电子式:
2
C.石墨的平行六面体晶胞: D.2-甲基-1-丁醇的键线式:
2. 关于物质的鉴别、分离、提纯,下列说法错误的是
A.用过滤法分离Fe(OH) 胶体和FeCl 溶液
3 3
B.分离苯酚和苯先后用NaOH溶液、盐酸
C.用酸性KMnO 溶液检验1-溴丁烷消去产物要先用水洗气
4
D.重油经过减压蒸馏可以得到石蜡油
3. 化学与生活经验密不可分。下列对生活经验的化学原理解释错误的是
选项 生活经验 化学原理
A 明矾水去除青铜器上的铜锈 盐类水解产生的酸与碱式盐反应
B 锡纸装食盐水让银饰由黑变回银色 Sn未经过外电路直接把电子转移给Ag+
C 古代渔民“三天打鱼、两天晒网” 避免水与纤维素中羟基形成氢键
D 打霜后的萝卜白菜味道更甜美 淀粉水解产生葡萄糖
4. 壁虎爬墙是因其脚掌的特殊结构与墙壁产生一种作用力。下列事实可用该作用力解释的是
A.干冰晶体中CO 的配位数为12 B.数九寒冬,水塘中的冰浮在水面
2
C.NaCl具有较高的熔点和沸点 D.金刚石在已知晶体中硬度最大
湖北省新八校教科研协作体*化学试卷(共 8 页)第 1 页5. 基本概念和理论是化学思维的基石。下列叙述正确的是
A.若第八周期按照现有规则填满,则115号元素正下方将是147号元素
B.等离子体是由阴离子、阳离子和电中性微粒组成的一种特殊固体
C.原子轨道就是电子在原子核外的一个运动状态
D.化学反应总是向着自由能减小的方向进行,直到体系达到平衡
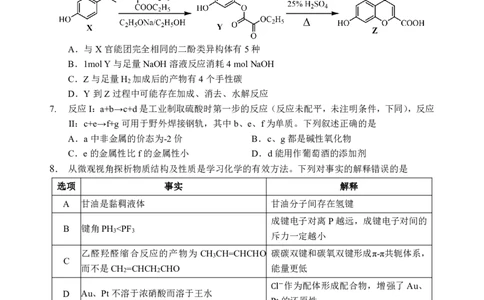
6. 异黄酮类是药用植物的有效成分之一,异黄酮类化合物Z的部分合成路线如图,下列有关说
法错误的是
A.与X官能团完全相同的二酚类异构体有5种
B.1molY与足量NaOH溶液反应消耗4molNaOH
C.Z与足量H 加成后的产物有4个手性碳
2
D.Y到Z过程中可能存在加成、消去、水解反应
7. 反应I:a+b→c+d是工业制取硫酸时第一步的反应(反应未配平,未注明条件,下同),反应
II:c+e→f+g可用于野外焊接钢轨,其中b、e、f为单质。下列叙述正确的是
A.a中非金属的价态为-2价 B.c、g都是碱性氧化物
C.e的金属性比f的金属性小 D.d能用作葡萄酒的添加剂
8. 从微观视角探析物质结构及性质是学习化学的有效方法。下列对事实的解释错误的是
选项 事实 解释
A 甘油是黏稠液体 甘油分子间存在氢键
成键电子对离P越远,成键电子对间的
B 键角PH Y=M>X,Y与W为同主族元素。下列说法错
误的是
A.该阴离子呈现锯齿状
B.该阴离子与季铵离子(R N+)能形成离子液体
4
C.第一电离能大小:X>Y>Z
D.M的氢化物的沸点不一定比Y的氢化物低
湖北省新八校教科研协作体*化学试卷(共 8 页)第 2 页10. 表面皿中都装有混合了饱和食盐水、酚酞和铁氰化钾溶液的琼脂,分别将缠有松散铜丝的铁
钉(图A)和缠有密实锌皮的铁钉(图B)放置其中,如图所示。下列说法错误的是
A.离子在半凝固态的琼脂内可定向移动
B.图A中出现蓝色的反应:Fe2++K++[Fe(CN) ]3-=KFe[Fe(CN) ]↓
6 6
C.图B中铁钉受到锌皮保护,该保护方法为外加电流法
D.图B中会出现两个红色色块
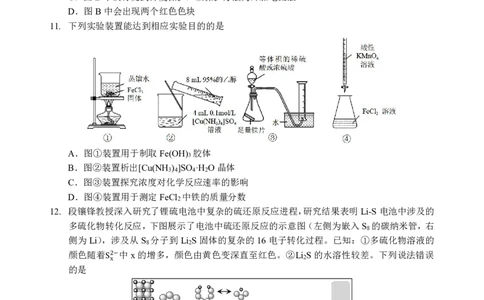
11. 下列实验装置能达到相应实验目的的是
A.图①装置用于制取Fe(OH) 胶体
3
B.图②装置析出[Cu(NH ) ]SO ·H O晶体
3 4 4 2
C.图③装置探究浓度对化学反应速率的影响
D.图④装置用于测定FeCl 中铁的质量分数
2
12. 段镶锋教授深入研究了锂硫电池中复杂的硫还原反应进程,研究结果表明Li-S电池中涉及的
多硫化物转化反应,下图展示了电池中硫还原反应的示意图(左侧为嵌入S 的碳纳米管,右
8
侧为Li),涉及从S 分子到Li S固体的复杂的16电子转化过程。已知:①多硫化物溶液的
8 2
颜色随着 中x的增多,颜色由黄色变深直至红色。②Li S的水溶性较差。下列说法错误
2
的是 2−
Sx
A.图示电池总反应为:16Li+S =8Li S
8 2
B.Li S 是控制整体硫还原反应过程的关键电化学中间体
2 4
C.充电时,正极附近颜色由红色变到黄色最后变成无色
D.选择合适的溶剂能让电池保持稳定的电流输出
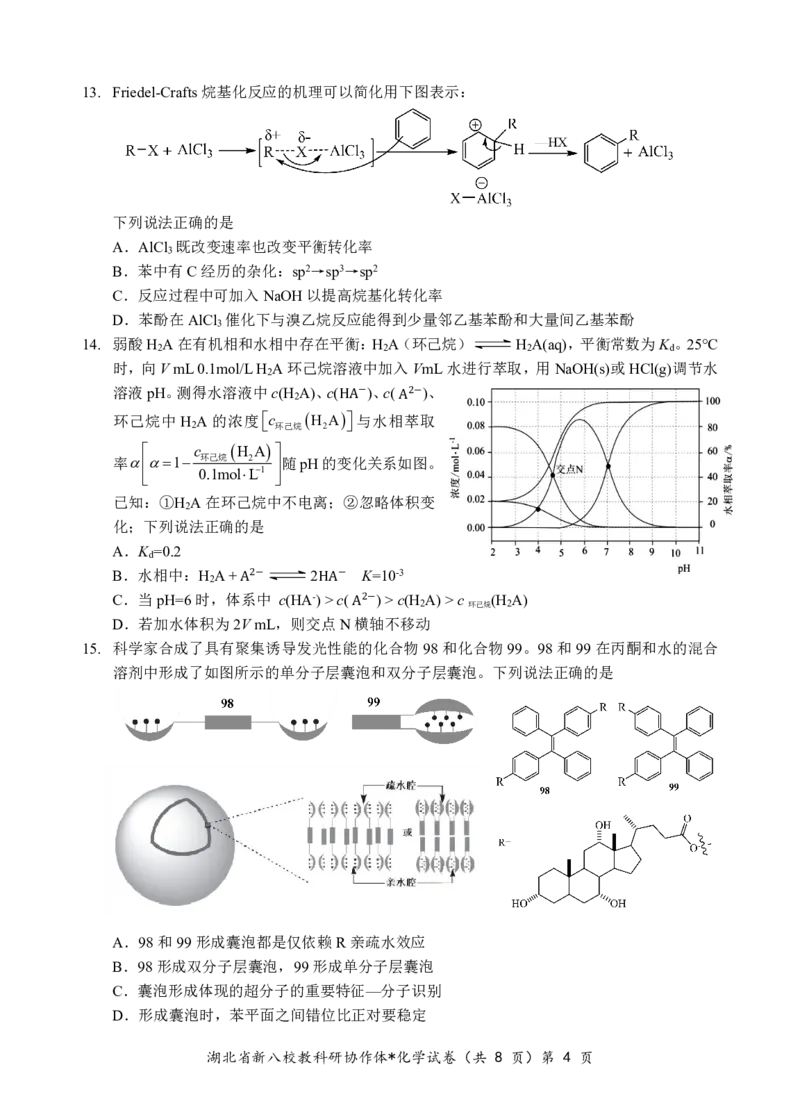
湖北省新八校教科研协作体*化学试卷(共 8 页)第 3 页13. Friedel-Crafts烷基化反应的机理可以简化用下图表示:
下列说法正确的是
A.AlCl 既改变速率也改变平衡转化率
3
B.苯中有C经历的杂化:sp2→sp3→sp2
C.反应过程中可加入NaOH以提高烷基化转化率
D.苯酚在AlCl 催化下与溴乙烷反应能得到少量邻乙基苯酚和大量间乙基苯酚
3
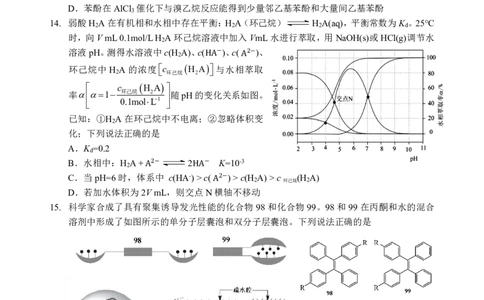
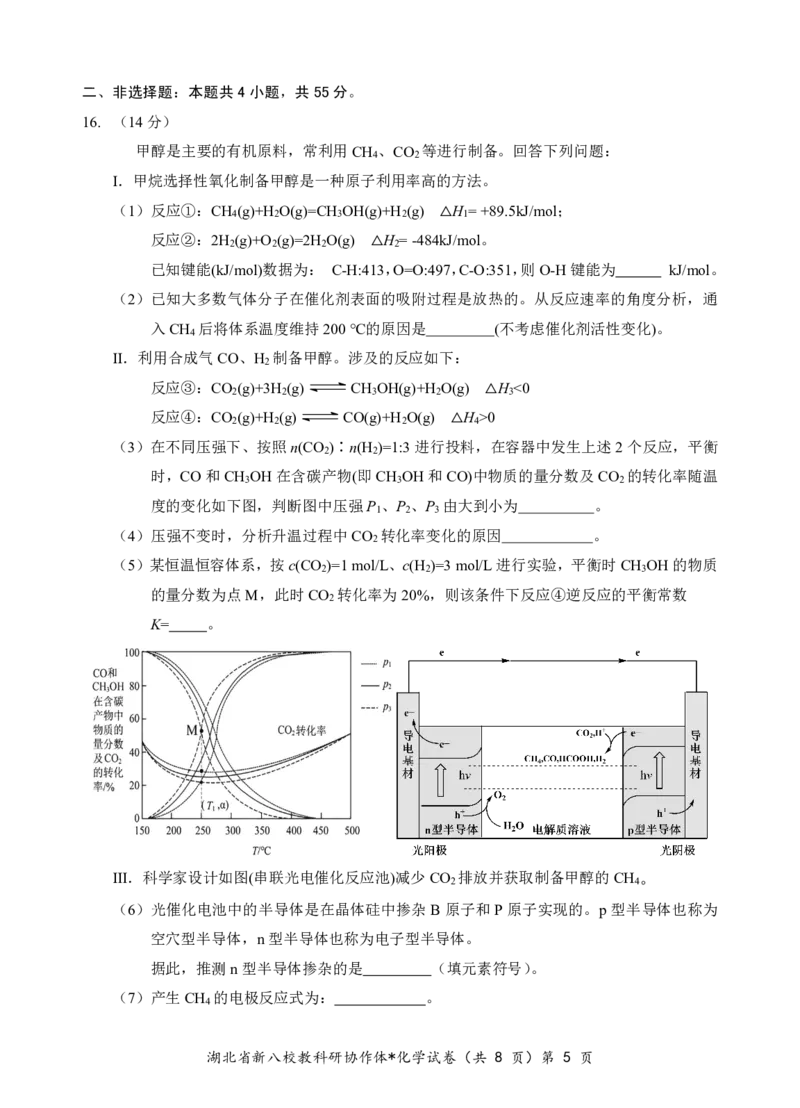
14. 弱酸H A在有机相和水相中存在平衡:H A(环己烷) H A(aq),平衡常数为K 。25℃
2 2 2 d
时,向VmL0.1mol/LH A环己烷溶液中加入VmL水进行萃取,用NaOH(s)或HCl(g)调节水
2
溶液pH。测得水溶液中c(H A)、c( )、c( )、
2
环己烷中 H 2 A 的浓度 c 环己烷 H 2 A H A 与 − 水相 A 萃 2− 取
c H A
率1 环己烷 2 随pH的变化关系如图。
0.1molL1
已知:①H A在环己烷中不电离;②忽略体积变
2
化;下列说法正确的是
A.K =0.2
d
B.水相中:H A+ 2 K=10-3
2
C.当pH=6时,体系2−中 c(HA-)>c−( )>c(H A)>c (H A)
A HA 2 环己烷 2
D.若加水体积为2VmL,则交点N横2−轴不移动
A
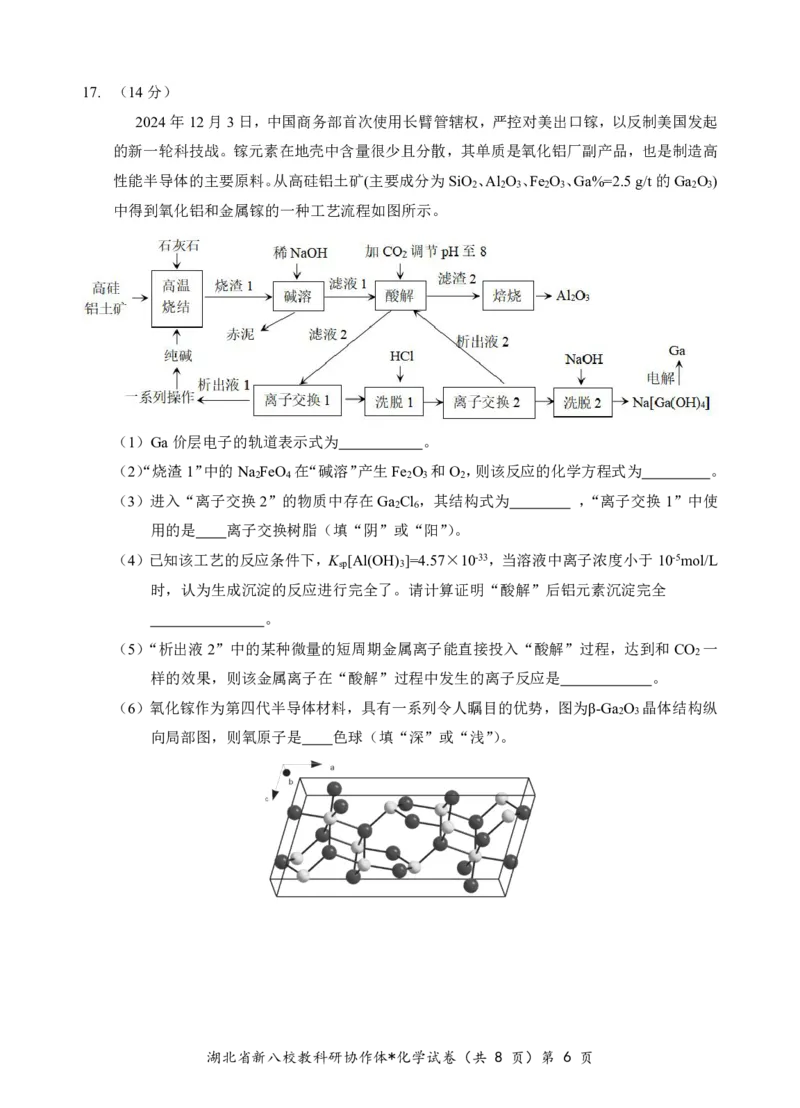
15. 科学家合成了具有聚集诱导发光性能的化合物98和化合物99。98和99在丙酮和水的混合
溶剂中形成了如图所示的单分子层囊泡和双分子层囊泡。下列说法正确的是
A.98和99形成囊泡都是仅依赖R亲疏水效应
B.98形成双分子层囊泡,99形成单分子层囊泡
C.囊泡形成体现的超分子的重要特征—分子识别
D.形成囊泡时,苯平面之间错位比正对要稳定
湖北省新八校教科研协作体*化学试卷(共 8 页)第 4 页二、非选择题:本题共4小题,共55分。
16. (14分)
甲醇是主要的有机原料,常利用CH 、CO 等进行制备。回答下列问题:
4 2
I.甲烷选择性氧化制备甲醇是一种原子利用率高的方法。
(1)反应①:CH (g)+H O(g)=CH OH(g)+H (g) H =+89.5kJ/mol;
4 2 3 2 1
反应②:2H
2
(g)+O
2
(g)=2H
2
O(g) H
2
=-484k△J/mol。
已知键能(kJ/mol)数据为: C-H:41△3,O=O:497,C-O:351,则O-H键能为 kJ/mol。
(2)已知大多数气体分子在催化剂表面的吸附过程是放热的。从反应速率的角度分析,通
入CH 后将体系温度维持200℃的原因是 (不考虑催化剂活性变化)。
4
ⅠI.利用合成气CO、H 制备甲醇。涉及的反应如下:
2
反应③:CO (g)+3H (g) CH OH(g)+H O(g) H <0
2 2 3 2 3
反应④:CO
2
(g)+H
2
(g) CO(g)+H
2
O(g) H
4
>△0
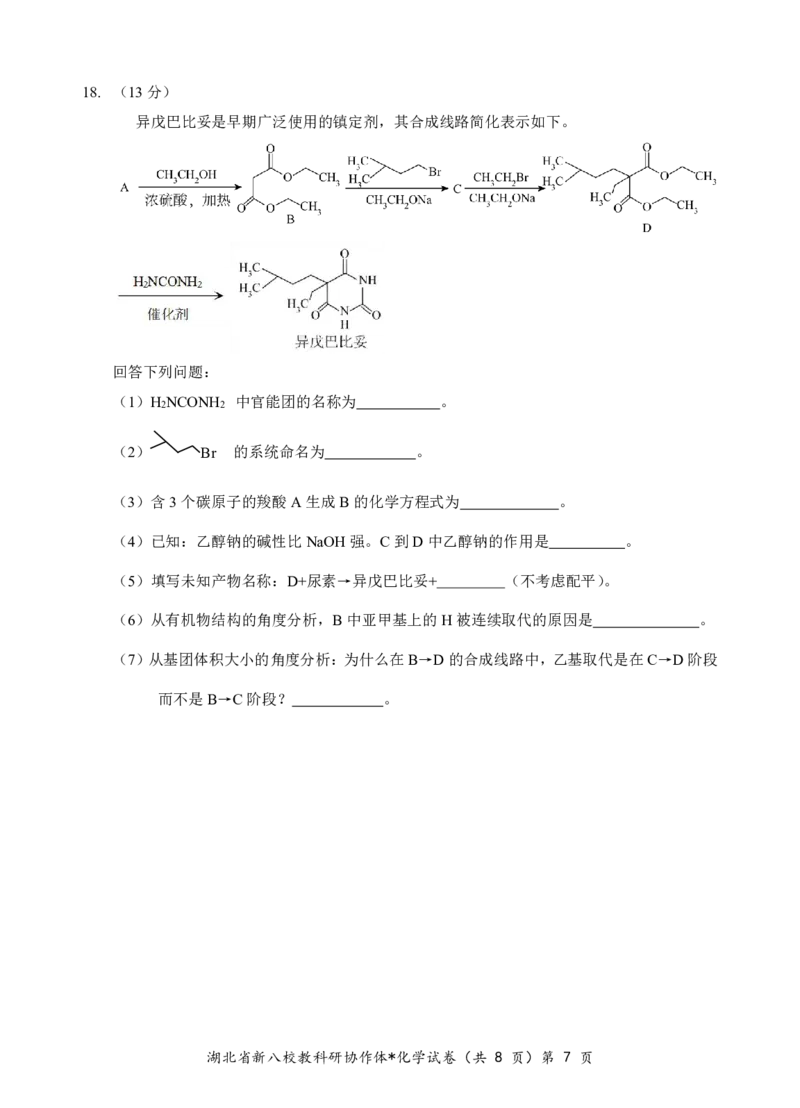
(3)在不同压强下、按照n(CO
2
)∶n(H
2
)=1:3进行投
△
料,在容器中发生上述2个反应,平衡
时,CO和CH OH在含碳产物(即CH OH和CO)中物质的量分数及CO 的转化率随温
3 3 2
度的变化如下图,判断图中压强P 、P 、P 由大到小为 。
1 2 3
(4)压强不变时,分析升温过程中CO 转化率变化的原因 。
2
(5)某恒温恒容体系,按c(CO )=1mol/L、c(H )=3mol/L进行实验,平衡时CH OH的物质
2 2 3
的量分数为点M,此时CO 转化率为20%,则该条件下反应④逆反应的平衡常数
2
K= 。
Ⅲ.科学家设计如图(串联光电催化反应池)减少CO 排放并获取制备甲醇的CH 。
2 4
(6)光催化电池中的半导体是在晶体硅中掺杂B原子和P原子实现的。p型半导体也称为
空穴型半导体,n型半导体也称为电子型半导体。
据此,推测n型半导体掺杂的是 (填元素符号)。
(7)产生CH 的电极反应式为: 。
4
湖北省新八校教科研协作体*化学试卷(共 8 页)第 5 页17. (14分)
2024年12月3日,中国商务部首次使用长臂管辖权,严控对美出口镓,以反制美国发起
的新一轮科技战。镓元素在地壳中含量很少且分散,其单质是氧化铝厂副产品,也是制造高
性能半导体的主要原料。从高硅铝土矿(主要成分为SiO 、Al O 、Fe O 、Ga%=2.5g/t的Ga O )
2 2 3 2 3 2 3
中得到氧化铝和金属镓的一种工艺流程如图所示。
(1)Ga价层电子的轨道表示式为 。
(2)“烧渣1”中的Na FeO 在“碱溶”产生Fe O 和O ,则该反应的化学方程式为 。
2 4 2 3 2
(3)进入“离子交换2”的物质中存在Ga Cl ,其结构式为 ,“离子交换1”中使
2 6
用的是 离子交换树脂(填“阴”或“阳”)。
(4)已知该工艺的反应条件下,K [Al(OH) ]=4.57×10-33,当溶液中离子浓度小于10-5mol/L
sp 3
时,认为生成沉淀的反应进行完全了。请计算证明“酸解”后铝元素沉淀完全
。
(5)“析出液2”中的某种微量的短周期金属离子能直接投入“酸解”过程,达到和CO 一
2
样的效果,则该金属离子在“酸解”过程中发生的离子反应是 。
(6)氧化镓作为第四代半导体材料,具有一系列令人瞩目的优势,图为β-Ga O 晶体结构纵
2 3
向局部图,则氧原子是 色球(填“深”或“浅”)。
湖北省新八校教科研协作体*化学试卷(共 8 页)第 6 页18. (13分)
异戊巴比妥是早期广泛使用的镇定剂,其合成线路简化表示如下。
回答下列问题:
(1)H NCONH 中官能团的名称为 。
2 2
(2) Br 的系统命名为 。
(3)含3个碳原子的羧酸A生成B的化学方程式为 。
(4)已知:乙醇钠的碱性比NaOH强。C到D中乙醇钠的作用是 。
(5)填写未知产物名称:D+尿素→异戊巴比妥+ (不考虑配平)。
(6)从有机物结构的角度分析,B中亚甲基上的H被连续取代的原因是 。
(7)从基团体积大小的角度分析:为什么在B→D的合成线路中,乙基取代是在C→D阶段
而不是B→C阶段? 。
湖北省新八校教科研协作体*化学试卷(共 8 页)第 7 页19. (14分)
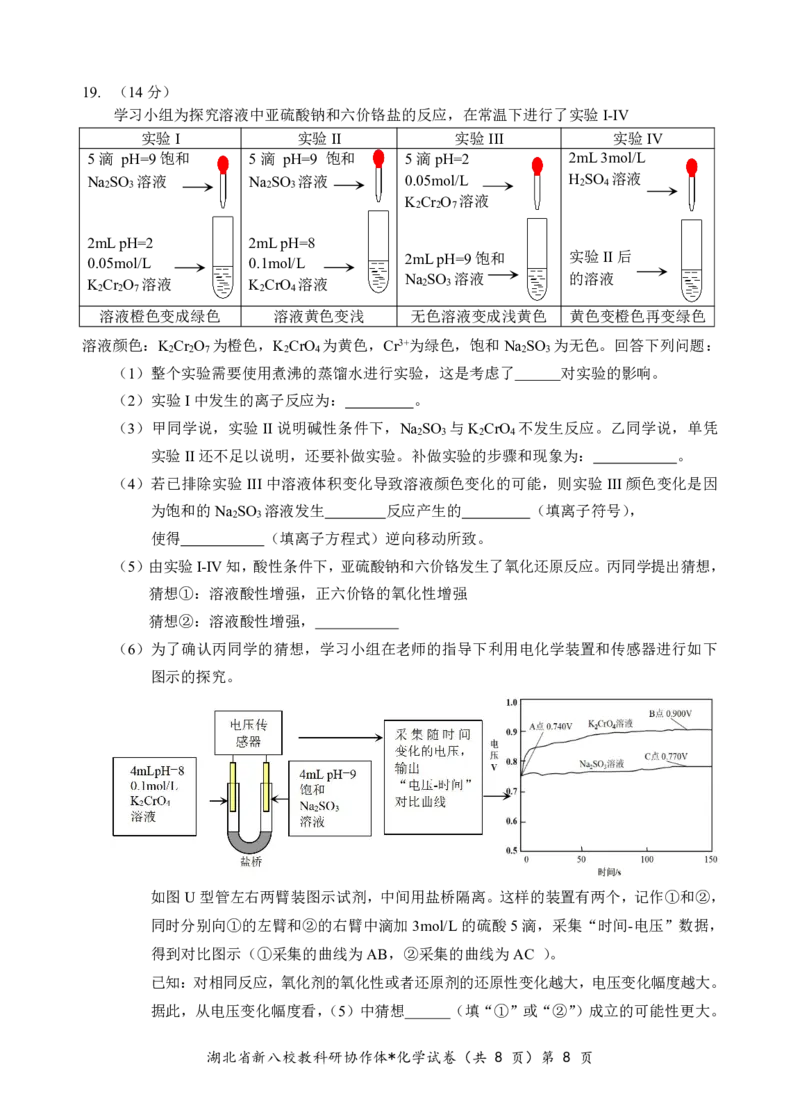
学习小组为探究溶液中亚硫酸钠和六价铬盐的反应,在常温下进行了实验I-IV
实验I 实验II 实验III 实验IV
5滴 pH=9饱和 5滴 pH=9 饱和 5滴pH=2 2mL3mol/L
Na 2 SO 3 溶液 Na 2 SO 3 溶液 0.05mol/L H 2 SO 4 溶液
K Cr O 溶液
2 2 7
2mLpH=2 2mLpH=8
0.05mol/L 0.1mol/L
2mLpH=9饱和 实验II后
K Cr O 溶液 K CrO 溶液 Na 2 SO 3 溶液 的溶液
2 2 7 2 4
溶液橙色变成绿色 溶液黄色变浅 无色溶液变成浅黄色 黄色变橙色再变绿色
溶液颜色:K Cr O 为橙色,K CrO 为黄色,Cr3+为绿色,饱和Na SO 为无色。回答下列问题:
2 2 7 2 4 2 3
(1)整个实验需要使用煮沸的蒸馏水进行实验,这是考虑了 对实验的影响。
(2)实验I中发生的离子反应为: 。
(3)甲同学说,实验II说明碱性条件下,Na SO 与K CrO 不发生反应。乙同学说,单凭
2 3 2 4
实验II还不足以说明,还要补做实验。补做实验的步骤和现象为: 。
(4)若已排除实验III中溶液体积变化导致溶液颜色变化的可能,则实验III颜色变化是因
为饱和的Na SO 溶液发生 反应产生的 (填离子符号),
2 3
使得 (填离子方程式)逆向移动所致。
(5)由实验I-IV知,酸性条件下,亚硫酸钠和六价铬发生了氧化还原反应。丙同学提出猜想,
猜想①:溶液酸性增强,正六价铬的氧化性增强
猜想②:溶液酸性增强,
(6)为了确认丙同学的猜想,学习小组在老师的指导下利用电化学装置和传感器进行如下
图示的探究。
如图U型管左右两臂装图示试剂,中间用盐桥隔离。这样的装置有两个,记作①和②,
同时分别向①的左臂和②的右臂中滴加3mol/L的硫酸5滴,采集“时间-电压”数据,
得到对比图示(①采集的曲线为AB,②采集的曲线为AC )。
已知:对相同反应,氧化剂的氧化性或者还原剂的还原性变化越大,电压变化幅度越大。
据此,从电压变化幅度看,(5)中猜想 (填“①”或“②”)成立的可能性更大。
湖北省新八校教科研协作体*化学试卷(共 8 页)第 8 页