文档内容
化学试题
可能用到的相对原子质量:Na 23;O 16;H 1;P 31;C 12;Ba 137;Cl 35.5;N 14;Cu
64;S 32
一、选择题(只有1个正确答案;共20小题,每小题3分,共60分)
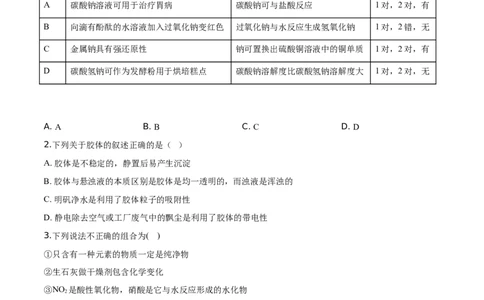
1.如下表所示,对陈述1和陈述2的正确性及两者间是否具有因果关系的判断都正确的是
选项 陈述1 陈述2 判断
A 碳酸钠溶液可用于治疗胃病 碳酸钠可与盐酸反应 1对,2对,有
B 向滴有酚酞的水溶液加入过氧化钠变红色 过氧化钠与水反应生成氢氧化钠 1对,2错,无
C 金属钠具有强还原性 钠可置换出硫酸铜溶液中的铜单质 1对,2对,有
D 碳酸氢钠可作为发酵粉用于烘培糕点 碳酸钠溶解度比碳酸氢钠溶解度大 1对,2对,无
A. A B. B C. C D. D
2.下列关于胶体的叙述正确的是( )
A. 胶体是不稳定的,静置后易产生沉淀
B. 胶体与悬浊液的本质区别是胶体是均一透明的,而浊液是浑浊的
C. 明矾净水是利用了胶体粒子的吸附性
D. 静电除去空气或工厂废气中的飘尘是利用了胶体的带电性
3.下列说法不正确的组合为( )
①只含有一种元素的物质一定是纯净物
②生石灰做干燥剂包含化学变化
③NO 是酸性氧化物,硝酸是它与水反应形成的水化物
2
④碱性氧化物一定是金属氧化物
⑤电解质溶液导电一定发生化学变化
⑥能与酸反应生成盐和水的氧化物一定是碱性氧化物
⑦用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐不涉及化学变化
⑧两种盐反应一定生成两种新盐
A. ①③⑥⑧ B. ①②③④⑥ C. ②④⑤⑧ D. ②④⑥⑧
4.用N 表示阿伏加德罗常数的值,下列说法中正确的是( )
AA. 0.01molNH +含有质子数为0.1N
4 A
B. 4.48 L N 与CO的混合物所含分子数为0.2N
2 A
C. 6.2 g白磷与红磷的混合物中所含磷原子数为0.2N
A
D. 10.0mL 12 mol·L-1浓盐酸与足量二氧化锰反应,转移电子数为0.06N
A
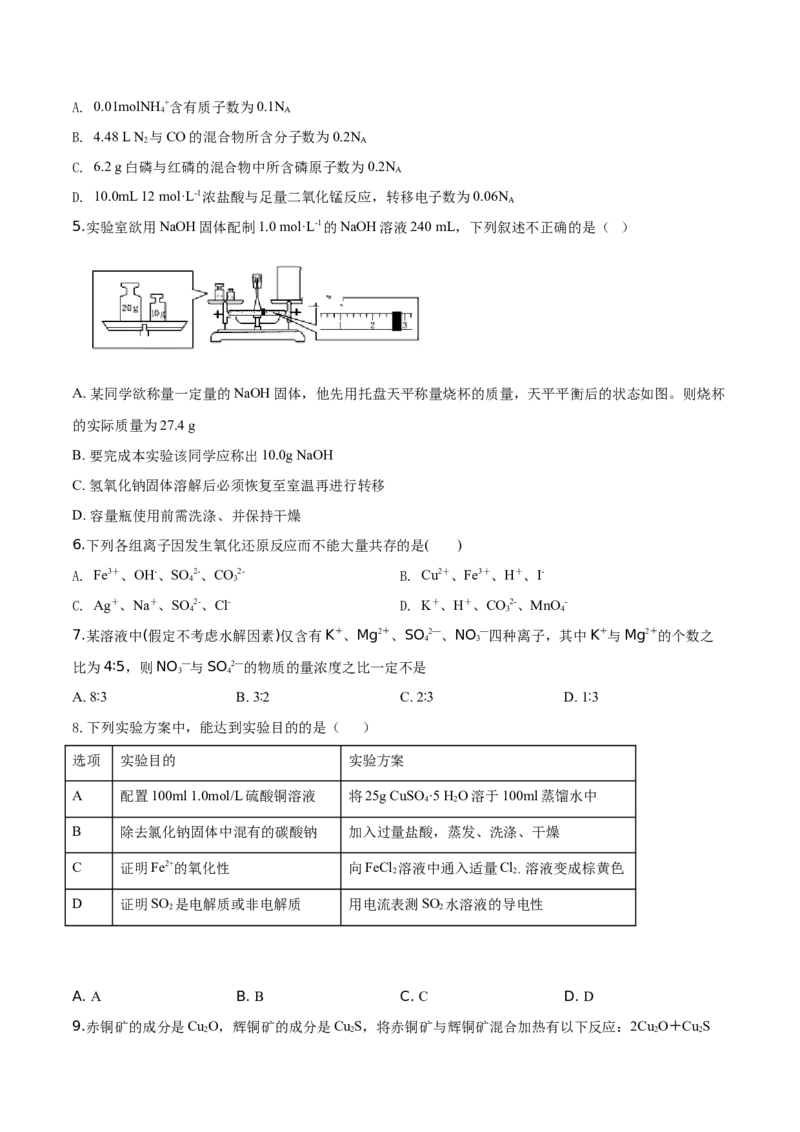
5.实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL,下列叙述不正确的是( )
A. 某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。则烧杯
的实际质量为27.4 g
B. 要完成本实验该同学应称出10.0g NaOH
C. 氢氧化钠固体溶解后必须恢复至室温再进行转移
D. 容量瓶使用前需洗涤、并保持干燥
6.下列各组离子因发生氧化还原反应而不能大量共存的是( )
A. Fe3+、OH-、SO 2-、CO2- B. Cu2+、Fe3+、H+、I-
4 3
C. Ag+、Na+、SO 2-、Cl- D. K+、H+、CO2-、MnO -
4 3 4
7.某溶液中(假定不考虑水解因素)仅含有K+、Mg2+、SO2—、NO—四种离子,其中K+与Mg2+的个数之
4 3
比为4∶5,则NO—与SO2—的物质的量浓度之比一定不是
3 4
A. 8∶3 B. 3∶2 C. 2∶3 D. 1∶3
8.下列实验方案中,能达到实验目的的是( )
选项 实验目的 实验方案
A 配置100ml 1.0mol/L硫酸铜溶液 将25g CuSO ·5 H O溶于100ml蒸馏水中
4 2
B 除去氯化钠固体中混有的碳酸钠 加入过量盐酸,蒸发、洗涤、干燥
C 证明Fe2+的氧化性 向FeCl 溶液中通入适量Cl 溶液变成棕黄色
2 2,
D 证明SO 是电解质或非电解质 用电流表测SO 水溶液的导电性
2 2
A. A B. B C. C D. D
9.赤铜矿的成分是Cu O,辉铜矿的成分是Cu S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu O+Cu S
2 2 2 26Cu+SO ↑,对于该反应,下列说法正确的是
2
A. 该反应的氧化剂只有Cu O
2
B. Cu既是氧化产物,又是还原产物
C. Cu S既 是氧化剂又是还原剂
2
D. 还原产物与氧化产物的物质的量之比为1∶6
10.下列两种气体的分子数一定相等的是( )
A. 等体积的CO和N B. 质量相等、密度不等的N 和CO
2 2
C. 原子数目相等的O 和N D. 质量相等的N 和CO
3 2 2 2
11.碘在地壳中主要以NaIO 的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所
3
示。
下列说法中不正确的是
A. 用淀粉KI试纸和食醋检验加碘盐时淀粉KI试纸会变蓝
B. 足量Cl 能使湿润的、已变蓝的淀粉KI试纸褪色的原因可能是5Cl+I+6HO=2HIO+10HCl
2 2 2 2 3
C. 由图可知氧化性的强弱顺序为Cl>I>IO—
2 2 3
D. 途径Ⅱ中若生成1molI,则反应中转移的电子数为10N
2 A
12.下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的有( )
①向饱和碳酸钠溶液中通入过量的CO
2
②向氢氧化铁胶体中逐滴稀盐酸
③向FeCl 溶液中逐滴加入过量稀氢氧化钠溶液
3
④向澄清的石灰水中通入过量的CO
2
⑤向氯化钠的饱和溶液中通入大量氨气再通入过量CO
2
A. 1个 B. 2个 C. 3个 D. 4个
13.下列离子方程正确的是( )
A. 饱和石灰水中通入过量二氧化碳:OH- + CO = HCO-
2 3
B. 将Cl 溶于水制备次氯酸: Cl + H O = 2H++ Cl- + ClO-
2 2 2
C. 实验室制取二氧化碳:CO2- + 2H+ = H O + CO ↑
3 2 2
D. 将少量SO 通入NaClO溶液中: SO + H O + 2ClO-= SO 2- + 2HClO
2 2 2 3
14.把VL含有MgSO 和KSO 的混合溶液分成两等份,一份加入含a mol BaCl 的溶液,恰好使硫酸根
4 2 4 2离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁。则原混
合溶液中钾离子的浓度为
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
15.下列除杂试剂及方法选择正确的是( )
A. NaHCO (混有NaCO)将固体在空气中充分加热
3 2 3
B. Cl(混有HO和HCl)将混合气体依次通过浓硫酸和饱和食盐水洗气
2 2
C. NaCl溶液(混有NaSO )向溶液中依次加入BaCl -Na CO-盐酸(每种试剂均过量)最后加热
2 4 2 2 3
D. FeCl (混有FeCl )向混合溶液中通入过量氯气
2 3
16.某同学结合所学知识探究NaO 与H 能否反应,设计装置如下,下列说法正确 的是( )
2 2 2
A. 若D中无水硫酸铜变蓝,则说明NaO 与H 反应生成水
2 2 2
B. 装置B中盛放浓硫酸,目的是除去A中挥发出来的少量水蒸气
C. 装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度
D. 装置A也可直接用于二氧化锰与浓盐酸反应制取氯气
17. 下列说法正确的是
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水
④检验HCl气体中是否混有Cl 方法是将气体通入硝酸银溶液
2
⑤除去HCl气体中的Cl,可将气体通入饱和食盐水中
2
A. ①②③ B. ③ C. ②③④ D. ③⑤
18.根据下列实验事实得出的相应结论正确的是( )序号 实验事实 结论
A CO 的水溶液可以导电 CO 是电解质
2 2
B Ca(ClO) 溶液中通入CO 产生白色沉淀 酸性:HCO>HClO
2 2 2 3
向无色溶液中加入氯化钡溶液有白色沉淀生
C 原溶液中一定含有SO 2-
成,再加盐酸,沉淀不消失 4
用铂丝蘸取某溶液在酒精灯火焰上灼烧直接
D 原溶液中不含K+
观察火焰颜色,未见紫色
A. A B. B C. C D. D
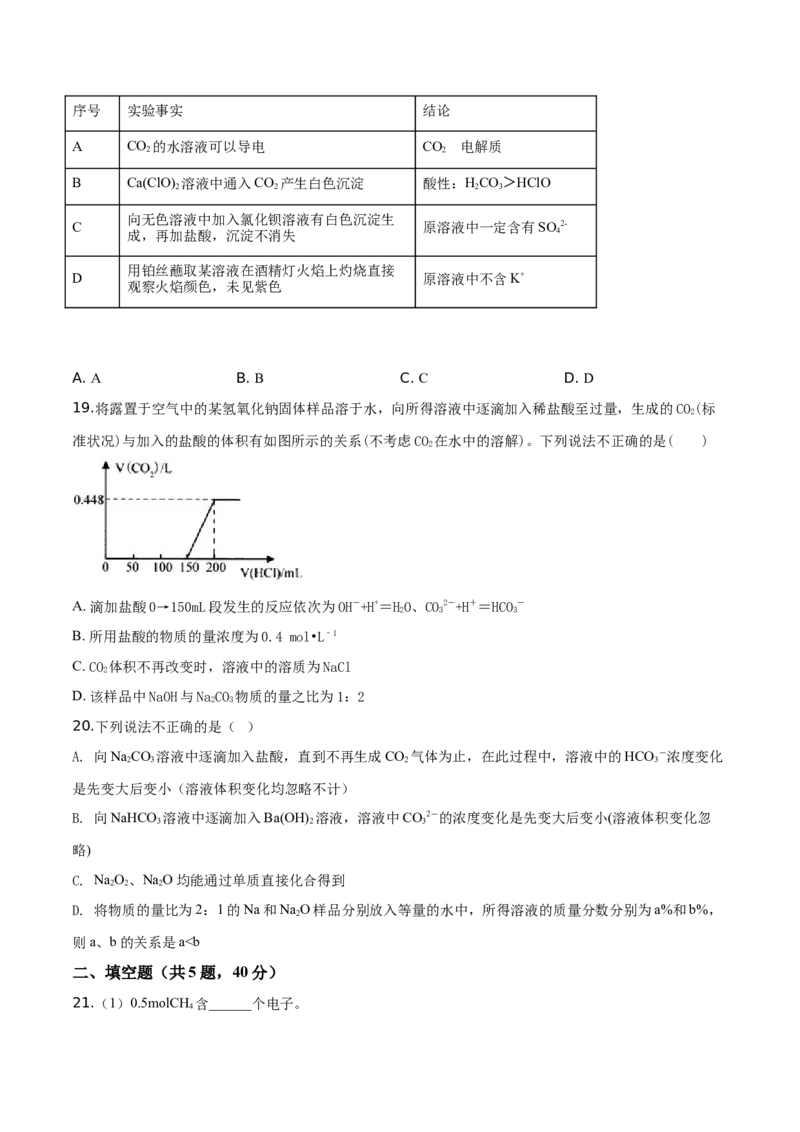
19.将露置于空气中的某氢氧化钠固体样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的CO(标
2
准状况)与加入的盐酸的体积有如图所示的关系(不考虑CO 在水中的溶解)。下列说法不正确的是( )
2
A. 滴加盐酸0→150mL段发生的反应依次为OH-+H+=HO、CO2-+H+=HCO-
2 3 3
B. 所用盐酸的物质的量浓度为0.4 mol•L﹣1
C. CO 体积不再改变时,溶液中的溶质为NaCl
2
D. 该样品中NaOH与NaCO 物质的量之比为1:2
2 3
20.下列说法不正确的是( )
A. 向NaCO 溶液中逐滴加入盐酸,直到不再生成CO 气体为止,在此过程中,溶液中的HCO -浓度变化
2 3 2 3
是先变大后变小(溶液体积变化均忽略不计)
B. 向NaHCO 溶液中逐滴加入Ba(OH) 溶液,溶液中CO2-的浓度变化是先变大后变小(溶液体积变化忽
3 2 3
略)
C. NaO、NaO均能通过单质直接化合得到
2 2 2
D. 将物质的量比为2:1的Na和NaO样品分别放入等量的水中,所得溶液的质量分数分别为a%和b%,
2
则a、b的关系是a