文档内容
专题 02 化学计量
考点 三年考情(2022-2024) 命题趋势
近几年高考对化学计量的考查命题变动不大,
但不再是选择题单独必考内容了,有时会分散
到其他选择题当中,如氧化还原反应类、电化
学类、化学实验类选择题中。有关阿伏伽德罗
常数的判断与相关计算依然是核心考查形式,
◆有关阿伏加德罗常数的判断:
该考查形式涉及很多知识板块,常考点主要
2024浙江卷、2024安徽卷、2024黑
有:①微粒中所含分子数、原子数、离子数、
吉辽卷、2024河北卷、2023全国甲
考点1 化学计 中子数、质子数、化学键数;溶液中所含离子
卷、2023辽宁卷、2023浙江卷、2022
量 数。②反应中转移电子数。③电化学装置中电
全国甲卷、2022福建卷、2022辽宁
路中通过的电子数、电极产物的物质的量。另
卷、2022重庆卷、2022浙江卷、2022
外,随着新高考的推进,选择题当中会考查到
广东卷、2022河北卷、2022海南卷
选择性必修2的知识,能与化学计量很好地结
合起来,如 键或 键数目、极性键或非极性
键数目、配位键数目、晶体中化学键数目、孤
电子对数目、共用电子对数目等。有关物质的
量浓度
考点1 化学计量
考法01 有关阿伏加德罗常数的判断
1. (2024·浙江卷)汽车尾气中的NO和CO在催化剂作用下发生反应: ,
列说法不正确的是(N 为阿伏加德罗常数的值)
AA. 生成1molCO 转移电子的数目为2N
2 A
B. 催化剂降低NO与CO反应的活化能
C. NO是氧化剂,CO是还原剂
D. N 既是氧化产物又是还原产物
2
【答案】D
【解析】NO中N的化合价为+2价,降低为0价的N ,1个NO得2个电子,作氧化剂,发生还原反应,
2
CO中C为+2价,化合价升高为+4价的CO,失去2个电子,作还原剂发生氧化反应;
2
【详解】A.根据分析,1molCO 转移2N 的电子,A正确;
2 A
B.催化剂通过降低活化能,提高反应速率,B正确;
C.根据分析,NO是氧化剂,CO是还原剂,C正确;
D.根据分析,N 为还原产物,CO 为氧化产物,D错误;
2 2
故答案为:D。
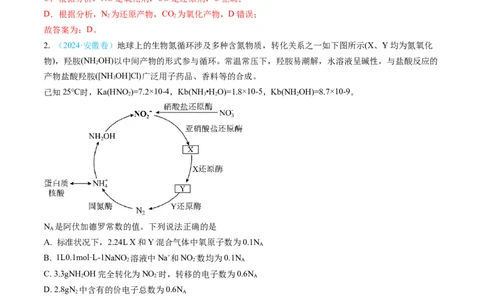
2. (2024·安徽卷)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y均为氮氧化
物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反应的
2
产物盐酸羟胺([NH OH]Cl)广泛用子药品、香料等的合成。
3
已知25℃时,Ka(HNO)=7.2×10-4,Kb(NH•HO)=1.8×10-5,Kb(NHOH)=8.7×10-9。
2 3 2 2
N 是阿伏加德罗常数的值。下列说法正确的是
A
A. 标准状况下,2.24L X和Y混合气体中氧原子数为0.1N
A
B. 1L0.1mol·L-1NaNO 溶液中Na+和NO -数均为0.1N
2 2 A
C. 3.3gNHOH完全转化为NO -时,转移的电子数为0.6N
2 2 A
D. 2.8gN 中含有的价电子总数为0.6N
2 A
【答案】A
【解析】 在亚硝酸盐还原酶的作用下转化为X,X在X还原酶的作用下转化为Y,X、Y均为氮氧化
物,即X为NO,Y为NO。
2
A.标准状况下, 和NO混合气体物质的量为0.1mol,氧原子数为 ,故A正确;
2
B.HNO 为弱酸,因此 能够水解为HNO, 溶液中 数目小于 ,故
2 2
B错误;
C. 完全转化为 时,N的化合价由-1上升到+3, 物质的量为0.1mol,转移的电子数为 ,故C错误;
D. 物质的量为0.1mol,N的价电子数等于最外层电子数为5, 含有的价电子总数为 ,
故D错误;
故选A。
3. (2024·黑吉辽卷)硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下, 中原子总数为
B. 溶液中, 数目 为
C. 反应①每消耗 ,生成物中硫原子数目为
D. 反应②每生成 还原产物,转移电子数目为
【答案】D
【解析】
【详解】A.标况下SO 为气体,11.2L SO 为0.5mol,其含有1.5mol原子,原子数为1.5N ,A错误;
2 2 A
B.SO 为弱酸阴离子,其在水中易发生水解,因此,100mL 0.1mol L-1 Na SO 溶液中SO 数目小于
2 3
0.01N ,B错误;
A
C.反应①的方程式为SO +2H S=3S +2H O,反应中每生成3mol S消耗2mol HS,3.4g HS为0.1mol,故
2 2 2 2 2
可以生成0.15mol S,生成的原子数目为0.15N ,C错误;
A
D.反应②的离子方程式为3S+6OH-=SO +2S2-+3H O,反应的还原产物为 S2-,每生成2mol S2-共转移
2
4mol电子,因此,每生成1mol S2-,转移2mol电子,数目为2N ,D正确;
A
故答案选D 。
4. (2024·河北卷)超氧化钾 可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
, 为阿伏加德罗常数的值。下列说法正确的是
A. 中 键的数目为
B. 晶体中离子的数目为
C. 溶液中 的数目为
D. 该反应中每转移 电子生成 的数目为
【答案】A
【解析】
【详解】A. (即 ) 中 键的数目为 ,A正确;B. 由 和 构成, 晶体中离子的数目为 ,B错误;
C. 在水溶液中会发生水解: ,故 溶液中 的数
目小于 ,C错误;
D.该反应中部分氧元素化合价由 价升至0价,部分氧元素化合价由 价降至 价,则每
参加反应转移 电子,每转移 电子生成 的数目为 ,D错误;
故选A。
5.(2023·全国甲卷) 为阿伏加德罗常数的值。下列叙述正确的是
A. 异丁烷分子中共价键的数目为
B.标准状况下, 中电子的数目为
C. 的 溶液中 的数目为
D. 的 溶液中 的数目为
【答案】A
【解析】A.异丁烷的结构式为 ,1mol异丁烷分子含有13N 共价键,所以0.50mol异丁烷分
A
子中共价键的数目为6.5N ,A正确;
A
B.在标准状况下,SO 状态为固态,不能计算出2.24L SO 物质的量,故无法求出其电子数目,B错误;
3 3
C.pH=2的硫酸溶液中氢离子浓度为c(H+)=0.01mol/L,则1.0L pH=2的硫酸溶液中氢离子数目为0.01N ,
A
C错误;
D. 属于强碱弱酸盐,在水溶液中CO 会发生水解,所以1.0L 1.0 mol/L的NaCO 溶液中CO 的
2 3
数目小于1.0N ,D错误;
A
故选A。
6.(2023·辽宁卷)我国古代四大发明之一黑火药的爆炸反应为: 。
设 为阿伏加德罗常数的值,下列说法正确的是
A. 含 键数目为
B.每生成 转移电子数目为
C. 晶体中含离子数目为
D. 溶液中含 数目为
【答案】C
【解析】A. 分子含有2个 键,题中没有说是标况条件下,气体摩尔体积未知,无法计算 键个数,
A项错误;B.2.8g 的物质的量 ,1mol 生成转移的电子数为12 ,则0.1mol 转移的
电子数为1.2 ,B项错误;
C.0.1mol 晶体含有离子为 、 ,含有离子数目为0.2 ,C项正确;
D.因为 水解使溶液中 的数目小于0.1 ,D项错误;
答案选C。
7.(2023·浙江卷)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.4.4gC HO中含有σ键数目最多为0.7N
2 4 A
B.1.7gH O 中含有氧原子数为0.2N
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,铵根离子数为0.1N
3 A
D.标准状况下,11.2LCl 通入水中,溶液中氯离子数为0.5N
2 A
【答案】A
【解析】A.1个C HO中含有6个σ键和1个π键(乙醛)或7个σ键(环氧乙烷),4.4gC HO的物质的量为
2 4 2 4
0.1mol,则含有σ键数目最多为0.7N ,A正确;
A
B.1.7gH O 的物质的量为 =0.05mol,则含有氧原子数为0.1N ,B不正确;
2 2 A
C.向1L0.1mol/LCHCOOH溶液通氨气至中性,溶液中存在电荷守恒关系:c(CHCOO-)+c(OH-)=c(NH )
3 3
+c(H+),中性溶液c(OH-)=c(H+),则c(CHCOO-)=c(NH ),再根据物料守恒:n(CHCOO-)
3 3
+n(CH COOH)=0.1mol,得出铵根离子数小于0.1N ,C不正确;
3 A
D.标准状况下,11.2LCl 的物质的量为0.5mol,通入水中后只有一部分Cl 与水反应生成H+、Cl-和
2 2
HClO,所以溶液中氯离子数小于0.5N ,D不正确;
A
故选A。
N
8.(2022·全国甲卷) A为阿伏加德罗常数的值,下列说法正确的是( )
25 ℃ 101 kPa 28L 2.5N
A. , 下, 氢气中质子的数目为 A
B.
2.0 L 1.0 molL1 AlCl 3溶液中,Al3
的数目为
2.0N
A
0.20mol CO 1.4N
C. 苯甲酸完全燃烧,生成 2的数目为 A
CuCl 6.4g 0.10N
D.电解熔融 2,阴极增重 ,外电路中通过电子的数目为 A
【答案】C
【解析】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故B错
3 3 A
误;
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生成7molCO ,则
2
0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;
2 AD.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的重量为Cu的质
2
量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为
0.2N ,故D错误;
A
答案选C。
9.(2022·福建卷)常温常压下,电化学还原制氨气的总反应方程式: ,设
为阿伏加德罗常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每产生 失去的电子数为
C. 氨水中,含有的 分子数少于
D.消耗 (已折算为标况)时,产生的 分子数为
【答案】D
【解析】A.HO分子中孤电子对数为 =2, HO的物质的量为 =0.5mol,含有的孤电子
2 2
对数为 ,故A错误;
B.该反应中N 中N元素化合价由0价下降到-3价,34g 的物质的量为 =2mol,每产生
2
, 得到6mol电子,数目为6N ,故B错误;
A
C.氨水的体积未知,无法计算 的分子数,故C错误;
D. 的物质的量为0.5mol,由方程式可知,消耗0.5mol ,产生的0.75mol ,数目为 ,
故D正确;
故选D。
10.(2022·辽宁卷)设 为阿伏加德罗常数的值。下列说法正确的是
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为0.01N
A
【答案】A
【解析】A.1个 原子中含有10个中子, 的物质的量为 ,故 中含有
中子的物质的量为 ,中子数为 ,故A正确;B.乙烯分子的结构式为 ,1个乙烯分子中含有5个 键, 的物质的量为 ,所
以 分子中含有的 键数目为 ,B错误;
C. 是共价化合物, 分子中不存在 ,故C错误;
D.没有给出 溶液的体积,无法计算 的 溶液中 的数目,故D错误;
选A。
11.(2022·重庆卷)工业上用N 和H 合成NH ,N 代表阿伏加德罗常数的值,下列说法正确的是
2 2 3 A
A.消耗14gN 生成NH 分子数为2 N
2 3 A
B.消耗1molH ,生成N-H键数为2 N
2 A
C.生成标准状况下22.4LNH ,电子转移数为2 N
3 A
D.氧化1molNH 生成NO,需O 分子数为2 N
3 2 A
【答案】B
【解析】A.由方程式可知,消耗14g氮气生成氨气的分子数为 ×2×N mol—1=N ,故A错误;
A A
B.由方程式可知,消耗1mol氢气生成N-H键数为1mol× ×3×N mol—1=2N ,故B正确;
A A
C.由方程式可知,生成标准状况下22.4L氨气,反应电子转移数为 ×3×N mol—1=3N ,故C错
A A
误;
D.由得失电子数目守恒可知,1mol氨气与氧气反应生成一氧化氮,需氧气分子数为1mol× ×N mol—
A
1=1.25N ,故D错误;
A
故选B。
12.(2022·浙江卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
【答案】C
【解析】A. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物质的量
为0.1mol,因此,其中只含有 个阳离子,A说法不正确;
B.没有指明气体的温度和压强,无法确定 乙烷和丙烯的混合气体的物质的量是多少,因此,无法确
定其中所含碳氢键的数目,B说法不正确;
C. 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为 ,C说法正
确;D. 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此, 和
于密闭容器中充分反应后, 分子总数小于 ,D说法不正确。
综上所述,本题选C。
13.(2022·浙江卷)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
【答案】A
【详解】A.1LpH为12的Ba(OH) 溶液中含有OH-的浓度为0.01mol/L,物质的量0.01mol/L
2
1L=0.01mol,OH-的数目为0.01N ,A正确;
A
B.1.8g重水(D O)的物质的量为:0.09mol,所含质子数为0.9N ,B错误;
2 A
C.足量的浓盐酸与8.7gMnO(0.1mol)反应,+4价Mn转化生成Mn2+,转移电子的数目为0.2N ,C错误;
2 A
D.甲醇的结构简式为:CHOH,32g (1mol)的分子中含有C—H键的数目为3N ,D错误;
3 A
答案选A。
14.(2022·广东卷)我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子
D. 被还原生成
【答案】A
【解析】A.淀粉是由葡萄糖分子聚合而成的多糖,在一定条件下水解可得到葡萄糖,故A正确;
B.葡萄糖与果糖的分子式均为C H O,结构不同,二者互为同分异构体,但含有O元素,不是烃类,属
6 12 6
于烃的衍生物,故B错误;
C.一个CO分子含有14个电子,则1molCO中含有14×6.02×1023=8.428×1024个电子,故C错误;
D.未指明气体处于标况下,不能用标况下的气体摩尔体积计算其物质的量,故D错误;
答案选A。
15.(2022·河北卷)N 是阿伏加德罗常数的值。下列说法正确的是
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 AD.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
【答案】B
【详解】A.过氧化钠与水反应生成氢氧化钠和氧气,则3.9g过氧化钠与足量水反应,转移电子个数为
×1×N mol-1=0.05N ,故A错误;
A A
B.镁在空气中燃烧无论生成氧化镁,还是氮化镁,镁均转化为镁离子,则1.2gMg在空气中燃烧生成氧化
镁和氮化镁时,转移电子个数为 ×2×N mol-1=0.1N ,故B正确;
A A
C.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,则2.7g铝与足量氢氧化钠溶液反应生成氢气的个数为
× ×N mol-1=0.15N ,故C错误;
A A
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,硅酸钠在溶液中发生水解反应,则由原子个数守恒可
知,6.0g二氧化硅与足量氢氧化钠溶液反应所得溶液中硅酸根离子的个数小于 ×N mol-1=0.1N ,故
A A
D错误;
故选B。
16.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下
A
列说法正确的是
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
【答案】A
【解析】2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为0.3mol,两者发生
反应后,Fe完全溶解,而盐酸过量。
A.Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;
B.HCl溶液中Cl-的物质的量为0.3mol,因此,Cl-数为0.3N ,B不正确;
A
C.56Fe 的质子数为26、中子数为30,2.8g56Fe的物质的量为0.05mol,因此,2.8g56Fe含有的中子数为
1.5N ,C不正确;
A
D.反应生成H 的物质的量为0.05mol,在标准状况下的体积为1.12L ,D不正确;
2
综上所述,本题A。