文档内容
江西省景德镇市2026届高三第一次质量检测化学试卷
本试卷满分100分,考试用时75分钟
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。回答非
选择题时,将答案写在答题卡上指定区域,超出答题框无效。
3. 可能用到的相对原子质量: H-1 Li-7 C-12 N-14 O-16 S-32 Cl-35.5 W-183.8
Se-79 Cd-112
一、选择题,每小题只有1个正确选项(每小题3分,共42分)
1、江西素有“物华天宝、人杰地灵”的美誉,下列有关说法错误的是
A.景德镇瓷器“薄如纸,声如磬”,瓷器的主要原料是黏土
B.赣州美食黄元米果的制作过程中用到黄元柴灰加水制的灰碱水,呈碱性
C.安福火腿色泽红润,鲜香可口,可适量添加亚硝酸钠防腐,提升风味
D.江西稻谷烧酒香气浓郁,酿酒时粮食中的淀粉在酒化酶作用下水解生成酒精
2.2024年12月11日中央经济工作会议在北京举行,会议明确2025年经济工作的九项重点任务之
一,是以科技创新引领新质生产力发展,建设现代化产业体系。“新质生产力”的概念中,
“新”的核心在于科技创新。下列说法正确的是
A.利用 CO 合成的脂肪酸,属于有机高分子化合物
B.5G手机搭载的麒麟9000S芯片的主要成分是SiO
₂
C.“神舟十九号”发动机的耐高温结构材料Si N 是一种熔沸点很高的共价晶体
₂
D.“嫦娥六号”探测器使用 GaAs太阳能电池,该电池将化学能转化为电能
₃ ₄
3.下列化学用语表示正确的是
A. H O⁺的电子式:
B.基态₃ Cr原子的价层电子轨道表示式:
C.用电子云轮廓图示意p-pπ键的形成:
D.聚苯乙烯的结构简式:
4.下列化学反应的离子方程式正确的是
A.用食醋除去水壶内的水垢: CaCO +2H+=Ca2++CO ↑+H O
3 2 2
B.硫化钠溶液呈碱性的原因:
C. 少量SO 气体通入 NaClO溶液中: 3ClO-+H O+SO =SO2-+Cl-+2HClO
2 2 4
D.氢氧化钡溶液与稀硫酸反应: Ba2++SO2-+H++OH-=BaSO ↓+H O
₂ 4 4 2
高三化学 第 1 页 共8页5.设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4 LHF所含的分子数目为NA
B. 常温下,1 1L0.1mol/lnH HSO 溶液中,由水电离出的 H⁺数目大于 10-13N
4 4 A
C.1L0.1mol⋅L-1的 NaHSO 溶液中含有 0.1NA个 SO2-
3 ₄ 3
D.标准状况下, 11.2lnH 溶于水溶液中 N H+ 、N H ⋅H O的微粒数之和为 0.5N
3 4 3 2 A
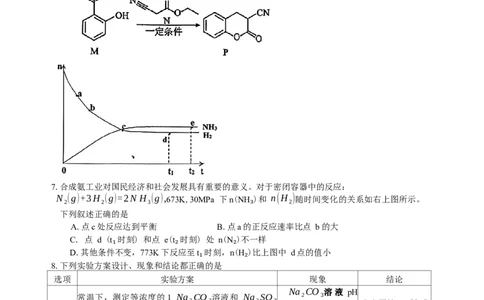
6.色并[4,3-d]嘧啶衍生物具有显著的生物学特性,其合成过程的某步反应如左下图所示。下列说
法正确的是
A. N与水以任意比例互溶 B.1mol M与足量溴水反应最多可消耗 3molBr
2
C.一分子P 酸性环境下水解的有机产物中含有2个含氧官能团
D.M、N、P分子中所有原子均可能共面
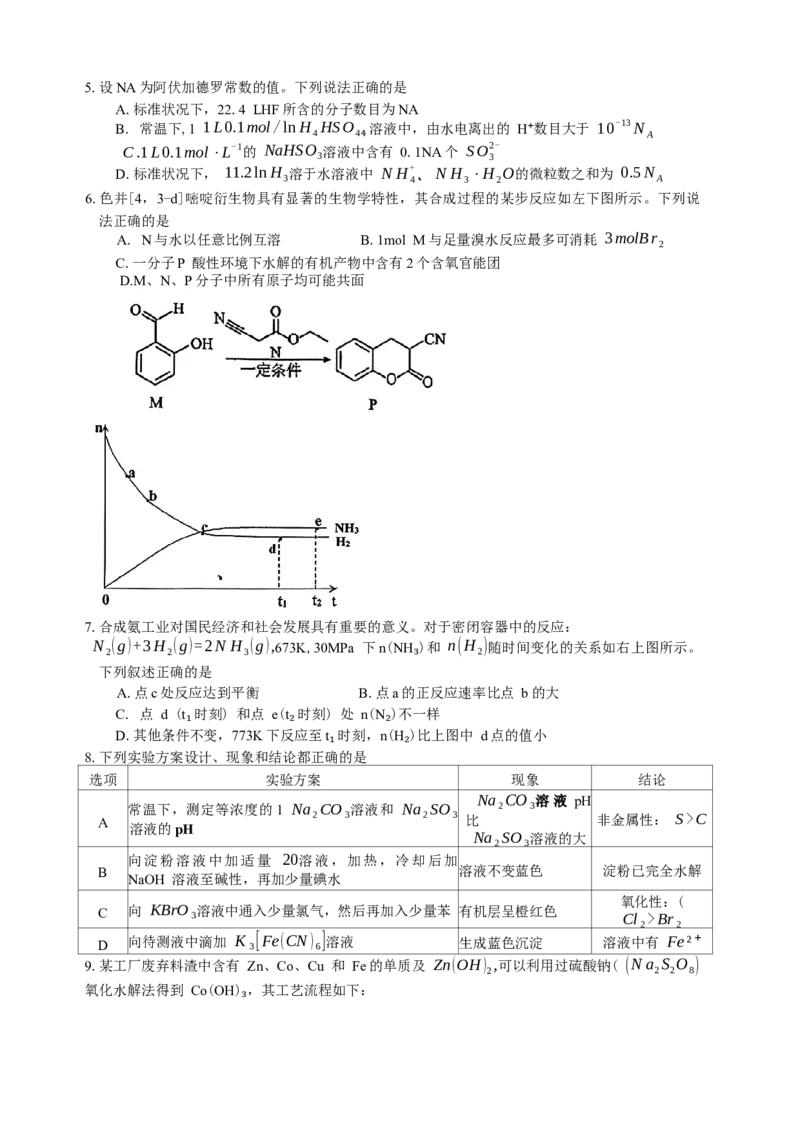
7.合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N (g)+3H (g)=2N H (g),673K,30MPa 下n(NH )和 n(H )随时间变化的关系如右上图所示。
2 2 3 2
下列叙述正确的是
₃
A.点c处反应达到平衡 B.点a的正反应速率比点 b的大
C. 点 d (t 时刻) 和点 e(t 时刻) 处 n(N )不一样
D.其他条件不变,773K下反应至t 时刻,n(H )比上图中 d点的值小
₁ ₂ ₂
8.下列实验方案设计、现象和结论都正确的是
₁ ₂
选项 实验方案 现象 结论
Na₂CO₃溶液 pH
常温下,测定等浓度的1 Na₂CO₃溶液和 Na₂SO₃
A 比 非金属性: S>C
溶液的pH
Na₂SO₃溶液的大
向淀粉溶液中加适量 20溶液,加热,冷却后加
B 溶液不变蓝色 淀粉已完全水解
NaOH 溶液至碱性,再加少量碘水
氧化性:(
C 向 KBrO₃溶液中通入少量氯气,然后再加入少量苯 有机层呈橙红色 Cl₂>Br₂
D 向待测液中滴加 K₃[Fe(CN)₆]溶液 生成蓝色沉淀 溶液中有 Fe²⁺
9.某工厂废弃料渣中含有 Zn、Co、Cu 和 Fe的单质及 Zn(OH) ,可以利用过硫酸钠( (Na S O )
2 2 2 8
氧化水解法得到 Co(OH) ,其工艺流程如下:
₃高三化学 第 2 页 共8页下列说法错误的是
A.Na S O 中硫的化合价为+6
2 2 8
B. 滤渣 1的主要成分是 Fe(OH)
C.依据上述流程, Co2+的还原性小于 Fe2+
D.沉钻时的离子方程式为 2Co2+₃ +Na S O +6OH-=2Co(OH) ↓+2SO2-+2Na+
2 2 3 3 4
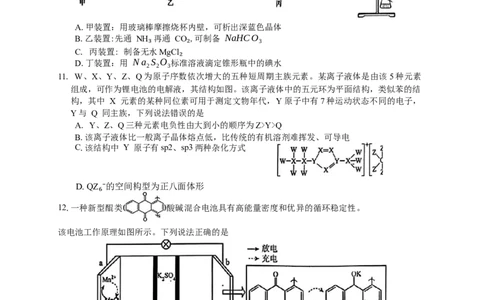
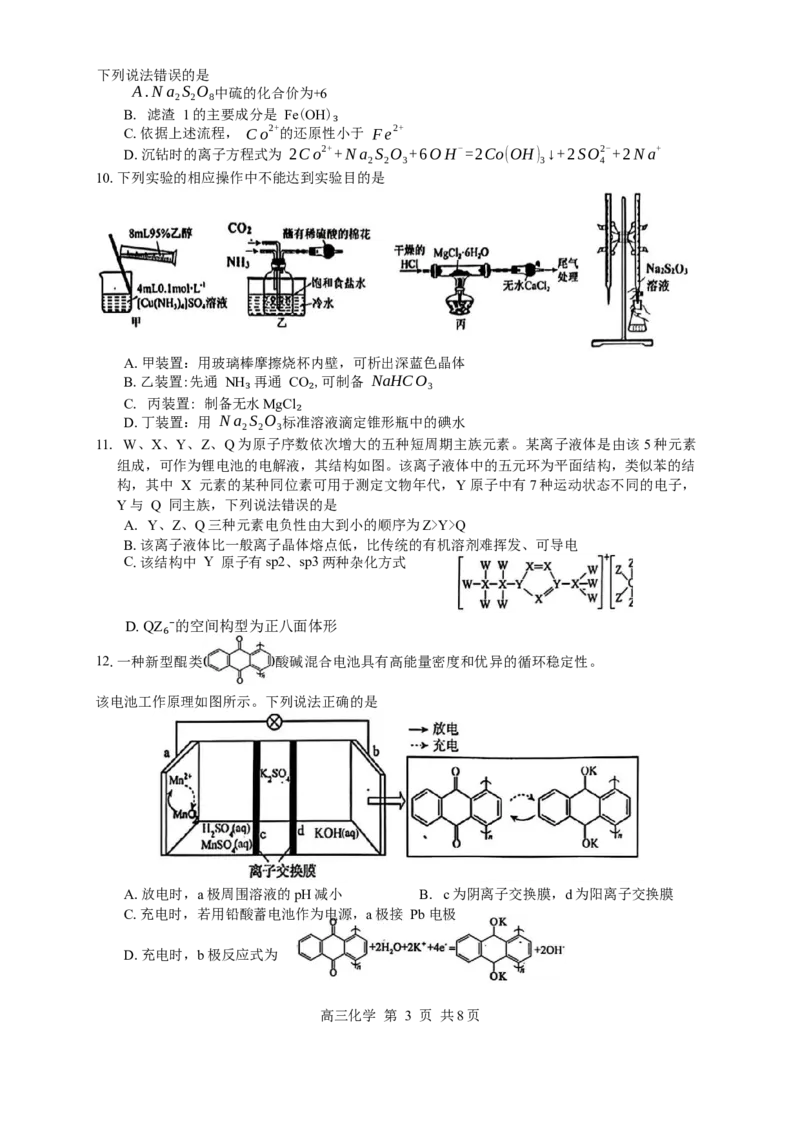
10.下列实验的相应操作中不能达到实验目的是
A.甲装置:用玻璃棒摩擦烧杯内壁,可析出深蓝色晶体
B.乙装置:先通 NH 再通 CO ,可制备 NaHCO
3
C. 丙装置: 制备无水MgCl
₃ ₂
D.丁装置:用 Na S O 标准溶液滴定锥形瓶中的碘水
2 2 3
₂
11. W、X、Y、Z、Q为原子序数依次增大的五种短周期主族元素。某离子液体是由该5种元素
组成,可作为锂电池的电解液,其结构如图。该离子液体中的五元环为平面结构,类似苯的结
构,其中 X 元素的某种同位素可用于测定文物年代,Y原子中有7种运动状态不同的电子,
Y与 Q 同主族,下列说法错误的是
A. Y、Z、Q三种元素电负性由大到小的顺序为Z>Y>Q
B.该离子液体比一般离子晶体熔点低,比传统的有机溶剂难挥发、可导电
C.该结构中 Y 原子有sp2、sp3两种杂化方式
D. QZ 的空间构型为正八面体形
12.一种新型₆⁻醌类 酸碱混合电池具有高能量密度和优异的循环稳定性。
该电池工作原理如图所示。下列说法正确的是
A.放电时,a极周围溶液的pH减小 B. c为阴离子交换膜,d为阳离子交换膜
C.充电时,若用铅酸蓄电池作为电源,a极接 Pb电极
D.充电时,b极反应式为
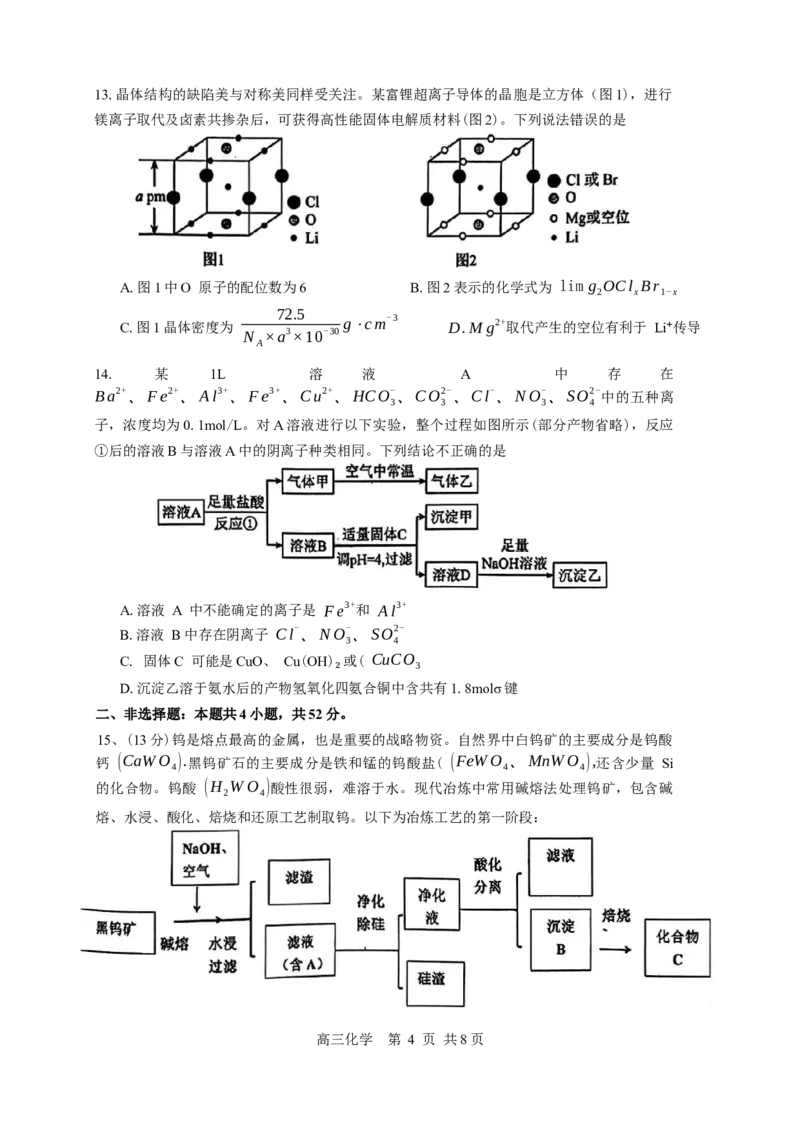
高三化学 第 3 页 共8页13.晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行
镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1中O 原子的配位数为6 B.图2表示的化学式为 lim g OCl Br
2 x 1-x
72.5
C.图1晶体密度为
N ×a3×10-30
g⋅cm-3
D.Mg2+取代产生的空位有利于 Li⁺传导
A
14. 某 1L 溶 液 A 中 存 在
Ba2+ 、Fe2+ 、Al3+ 、Fe3+ 、Cu2+ 、HCO- 、CO2- 、Cl- 、NO- 、SO2-
中的五种离
3 3 3 4
子,浓度均为0.1mol/L。对A溶液进行以下实验,整个过程如图所示(部分产物省略),反应
①后的溶液B与溶液A中的阴离子种类相同。下列结论不正确的是
A.溶液 A 中不能确定的离子是 Fe3+和 Al3+
B.溶液 B中存在阴离子
Cl- 、NO- 、SO2-
3 4
C. 固体C 可能是CuO、 Cu(OH) 或( CuCO
3
D.沉淀乙溶于氨水后的产物氢氧化四氨合铜中含共有1.8molσ键
₂
二、非选择题:本题共4小题,共52分。
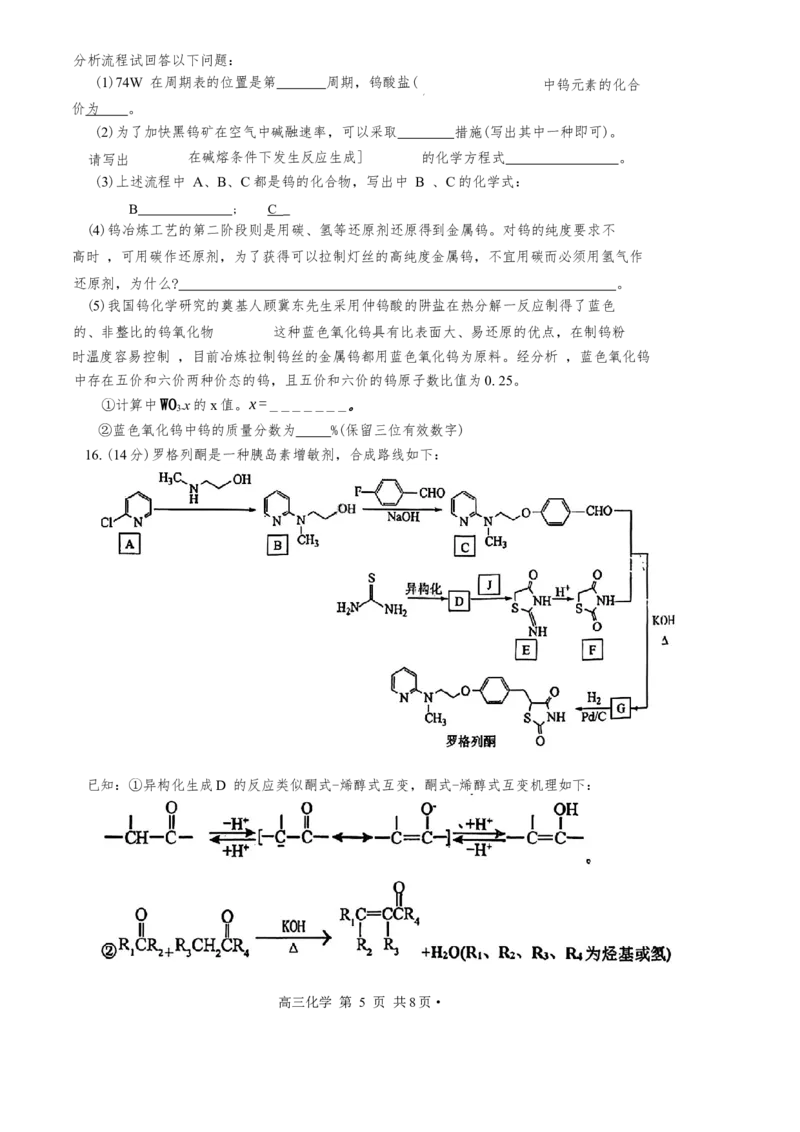
15、(13分)钨是熔点最高的金属,也是重要的战略物资。自然界中白钨矿的主要成分是钨酸
钙 (CaWO ).黑钨矿石的主要成分是铁和锰的钨酸盐( (FeWO 、MnWO ),还含少量 Si
4 4 4
的化合物。钨酸 (H WO )酸性很弱,难溶于水。现代冶炼中常用碱熔法处理钨矿,包含碱
2 4
熔、水浸、酸化、焙烧和还原工艺制取钨。以下为冶炼工艺的第一阶段:
高三化学 第 4 页 共8页分析流程试回答以下问题:
(1)74W 在周期表的位置是第 周期,钨酸盐( 中钨元素的化合
(FeWO 、MnWO )
价为 。 4 4
(2)为了加快黑钨矿在空气中碱融速率,可以采取 措施(写出其中一种即可)。
请写出 在碱熔条件下发生反应生成] 的化学方程式 。
FeWO Fe O
(3)上述流程中4 A、B、C都是钨的化合物,写出2中3 B 、C的化学式:
B ; C
(4)钨冶炼工艺的第二阶段则是用碳、氢等还原剂还原得到金属钨。对钨的纯度要求不
高时 ,可用碳作还原剂,为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作
还原剂,为什么? 。
(5)我国钨化学研究的奠基人顾冀东先生采用仲钨酸的阱盐在热分解一反应制得了蓝色
的、非整比的钨氧化物 这种蓝色氧化钨具有比表面大、易还原的优点,在制钨粉
WO 。
时温度容易控制 ,目前冶炼拉3-制x 钨丝的金属钨都用蓝色氧化钨为原料。经分析 ,蓝色氧化钨
中存在五价和六价两种价态的钨,且五价和六价的钨原子数比值为0.25。
①计算中WO x的x值。x=_______。
3-
②蓝色氧化钨中钨的质量分数为 %(保留三位有效数字)
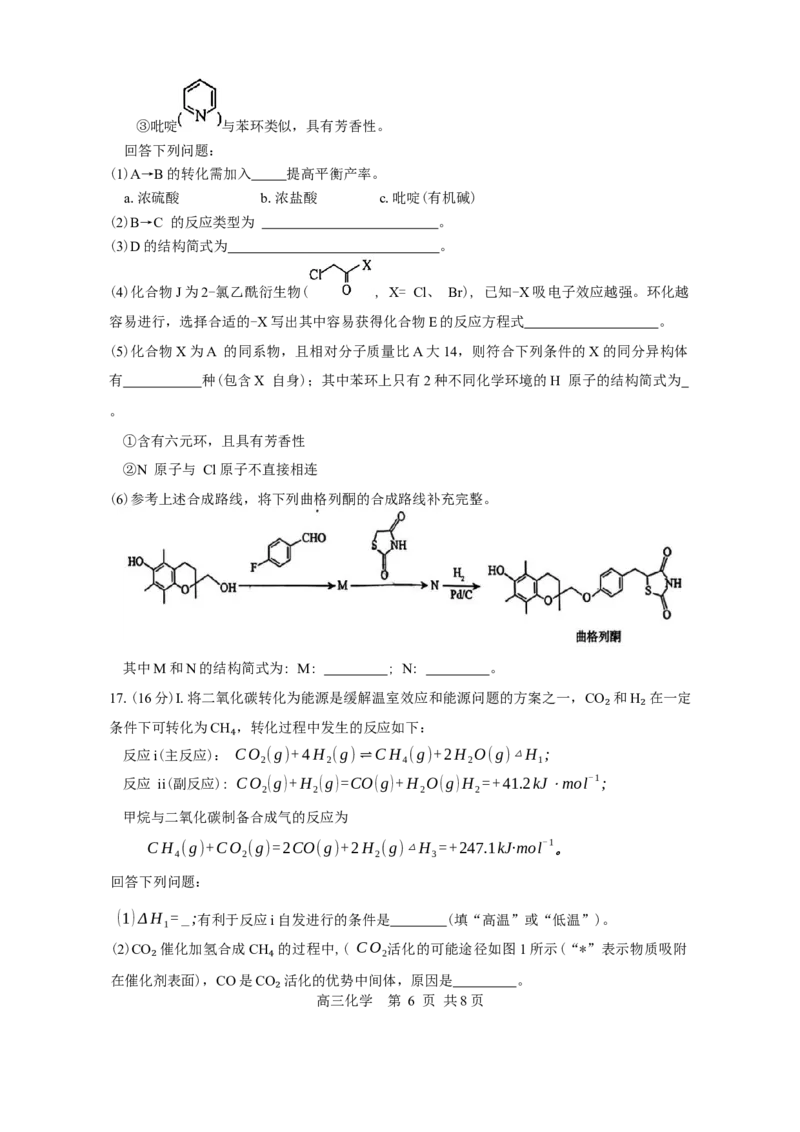
16.(14分)罗格列酮是一种胰岛素增敏剂,合成路线如下:
2000 2024
异构化
J H⁺
D
KOH
△
E F
G
Pd/C
已知:①异构化生成D 的反应类似酮式-烯醇式互变,酮式-烯醇式互变机理如下:
高三化学 第 5 页 共8页·③吡啶 与苯环类似,具有芳香性。
回答下列问题:
(1)A→B的转化需加入 提高平衡产率。
a.浓硫酸 b.浓盐酸 c.吡啶(有机碱)
(2)B→C 的反应类型为 。
(3)D的结构简式为 。
(4)化合物J为2-氯乙酰衍生物( , X= Cl、 Br), 已知-X吸电子效应越强。环化越
容易进行,选择合适的-X写出其中容易获得化合物E的反应方程式 。
(5)化合物X为A 的同系物,且相对分子质量比A大14,则符合下列条件的X的同分异构体
有 种(包含X 自身);其中苯环上只有2种不同化学环境的H 原子的结构简式为
。
①含有六元环,且具有芳香性
②N 原子与 Cl原子不直接相连
(6)参考上述合成路线,将下列曲格列酮的合成路线补充完整。
其中M和N的结构简式为: M: ; N: 。
17.(16分)I.将二氧化碳转化为能源是缓解温室效应和能源问题的方案之一,CO 和H 在一定
条件下可转化为CH ,转化过程中发生的反应如下: ₂ ₂
反应i(主反应):
₄
CO
2
(g)+4H
2
(g)⇌CH
4
(g)+2H
2
O(g)△H
1
;
反应 ii(副反应): CO (g)+H (g)=CO(g)+H O(g)H =+41.2kJ⋅mol-1;
2 2 2 2
甲烷与二氧化碳制备合成气的反应为
CH (g)+CO (g)=2CO(g)+2H (g)△H =+247.1kJ·mol-1。
4 2 2 3
回答下列问题:
(1)ΔH =_;有利于反应i自发进行的条件是 (填“高温”或“低温”)。
1
(2)CO 催化加氢合成CH 的过程中,( CO 活化的可能途径如图1所示(“*”表示物质吸附
2
在催化₂剂表面),CO是CO₄ 活化的优势中间体,原因是 。
高三化学 第 6 页 共8页
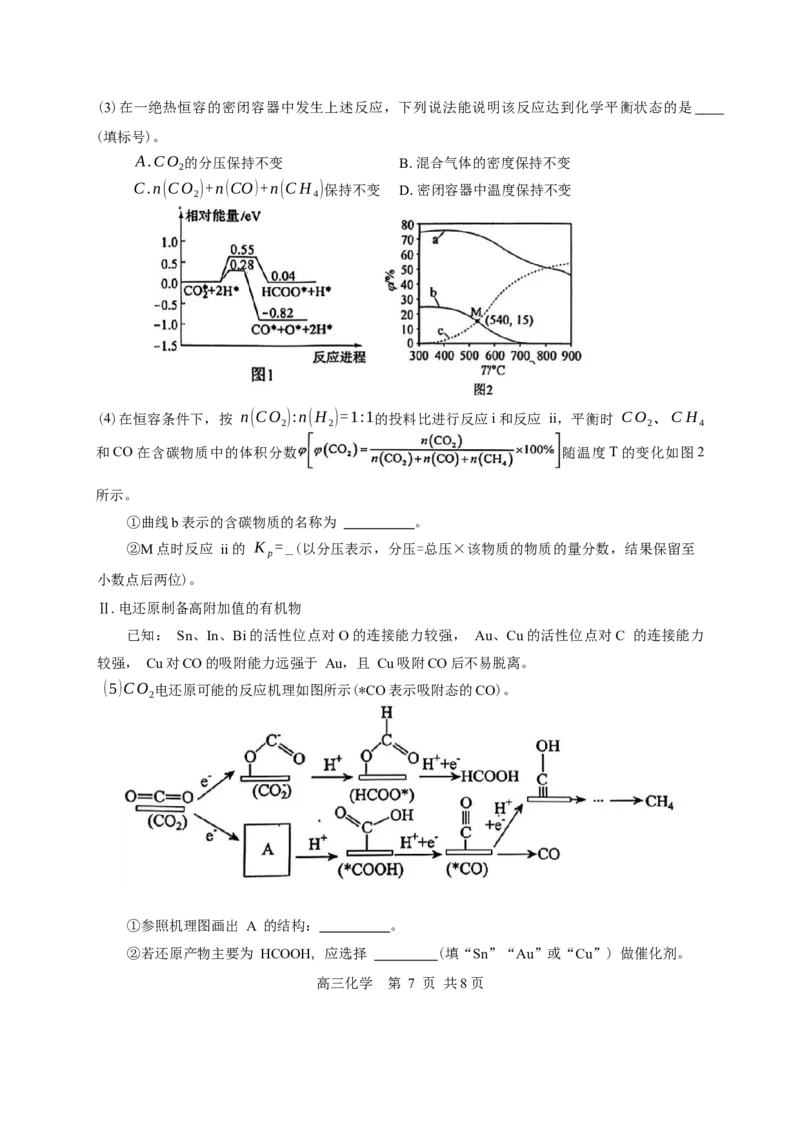
₂(3)在一绝热恒容的密闭容器中发生上述反应,下列说法能说明该反应达到化学平衡状态的是
(填标号)。
A.CO 的分压保持不变 B.混合气体的密度保持不变
2
C.n(CO )+n(CO)+n(CH )保持不变 D.密闭容器中温度保持不变
2 4
(4)在恒容条件下,按 n(CO ):n(H )=1:1的投料比进行反应i和反应 ii,平衡时 CO 、CH
2 2 2 4
和CO在含碳物质中的体积分数 随温度T的变化如图2
所示。
①曲线b表示的含碳物质的名称为 。
②M点时反应 ii的 K =_(以分压表示,分压=总压×该物质的物质的量分数,结果保留至
p
小数点后两位)。
Ⅱ.电还原制备高附加值的有机物
已知: Sn、In、Bi的活性位点对O的连接能力较强, Au、Cu的活性位点对C 的连接能力
较强, Cu对CO的吸附能力远强于 Au,且 Cu吸附CO后不易脱离。
(5)CO 电还原可能的反应机理如图所示(*CO表示吸附态的CO)。
2
①参照机理图画出 A 的结构: 。
②若还原产物主要为 HCOOH, 应选择 (填“Sn”“Au”或“Cu”) 做催化剂。
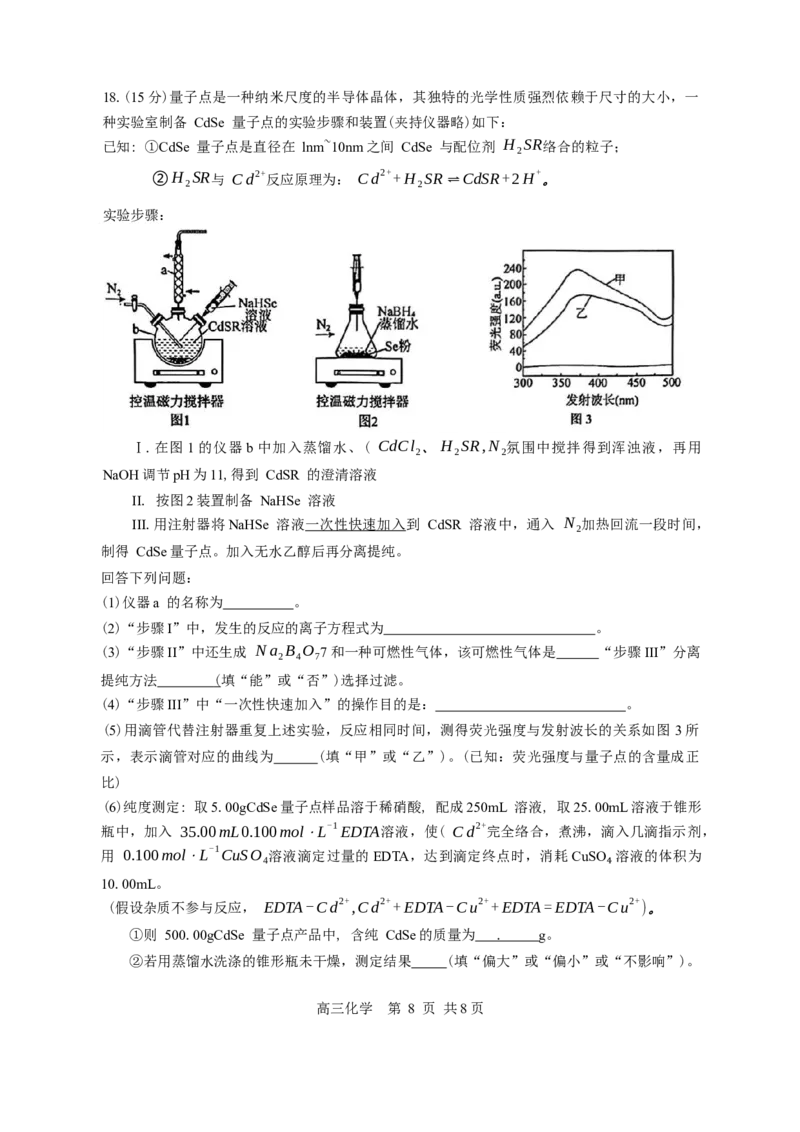
高三化学 第 7 页 共8页18.(15分)量子点是一种纳米尺度的半导体晶体,其独特的光学性质强烈依赖于尺寸的大小,一
种实验室制备 CdSe 量子点的实验步骤和装置(夹持仪器略)如下:
已知: ①CdSe 量子点是直径在 lnm~10nm之间 CdSe 与配位剂 H SR络合的粒子;
2
②H
2
SR与 Cd2+反应原理为: Cd2++H
2
SR⇌CdSR+2H+ 。
实验步骤:
Ⅰ.在图1的仪器b中加入蒸馏水、( CdCl 、H SR,N 氛围中搅拌得到浑浊液,再用
2 2 2
NaOH调节pH为11,得到 CdSR 的澄清溶液
II. 按图2装置制备 NaHSe 溶液
III.用注射器将NaHSe 溶液一次性快速加入到 CdSR 溶液中,通入 N 加热回流一段时间,
2
制得 CdSe量子点。加入无水乙醇后再分离提纯。
回答下列问题:
(1)仪器a 的名称为 。
(2)“步骤I”中,发生的反应的离子方程式为 。
(3)“步骤II”中还生成 Na B O 7和一种可燃性气体,该可燃性气体是 “步骤III”分离
2 4 7
提纯方法 (填“能”或“否”)选择过滤。
(4)“步骤III”中“一次性快速加入”的操作目的是: 。
(5)用滴管代替注射器重复上述实验,反应相同时间,测得荧光强度与发射波长的关系如图 3所
示,表示滴管对应的曲线为 (填“甲”或“乙”)。(已知:荧光强度与量子点的含量成正
比)
(6)纯度测定: 取5.00gCdSe量子点样品溶于稀硝酸, 配成250mL 溶液, 取25.00mL溶液于锥形
瓶中,加入 35.00mL0.100mol⋅L-1EDTA溶液,使( Cd2+完全络合,煮沸,滴入几滴指示剂,
用
0.100mol⋅L-1CuSO
溶液滴定过量的EDTA,达到滴定终点时,消耗CuSO 溶液的体积为
4
10.00mL。
₄
(假设杂质不参与反应,
EDTA-Cd2+,Cd2++EDTA-Cu2++EDTA=EDTA-Cu2+
)。
①则 500.00gCdSe 量子点产品中, 含纯 CdSe的质量为 . g。
②若用蒸馏水洗涤的锥形瓶未干燥,测定结果 (填“偏大”或“偏小”或“不影响”)。
高三化学 第 8 页 共8页景德镇市 2026 届高三第一次质量检测试卷
化学参考答案
一、选择题
序号 1 2 3 4 5 6 7 8 9 10
答案 D C C C B B B D D D
序号 11 12 13 14
答案 C B B A
二、非选择题
15、(13分)
(1) 六 (1分) +6(1分)
(2)粉碎矿石、升温、搅拌均可(1分,答对其中一点给分)
4FeWO +8NaOH+O =4Na WO +2Fe O +4H O (2分)
4 2 2 4 2 3 2
(3) B:H WO (1分) C: WO (1分)
(4)因为钨的熔点很高,不容易转变为液态,如果用碳做还原剂 ,混杂在金属中的碳不易除
₂ ₄ ₃
去 ,而且碳会在高温下和金属钨反应形成碳化钨,不容易获得纯的金属钨。用氢气作还原剂
就不存在这些问题。(答案合理即给分,2分)
(5) ①X=0.10 (2分) ② 79.8 (2分)
16、(14分)
(1)c(1分)
(2)取代反应(1分)
(2分)
(4)Cl+(-Cl+H NH)=-(-NH) NH+2HCl(2分)
2 2
(5)16(2分) (2分)
(6) (2分)
(2分)
17、(16分)
(1)-164.7kJ⋅mol-1
(2分) 低温(2分)
(2)生成中间体CO 的反应的活化能小、反应速率快,且产物能量低、稳定,有利于生成(2
分)
(3)AD(2分)(4)甲烷(2分) 0.39(2分)
(5) (2分) Sn(2分)
18、(15分)
(1)仪器a的名称为球形冷凝管。(1分)
(2)2OH-+Cd2++H SR=CdSR+2H O。(2分)
2 2
(3) H (2分) 否(2分)
(4)①可以隔绝空气防止 Se元素被氧化,提高生成CdSe量子点的产量;
₂
②为了瞬时成核,极短时间内形成大量尺寸相近的晶核,为后续生成尺寸均一量子点奠
定基础。(2分,答案合理,答到其中一点即可给分)
(5) 乙(2分)
(6) ①477.5g; (2分)
②不影响。(2分)