文档内容
2025-2026 学年高三开学摸底考试
化学试题
全卷满分 100 分 考试时间 60 分钟
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1.“嫦娥五号”月球采样、北斗导航系统实现信号全覆盖、国产航母福建舰下水、国产大型飞机 C919
正式交付,这都向世界展示了我国的科技实力。下列材料为金属材料的是
A.“嫦娥五号”采回来的 B.北斗卫星中的光伏太阳 C.舰体材料中用到的耐腐
D.飞机机身使用的碳纤维
月壤“嫦娥石” 能电池板 蚀低磁合金钢
2.进行化学实验要注意实验安全,正确的实验操作是获得正确的实验结果和保障人身安全的前提。下
列实验操作正确的是
3.冬季气候寒冷,宜多吃肉类和根茎食物,以补充人体活动所需的能量。下列说法错误的是
..
A.淀粉和纤维素互为同分异构体
B.将碘酒滴到土豆片上,其表面出现蓝色
C.驴皮制作的阿胶的主要成分为蛋白质
D.液态植物油和氢气加成可制得人造脂肪
4.反应 3Fe OH可应用于铁强
化剂 2+ 2的− 制备。下列−说法正确的是
푒 +2퐻푃푂4 +2퐶퐻3퐶푂푂 +8퐻2푂= 퐹푒3 푃푂4 2⋅8퐻2푂↓+2퐶퐻3퐶푂푂
A.基态
퐹푒3
Fe
푃
²
푂⁺ 4
的
2⋅
价
8퐻
层
2
电
푂
子排布式为3d⁵
B. PO³ 的VSEPR 模型为四面体形
⁻
C. H₂ O分子的空间填充模型为(
D. CH₃ COOH晶体属于共价晶体
5.肼( 可用作火箭燃料,还是一种良好的极性溶剂。沿肼分子球棍模型的氮氮键方向
观察,看到的平面图如图所示。下列说法正确的是
퐻2푁−푁퐻2
A.肼分子中含π键
B.肼分子中的氮原子采用 sp² 杂化
C.肼晶体中分子间只存在范德华力
D.肼能与水混溶
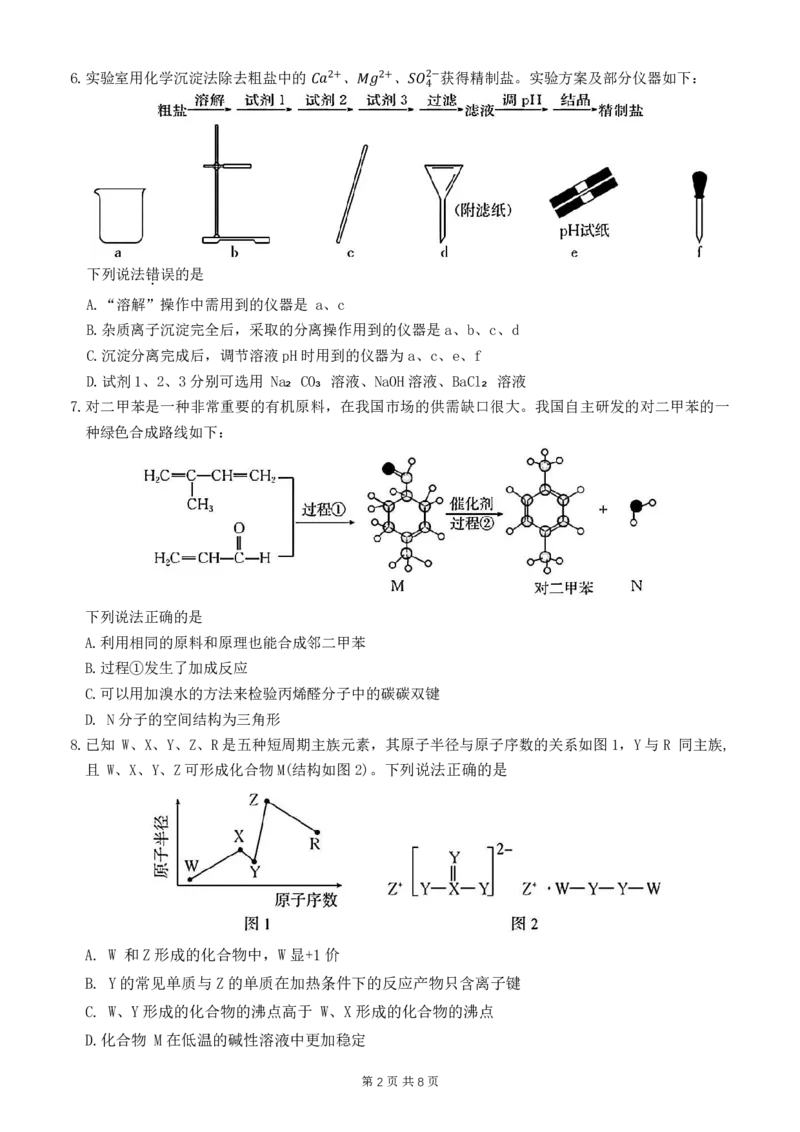
第1页共8页6.实验室用化学沉淀法除去粗盐中的 、 、 获得精制盐。实验方案及部分仪器如下:
2+ 2+ 2−
퐶푎 푀푔 푆푂4
下列说法错误的是
.
A.“溶解”操作中需用到的仪器是 a、c
B.杂质离子沉淀完全后,采取的分离操作用到的仪器是a、b、c、d
C.沉淀分离完成后,调节溶液pH时用到的仪器为a、c、e、f
D.试剂1、2、3分别可选用 Na₂ CO₃ 溶液、NaOH溶液、BaCl₂ 溶液
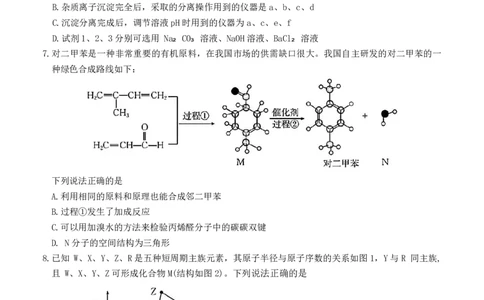
7.对二甲苯是一种非常重要的有机原料,在我国市场的供需缺口很大。我国自主研发的对二甲苯的一
种绿色合成路线如下:
下列说法正确的是
A.利用相同的原料和原理也能合成邻二甲苯
B.过程①发生了加成反应
C.可以用加溴水的方法来检验丙烯醛分子中的碳碳双键
D. N分子的空间结构为三角形
8.已知 W、X、Y、Z、R是五种短周期主族元素,其原子半径与原子序数的关系如图1,Y与R 同主族,
且 W、X、Y、Z可形成化合物M(结构如图2)。下列说法正确的是
A. W 和Z形成的化合物中,W显+1价
B. Y的常见单质与 Z的单质在加热条件下的反应产物只含离子键
C. W、Y形成的化合物的沸点高于 W、X形成的化合物的沸点
D.化合物 M在低温的碱性溶液中更加稳定
第2页共8页9.已知部分弱酸的电离平衡常数如下表所示。下列说法错误的是
弱酸 CH₃ COOH HCN H₂ CO₃
电离平衡 ₂퐻 푆₃푂
常数(25℃)
ₐ퐾₁ =5.0×1⁻0⁷ ₐ퐾₁ =1.3×1⁻0 ²
ₐ퐾 =1.8×1⁻0⁵ ₐ퐾 = 6.2 ×
ₙ퐾₂ =5.6×1⁻0 ¹¹ ₃퐾₂ =6.2×1⁻0⁸
A.常温下,物质的量浓度相同的四种溶液1⁻0,⁰¹pH 由大到小的顺序是 C
H₃ COONa 푁푎2퐶푂3 > 푁푎퐶푁> 푁푎2푆푂3 >
B.将少量SO₂ 通入 Na₂ CO₃ 溶液中,离子方程式是
的 Na₂ SO₃ 溶液中,存在 2− 2− −
푆푂2+퐻2푂+2퐶푂3 =푆푂3 +2퐻퐶푂3
D.向 NaCN 溶−液1 中加水稀释,溶液的 pH增大 − + −
퐶.0.1푚표푙⋅퐿 푐 푂퐻 =푐 퐻 +푐 퐻푆푂3 +2푐 퐻2푆푂3
10.探究氮及其化合物的性质,下列实验方案、现象和结论都正确的是选项
实验方案 现象 结论
压缩盛有 NO₂ 气体的容器体积 证明 NO₂ 气体中存在平衡 2NO₂ (g)
A 红棕色先变深,后变浅
至原来的一半
B
将 Fe(NO₃ )₂ 样品溶于稀硫酸
溶液变红 Fe(NO₃ ) = ₂ ₂푁 晶 ₄푂 体已 푔 氧化变质
后,滴加 KSCN溶液
常温下,将铁片分别插入稀硝酸 前者产生无色气体,后者
C 稀硝酸的氧化性比浓硝酸强
和浓硝酸中 无明显现象
将某固体试样加水溶解,然后滴 没有产生使湿润红色石蕊
D 该固体试样中不存在 NH⁺
加 NaOH溶液 试纸变蓝的气体
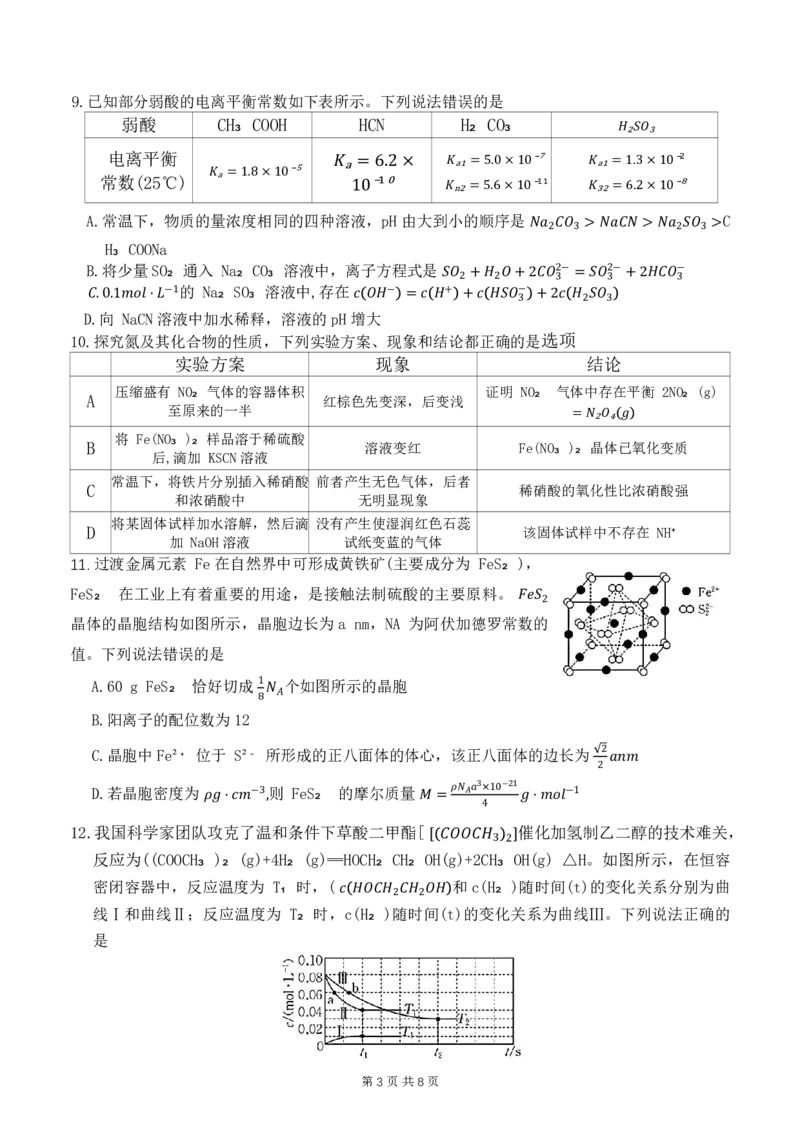
11. 过渡金属元素 Fe 在自然界中可形成黄铁矿(主要成分为 FeS₂ ),
FeS₂ 在工业上有着重要的用途,是接触法制硫酸的主要原料。
晶体的晶胞结构如图所示,晶胞边长为 a nm,NA 为阿伏加德罗常数 퐹푒 的 푆2
值。下列说法错误的是
A.60 g FeS₂ 恰好切成 个如图所示的晶胞
1
B.阳离子的配位数为 12 8푁퐴
C.晶胞中Fe² 位于 S² 所形成的正八面体的体心,该正八面体的边长为
⁺ ⁻
2
D.若晶胞密度为 则 FeS₂ 的摩尔质量 2 푎푛푚
3 −21
−3 휌푁퐴푎 ×10 −1
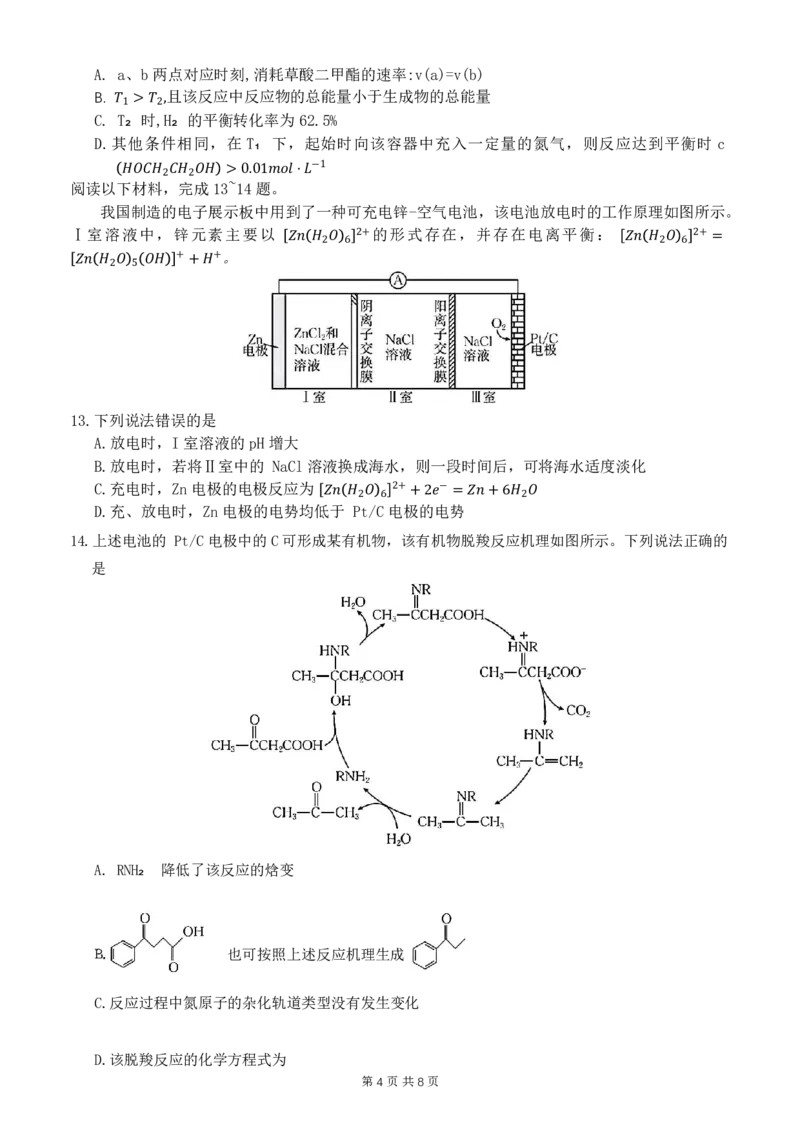
12.我国科学家团队 휌 攻 푔 克 ⋅푐푚 了温 , 和条件下草酸二甲酯[ 푀= 4 催 푔⋅ 化 푚 加 표푙 氢制乙二醇的技术难关,
反应为((COOCH₃ )₂ (g)+4H₂ (g)═HOCH₂ CH₂ OH(g)+2CH₃ OH(g) △H。如图所示,在恒容
퐶푂푂퐶퐻3 2
密闭容器中,反应温度为 T₁ 时,( 和 c(H₂ )随时间(t)的变化关系分别为曲
线Ⅰ和曲线Ⅱ;反应温度为 T₂ 时, 푐 c( 퐻 H 푂 ₂ 퐶퐻 )随 2퐶 时 퐻2 间 푂퐻 (t)的变化关系为曲线Ⅲ。下列说法正确的
是
第3页共8页A. a、b两点对应时刻,消耗草酸二甲酯的速率:v(a)=v(b)
B. 且该反应中反应物的总能量小于生成物的总能量
C. T₂ 时,H₂ 的平衡转化率为 62.5%
푇1 > 푇2,
D.其他条件相同,在 T₁ 下,起始时向该容器中充入一定量的氮气,则反应达到平衡时 c
阅读以下材料,完成 13~14题。 −1
퐻푂퐶퐻2퐶퐻2푂퐻 >0.01푚표푙⋅퐿
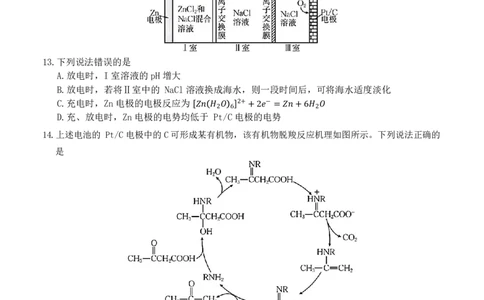
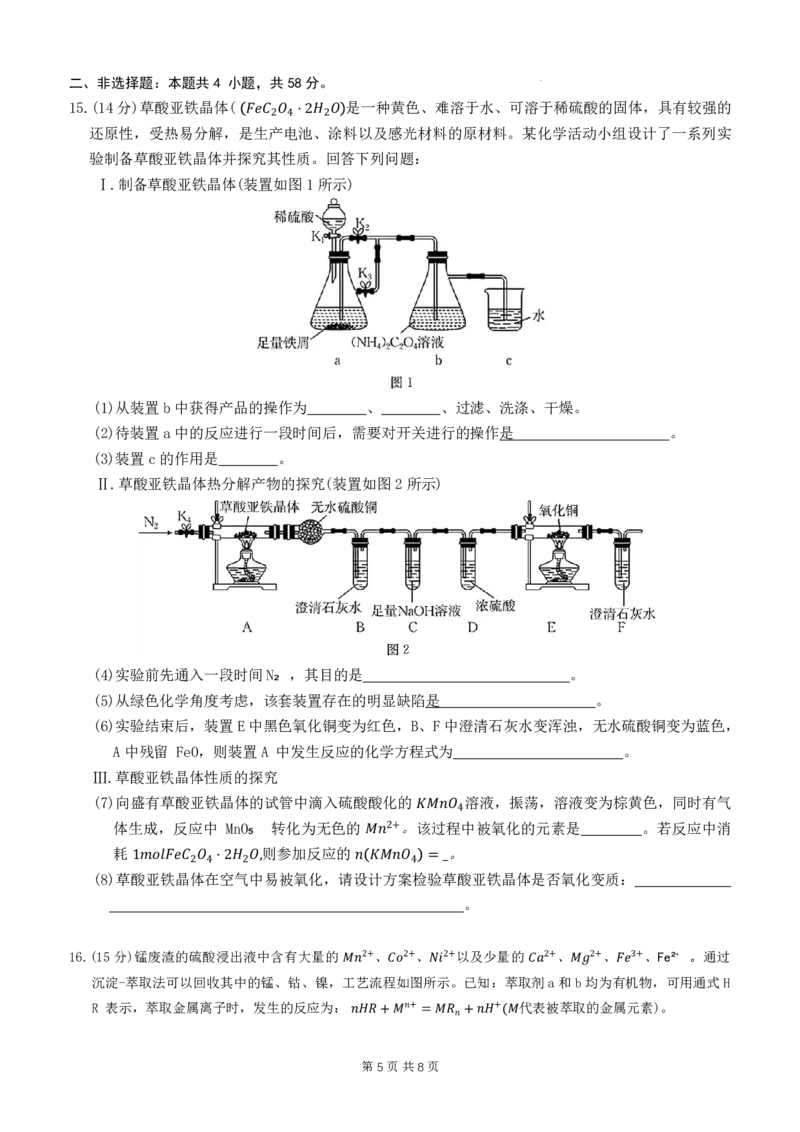
我国制造的电子展示板中用到了一种可充电锌-空气电池,该电池放电时的工作原理如图所示。
Ⅰ室溶液中,锌元素主要以 的形式存在,并存在电离平衡:
。 2+ 2+
푍푛 퐻2푂 6 푍푛 퐻2푂 6 =
+ +
푍푛 퐻2푂 5 푂퐻 +퐻
13.下列说法错误的是
A.放电时,I室溶液的 pH增大
B.放电时,若将Ⅱ室中的 NaCl溶液换成海水,则一段时间后,可将海水适度淡化
C.充电时,Zn电极的电极反应为
D.充、放电时,Zn电极的电势均低于 Pt/C电2+极的电−势
푍푛 퐻2푂 6 +2푒 = 푍푛+6퐻2푂
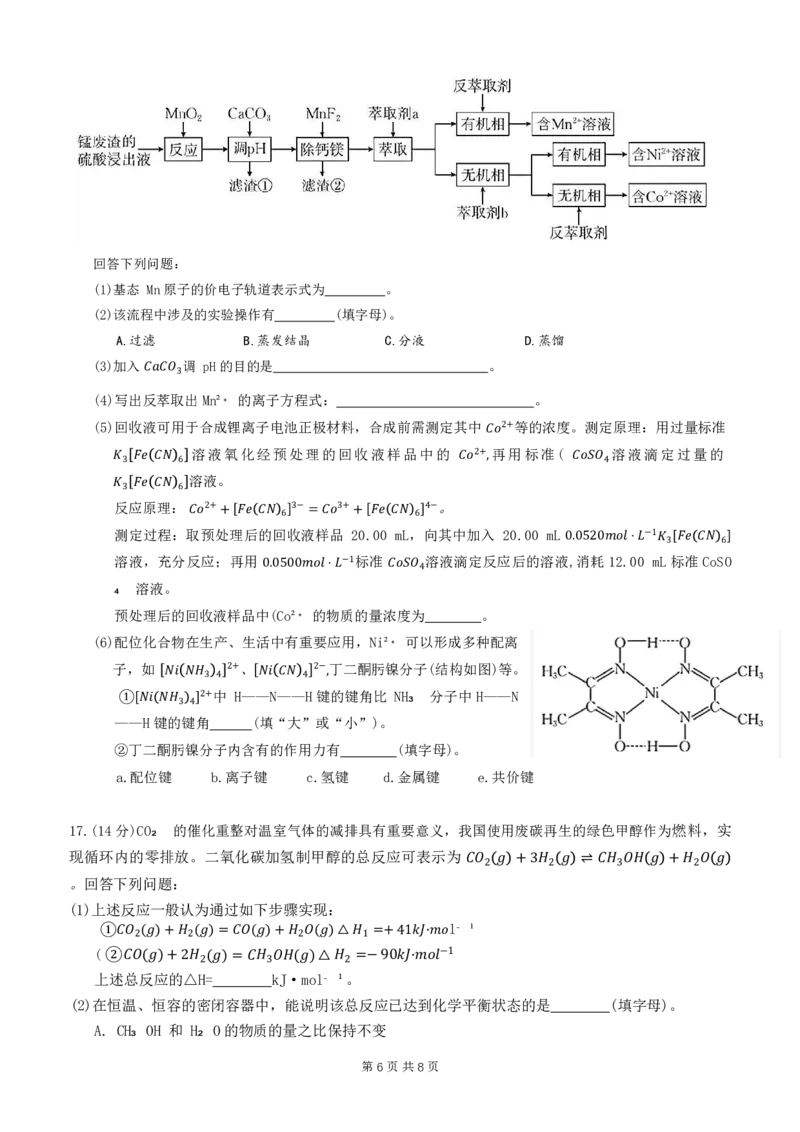
14.上述电池的 Pt/C电极中的C可形成某有机物,该有机物脱羧反应机理如图所示。下列说法正确的
是
A. RNH₂ 降低了该反应的焓变
也可按照上述反应机理生成
C.反应过程中氮原子的杂化轨道类型没有发生变化
D.该脱羧反应的化学方程式为
第4页共8页二、非选择题:本题共4 小题,共58分。
15.(14分)草酸亚铁晶体( 是一种黄色、难溶于水、可溶于稀硫酸的固体,具有较强的
还原性,受热易分解,是生产电池、涂料以及感光材料的原材料。某化学活动小组设计了一系列实
퐹푒퐶2푂4⋅2퐻2푂
验制备草酸亚铁晶体并探究其性质。回答下列问题:
Ⅰ.制备草酸亚铁晶体(装置如图1所示)
(1)从装置b中获得产品的操作为 、 、过滤、洗涤、干燥。
(2)待装置a中的反应进行一段时间后,需要对开关进行的操作是 。
(3)装置c的作用是 。
Ⅱ.草酸亚铁晶体热分解产物的探究(装置如图2所示)
(4)实验前先通入一段时间N₂ ,其目的是 。
(5)从绿色化学角度考虑,该套装置存在的明显缺陷是 。
(6)实验结束后,装置E中黑色氧化铜变为红色,B、F中澄清石灰水变浑浊,无水硫酸铜变为蓝色,
A中残留 FeO,则装置A 中发生反应的化学方程式为 。
Ⅲ.草酸亚铁晶体性质的探究
(7)向盛有草酸亚铁晶体的试管中滴入硫酸酸化的 溶液,振荡,溶液变为棕黄色,同时有气
体生成,反应中 MnO₅ 转化为无色的 。该过程中被氧化的元素是 。若反应中消
퐾푀푛푂4
耗 则参加反应的 2+ 。
푀푛
(8)草酸亚铁晶体在空气中易被氧化,请设计方案检验草酸亚铁晶体是否氧化变质:
1푚표푙퐹푒퐶2푂4⋅2퐻2푂, 푛 퐾푀푛푂4 =_
。
16.(15分)锰废渣的硫酸浸出液中含有大量的 、 、 以及少量的 、 、 、Fe²⁺ 。通过
2+ 2+ 2+ 2+ 2+ 3+
沉淀-萃取法可以回收其中的锰、钴、镍,工艺流程如图所示。已知:萃取剂a和b均为有机物,可用通式H
푀푛 퐶표 푁푖 퐶푎 푀푔 퐹푒
R 表示,萃取金属离子时,发生的反应为: 代表被萃取的金属元素)。
푛+ +
푛퐻푅+푀 =푀푅푛+푛퐻 (푀
第5页共8页回答下列问题:
(1)基态 Mn原子的价电子轨道表示式为 。
(2)该流程中涉及的实验操作有 (填字母)。
A.过滤 B.蒸发结晶 C.分液 D.蒸馏
(3)加入 调 pH的目的是 。
(4)写出反퐶푎萃퐶푂取 3 出Mn² 的离子方程式: 。
⁺
(5)回收液可用于合成锂离子电池正极材料,合成前需测定其中 等的浓度。测定原理:用过量标准
2+
溶液氧化经预处理的回收液样品中的 再用标准( 溶液滴定过量的
퐶표
2+
퐾3 퐹푒 퐶푁 6 溶液。 퐶표 , 퐶표푆푂4
퐾 反3应 퐹푒 原 퐶 理 푁 :6 。
2+ 3− 3+ 4−
测定过程:取
퐶표
预处
+
理
퐹
后
푒
的
퐶푁
回6收液
=
样
퐶
品
표
2
+
0.
퐹
0
푒
0
퐶
m
푁
L,6向其中加入 20.00 mL
−1
溶液,充分反应;再用 标准 溶液滴定反应后的溶液
0
,
.0
消
52
耗
0푚
12
표
.
푙
0
⋅
0
퐿
m
퐾
L3标
퐹
准
푒 퐶
C
푁
oS6O
−1
₄ 溶液。 0.0500푚표푙⋅퐿 퐶표푆푂4
预处理后的回收液样品中(Co² 的物质的量浓度为 。
⁺
(6)配位化合物在生产、生活中有重要应用,Ni² 可以形成多种配离
⁺
子,如 、 丁二酮肟镍分子(结构如图)等。
2+ 2−
푁푖
푁퐻3中4 H——
푁푖
N—
퐶푁
—4H键
,
的键角比 NH₃ 分子中H——N
2+
—
①
—
푁
H
푖
键
푁
的 퐻3键4角 (填“大”或“小”)。
②丁二酮肟镍分子内含有的作用力有 (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键 e.共价键
17.(14分)CO₂ 的催化重整对温室气体的减排具有重要意义,我国使用废碳再生的绿色甲醇作为燃料,实
现循环内的零排放。二氧化碳加氢制甲醇的总反应可表示为
。回答下列问题:
퐶푂2 푔 +3퐻2 푔 ⇌ 퐶퐻3푂퐻 푔 +퐻2푂 푔
(1)上述反应一般认为通过如下步骤实现:
l ¹
⁻
( ①퐶푂2(푔)+퐻2(푔)= 퐶푂(푔)+퐻2푂(푔)△퐻1 =+41푘퐽·푚표
上述总反应的△H= kJ·mol ¹。 −1
②퐶푂(푔)+2퐻2(푔)= 퐶퐻3푂퐻(푔)△⁻ 퐻2 =−90푘퐽·푚표푙
(2)在恒温、恒容的密闭容器中,能说明该总反应已达到化学平衡状态的是 (填字母)。
A. CH₃ OH 和 H₂ O的物质的量之比保持不变
第6页共8页B.气体的平均相对分子质量保持不变
C.单位时间内断裂3m ol H—H键的同时断裂2m ol H—O键
追
(3)在
퐷.
某
푣
催 퐻2化2: 剂
푣
作
퐶퐻
用3푂 下
퐻
,只
=
发
3
生
:1
反应( 。 该反应的速率方程为
),k为速率常数,只与温度、催化剂有关。830℃时
正 正 追 追 퐶푂2 푔 +퐻2 푔 =퐶푂 푔 +퐻2푂 푔
푣 该反 = 应 푘 的 푐 平 퐶 衡 푂 常2 数 ⋅푐 퐻 K=21, ,푣 达到 = 平 푘 衡 푐 后 퐶 , 푂 kRE ⋅푐 퐻2푂 (填“>”“<”或“=”,下同)k逆;900 ℃时,k正
k逆。
(4)在2 L 密闭容器中充入 1m ol CO₂ (g)和3 mol H₂ (g),发生反应
测得一定时间内混合气体中CH₃ OH(g)的体积
퐶푂2 푔 +
分数 与温度(T)的关系如图所示(不考虑催化剂失去活性)。
3퐻2 푔 = 퐶퐻3푂퐻 푔 +퐻2푂 푔 ,
①温度 퐶 为 퐻3 T 푂 ₁ 퐻 时,若反应15 min,φ(CH₃ OH)=30%,则0~15 min内,CH₃ OH的
平均反应速率v= 。
②b点对应的 ,则反应的平衡常数. 。
(5)向一定浓度的K
퐶
N
퐻
O₃3푂 溶
퐻
液
=
中
2
通
5%
入
,
CO₂ 至饱和,在电极上
퐾
反
=
应
_
生成 电解原理如图所示(阴、
阳极区溶液均为 KNO₃ 溶液)。电解过程中生成尿素的电极反应为 。
퐶푂 푁퐻2 2,
18.(15分)萘氧啶是一种抗肿瘤药物,其一种合成路线如下:
回答下列问题:
第7页共8页(1)A (填“有”或“无”)顺反异构体,萘氧啶的分子式为 。
(2)B中有 个手性碳原子。C中所含的官能团为羧基和 。
(3)A→B、C→D的反应类型分别是 、 。
(4)1mol C最多能与 mol H₂ 发生加成反应,C完全加成后的产物与足量金属 Na反应的化学方程式
为 。
(5)T除碳氢外仅含一个氧原子且相对分子质量比E少106,在T的芳香族同分异构体中,同时满足下列条件
的有 种(不考虑立体异构)。
①能发生银镜反应 ②苯环上含2个侧链 ③分子只含一个环
第8页共8页2025-2026 学年高三开学摸底考试
化学答案
题序 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C C A B D D B D D A B C A D
15.答案 (1)蒸发浓缩(1分);冷却结晶(1分)
(2)打开K ,关闭K (1分)
(3)隔离空气,防止生成的草酸亚铁晶体被空气中的氧气氧化(2分)
₂ ₃
(4)排尽装置内的空气,防止空气中 H O和CO 的干扰(2分)
(5)缺少处理CO尾气的装置(1分)
₂ ₂
(2分)
((76))퐹F푒e퐶、2C푂(41·2分퐻2)푂;\xmloonlg(e或qu(0al.△6m퐹o푒l푂)(+1퐶分푂)2 ↑+퐶푂 ↑+2퐻2푂
3
(8)取少量草酸亚铁5晶体于试管中,加入稀硫酸溶解后滴加KSCN溶液,若溶液变红色,则草酸亚铁晶体已氧化
变质,若溶液不变红色,则草酸亚铁晶体未氧化变质(2分)
16.
(2)AC(2分)
(3)使 Fe³ 转化成Fe(OH) 沉淀而除去(2分)
2分)
⁺ ₃
+ 2+
(
4
5)
푀
0.
푛
0
푅
222
+
mo
2
l
퐻
·L
=
¹
2
(
퐻
3
푅
分
+
)
푀푛 (2
(6)①大(2分)
⁻
②ace(2分)
17.(1)-49(2分) (2)BD(2分) (3)=(2分);>(2分)
(2 分) ② (2分)
−1 −1 16
4 ①0.025푚표푙⋅퐿 ⋅min 3 分)
− − +
18.( 5 1) 2 有 푁 ( 푂 13分 + ) 1 ; 6 C 푒 H + N 퐶 O 푂2Cl + (2 18 分 퐻 ) =퐶푂 푁퐻2 2+7퐻2푂(2
(2)1(1分);醚键、酮羰基(1分)
₂₉ ₃₂ ₂
(3)加成反应(1分);还原反应(1分)
(4)7(1分);
(5)18(2分)
第 1 页 共 1 页