文档内容
南阳一中2025 年秋期高三年级第一次月考
化学答案
选择题 1-5CCBDC 6-10BCBCB 11-14 CDDA
非选择题 除标注外 每空2 分
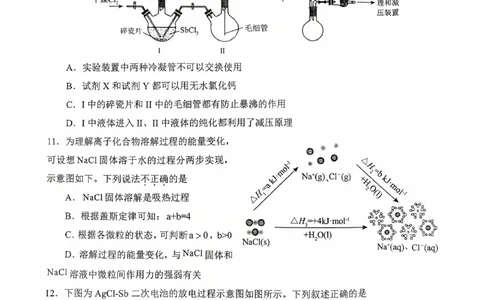
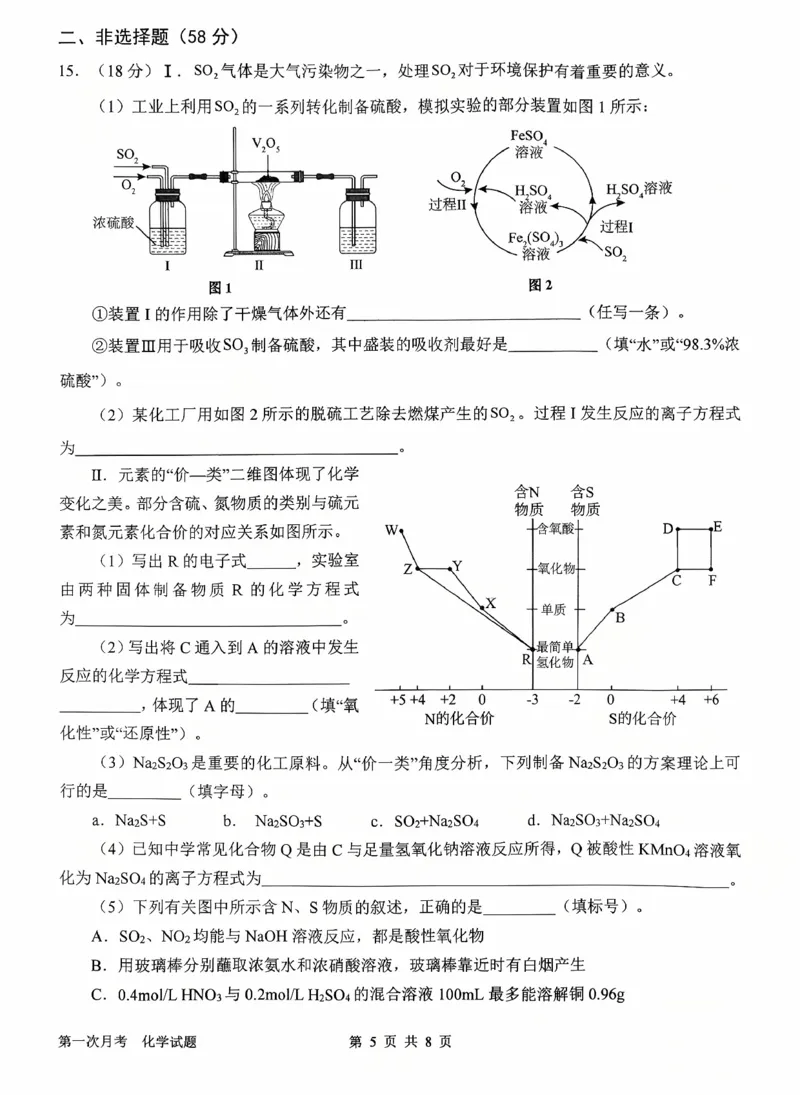
15.(18 分)Ⅰ.(1) 使气体充分混合或观察气泡产生速率来控制气体流速 98.3%浓硫酸(1 分)
(2)
3
2
2
2
2
4
2Fe
SO
2H O
2Fe
4H
SO
Ⅱ.(1)
4
2
2
3
2
2NH Cl
Ca(OH)
CaCl
2NH
2H O
(2)
2
2
2
2H S
SO
3S
2H O
还原性(1 分) (3)b (4)
-
2
2
2
4
3
4
2
2MnO
5SO
6H
2Mn
5SO
3H O
(5)B
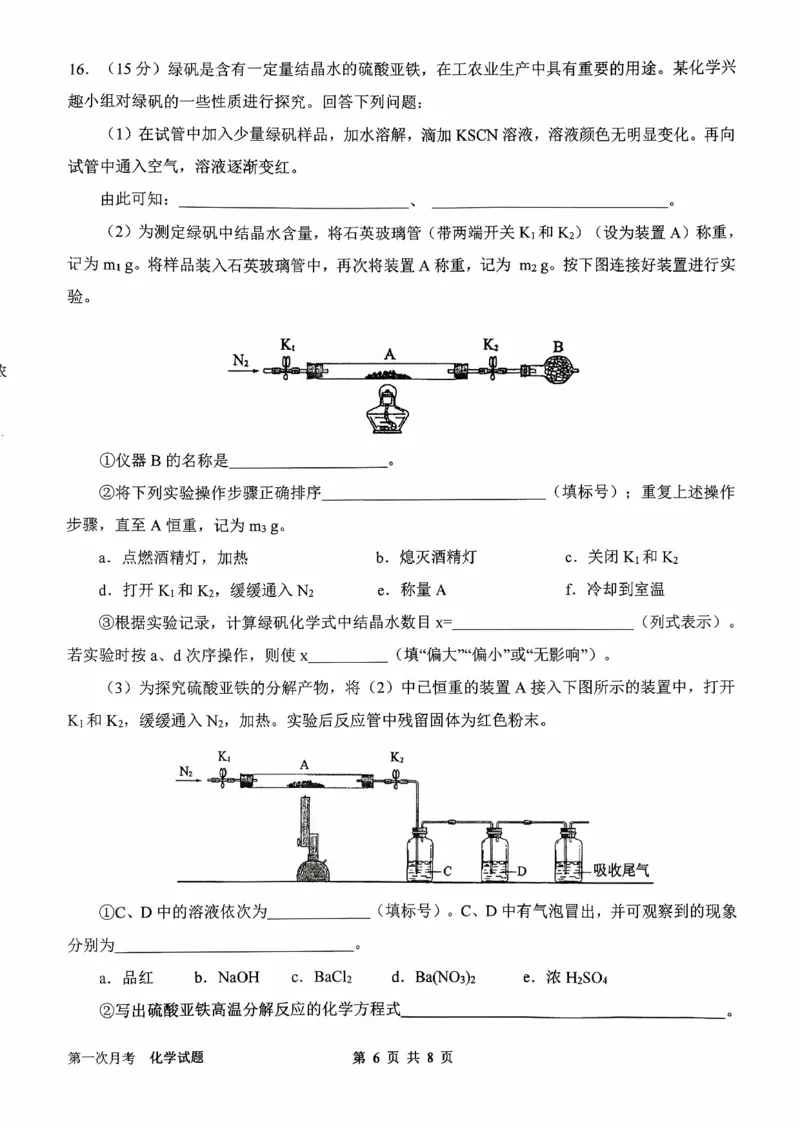
16.(15 分)样品中没有Fe3+(1 分) Fe2+易被氧气氧化为Fe3+ (1 分) 干燥管(1 分) dabfce
2
3
3
1
76(
)
9(
)
m
m
m
m
偏小 c、a 生成白色沉淀、褪色 2FeSO4
Fe2O3+SO2↑+SO3↑
【详解】(1)样品溶于水滴加KSCN 溶液,溶液颜色无明显变化,说明样品中无Fe3+;再向试管中通入
空气,溶液逐渐变红,这说明有铁离子产生,即硫酸亚铁易被空气氧化为硫酸铁,铁离子遇KSCN 溶液显红
色;
(2)①根据仪器构造可知B 是干燥管;
②由于装置中含有空气,空气能氧化硫酸亚铁,所以加热前需要排尽装置中空气,利用氮气排出空气,
为了使生成的水蒸气完全排除,应该先熄灭酒精灯再冷却,然后关闭K1 和K2,最后称量,即正确的排序是
dabfce;
③样品的质量是(m2-m1)g,加热后剩余固体是硫酸亚铁,质量为(m3-m1)g,生成水的质量为(m2-
m3)g,
FeSO4·xH2O
FeSO4 + xH2O
152 18x
(m3-m1)g (m2-m3)g
则:
3
1
2
3
152
18x
m
m
g
m
m
g
,解得:x=
2
3
3
1
76
9
m
m
m
m
;
若实验时按a、d 次序操作,在加热过程中硫酸亚铁被空气氧化为硫酸铁,导致m3 增加,因此x 偏小;
(3)①最终得到红棕色固体,说明有氧化铁生成,即分解过程发生了氧化还原反应,根据化合价变化
可知一定有SO2 生成,这说明硫酸亚铁分解生成氧化铁、SO2 和三氧化硫。三氧化硫溶于水生成硫酸,硫酸
和钡离子结合生成白色沉淀硫酸钡,由于硝酸钡在酸性溶液中有氧化性,能氧化SO2,所以应该用氯化钡,
检验SO2 用品红溶液,所以C、D 的溶液依次为氯化钡溶液和品红溶液,实验现象是C 中溶液变浑浊产生白
色沉淀,D 中品红溶液褪色,故答案为c、a;
②根据以上分析可知硫酸亚铁高温分解生成氧化铁、SO2 和SO3,根据电子守恒和原子守恒得此反应的
方程式为2FeSO4
Fe2O3+SO2↑+SO3。
17. (10 分)ZnO(1 分) 浸出(1 分) 锌粉或者ZnO 等(1 分) 置换出Fe 或调节pH
使铁离子转化为Fe(OH)3 O2 (1 分) 2ZnS+4H++ O2=2Zn2++2S↓+2H2O ZnCO3+2C
高温
Zn+3CO↑
解析:(1) 由于硫化锌精矿的成分是ZnS,焙烧在氧气气氛的沸腾炉中进行,发生反应:
2ZnS+3O2
高温
2ZnO+2SO2。因此所产生焙砂的主要成分是ZnO。(2)焙烧过程中产生的含尘烟气主要成分是
SO2 可净化制酸,该酸可用于后续的浸出操作。(3)浸出液“净化”过程中加入的主要物质为锌粉,其作用
是置换出Fe 等;(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag 合金惰性电极,由于电极是惰性电
极,所以在阳极是溶液中的OH-放电,电极反应是:4OH--4e-=2H2O+ O2↑.所以阳极逸出的气体是氧气。
(5)根据题意可得 “氧压酸浸”中发生的主要反应的离子方程式为2ZnS+4H++
O2=2Zn2++2S↓+2H2O. (6) 用焦炭煅烧炉甘石的化学反应方程式为ZnCO3+2C
高温
Zn+3CO↑。
18.(15 分)(1)
2
2
2
2
2H S(g)+3O (g)=2SO (g)+2H O(g)
-1
ΔH
-1036 kJ mol
(可以写分数)
(2)
3
2
2
5
2
2NaHSO
Na S O
H O
3
2
3
3
2
3
NaHSO
Na
O
NaHCO
Na
O
C
S
2
4
SO
2
CO 、SO2 (3)
2
3
SO a~b mol 时,产生的二氧化碳逸出,使反应正向进行,
-
3
HCO 平衡转化
率上升,亚硫酸氢根浓度增大,抑制了的亚硫酸根和二氧化硫的反应,所以
-
3
HCO 平衡转化率上升而
2-
3
SO 平
衡转化率下降(3 分)
【详解】(1)已知:
反应Ⅰ:
2
2
2
1
H S(g)+
O (g)=S(s)+H O(g)
2
-1
ΔH=-221.2kJ mol
反应Ⅱ:
2
2
S(s)+O (g)=SO (g)
-1
ΔH=-296.8kJ mol
将Ⅰ×2+Ⅱ×2 得:
2
2
2
2
2H S(g)+3O (g)=2SO (g)+2H O(g)
-1
-1
ΔH=(-221.2 2)+(-296.8 2) kJ mol
-1036 kJ mol
,所以由
2
H S制
2
SO
的热化学方程式为
2
2
2
2
2H S(g)+3O (g)=2SO (g)+2H O(g)
-1
ΔH
-1036 kJ mol
;
(2)① 当反应釜中溶液pH 达到3.8~4.1 时,形成的
3
NaHSO 悬浊液转化为
2
2
5
Na S O 固体,根据元
素守恒,还有水生成,化学方程式:
3
2
2
5
2
2NaHSO
Na S O
H O
;
②根据多级串联反应釜中的化学方程式可知,除了生成的焦亚硫酸钠外,母液中有亚硫酸氢钠剩余,
又因为
a2
2
3
K
H SO
>
a2
2
3
K
H CO
,亚硫酸氢钠与过量
2
3
Na CO 发生反应的化学方程式为:
3
2
3
3
2
3
NaHSO
Na
O
NaHCO
Na
O
C
S
;
③在燃烧炉中反应冷却后的气体中混有氧气,氧气能氧化亚硫酸钠或亚硫酸氢钠,生成硫酸钠,所以
多次循环后,母液中逐渐增多的杂质离子是
2
4
SO ,需除去;
④碳酸氢钠与二氧化硫发生的化学方程式为
3
2
3
2
NaHCO +SO
NaHSO +CO
ƒ
,生成了二氧化碳,二氧化
碳用氢氧化钠吸收,转化成碳酸钠,可到多级串联反应釜中循环使用,所以尾气吸收器中吸收的气体有
2
CO ,在多级串联反应釜中持续通入的
2
SO ,则尾气吸收器中吸收的气体还有
2
SO ;
故答案为:
3
2
2
5
2
2NaHSO
Na S O
H O
;
3
2
3
3
2
3
NaHSO
Na
O
NaHCO
Na
O
C
S
;
2
4
SO ;
2
CO 、SO2;
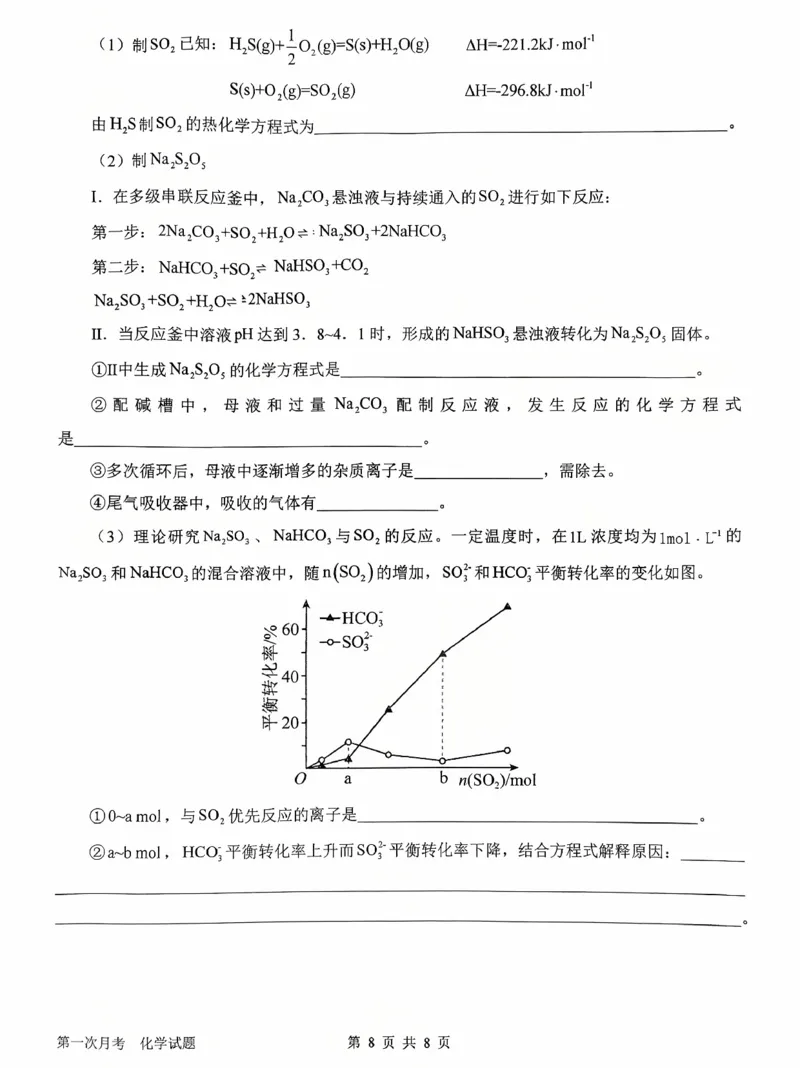
(3)① 由图可知,①0~a mol ,时,碳酸氢根平衡转化率较低,而亚硫酸根的平衡转化率较高,所以
2
3
SO 与
2
SO 优先反应;
②一定温度时,在1L 浓度均为
- 1
1mol
L
的
2
3
Na SO 和
3
NaHCO 的混合溶液中,发生的反应为:
2
3
2
2
3
SO
H O
2
SO
HSO
ƒ
,
3
2
3
2
HCO
SO
HSO
CO
ƒ
,a~b mol 时,产生的二氧化碳逸出,使反应正向
进行,
-
3
HCO 平衡转化率上升,亚硫酸氢根浓度增大,抑制了的亚硫酸根和二氧化硫的反应,所以
-
3
HCO 平
衡转化率上升而
2-
3
SO 平衡转化率下降。