文档内容
姓 名 准考证号_________________
岳阳市2025届高三教学质量监测(二)
化学
本试卷共8页,18道题,满分100分,考试用时75分钟。
注意事项:
1 .答落前,考生务必膈自己的学校、班级、考号和姓名填写在答题卡指定位置。
2 .回答选择题时,选出每小题答案后,用2B铅笔把答题卡对应的标号涂黑,如需改
动,用棣皮擦干净后,再选涂其他答案标号。
3,非选择题必须用黑色签字第作答,答案必须写在答题卡各题目指定区域内;如需改动,
先划掉原来的答案,然后再写上新答案;不准使用铅笔和涂改液。不按以上要求作答无效。
4.考生必须保证答题卡的整洁。考试结束后,只交答题卡。
可能用到的相对原子质量:
H-l C-12 N-14 0-16 Cl-35.5 Fe-56
一、选择题(本大题共14小题,每小.题3分,共42分。在每小题给出的四个选项中,只•有
一项是符合题目要求的)
1 .第四届湖南旅游发展大会将于5月24—26日在岳阳市举行。在旅游过程中,我们可以
学习到很多化学知识。以下说法正确的是
A.君山银针茶叶中含有的茶多酚不易被氧化,具有抗氧化功效
B.巴陵石化生产的乙烯是一种精细化学品在其产量可衡量国家石油化T水平
C.洞庭湖的芦苇含纤维素,纤维素属于有机高分子化合物
D.岳阳楼使用的红色油漆中含有的三翱匕二铁属于金属材料
2 .下列化学用语或描述错误的是
A,甲烷分子式和实验式均可表示为“CH/'
B,中子数为16的磷原子::;P
C.石墨的层状结构(如右图):
D. SiC(俗称金刚砂)的晶体类型:共价晶体
3 .下列有关实验操作的说法,正确的是
A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干
B-用二硫化碳清洗试管内壁附着的硫
C;实验室未用完的钠、钾等试剂不能放回原试剂瓶
D.蒸储操作中需要使用球形冷凝管
南三二模化学试卷第1页(共8页)4 .下列有关物质结构或性质的说法错误的是
A.氢键(X-H…Y)中三原子在一条直线上时,氢键的强度最大
B.低温石英(a-石英)具有手性结构,可用作压电材料,如制作石英手表
C.根据原子半径推知,F-F键的键能大于C1-C1键
D.含有阳离子的晶体中不一定含有阴离子
5 .谷氨酸单钠是味精的主要成分,利用发酵法制备该物质的流程如下:
0
淀粉JI型空葡萄糖二定发纥 Na2cO3
0H
水解 发酵、提取 中和 NaO
nh2
谷氨酸 谷氨酸单钠
下列说法正确的是
谷氨酸的分子式为C5H8O4N
B. 可用红外光谱仪检测谷氨酸中所含官能团的类型
等物质的量的谷氨酸和谷氨酸单钠中,手性碳原子的数目相同,均约为6.02X10"
D. “中和”时,为了提高谷氨酸单钠盐的产率,需要添加过量的Na2c03
6 .下列过程中的化学方程式或离子方程式书写错误的是
A.向硫化钠溶液中通入足量二氧化硫:2S2-+5SO2+2H2O=3S1+4HSO j
B.黄铁矿(主要成分为FeSz)的燃烧:绮4FeS2+1102里 2Fe2O3 + 8SO2
C.氟化物预防龌齿的化学原理:Ca5(PO4)3OH(s)+F"(aq) U Ca5(PO4)3F(s)+OH-(aq)
D,氮化硅可由石英与焦炭在高温的氮气流中制备:3SiO2 + 3C + 2N23:Si3N4 + 3CO2
7,哂是极强的氧化剂,可与稀有气体制彳嬲有气体离子化合物,六氟合景氤P&FTPbFiF的制
备方式如右图所示,下列说法错误的是
A.整个反应过程中,属于氧化还原反应的是
②③⑤
B.整个回蜘程中,F-起W了翻冽的作用
c.豺反l&ffi中既痢场
D.反应过程中消耗1 mol氤气,理论上可生成1 mol六氟合粕氤
8.某催化剂结构简式如右图所示。下列说法正确的是
A.该配合物中银的化合价为+4
B.基态原子的第一电离能关系:C>H
高三二模化学试卷 第2页(共8页)C.该配合物中氯元素以中性氯原子的形式参与配位
D. Ni元素在周期表中位于第四周期第VH[族
9.下列实验操作与预期实验目的或结论一致的是
选项 实验操作 预期实验目的或结论
向两份相同蛋白质溶液中分别滴加饱和
蛋白质均发生变性
A
NaCl溶液和CuSO」溶液,均有固体析出
常温下,向饱和Na2c03溶液中加少量
B BaSCh粉末,过滤,向洗净的沉淀中加稀 说明常温下,7rSp(BaCO3)<^8p(BaSO4)
盐酸,有气泡产生
向含有少量FeCh的MgCL溶液中加入足量
C 除去MgCL溶液中少量FeCL
Mg(0H)2粉末,搅拌一段时间后过滤
向浓HNO3中插入红热的炭,产生红棕色气
D 炭可与浓HNO3反应生成NO2
体
10.电解法处理酸性含偌废水(主要含有50})时,以铁板作阴、阳极,处理过程中存
在反应CT2O;-+6Fe2+ + 14H+=2Cr3+ + 6Fe3+ + 7H2O,最后 Cr3+以 Cr(OH)3 形式除去?下列
说法错误的是
A.阴啦酬2H++2©-=町
B.电解过程中废水的pH变大
C.电路中每转移6 moi电子,最多有ImolCqO?"被还原
D.该条件下Fe?+的还原性强于CS
11.从炼钢粉尘(主要含Fe3O4、&2O3和Zn。)中提取锌的流程如下:
炼钢粉尘一> 盐浸——U氧化I——-沉锌 ―Zus
I I
滤渣 滤液
“盐浸”过程ZnO转化为[Zn(NH3)4]2+,并有少量Fe?+和Fe3+浸出。下列说法正确的是
A. “盐浸”过程若浸液pH下降,需补充NH4cl
B. “滤渣”的主要成分为Fe(OH)3
C. “沉锌”过程发生反应Zh2++s2-=ZnSl
D.应合理控制(NH4)2S用量,以便滤液循环使用
南三二模化学试卷第3页(共8页)12.研究笼形包合物结构和性质具有重要意义,化学式为Ni(CN”Zn(NH3)y・zC6H6的笼形
包合物四方晶胞结构如图所示(H原子未画出)。每个苯环只有一半属于该晶胞,晶胞参数
为@=1)«, a=p=y=90。。晶胞中N原子均参与形成配位犍。
下列说法正确的是
A.基态Zn原子的价电子排布式为3d84s2
B. Ni2+与ZM+的配位数之比为2:1
C.晶胞中Ni?+采取sp3杂化
D. x:y:z=2:l:l
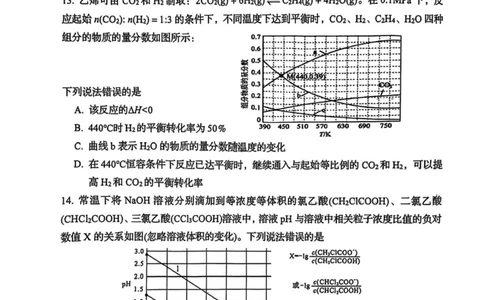
13.乙烯可由 82 和 H2 制取:2co2(g)+ 6Hz(g)UC2H4(g)+ 4上0值)。在 O.IMPa 下,反
应起始〃(CO2):〃(H2)=L:3的条件下,不同温度下达到平衡时,C02、出、C2H4、H2O四种
组分的物质的量分数如图所示: 0.7
0.6
下列说法错误的是
A.该反应的加0
B. 440。C时H2的平衡转化率为50%
C.曲线b表示HaO的物质的量分数随温度的变化
D.在440(恒容条件下反应已达平衡时,继续通入与起始等比例的CO2和H2,可以提
高H2和CO2的平衡转化率
14.常温下将NaOH溶液分别滴加到等浓度等体积的氯乙酸(CHzCICOOH)、二氯乙酸
(CHCLCOOH)、三氯乙酸(CCbCOOH)溶液中,溶液pH与溶液中相关粒子浓度比值的负对
数值X的关系如图(忽略溶液体积的变化)。下列说法错误的是
A.三种酸的电离常数:Ka(CH2cleOOH)〈Ka(CHCl2coOH)vKa(CCbCOOH)
B.常温下Ka(CCbCOOH)的数量级为10、
C.等浓度的三种酸溶液中,水的电离程度最大的是CHzCICOOH
D,当三种溶液中 c(CCl3COO")= c(CHC12COO") = c(CH2cle00)消耗 n(NaOH)最少
的为氯乙酸
南三二模化学试卷第4页(共8页)二、非选择题:(共58分)
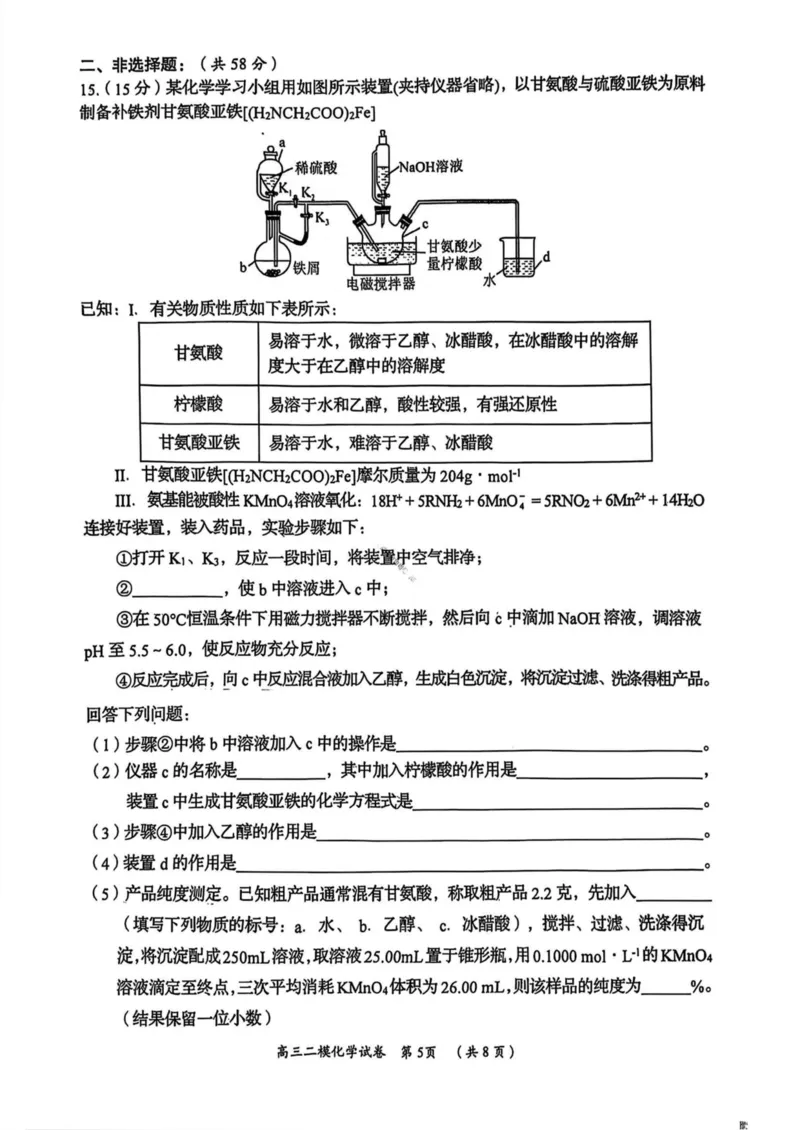
15. ( 15分)某化学学习小组用如图所示装置(夹持仪器省略),以甘氨酸与硫酸亚铁为原料
制备补铁剂甘氨酸亚铁[(FhNCH2co0)2Fe]
已知:I.有关物质性质如下表所示:
易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中的溶解
甘氨酸
度大于在乙醇中的溶解度
柠檬酸 易溶于水和乙醇,酸性较强,有强还原性
甘氨酸亚铁 易溶于水,难溶于乙醇、冰醋酸
n.甘氨酸亚铁[(H2NCH2co0)也]摩尔质量为204g - mol-1
HL 氨基能被脸 KM1Q4溶液氧化:18H+ + 5RNH2 + 6MnO; =5RNO2 + 6Mn2++i4H2O
连接好装置,装入药品,实验步骤如下:
①打开R、K3,反应一段时间,将装置中空气排净;
②,使b中溶液进入c中;
③在50。(:恒温条件下用磁力搅拌器不断搅拌,然后向6中滴加NaOH溶液,调溶液
pH至5.5 ~ 6.0,使反应物充分反应;
④反应完成后,回c中反应混合液加A乙醇,生成白色沉淀,将沉淀过滤、阚得粗产品。
回答下列问题:
(1)步骤②中将b中溶液加入c中的操作是
o
(2)仪器c的名称是,其中加入柠檬酸的作用是_______________________,
装置c中生成甘氨酸亚铁的化学方程式是____________________________________
o
步骤④中加入乙醇的作用是____________________________________________
(3 ) o
(4)装置d的作用是__________________________________________________________
o
(5)产品纯度测定。已知粗产品通常混有甘氨酸,称取粗产品2.2克,先加入
(填写下列物质的标号:a.水、b.乙醇、c.冰醋酸),搅拌、过滤、洗涤得沉
淀,将沉淀配成250mL溶液,取溶液25.00mL置于锥形瓶,用0.1000mol • L」的KMnCU
溶液滴定至终点,三次平均消耗KMnO4体积为26.00 mL,则该样品的纯度为%。
(结果保留一位小数)
高三二模化学试卷第5页(共8页)16. (15分)稀土铁铁硼永磁材料广泛应用于新能源汽车、节能环保家电、国防军事等工
业领域。:Dlk上以铁铁硼废料[含铁(Nd,质量分数为28.8%)、Fe、B]为主要原料回收
高纯度铁的工艺流程如下。
桶流酸 NqH2PO4 过最NopH溶液稀硫酸H1c溶液 0,
上上 -i— 上上一些列操作.
MW—>fWl—4WMW ,N djOj-电解 |—>Nd
渔港 滤液I
已知:①Nd的稳定价态为+3价;Nd的活动性较强,与稀硫酸反应产生H2;硼难溶
于稀硫酸。铁离子可与过量H2c2。4生成可溶性配合物;
②常温下,/Csp[Fe(OH)2]=4.9xlO-l7o
回答下列问题;
(1)“酸溶”时,下列措施可以提高酸溶速率的是(填序号)。
A.适当升高温度 B.适当增大硫酸的浓度
C.适当延长浸取时间 D.将被铁硼废料粉碎
(2 )常温下,“沉钛”过程中调节溶液的pH为2.3,钛全部以Nd(H2P04)沉淀完全,若
此时溶液中c(Fe2+)=l,O mol-L->, (填“有”或“无”)Fe(0H)2沉淀生成;酸
性太强会使“沉钛”不完全,原因是_______________________________________
_0
(3 )①“沉淀”过程得到Nd2(C2O4)3 - 10H2O晶体。写出“沉淀”时发生反应的离子方程
式:
O
②此过程中,草酸实际用量与理论计算量的比值(n)和沉钛率的关系如下图所示。
对沉铁率变化趋势进行解释:
0
③“滤液3”中的(填化学式)可在上述流程中循环利用。
(4)“一系列操作"包括;空气中“燃烧”时生成无毒的气体,
反应的化学方程式______________________________________________________O
高三二模化学试卷第6页(共8页)17,(14分)研究含碳和含氮物质的反应对生产、生活、科研等方面具有重要的意义。回
答下列问题:
(1)消除汽车尾气中的NO、NO2,有利于减少PM2.5的排放。已知如下信息:
i .C(s)+O2(g) U CO2(g) -400 kJ/mol
ii .N2(g)+O2(g) = 2N0(g) 岫2= +180 kJ/mol
iii .2NO(g)+O2(g) U 2NO2(g)内2 -110 kJ/mol
则C(s)与NCh(g)反应生成Nz(g)和C02(g)的热化学方程式为
o
(2)在一定温度下,向2 L刚性容器中充入2 mol NO和1 mol O2只发生反应出
①下列描述可表示该反应达到平衡状态的有(填序号)
a,容器内颜色深浅不再改变 b.混合气体密度保持不变 c,需科=2
d,单位时间内生成NO2和生成O2的物质的量之比为2:1
②该反应的反应速率加v正-v逆=左正c2(no)・4O2)-上逆iCNOz); k正、心分别为正、
逆反应速率常数,已知平衡时。2的转化率为50%,则%为(计算时不考
虑其他反应)。
(3 )在一定温度下,向起始压强为100kP0的1 L恒容密闭容器中通入1 molN2和1 molO2
的混合气体发生反应ii和出,4 min时反应达到平衡,测得体系总压强为90 kPa,且
p(N2):p(O2):p(NO)=3:2:2(p为气体分压,单位为kPa),达到平衡时NO2的平均反应速
率为,反应iii的压强平衡常数Kp=__________________
0
(4)在两个初始体积相同且容积可变的容器内分别充入
2 mol NO和1 mol O2,在总压为pi、pz条件下仅发生
反应出。待两容器均达到平衡时,测得02转化率随温
度的变化如右图所示。试解释m点的容器容积大于n
点的原因、
(5)近年研究发现,电催化C02和含氮物质(N03-等)在 co.
常温常压下合成尿素,有助于实现碳中和及解决含氮废
水污染问题。向一定浓度的KNO3溶液通C02至饱和,
在电极上反应生成CO(NH2)2,电解原理如右图所示。
电解过程中,在a电极上的反应式为
o
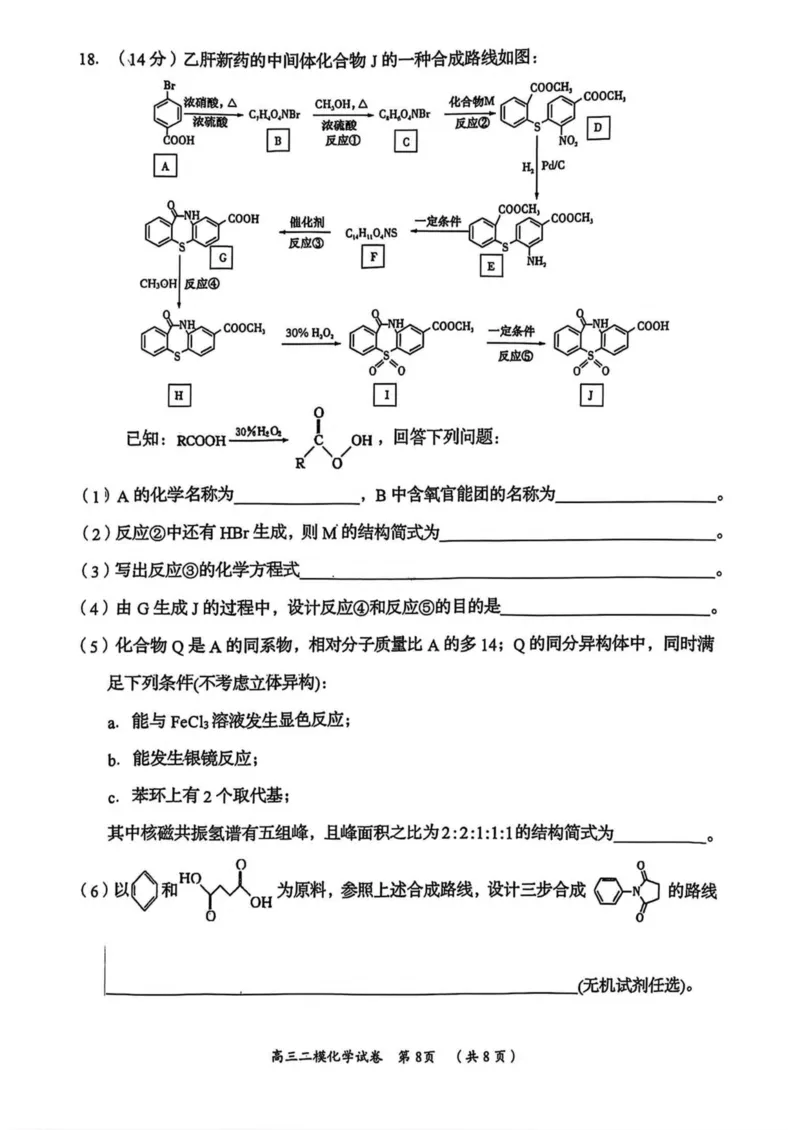
高三二模化学试卷 第7页(共8页)18. (、14分)乙肝新药的中间体化合物J的一种合成路线如图:
Br C00CHj COOCH,
入浓硝酸,△ CH.OH, A 化合物M
硫酸 , GH 回 ANBr 浓硫酸’ c ,皿怖下骸 □
COOH 反应① □
□ 一
Pd/C
COOCH)
COOH 催化剂 一定条件 COOCHj
C“HiQNS --------
反应③
G
CHjOH 反应④
COOCH, 30% H,0, COOCH, 一定条件 COOH
反应⑤
□ □
已知:R8OH^2 C OH ,回答下列问题:
/ \ /
R O
(i)a的化学名称为 , B中含氧官能团的名称为
o
(2 )反应②中还有HBr生成,则M的结构简式为
O
(3 )写出反应③的化学方程式.
O
(4)由G生成J的过程中,设计反应④和反应⑤的目的是.
(5)化合物Q是A的同系物,相对分子质量比A的多14; Q的同分异构体中,同时满
足下列条件(不考虑立体异构):
a.能与FeCL溶液发生显色反应;
b.能发生银镜反应;
c.苯环上有2个取代基;
其中核磁共振氢谱有五组峰,且峰面积之比为的结构简式为
O
为原料,参照上述合成路线,设计三步合成 的路线
(无机试剂任选)。
高三二模化学试卷第8页(共8页)岳阳市2025届高三教学质量监测(二)
化学参考答案及评分标准
本试卷共12页,18道幽,满分100分,考试用时75分钟。
一、选择题(本大题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的)
题号 1 2 3 4 5 6 7
答案 C C B C B D A
题号 8 9 10 11 12 13 14
答案 D C C D D B D
二、非选择题:(共58分)
15,(15分,除标注外每空两分2分)【答案】
(1)打开。,关闭K、
(2)三颈烧瓶(I分);防止亚铁离子被氧化且能抑制亚铁离子水解;
FeSO.,+2H2NCH2COOH+2NaOH =(H,NCH2COO)2 Fe+Na2SO4+2H,O
(3)降低甘氨酸亚铁的溶解度,使其柝出
(4)液封或水封,防止空气进入c中
(5)c; 92.7%
16 . (15分,除标注外每空两分2分)【答案】
(1 )ABD
(2)无(I分);酸性太强,H+与HJO:反应生成导致凡PO:浓度太小,沉
淀不完全
(3)① 2Nd3++ 3H2c2。4 + 10H2O= Nd2(C2O4) 310H2O| + 6H+ ;
②适当增大草酸的用量,可增加g0丁的浓度,有利于提高沉铉率;草酸浓度过大
铉离子可与过量H2C2O4生成可溶性配合物,从而降低沉铉率;
③ H2so4
高温
(4)过滤、洗涤、干燥 2Nd2(C2O4)}• 10H2O+3O2 - Nd,O3 +12CO2 + 20H2O
17. (14分,每空2分)【答案】
(1 ) 2C(s)+2NO2(g)=2CO2(g)+N2(g) AH=-870 kJ/mol
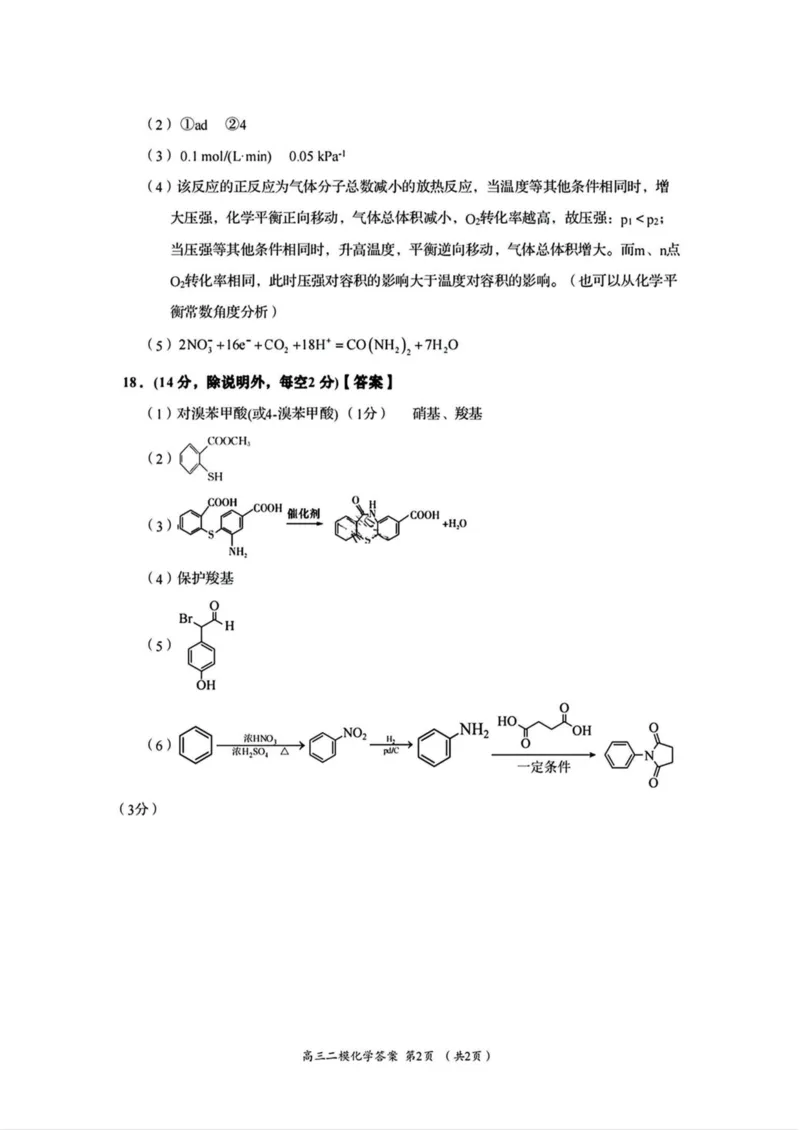
高三二模化学答案第I页(共2页)(2)①ad②4
(3) 0.1 mol/(L min) 0.05 kPa-1
(4)该反应的正反应为气体分子总数减小的放热反应,当温度等其他条件相同时,增
大压强,化学平衡正向移动,气体总体积减小,02转化率越高,故压强:pi