文档内容
专题49 化学电源——可充电电池
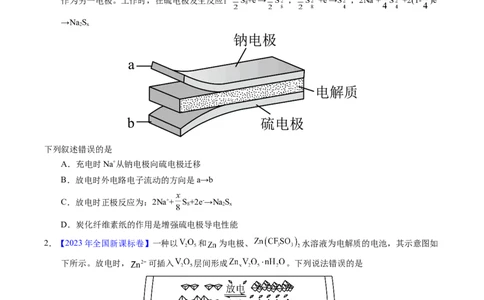
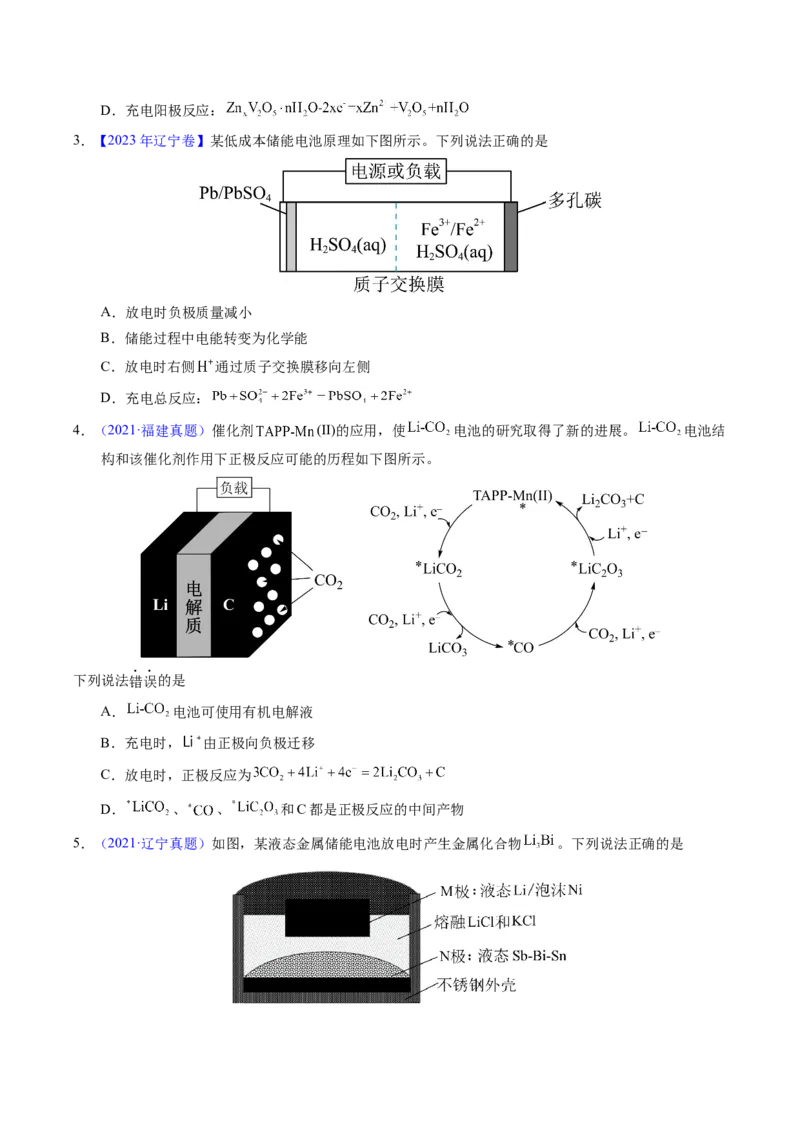
1.【2023年全国乙卷】室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电
池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸
作为另一电极。工作时,在硫电极发生反应: S+e-→ S , S +e-→S ,2Na++ S +2(1- )e-
8
→NaS
2 x
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++ S+2e-→NaS
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
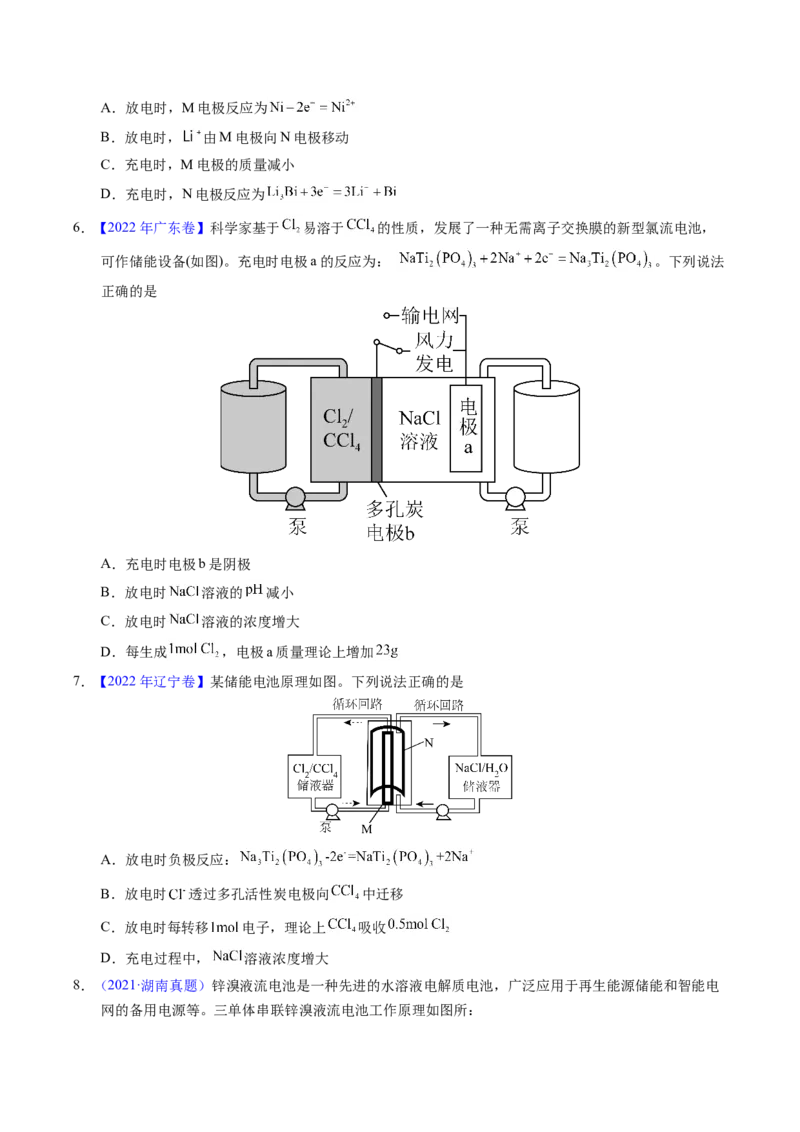
2.【2023年全国新课标卷】一种以 和 为电极、 水溶液为电解质的电池,其示意图如
下所示。放电时, 可插入 层间形成 。下列说法错误的是
A.放电时 为正极
B.放电时 由负极向正极迁移
C.充电总反应:D.充电阳极反应:
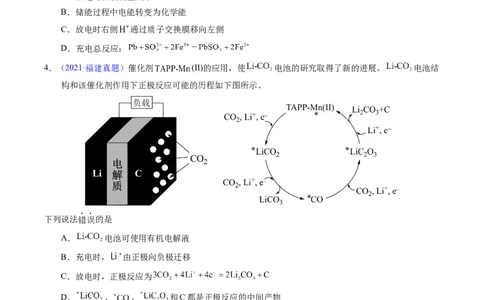
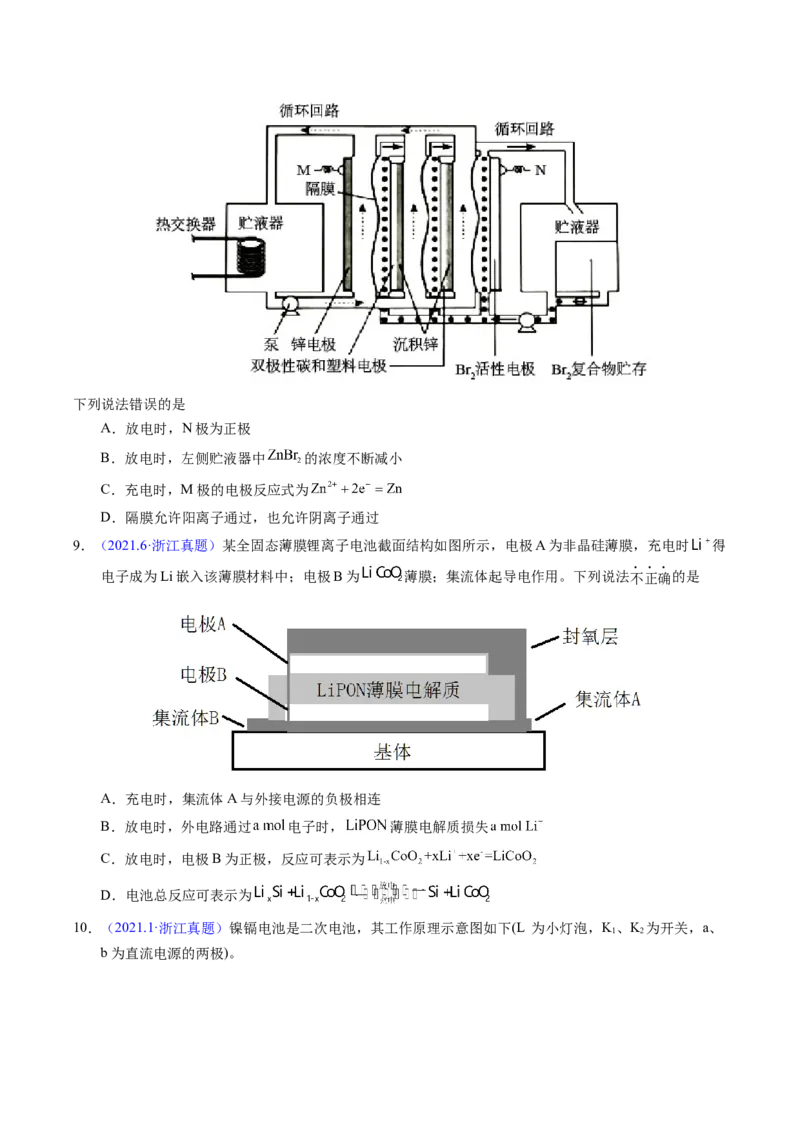
3.【2023年辽宁卷】某低成本储能电池原理如下图所示。下列说法正确的是
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:
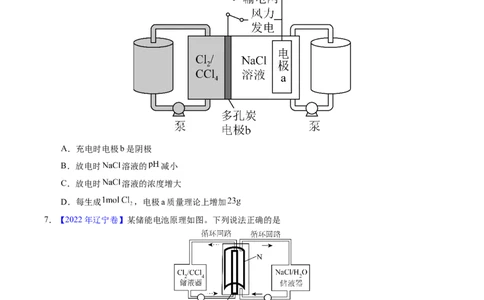
4.(2021·福建真题)催化剂 (Ⅱ)的应用,使 电池的研究取得了新的进展。 电池结
构和该催化剂作用下正极反应可能的历程如下图所示。
下列说法错误的是
A. 电池可使用有机电解液
B.充电时, 由正极向负极迁移
C.放电时,正极反应为
D. 、 、 和C都是正极反应的中间产物
5.(2021·辽宁真题)如图,某液态金属储能电池放电时产生金属化合物 。下列说法正确的是A.放电时,M电极反应为
B.放电时, 由M电极向N电极移动
C.充电时,M电极的质量减小
D.充电时,N电极反应为
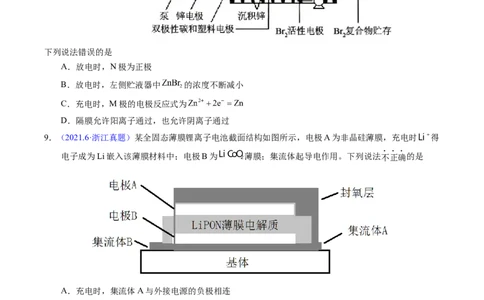
6.【2022年广东卷】科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电池,
可作储能设备(如图)。充电时电极a的反应为: 。下列说法
正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
7.【2022年辽宁卷】某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时 透过多孔活性炭电极向 中迁移
C.放电时每转移 电子,理论上 吸收
D.充电过程中, 溶液浓度增大
8.(2021·湖南真题)锌溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储能和智能电
网的备用电源等。三单体串联锌溴液流电池工作原理如图所:下列说法错误的是
A.放电时,N极为正极
B.放电时,左侧贮液器中 的浓度不断减小
C.充电时,M极的电极反应式为
D.隔膜允许阳离子通过,也允许阴离子通过
9.(2021.6·浙江真题)某全固态薄膜锂离子电池截面结构如图所示,电极A为非晶硅薄膜,充电时 得
电子成为Li嵌入该薄膜材料中;电极B为 薄膜;集流体起导电作用。下列说法不正确的是
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过 电子时, 薄膜电解质损失
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为
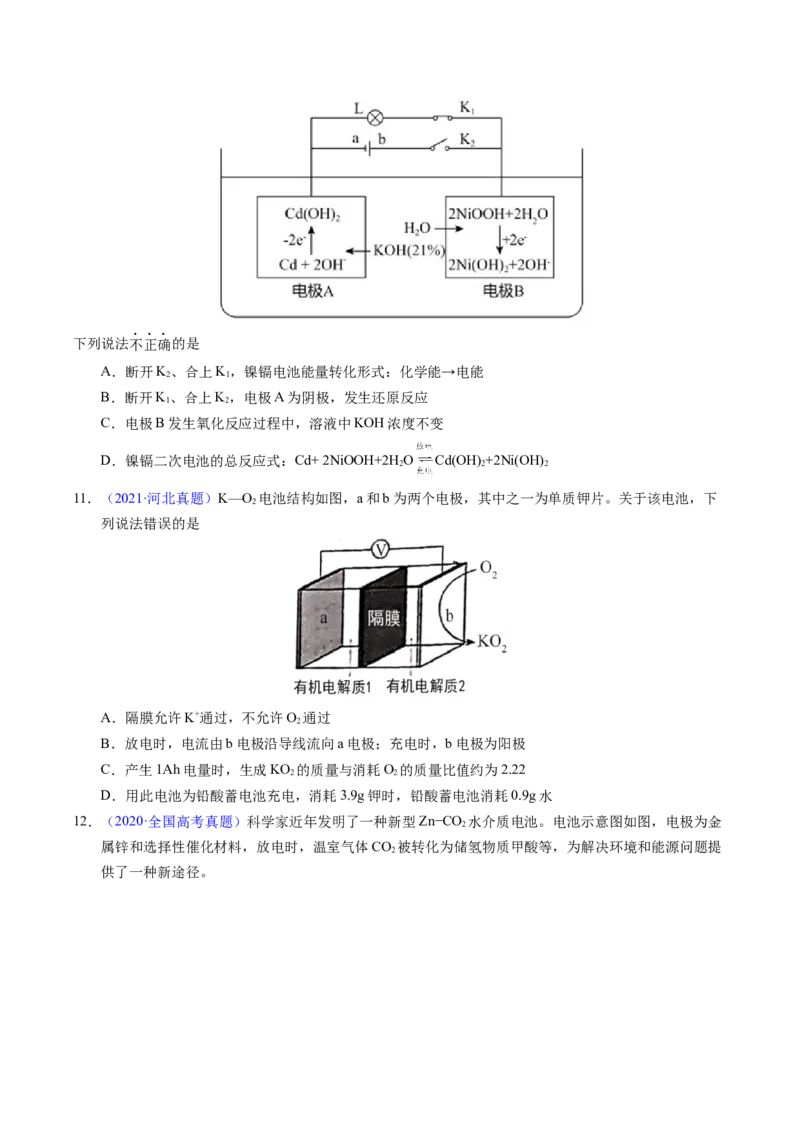
10.(2021.1·浙江真题)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开关,a、
1 2
b为直流电源的两极)。下列说法不正确的是
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Cd(OH) +2Ni(OH)
2 2 2
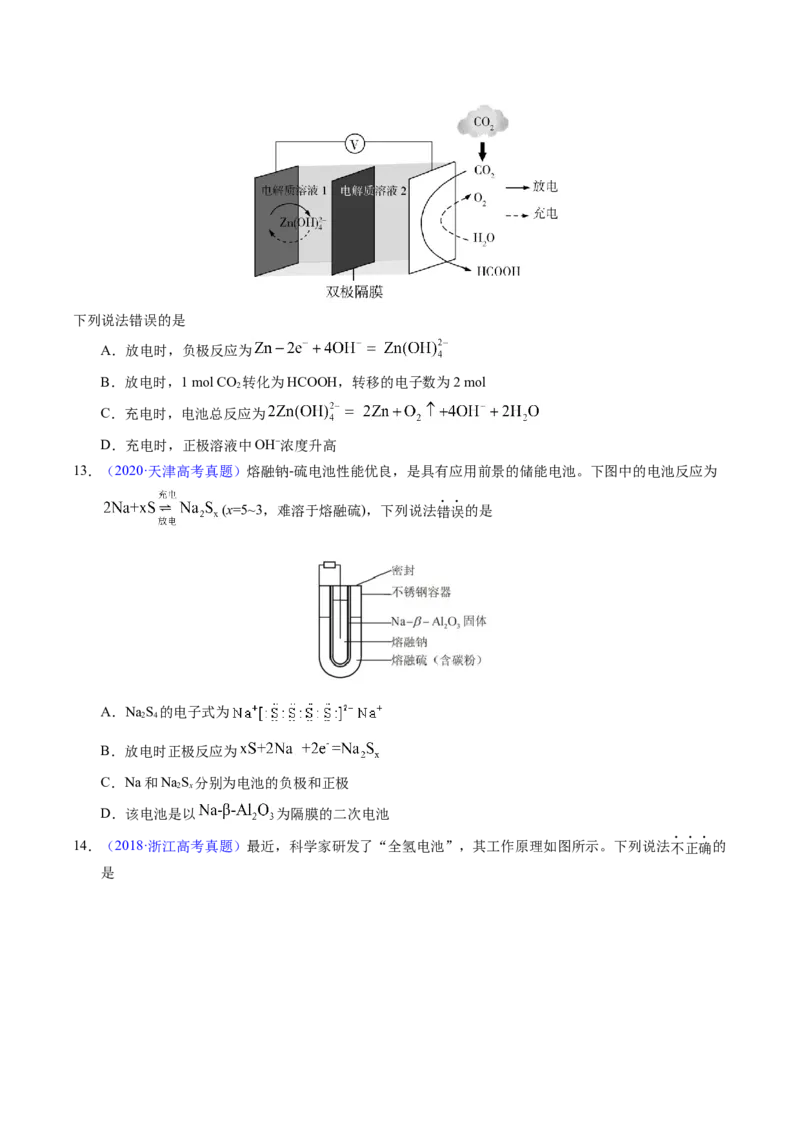
11.(2021·河北真题)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该电池,下
2
列说法错误的是
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2
D.用此电池为铅酸蓄电池充电,消耗3.9g钾时,铅酸蓄电池消耗0.9g水
12.(2020·全国高考真题)科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极为金
2
属锌和选择性催化材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提
2
供了一种新途径。下列说法错误的是
A.放电时,负极反应为
B.放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C.充电时,电池总反应为
D.充电时,正极溶液中OH−浓度升高
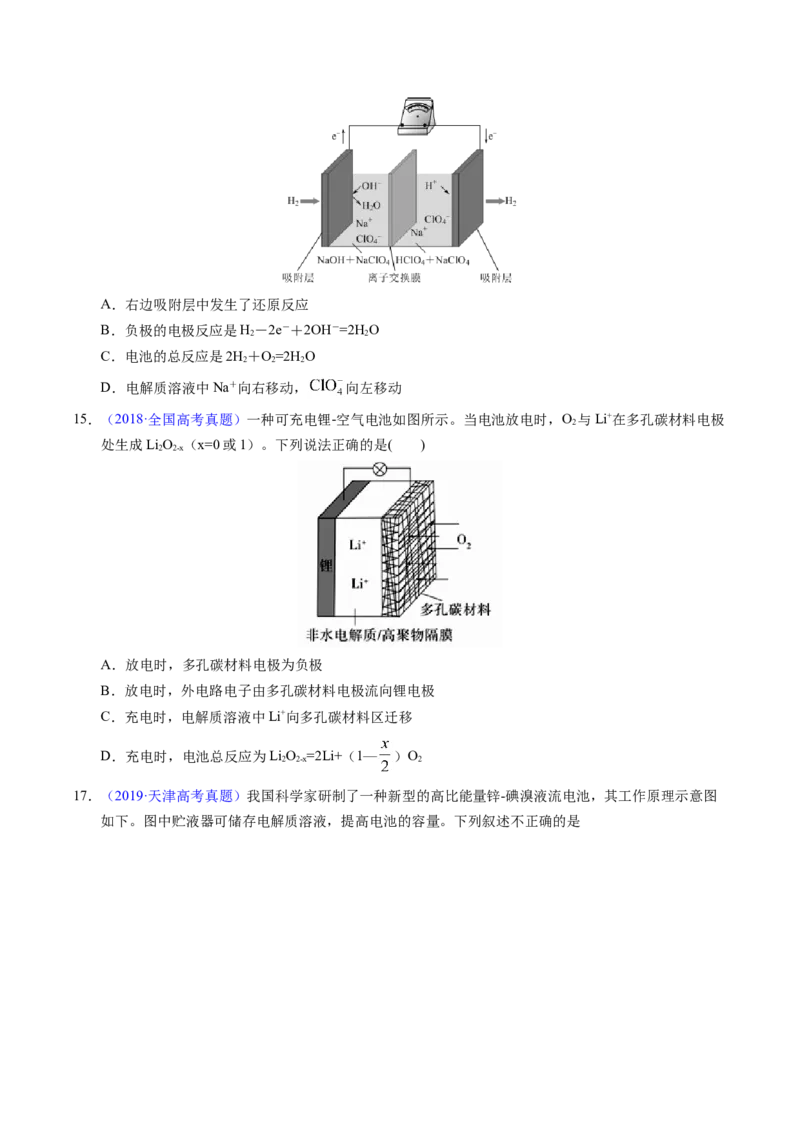
13.(2020·天津高考真题)熔融钠-硫电池性能优良,是具有应用前景的储能电池。下图中的电池反应为
(x=5~3,难溶于熔融硫),下列说法错误的是
A.NaS 的电子式为
2 4
B.放电时正极反应为
C.Na和NaS 分别为电池的负极和正极
2 x
D.该电池是以 为隔膜的二次电池
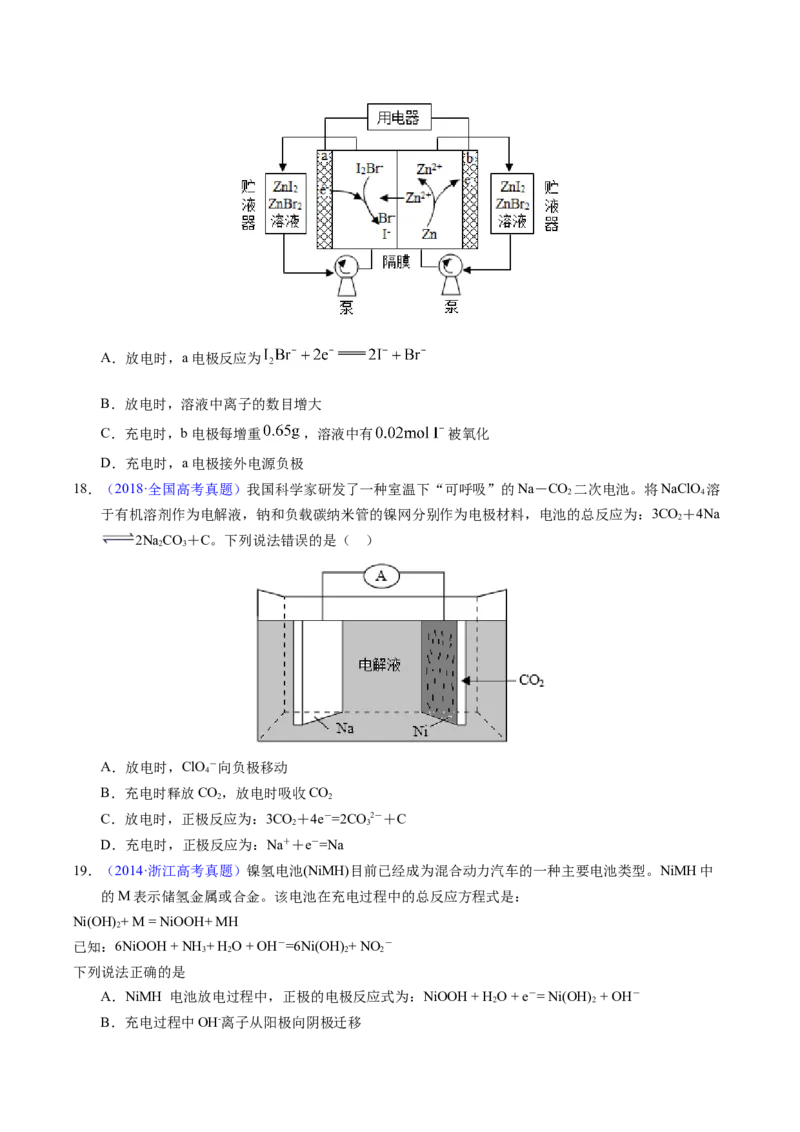
14.(2018·浙江高考真题)最近,科学家研发了“全氢电池”,其工作原理如图所示。下列说法不正确的
是A.右边吸附层中发生了还原反应
B.负极的电极反应是H-2e-+2OH-=2H O
2 2
C.电池的总反应是2H+O=2H O
2 2 2
D.电解质溶液中Na+向右移动, 向左移动
15.(2018·全国高考真题)一种可充电锂-空气电池如图所示。当电池放电时,O 与Li+在多孔碳材料电极
2
处生成LiO (x=0或1)。下列说法正确的是( )
2 2-x
A.放电时,多孔碳材料电极为负极
B.放电时,外电路电子由多孔碳材料电极流向锂电极
C.充电时,电解质溶液中Li+向多孔碳材料区迁移
D.充电时,电池总反应为LiO =2Li+(1— )O
2 2-x 2
17.(2019·天津高考真题)我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图
如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是A.放电时,a电极反应为
B.放电时,溶液中离子的数目增大
C.充电时,b电极每增重 ,溶液中有 被氧化
D.充电时,a电极接外电源负极
18.(2018·全国高考真题)我国科学家研发了一种室温下“可呼吸”的Na-CO 二次电池。将NaClO 溶
2 4
于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO+4Na
2
2NaCO+C。下列说法错误的是( )
2 3
A.放电时,ClO -向负极移动
4
B.充电时释放CO,放电时吸收CO
2 2
C.放电时,正极反应为:3CO+4e-=2CO 2-+C
2 3
D.充电时,正极反应为:Na++e-=Na
19.(2014·浙江高考真题)镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中
的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:
Ni(OH) + M = NiOOH+ MH
2
已知:6NiOOH + NH + H O + OH-=6Ni(OH) + NO -
3 2 2 2
下列说法正确的是
A.NiMH 电池放电过程中,正极的电极反应式为:NiOOH + H O + e-= Ni(OH) + OH-
2 2
B.充电过程中OH-离子从阳极向阴极迁移C.充电过程中阴极的电极反应式:HO + M + e-= MH + OH-,HO中的H被M还原
2 2
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
20.(2016·浙江高考真题)金属(M)–空气电池(如图)具有原料易得、能量密度高等优点,有望成为
新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO+2nH O=4M(OH) 。已知:
2 2 n
电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
C.M–空气电池放电过程的正极反应式:4Mn++nO +2nH O+4ne–=4M(OH)
2 2 n
D.在M–空气电池中,为防止负极区沉积Mg(OH) ,宜采用中性电解质及阳离子交换膜
2
21.(2017·全国高考真题)全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用
掺有石墨烯的S 材料,电池反应为:16Li+xS=8Li S(2≤x≤8)。下列说法错误的是
8 8 2 x
A.电池工作时,正极可发生反应:2LiS+2Li++2e−=3Li S
2 6 2 4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中LiS 的量越多
2 2
22.(2014·全国高考真题)2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述
错误的是
A.a为电池的正极
B.电池充电反应为LiMn O Li MnO+xLi
2 4 1-x 2 4C.放电时,a极锂的化合价发生变化
D.放电时,溶液中Li+从b向a迁移
23.(2008·江苏高考真题)镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电
解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H O Cd(OH) + 2Ni(OH) 。
2 2 2
有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH) -e—+ OH-=" NiOOH" + H O
2 2
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
24.(2014·天津高考真题)已知:锂离子电池的总反应为:LiC+Li CoO C+LiCoO,锂硫电池的总
x 1-x 2 2
反应为:2Li+S LiS,有关上述两种电池说法正确的是
2
A.锂离子电池放电时,Li+向负极迁移
B.锂硫电池充电时,锂电极发生还原反应
C.理论上两种电池的比能量相同
D.上图表示用锂离子电池给锂硫电池充电
25.(2014·全国高考真题)如图所示是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池
(MHNi电池)。下列有关说法不正确的是
A.放电时正极反应为NiOOH+HO+e-=Ni(OH) +OH-
2 2
B.电池的电解液可为KOH溶液
C.充电时负极反应为MH+OH-=H O+M+e-
2
D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高
26.(2017·浙江高考真题)银锌电池是一种常见化学电源,其反应原理:Zn+Ag O+HO=Zn(OH) +2Ag,
2 2 2其工作示意图如下。下列说法不正确的是
A.Zn电极是负极
B.Ag O电极发生还原反应
2
C.Zn电极的电极反应式:Zn-2e-++2OH-=Zn(OH)
2
D.放电前后电解质溶液的pH保持不变
27.(2007·天津高考真题)天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的
二氧化钴(LiCoO ),充电时LiCoO 中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C )
2 2 6
中,以LiC 表示。电池反应为LiCoO + C CoO+ LiC ,下列说法正确的是
6 2 6 2 6
A.充电时,电池的负极反应为 LiC - e-= Li + C
6 6
B.放电时,电池的正极反应为 CoO+ Li++ e-= LiCoO
2 2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
28.(2019·全国高考真题)为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn
(3D−Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构
如下图所示。电池反应为Zn(s)+2NiOOH(s)+H O(l) ZnO(s)+2Ni(OH) (s)。以下说法不正确的是
2 2
A.三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B.充电时阳极反应为Ni(OH) (s)+OH−(aq)−e− NiOOH(s)+H O(l)
2 2
C.放电时负极反应为Zn(s)+2OH−(aq)−2e− ZnO(s)+H O(l)
2
D.放电过程中OH−通过隔膜从负极区移向正极区
29.(2013·海南高考真题)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:
2AgCl+ Mg = Mg2++ 2Ag +2Cl-。有关该电池的说法正确的是
A.Mg为电池的正极
B.负极反应为AgCl+e-=Ag+Cl-
C.不能被KCl 溶液激活
D.可用于海上应急照明供电30.(2016·海南高考真题)某电池以KFeO 和Zn为电极材料,KOH溶液为电解溶质溶液。下列说法正
2 4
确的是
A.Zn为电池的负极
B.正极反应式为2FeO2−+10H++6e-=Fe O+5H O
4 2 3 2
C.该电池放电过程中电解质溶液浓度不变
D.电池工作时OH−向负极迁移
31.(2008·广东高考真题)LiFePO 电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电
4
池反应为:FePO +Li LiFePO ,电池的正极材料是LiFePO ,负极材料是石墨,含U导电固体
4 4 4
为电解质。下列有关LiFePO 电池说法正确的是( )
4
A.可加入硫酸以提高电解质的导电性
B.放电时电池内部Li+向负极移动.
C.充电过程中,电池正极材料的质量减少
D.放电时电池正极反应为:FePO +Li++e-=LiFePO
4 4
32.(2019·海南高考真题)微型银-锌电池可用作电子仪器的电源,其电极分别是 和 ,电解
质为 溶液,电池总反应为 ,下列说法正确的是( )
A.电池工作过程中, 溶液浓度降低
B.电池工作过程中,电解液中 向负极迁移
C.负极发生反应
D.正极发生反应
33.(2010·浙江高考真题)Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
2Li++FeS+2e-=Li S+Fe;有关该电池的下列说法中,正确的是
2
A.Li-Al在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为:2Li+FeS=Li S+Fe
2
C.负极的电极反应式为Al-3e-=Al3+
D.充电时,阴极发生的电极反应式为:LiS+Fe-2e-=2Li++FeS
2
34.(2011·全国高考真题)铁镍蓄电池又称爱迪生电池,放电时的总反应为:
Fe+Ni O+3H O=Fe(OH) +2Ni(OH) ,下列有关该电池的说法不正确的是
2 3 2 2 2
A.电池的电解液为碱性溶液,正极为Ni O,负极为Fe
2 3
B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)
2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH) +2OH--2e-=NiO+3H O
2 2 3 2
35.(2009·海南高考真题)Li—SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解质
2
溶液是LiAlCl —SOCl 。电池的总反应可表示为4Li+2SOCl ===4LiCl+S+SO ↑。请回答下列问题:
4 2 2 2(1)电池的负极材料为________,发生的电极反应为__________________。
(2)电池正极发生的电极反应为___________________________。
(3)SOCl 易挥发,实验室中常用NaOH溶液吸收SOCl ,有NaSO 和NaCl生成。如果把少量水滴到
2 2 2 3
SOCl 中,实验现象是___________________,反应的化学方程式为______。
2
(4)组装该电池必须在无水、无氧的条件下进行,原因是__________________。