文档内容
专题53 化学平衡的建立与移动(A)
1.【2023年北京卷】下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 固体,促进 分解
B.密闭烧瓶内的 和 的混合气体,受热后颜色加深
C.铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体
D.锌片与稀 反应过程中,加入少量 固体,促进 的产生
。
2.(2021·福建真题)实验室配制碘水时,通常将 溶于 溶液: 。关于该溶液,
下列说法正确的是
A. 的电子式为 B.滴入淀粉溶液,不变蓝
C.加水稀释,平衡逆向移动 D.加少量 固体平衡正向移动
3.(2021·海南真题)制备水煤气的反应 ,下列说法正确的是
A.该反应
B.升高温度,反应速率增大
C.恒温下,增大总压,HO(g)的平衡转化率不变
2
D.恒温恒压下,加入催化剂,平衡常数增大
4.(2021·辽宁真题)某温度下,在恒容密闭容器中加入一定量X,发生反应 ,一段
时间后达到平衡。下列说法错误的是
A.升高温度,若 增大,则
B.加入一定量Z,达新平衡后 减小
C.加入等物质的量的Y和Z,达新平衡后 增大
D.加入一定量氩气,平衡不移动
5.【2022年河北卷】恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为① ;②
。反应①的速率 ,反应②的速率 ,式中 为速率常数。图甲为该体系
中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的 曲线。下列说法错误的是A.随 的减小,反应①、②的速率均降低
B.体系中
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于 时,总反应速率由反应②决定
6.【2022年湖北卷】硫代碳酸钠能用于处理废水中的重金属离子,可通过如下反应制备:
,下列说法正确的是
A. 不能被氧化 B. 溶液显碱性
C.该制备反应是熵减过程 D. 的热稳定性比 的高
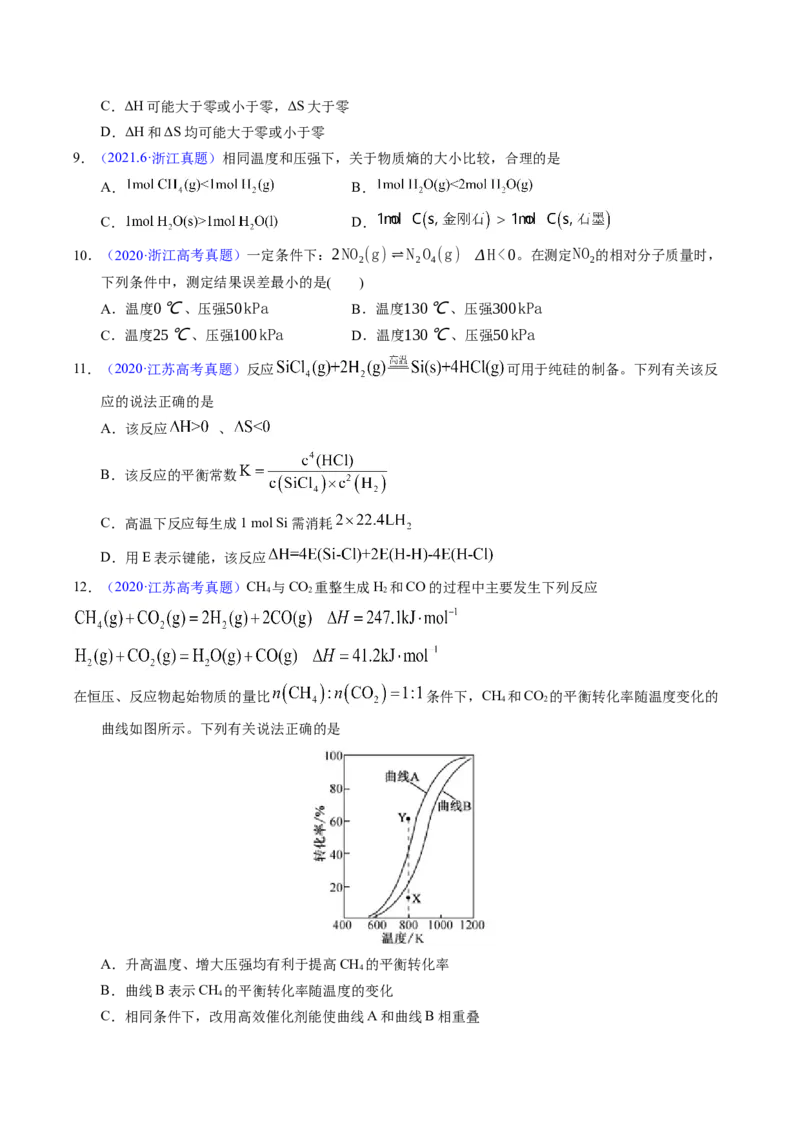
7.【2022年北京卷】某 的多孔材料刚好可将 “固定”,实现了 与 分离并制备 ,
如图所示:
己知:
下列说法不正确的是
A.气体温度升高后,不利于 的固定
B. 被固定后,平衡正移,有利于 的去除
C.制备 的原理为:
D.每制备 ,转移电子数约为
8.【2022年1月浙江卷】AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)+Bn-
(aq),其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是
A.ΔH和ΔS均大于零
B.ΔH和ΔS均小于零C.ΔH可能大于零或小于零,ΔS大于零
D.ΔH和ΔS均可能大于零或小于零
9.(2021.6·浙江真题)相同温度和压强下,关于物质熵的大小比较,合理的是
A. B.
C. D.
10.(2020·浙江高考真题)一定条件下:2NO (g)⇌ N O (g) ΔH<0。在测定NO 的相对分子质量时,
2 2 4 2
下列条件中,测定结果误差最小的是( )
A.温度0℃、压强50kPa B.温度130℃、压强300kPa
C.温度25℃、压强100kPa D.温度130℃、压强50kPa
11.(2020·江苏高考真题)反应 可用于纯硅的制备。下列有关该反
应的说法正确的是
A.该反应 、
B.该反应的平衡常数
C.高温下反应每生成1 mol Si需消耗
D.用E表示键能,该反应
12.(2020·江苏高考真题)CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
在恒压、反应物起始物质的量比 条件下,CH 和CO 的平衡转化率随温度变化的
4 2
曲线如图所示。下列有关说法正确的是
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线B表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠D.恒压、800K、n(CH):n(CO)=1:1条件下,反应至CH 转化率达到X点的值,改变除温度外的特
4 2 4
定条件继续反应,CH 转化率能达到Y点的值
4
13.(2019·海南高考真题)反应C H(g) C H(g)+H(g) △H>0,在一定条件下于密闭容器中达到平衡。
2 6 2 4 2
下列各项措施中,不能提高乙烷平衡转化率的是( )
A.增大容器容积 B.升高反应温度
C.分离出部分氢气 D.等容下通入惰性气体
14.(2019·上海高考真题)已知反应式:mX(g)+nY(?) pQ(s)+2mZ(g),已知反应已达平衡,此时
c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的 ,c(X)=0.5mol/L,下列说法正确的是( )
A.反应向逆方向移动 B.Y可能是固体或液体
C.系数n>m D.Z的体积分数减小
15.(2018·上海高考真题)关于硫酸工业中的催化氧化反应,叙述正确的是( )
A.是吸热反应 B.在常压下进行
C.在沸腾炉中进行 D.使用铁触媒作催化剂
16.(2018·天津高考真题)室温下,向圆底烧瓶中加入1 molC HOH和含1molHBr的氢溴酸,溶液中发
2 5
生反应;C HOH+HBr C HBr+H O,充分反应后达到平衡。已知常压下,C HBr和C HOH的沸
2 5 2 5 2 2 5 2 5
点分别为38.4℃和78.5℃。下列有关叙述错误的是
A.加入NaOH,可增大乙醇的物质的量
B.增大HBr浓度,有利于生成C HBr
2 5
C.若反应物增大至2 mol,则两种反应物平衡转化率之比不变
D.若起始温度提高至60℃,可缩短反应达到平衡的时间
17.(2018·浙江高考真题)已知X(g)+3Y (g) 2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温
度下,在体积恒定的密闭容器中,加入1 mol X(g) 与1mol Y (g),下列说法正确的是
A.充分反应后,放出热量为a kJ
B.当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
C.当X的物质的量分数不再改变,表明该反应已达平衡
D.若增大Y的浓度,正反应速率增大,逆反应速率减小
18.(2018·浙江高考真题)已知:2SO (g)+ O (g)= 2SO (g) △H =-197.8kJ•mol—1。起始反应物为SO
2 2 3 2
和 O(物质的量之比为2:1,且总物质的量不变)。SO 的平衡转化率(%)随温度和压强的变化
2 2
如下表,下列说法不正确的是
压强/(105Pa)
温度/K
1.01 5.07 10.1 25.3 50.7
673 99.2 99.6 99.7 99.8 99.9
723 97.5 98.9 99.2 99.5 99.6773 93.5 96.9 97.8 98.6 99.0
A.一定压强下降低温度,SO 的转化率增大
2
B.在不同温度、压强下,转化相同物质的量的SO 所需要的时间相等
2
C.使用催化剂可以缩短反应达到平衡所需的时间
D.工业生产通常不采取加压措施是因为常压下SO 的转化率已相当高
2
19.(2017·海南高考真题)已知反应CO(g)+HO(g) CO(g)+H(g) ΔH<0。在一定温度和压强下
2 2 2
于密闭容器中,反应达到平衡。下列叙述正确的是
A.升高温度,K减小 B.减小压强,n(CO)增加
2
C.更换高效催化剂,α(CO)增大 D.充入一定量的氮气,n(H )不变
2
20.(2017·上海高考真题)在N+3H 2NH (正反应为放热反应)的反应中,为了提高H 的利用
2 2 3 2
率,可以采取的措施为
A.升温 B.增大压强 C.使用催化剂 D.增大H 的浓度
2
❑
21.(2017·浙江高考真题)在一定条件下,可逆反应X(g)+2Y(g) ⇌2Z(g) ΔH=-akJ•mol-1,达到化学平衡时,下
❑
列说法一定正确的是 ( )
A.反应放出akJ热量 B.反应物和生成物的浓度都不再发生变化
C.X和Y的物质的量之比为1∶2 D.X的正反应速率等于Z的逆反应速率
22.(2013·北京高考真题)下列实验事实不能用平衡移动原理解释的是
A.
B.
C.
D.
23.(2012·上海高考真题)下列关于硫酸工业生产过程的叙述错误的是( )
A.在接触室中使用铁粉作催化剂B.在接触室中运用热交换技术可充分利用能源
C.把硫铁矿磨成细粉末,可以提高原料的利用率
D.该反应采用450~500°C主要是因为该温度下催化剂活性好
24.(2013·山东高考真题)对于反应CO(g)+H O(g) CO (g)+ H (g) △H﹤0,在其他条件
2 2 2
不变的情况下
A.加入催化剂,改变了反应的途径,反应的△H也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
25.(2015·上海高考真题)对于合成氨反应,达到平衡后,以下分析正确的是( )。
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大
D.加入催化剂,对逆反应的反应速率影响更大
26.(2017·浙江高考真题)已知:X(g)+2Y(g) 3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是
A.0.1molX和0.2molY充分反应生成Z的物质的量一定小于0.3mol
B.达到化学平衡状态时,X、Y、Z的浓度不再发生变化
C.达到化学平衡状态时,反应放出的总热量可达a kJ
D.升高反应温度,逆反应速率增大,正反应速率减小
27.(2009·四川高考真题)在一体积可变的密闭容器中,加入一定量的X、Y,发生反应:mX(g)
⇌nY(g);ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
下列说法正确的是
A.m>n B.Q<0
C.温度不变,压强增大,Y的质量分数减少 D.体积不变,温度升高,平衡向逆反应方向移动
28.(2008·天津高考真题)对平衡CO(g) CO(aq) △H= -19.75kJ/mol,为增大二氧化碳气体在
2 2
水中的溶解度,应采用的方法是( )
A.升温增压 B.降温减压C.升温减压 D.降温增压
29.(2010·上海高考真题)1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了
当时日益增长的人口对粮食的需求。下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是
( )。
A.①②③ B.②④⑤ C.①③⑤ D.②③④
30.(2012·安徽高考真题)一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
SO (g)+2CO(g) 2CO(g)+S(l)△H<0 若反应在恒容的密闭容器中进行,下列有关说法正确的是
2 2
A.平衡前,随着反应的进行,容器内压强始终不变
B.平衡时,其他条件不变,分离出硫,正反应速率加快
C.平衡时,其他条件不变,升高温度可提高SO 的转化率
2
D.其他条件不变,使用不同催化剂,该反应平衡常数不变
31.(2009·广东高考真题)已知汽车尾气无害化处理反应为
。
下列说法不正确的是 ( )
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高正反应速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO 的物质的量相等时,反应达到平衡
2
32.(2008·广东高考真题)将H(g)和Br (g)充入恒容密闭容器,恒温下发生反应H(g)+Br (g)
2 2 2 2
2HBr(g) H<0;平衡时Br (g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时
2
Br (g)的转化率为b。a与b的关系是( )
2
A.a>b B.a=b C.a<b D.无法确定
33.(2007·全国高考真题)题文已知:C(s)+CO(g) 2CO(g) △H>0。该反应的达到平衡后,
2
下列条件有利于反应向正方向进行的是
A.升高温度和减小压强 B.降低温度和减小压强
C.降低温度和增大压强 D.升高温度和增大压强
34.(2012·重庆高考真题)在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)⇌2c(g);△H
1
<0
x(g)+3y(g)⇌2z(g);△H
2
>0
进行相关操作且达到平衡后(忽略体积改变所作的功),下列叙述错误的是( )
A.等压时,通入惰性气体,c的物质的量不变B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入z气体,y的物质的量浓度增大
35.(2010·重庆高考真题)COCl
2
(g)⇌CO(g)+Cl
2
(g)∆H>0,当反应达到平衡时,下列措施:①升
温,②恒压通入惰性气体,③增加CO的浓度,④减压,⑤加催化剂,⑥恒容通入惰性气体;能提高
COCl 转化率的是( )
2
A.①②④ B.①④⑥ C.②③⑥ D.③⑤⑥
36.(2012·全国高考真题)合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:
CO(g)+H O(g) CO(g)+H (g)△H<0反应达到平衡后,为提高CO的转化率,下列措
2 2 2
施中正确的是( )
A.增加压强 B.降低温度 C.增大CO的浓度 D.更换催化剂