文档内容
年湖北省七市州高三年级 月联合统一调研测试
2025 3
化 学 试 卷
命题单位:孝感市教科院 审题单位:宜昌市教科院 荆门市教研室
2025.3
本试卷共 页, 题。 全卷满分 分。 考试用时 分钟。
8 19 100 75
祝考试顺利
★ ★
注意事项:
答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并认
1.
真核准准考证号条形码上的以上信息,将条形码粘贴在答题卡上的指定位置。
请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上
2.
的非答题区域均无效。
选择题用 铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答
3. 2B
题卡上作答;字体工整,笔迹清楚。
考试结束后,请将试卷和答题卡一并上交。
4.
可能用到的相对原子质量:
H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Ca 40
一、选择题:本题共 小题。 每小题 分,共 分。 在每小题给出的四个选项中,只有一
15 3 45
项是符合题目要求的。
中华文明源远流长 化学与中华文明联系紧密 下列叙述错误的是
1. , 。
湖北随州出土的曾侯乙编钟是以铜为主要成分的合金制品
A.
四川蜀锦的主要原料蚕丝属于化学纤维
B.
唐陶彩绘女舞俑是以黏土为主要原料 经高温烧结而成
C. ,
云梦秦简是一种战国时期的竹简 主要成分纤维素属于天然有机高分子
D. ,
化学与生产 生活和科技密切相关 下列叙述错误的是
2. 、 。
市场上销售的暖贴通常是利用金属的电化学腐蚀原理制作的
A.
苯甲酸及其钠盐可用作食品防腐剂
B.
量子通信材料螺旋碳纳米管与富勒烯互为同素异形体
C.
稀土元素就是镧系元素 在科技 生产中有广泛的用途 被称为 冶金工业的维生素
D. , 、 , “ ”
用下列装置进行实验 能达到相应实验目的的是
3. ,
图甲装置用于测定氢氧化钠溶液的浓度 图乙装置用于灼烧碎海带
A. B.
图丙装置用于检验二氧化硫的酸性与漂白性 图丁装置用于制取氨气
C. D.
高三化学试卷 第 页 共 页
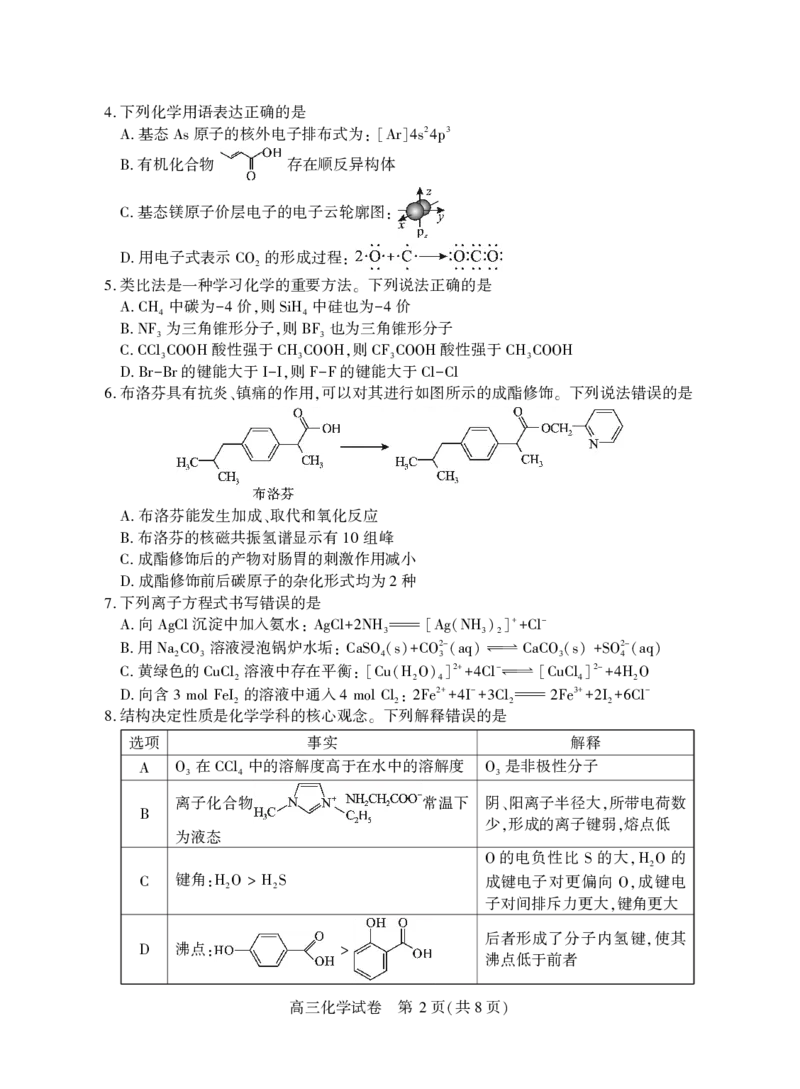
1 ( 8 )下列化学用语表达正确的是
4.
基态 原子的核外电子排布式为
2 3
A. As : [Ar]4s 4p
有机化合物 存在顺反异构体
B.
基态镁原子价层电子的电子云轮廓图
C. :
用电子式表示 的形成过程
D. CO2 :
类比法是一种学习化学的重要方法 下列说法正确的是
5. 。
中碳为 价 则 中硅也为 价
A.CH4 -4 , SiH4 -4
为三角锥形分子 则 也为三角锥形分子
B.NF3 , BF3
酸性强于 则 酸性强于
C.CCl3COOH CH3COOH, CF3COOH CH3COOH
的键能大于 则 的键能大于
D.Br-Br I-I, F-F Cl-Cl
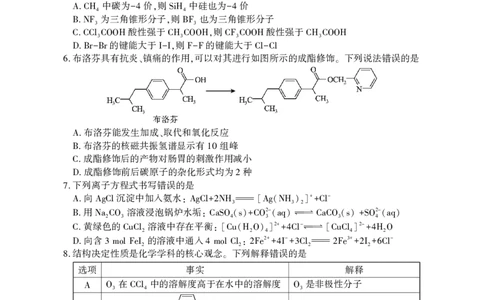
布洛芬具有抗炎 镇痛的作用 可以对其进行如图所示的成酯修饰 下列说法错误的是
6. 、 , 。
布洛芬能发生加成 取代和氧化反应
A. 、
布洛芬的核磁共振氢谱显示有 组峰
B. 10
成酯修饰后的产物对肠胃的刺激作用减小
C.
成酯修饰前后碳原子的杂化形式均为 种
D. 2
下列离子方程式书写错误的是
7.
向 沉淀中加入氨水
A. AgCl : AgCl+2NH3 [Ag(NH3)2]
+
+Cl
-
用 溶液浸泡锅炉水垢
B. Na2CO3 : CaSO4(s)+CO
2
3
-
(aq) CaCO3(s) +SO
2
4
-
(aq)
黄绿色的 溶液中存在平衡
2+ - 2-
C. CuCl2 : [Cu(H2O)4] +4Cl [CuCl4] +4H2O
向含 的溶液中通入
D. 3 mol FeI2 4 mol Cl2: 2Fe
2+
+4I
-
+3Cl2 2Fe
3+
+2I2+6Cl
-
结构决定性质是化学学科的核心观念 下列解释错误的是
8. 。
选项 事实 解释
在 中的溶解度高于在水中的溶解度 是非极性分子
A O3 CCl4 O3
离子化合物 常温下 阴 阳离子半径大 所带电荷数
、 ,
B 少 形成的离子键弱 熔点低
为液态 , ,
的电负性比 的大 的
O S ,H2O
键角 成键电子对更偏向 成键电
C :H2O > H2S O,
子对间排斥力更大 键角更大
,
后者形成了分子内氢键 使其
沸点 ,
D : > 沸点低于前者
高三化学试卷 第 页 共 页
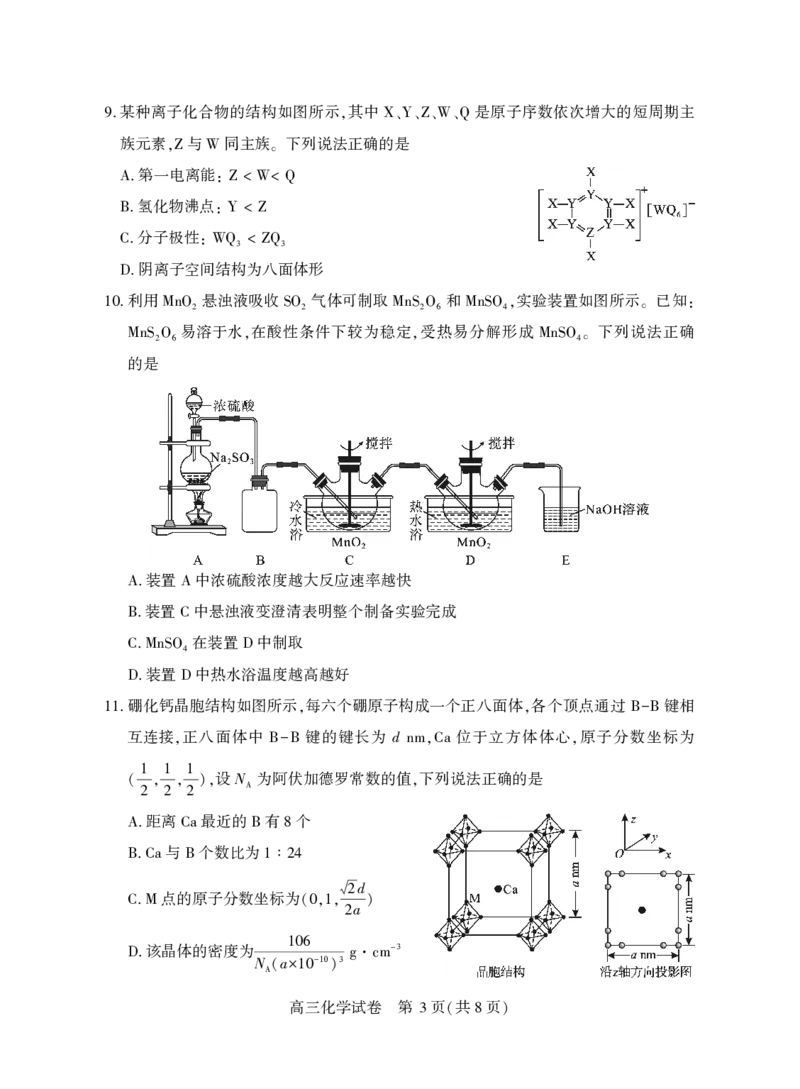
2 ( 8 )某种离子化合物的结构如图所示 其中 是原子序数依次增大的短周期主
9. , X、Y、Z、W、Q
族元素 与 同主族 下列说法正确的是
,Z W 。
第一电离能
A. : Z < W< Q
氢化物沸点
B. : Y < Z
分子极性
C. : WQ3 < ZQ3
阴离子空间结构为八面体形
D.
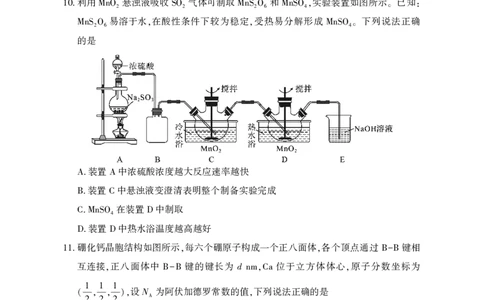
利用 悬浊液吸收 气体可制取 和 实验装置如图所示 已知
10. MnO2 SO2 MnS2O6 MnSO4, 。 :
易溶于水 在酸性条件下较为稳定 受热易分解形成 下列说法正确
MnS2O6 , , MnSO4。
的是
装置 中浓硫酸浓度越大反应速率越快
A. A
装置 中悬浊液变澄清表明整个制备实验完成
B. C
在装置 中制取
C.MnSO4 D
装置 中热水浴温度越高越好
D. D
硼化钙晶胞结构如图所示 每六个硼原子构成一个正八面体 各个顶点通过 键相
11. , , B-B
互连接 正八面体中 键的键长为 d 位于立方体体心 原子分数坐标为
, B-B nm,Ca ,
1 1 1 设N 为阿伏加德罗常数的值 下列说法正确的是
( , , ), A ,
2 2 2
距离 最近的 有 个
A. Ca B 8
与 个数比为
B.Ca B 1 ∶ 24
d
点的原子分数坐标为 2
C.M (0,1, a )
2
该晶体的密度为 106 -3
D. N a -10 3 g·cm
A( ×10 )
高三化学试卷 第 页 共 页
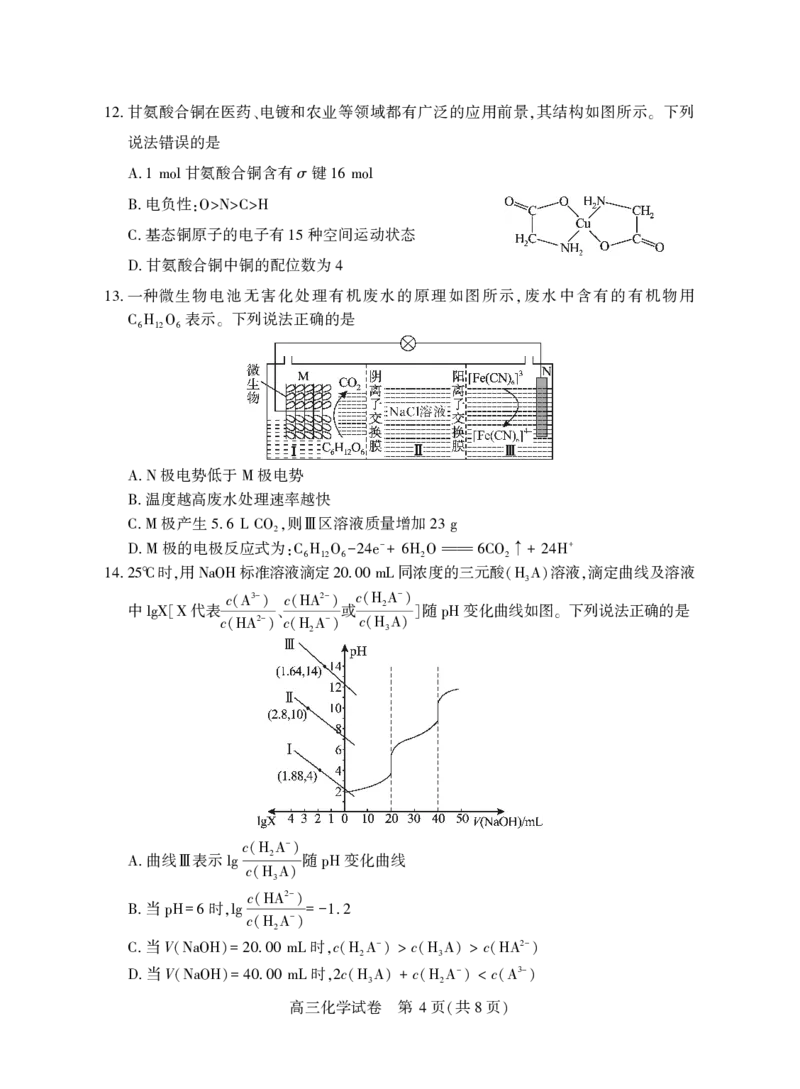
3 ( 8 )甘氨酸合铜在医药 电镀和农业等领域都有广泛的应用前景 其结构如图所示 下列
12. 、 , 。
说法错误的是
甘氨酸合铜含有σ键
A.1 mol 16 mol
电负性
B. :O>N>C>H
基态铜原子的电子有 种空间运动状态
C. 15
甘氨酸合铜中铜的配位数为
D. 4
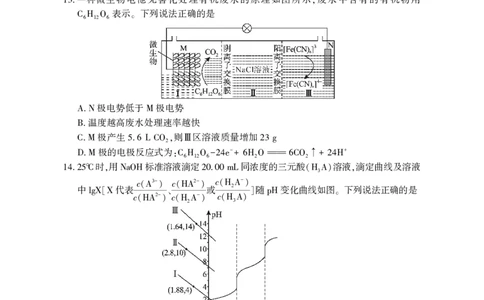
一种微生物电池无害化处理有机废水的原理如图所示 废水中含有的有机物用
13. ,
表示 下列说法正确的是
C6H12O6 。
极电势低于 极电势
A.N M
温度越高废水处理速率越快
B.
极产生 则 区溶液质量增加
C.M 5.6 L CO2, Ⅲ 23 g
极的电极反应式为
D.M :C6H12O6-24e
-
+ 6H2O 6CO2 ↑+ 24H
+
时 用 标准溶液滴定 同浓度的三元酸 溶液 滴定曲线及溶液
14.25℃ , NaOH 20.00 mL (H3A) ,
c 3- c 2- c -
中 代表 (A ) (HA )或 (H2A ) 随 变化曲线如图 下列说法正确的是
lgX[X c 2- 、c - c ] pH 。
(HA ) (H2A ) (H3A)
c -
曲线 表示 (H2A )随 变化曲线
A. Ⅲ lg c pH
(H3A)
c 2-
当 时 (HA )
B. pH=6 ,lg c - = -1.2
(H2A )
当V 时 c - c c 2-
C. (NaOH)= 20.00 mL , (H2A ) > (H3A) > (HA )
当V 时 c c - c 3-
D. (NaOH)= 40.00 mL ,2 (H3A) + (H2A ) < (A )
高三化学试卷 第 页 共 页
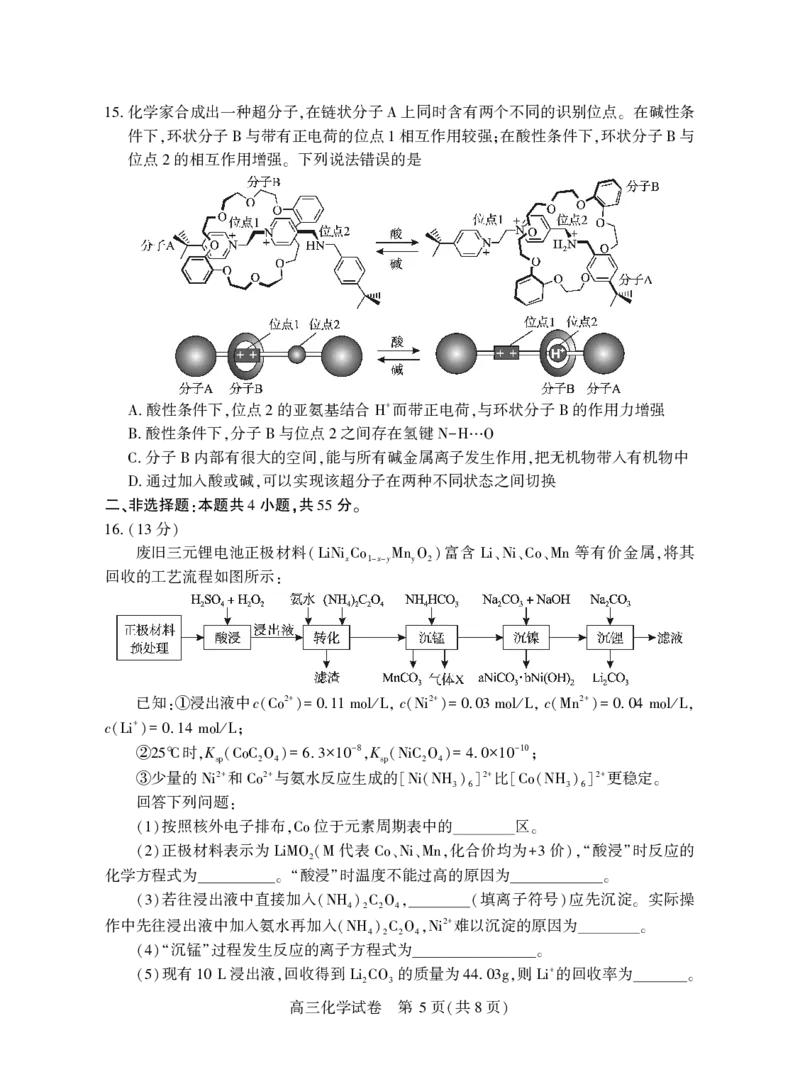
4 ( 8 )化学家合成出一种超分子 在链状分子 上同时含有两个不同的识别位点 在碱性条
15. , A 。
件下 环状分子 与带有正电荷的位点 相互作用较强 在酸性条件下 环状分子 与
, B 1 ; , B
位点 的相互作用增强 下列说法错误的是
2 。
酸性条件下 位点 的亚氨基结合 而带正电荷 与环状分子 的作用力增强
+
A. , 2 H , B
酸性条件下 分子 与位点 之间存在氢键
B. , B 2 N-H…O
分子 内部有很大的空间 能与所有碱金属离子发生作用 把无机物带入有机物中
C. B , ,
通过加入酸或碱 可以实现该超分子在两种不同状态之间切换
D. ,
二、非选择题:本题共 小题,共 分。
4 55
分
16.(13 )
废旧三元锂电池正极材料 富含 等有价金属 将其
(LiNixCo1- x - yMnyO2) Li、Ni、Co、Mn ,
回收的工艺流程如图所示
:
已知 浸出液中c 2+ c 2+ c 2+
:① (Co )=0.11 mol/L, (Ni )=0.03 mol/L, (Mn )= 0.04 mol/L,
c +
(Li )= 0.14 mol/L;
时 K -8 K -10
②25℃ , sp(CoC2O4)= 6.3×10 , sp(NiC2O4)= 4.0×10 ;
少量的 和 与氨水反应生成的 比 更稳定
2+ 2+ 2+ 2+
③ Ni Co [Ni(NH3)6] [Co(NH3)6] 。
回答下列问题
:
按照核外电子排布 位于元素周期表中的 区
(1) ,Co 。
正极材料表示为 代表 化合价均为 价 酸浸 时反应的
(2) LiMO2(M Co、Ni、Mn, +3 ),“ ”
化学方程式为 酸浸 时温度不能过高的原因为
。 “ ” 。
若往浸出液中直接加入 填离子符号 应先沉淀 实际操
(3) (NH4)2C2O4, ( ) 。
作中先往浸出液中加入氨水再加入 难以沉淀的原因为
2+
(NH4)2C2O4,Ni 。
沉锰 过程发生反应的离子方程式为
(4)“ ” 。
现有 浸出液 回收得到 的质量为 则 的回收率为
+
(5) 10 L , Li2CO3 44.03g, Li 。
高三化学试卷 第 页 共 页
5 ( 8 )分
17.(14 )
含碳化合物的回收是实现碳达峰 碳中和的有效途径 催化加氢选择合成甲醇
、 。 CO2
的主要反应如下
:
反应 ΔH
1:CO2(g)+3H2(g) CH3OH(g) +H2O(g) 1<0
反应 ΔH
2:CO2(g)+H2(g) CO(g) +H2O(g) 2 >0
反应 ΔH
3:CO(g)+2H2(g) CH3OH(g) 3
回答下列问题
:
已知在 下 由最稳定单质生成 某纯物质的焓变 称为该物质
(1) 25 ℃、101kPa , 1 mol ,
的标准摩尔生成焓 下表为几种常见物质的标准摩尔生成焓
。 。
物质
CO2(g) H2(g) CH3OH(g) H2O(g)
标准摩尔生成焓
-1
/( kJ·mol ) -393.5 0 -200.7 -241.8
则ΔH
-1
1= kJ·mol 。
反应 在 填 较高 或 较低 温度下能自发进行
(2) 3 ( “ ” “ ”) 。
对于上述反应体系 下列说法正确的是 填标号
(3) , ( )。
其他条件相同 反应 分别在恒容和恒压条件下进行 后者 的平衡转化率更高
a. , 1 , CO2
恒温恒容条件下 当容器内气体的压强不再改变 说明体系达到平衡状态
b. , ,
增加催化剂的表面积 可加快反应速率 提高 的平衡产率
c. , , CH3OH
其他条件相同 增大投料比 n n 可提高 的平衡转化率
d. , [ (CO2)/ (H2)], CO2
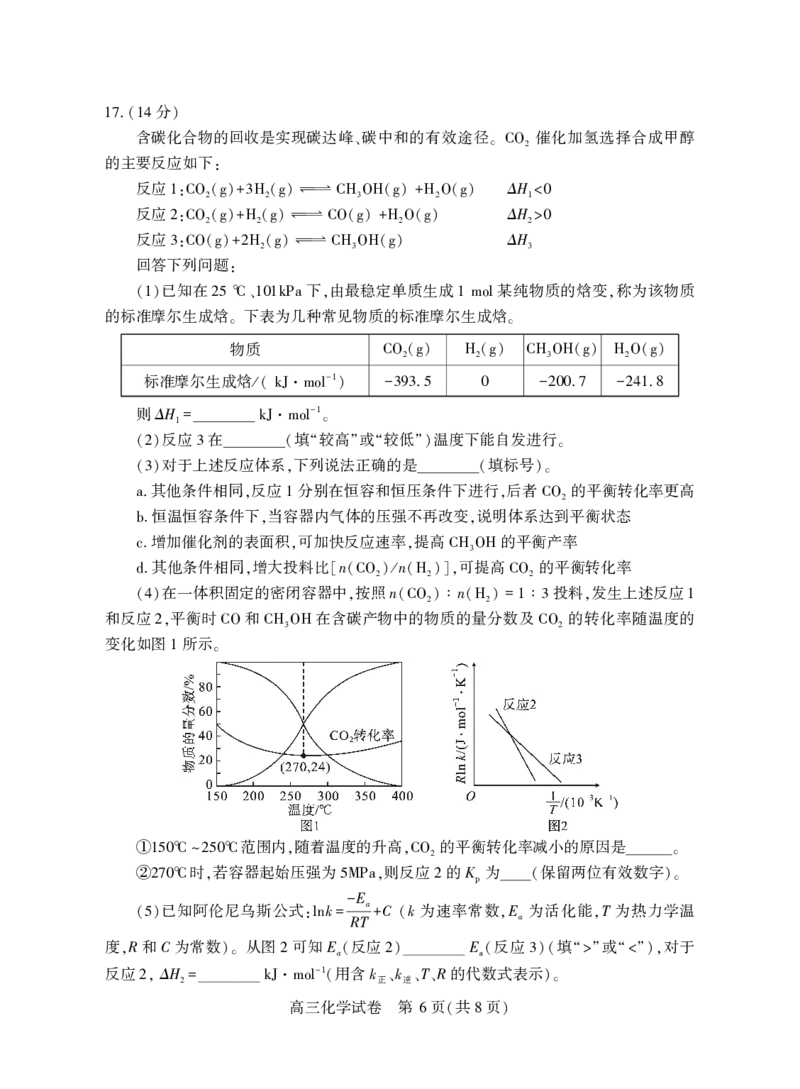
在一体积固定的密闭容器中 按照n n 投料 发生上述反应
(4) , (CO2) ∶ (H2) = 1 ∶ 3 , 1
和反应 平衡时 和 在含碳产物中的物质的量分数及 的转化率随温度的
2, CO CH3OH CO2
变化如图 所示
1 。
范围内 随着温度的升高 的平衡转化率减小的原因是
①150℃~250℃ , ,CO2 。
时 若容器起始压强为 则反应 的K 为 保留两位有效数字
②270℃ , 5MPa, 2 p ( )。
E
已知阿伦尼乌斯公式 k - a C k 为速率常数 E 为活化能 T 为热力学温
(5) :ln = RT + ( , a ,
度 R和C为常数 从图 可知E 反应 E 反应 填 或 对于
, )。 2 a( 2) a( 3)( “>” “<”),
反应 2, ΔH 2= kJ·mol -1 ( 用含k 正、 k 逆、 T 、 R的代数式表示 )。
高三化学试卷 第 页 共 页
6 ( 8 )分
18.(14 )
某化学学习小组探究 能否氧化 并分析相关转化
2+ 2+
Cu Fe 。
实验序号 实验操作与现象
向盛有 溶液的试管中加入过量铜粉 分钟
实验 2 mL 0.05 mol/L Fe2(SO4)3 ,5
1 后溶液变蓝
将实验 反应混合物长时间静置 取上层清液于另一试管 滴加 溶
1 , , KSCN
液 溶液变红 振荡红色消失 产生少量白色沉淀 如此反复多次滴加
实验 , , , ,
2 溶液 振荡观察到的现象相同 当加入大量 溶液后 红色不
KSCN , , KSCN ,
再褪去 生成较多白色沉淀
,
已知 为难溶于水的白色固体
:ⅰ.CuSCN
有较强还原性 易被氧化为 化学性质与卤素单质相似
-
ⅱ.SCN , (SCN)2,(SCN)2
向实验 充分反应后的溶液中滴加 溶液 溶液变红 对其原因进行探究
1 KSCN , , :
假设 静置过程中空气中的氧气将 氧化
2+
①: Fe 。
假设 发生反应 将 氧化为
2+ - 2+ 3+
②: 2Cu +4SCN 2CuSCN↓+ (SCN)2,(SCN)2 Fe Fe 。
假设 在 的影响下 将 氧化为
2+ - 2+ 3+
③:Cu SCN , Fe Fe 。
回答下列问题
:
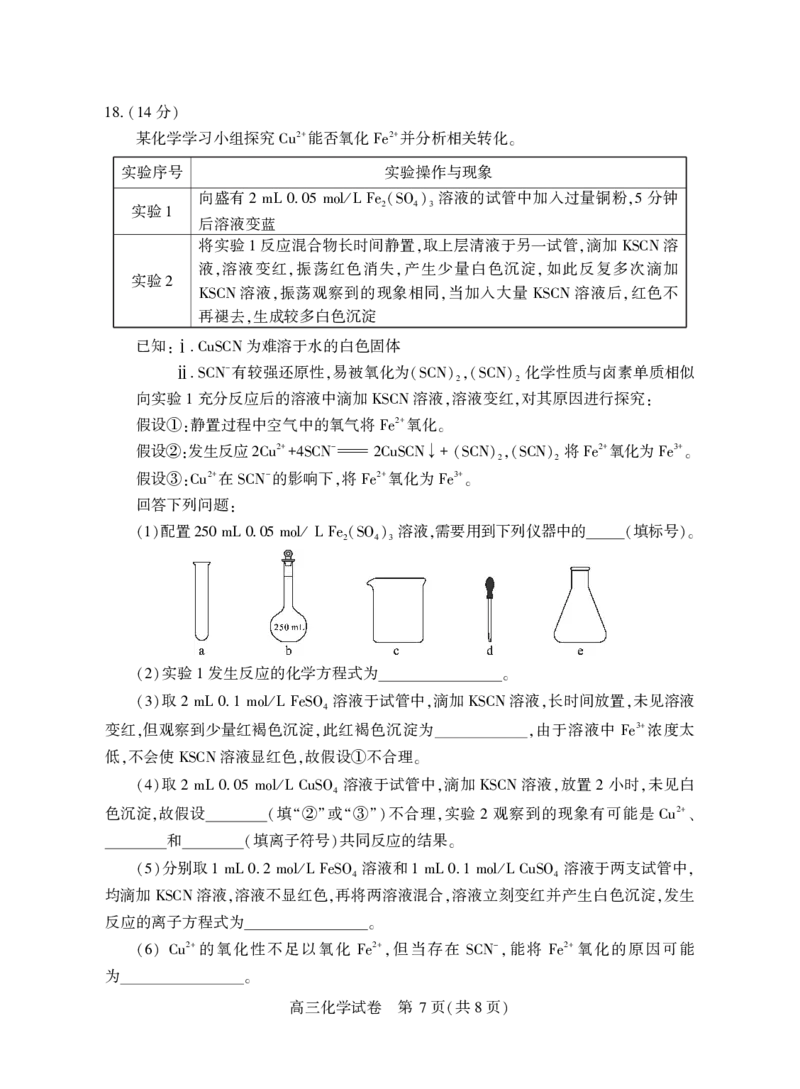
配置 溶液 需要用到下列仪器中的 填标号
(1) 250 mL 0.05 mol/ L Fe2(SO4)3 , ( )。
实验 发生反应的化学方程式为
(2) 1 。
取 溶液于试管中 滴加 溶液 长时间放置 未见溶液
(3) 2 mL 0.1 mol/L FeSO4 , KSCN , ,
变红 但观察到少量红褐色沉淀 此红褐色沉淀为 由于溶液中 浓度太
3+
, , , Fe
低 不会使 溶液显红色 故假设 不合理
, KSCN , ① 。
取 溶液于试管中 滴加 溶液 放置 小时 未见白
(4) 2 mL 0.05 mol/L CuSO4 , KSCN , 2 ,
色沉淀 故假设 填 或 不合理 实验 观察到的现象有可能是
2+
, ( “②” “③”) , 2 Cu 、
和 填离子符号 共同反应的结果
( ) 。
分别取 溶液和 溶液于两支试管中
(5) 1 mL 0.2 mol/L FeSO4 1 mL 0.1 mol/L CuSO4 ,
均滴加 溶液 溶液不显红色 再将两溶液混合 溶液立刻变红并产生白色沉淀 发生
KSCN , , , ,
反应的离子方程式为
。
的氧化性不足以氧化 但当存在 能将 氧化的原因可能
2+ 2+ - 2+
(6) Cu Fe , SCN , Fe
为
。
高三化学试卷 第 页 共 页
7 ( 8 )分
19. (14 )
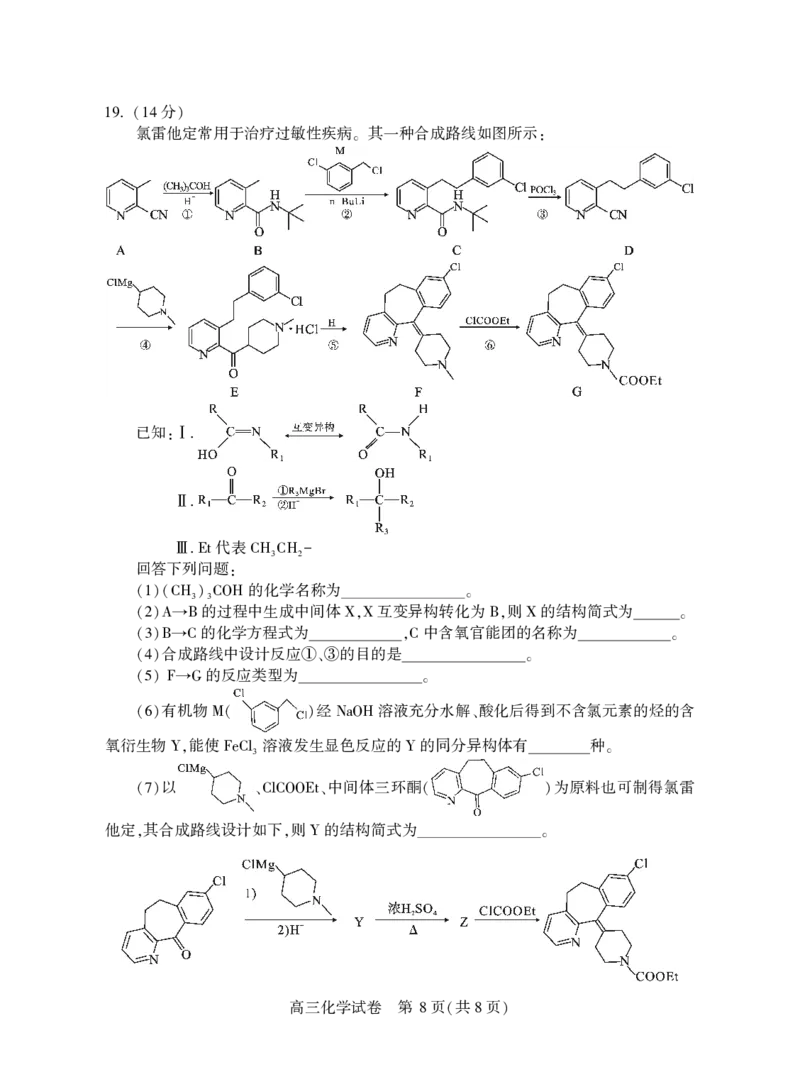
氯雷他定常用于治疗过敏性疾病 其一种合成路线如图所示
。 :
已知
:Ⅰ.
Ⅱ.
代表
Ⅲ.Et CH3CH2-
回答下列问题
:
的化学名称为
(1)(CH3)3COH 。
的过程中生成中间体 互变异构转化为 则 的结构简式为
(2)A→B X,X B, X 。
的化学方程式为 中含氧官能团的名称为
(3)B→C ,C 。
合成路线中设计反应 的目的是
(4) ①、③ 。
的反应类型为
(5) F→G 。
有机物 经 溶液充分水解 酸化后得到不含氯元素的烃的含
(6) M( ) NaOH 、
氧衍生物 能使 溶液发生显色反应的 的同分异构体有 种
Y, FeCl3 Y 。
以 中间体三环酮 为原料也可制得氯雷
(7) 、ClCOOEt、 ( )
他定 其合成路线设计如下 则 的结构简式为
, , Y 。
高三化学试卷 第 页 共 页
8 ( 8 )