文档内容
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
2023 年高考考前押题密卷(湖南卷) C.化合物甲和化合物丙均含有的官能团为氨基、酰胺基和羧基
D.化合物丙在一定条件下可发生水解反应,水解产物中有化合物乙
化 学
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标况下,2.24 L的NH 和HF的分子数均为0.1N
3 A
本卷满分100分,考试时间75分钟。
B.2L1mol·L-1的氯化铜溶液中H+数目为4N
A
注意事项:
C. 和 的混合气体中含有的孤电子对数为
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮 D.2LpH=5的0.05mol·L-1KCr O 溶液中 数目为0.1N
2 2 7 A
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
5.实验是化学研究的重要方法。下列实验设计能达到实验目的的是
3.考试结束后,将本试卷和答题卡一并交回。
选项 实验目的 实验设计
可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 35.5 K 39 Ca 40 Cr 52 Co 59 Cu 64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项 检验 溶液中是否存在 杂 用洁净的铂丝蘸取该溶液,在酒精灯外焰上灼烧,观察火焰
A
质 是否出现紫色
是符合题目要求的。
1.化学与生活、科技、社会发展息息相关。下列说法错误的是
B 测定氯水的 将待测液滴在湿润的 试纸上,与标准比色卡对照
A.自然界中“氮循环”过程一定包括氧化还原反应和非氧化还原反应
C 除去乙炔气体中的硫化氢 将混合气体通入盛有硫酸铜溶液的洗气瓶中。
B.重油裂解为轻质油作燃料有助于实现“碳中和”
D 配制 溶液 称取 固体溶解在 容量瓶中,再定容、摇匀
C.快餐餐盒使用的聚乳酸材料可由乳酸( )缩聚制得
6.下列离子反应方程式书写正确的是
D.量子通信材料螺旋碳纳米管、石墨烯互为同素异形体
A.向 中加入 :
2.工业上制备硫酸时,用98.3%的浓硫酸吸收 得到组成为 的发烟硫酸。当 时形成焦
B.小苏打溶液与明矾溶液混合:
硫酸( ),结构如图所示,它与水作用生成硫酸。下列关于焦硫酸的说法错误的是
C.向硫酸铜溶液中加入NaHS溶液生成黑色沉淀:
D.向 溶液中滴加少量 溶液:
7.某 样品中含少量 ,为测定样品的纯度,操作过程如下:(1)取一定质量的样品配制成
A.属于极性分子 B.具有强氧化性
250mL溶液;(2)准确量取25.00mL配制的溶液于锥形瓶中,滴几滴指示剂,用c 硝酸银溶液滴
C.所有S和O均为 杂化 D.其盐 的溶液呈酸性
定至终点。下列叙述错误的是
3.下图为合成药物M工艺过程中的某一步转化关系(反应条件已省略)。 A.需要用到250mL容量瓶、棕色滴定管
B.滴定过程中眼睛注视滴定管液面的变化
C.滴定管排气泡后调节液面至0或0刻度以下
D.如果盛标准溶液的滴定管没有润洗,所得结果会偏高
8.前四周期元素W、X、Y、Z的原子序数依次增大。基态W原子中有7个运动状态不同的电子,X元素
形成的某种单质是极性分子,基态Y原子的价层电子排布式为 ,基态Z原子次外层全充满,最
外层电子数为1,下列说法正确的是
A.W和X的简单氢化物的稳定性:W>X
下列说法正确的是 B.基态X原子的第一电离能比同周期相邻原子都要低
A.上述反应为取代反应,生成物有化合物丙和乙酸 C.YX 空间构型是直线形
2
B.化合物甲分子中含有4个手性碳原子 D.单质Z与单质Y反应生成ZY
第19页 第110页
学科网(北京)股份有限公司………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
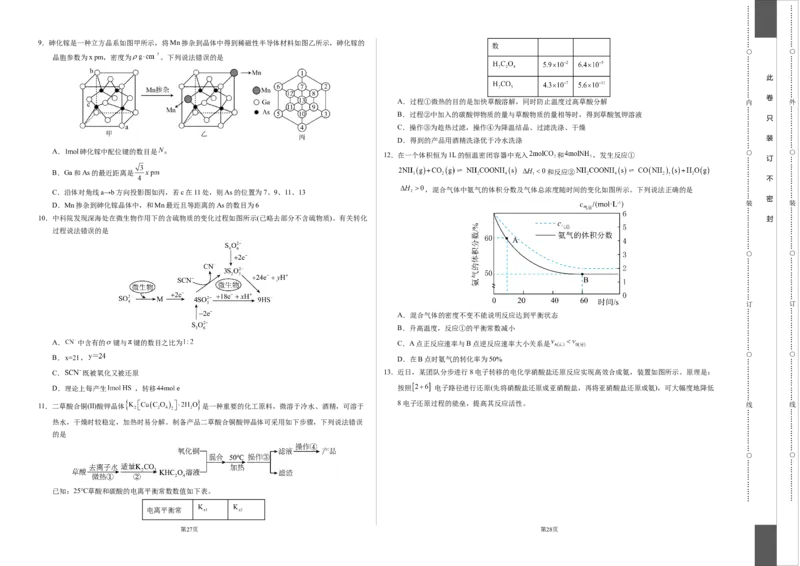
9.砷化镓是一种立方晶系如图甲所示,将Mn掺杂到晶体中得到稀磁性半导体材料如图乙所示,砷化镓的
数
晶胞参数为x pm,密度为 。下列说法错误的是
此
卷
A.过程①微热的目的是加快草酸溶解,同时防止温度过高草酸分解
B.过程②中加入的碳酸钾物质的量与草酸物质的量相等时,得到草酸氢钾溶液
只
C.操作③为趁热过滤,操作④为降温结晶、过滤洗涤、干燥
D.得到的产品用酒精洗涤优于冷水洗涤 装
A. 砷化镓中配位键的数目是
12.在一个体积恒为1L的恒温密闭容器中充入 和 ,发生反应①
订
B.Ga和As的最近距离是 和反应②
不
,混合气体中氨气的体积分数及气体总浓度随时间的变化如图所示。下列说法正确的是
C.沿体对角线a→b方向投影图如丙,若c在11处,则As的位置为7、9、11、13
密
D.Mn掺杂到砷化镓晶体中,和Mn最近且等距离的As的数目为6
10.中科院发现深海处在微生物作用下的含硫物质的变化过程如图所示(已略去部分不含硫物质)。有关转化 封
过程说法错误的是
A.混合气体的密度不变不能说明反应达到平衡状态
B.升高温度,反应①的平衡常数减小
A. 中含有的 键与 键的数目之比为 C.A点正反应速率与B点逆反应速率大小关系是
B. , D.在B点时氨气的转化率为50%
C. 既被氧化又被还原 13.近日,某团队分步进行8电子转移的电化学硝酸盐还原反应实现高效合成氨,装置如图所示。原理是:
D.理论上每产生 ,转移 按照 电子路径进行还原(先将硝酸盐还原成亚硝酸盐,再将亚硝酸盐还原成氨),可大幅度地降低
8电子还原过程的能垒,提高其反应活性。 11.二草酸合铜(Ⅱ)酸钾晶体 是一种重要的化工原料,微溶于冷水、酒精,可溶于
热水,干燥时较稳定,加热时易分解。制备产品二草酸合铜酸钾晶体可采用如下步骤,下列说法错误
的是
已知:25℃草酸和碳酸的电离平衡常数数值如下表。
电离平衡常
第27页 第28页………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
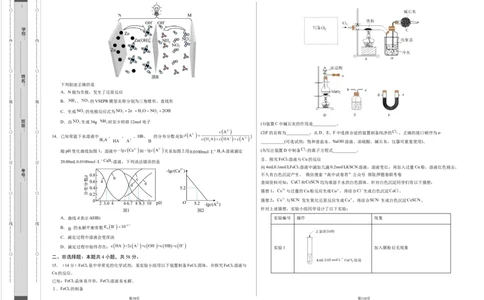
下列叙述正确的是
A.N极为负极,发生了还原反应
B. 、 的VSEPR模型名称分别为三角锥形、直线形
C.生成 的电极反应式为
D.由 生成34g 时至少转移12mol电子
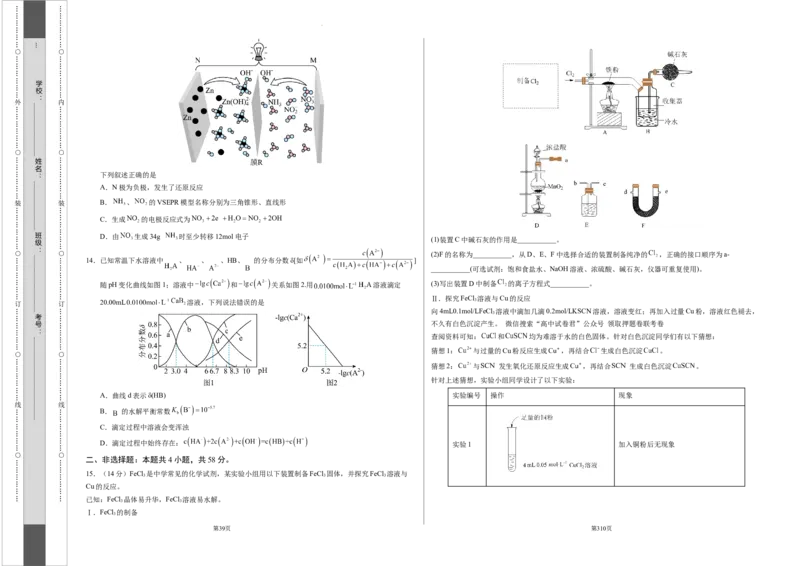
(1)装置C中碱石灰的作用是___________。
(2)F的名称为___________,从D、E、F中选择合适的装置制备纯净的 ,正确的接口顺序为a-
14.已知常温下水溶液中 、 、 、HB、 的分布分数δ[如 ]
___________(可选试剂:饱和食盐水、NaOH溶液、浓硫酸、碱石灰,仪器可重复使用)。
随pH变化曲线如图1;溶液中 和 关系如图2.用 溶液滴定 (3)写出装置D中制备 的离子方程式___________。
Ⅱ.探究FeCl 溶液与Cu的反应
20.00mL 溶液,下列说法错误的是 3
向4mL0.1mol/LFeCl 溶液中滴加几滴0.2mol/LKSCN溶液,溶液变红;再加入过量Cu粉,溶液红色褪去,
3
不久有白色沉淀产生。 微信搜索“高中试卷君”公众号 领取押题卷联考卷
查阅资料可知: 和 均为难溶于水的白色固体。针对白色沉淀同学们有以下猜想:
猜想1: 与过量的Cu粉反应生成 ,再结合 生成白色沉淀 。
猜想2: 与 发生氧化还原反应生成 ,再结合 生成白色沉淀 。
针对上述猜想,实验小组同学设计了以下实验:
A.曲线d表示δ(HB) 实验编号 操作 现象
B. 的水解平衡常数
C.滴定过程中溶液会变浑浊
D.滴定过程中始终存在: 实验1 加入铜粉后无现象
二、非选择题:本题共4小题,共58分。
15.(14分)FeCl 是中学常见的化学试剂,某实验小组用以下装置制备FeCl 固体,并探究FeCl 溶液与
3 3 3
Cu的反应。
已知:FeCl 晶体易升华,FeCl 溶液易水解。
3 3
Ⅰ.FeCl 的制备
3
第39页 第310页
学科网(北京)股份有限公司………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
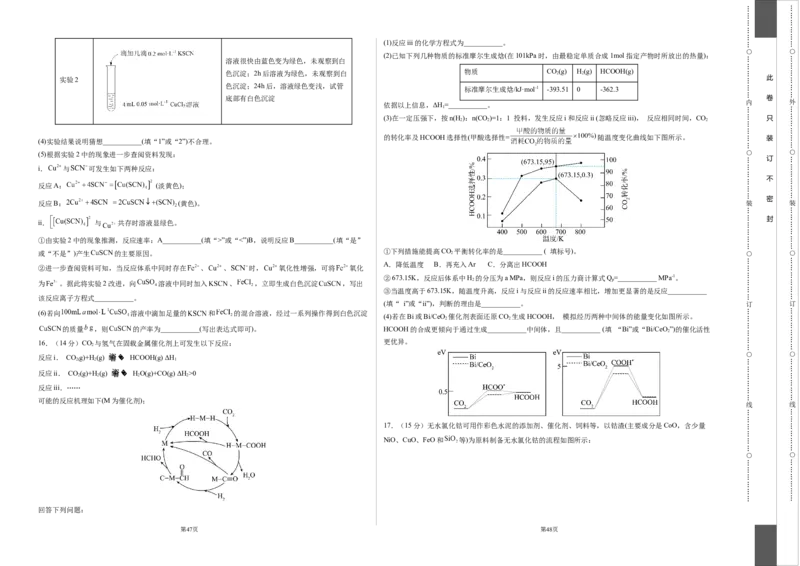
(1)反应iii的化学方程式为___________。
(2)已知下列几种物质的标准摩尔生成焓(在101kPa时,由最稳定单质合成1mol指定产物时所放出的热量):
溶液很快由蓝色变为绿色,未观察到白
色沉淀;2h后溶液为绿色,未观察到白 物质 CO 2 (g) H 2 (g) HCOOH(g)
实验2 此
色沉淀;24h后,溶液绿色变浅,试管
标准摩尔生成焓/kJ·mol-1 -393.51 0 -362.3
底部有白色沉淀 卷
依据以上信息,ΔH=___________。
1
(3)在一定压强下,按n(H ):n(CO)=1:1 投料,发生反应i和反应ii (忽略反应iii), 反应相同时间,CO 只
2 2 2
的转化率及HCOOH选择性(甲酸选择性= 随温度变化曲线如下图所示。 装
(4)实验结果说明猜想___________(填“1”或“2”)不合理。
(5)根据实验2中的现象进一步查阅资料发现:
订
i. 与 可发生如下两种反应:
不
反应A: (淡黄色);
密
反应B: (黄色)。
封
ii. 与 共存时溶液显绿色。
①由实验2中的现象推测,反应速率:A___________(填“>”或“<”)B,说明反应B___________(填“是”
①下列措施能提高CO 平衡转化率的是___________ ( 填标号)。 或“不是”)产生 的主要原因。 2
A.降低温度 B.再充入Ar C.分离出HCOOH
②进一步查阅资料可知,当反应体系中同时存在 、 、 时, 氧化性增强,可将 氧化
②673.15K,反应后体系中H 的分压为a MPa,则反应i的压力商计算式Q=___________ MPa-1。
2 p
为 。据此将实验2改进,向 溶液中同时加入 、 ,立即生成白色沉淀 ,写出
③当温度高于673.15K,随温度升高,反应i与反应ii的反应速率相比,增加更显著的是反应___________
该反应离子方程式___________。
(填“ i”或“ii”),判断的理由是___________。
(6)若向 溶液中滴加足量的 和 的混合溶液,经过一系列操作得到白色沉淀
(4)若在Bi或Bi/CeO 催化剂表面还原CO 生成HCOOH, 模拟经历两种中间体的能量变化如图所示。
2 2
的质量 ,则 的产率为___________(写出表达式即可)。 HCOOH的合成更倾向于通过生成___________中间体,且___________ (填 “Bi”或“Bi/CeO”)的催化活性
2
16.(14分)CO 与氢气在固载金属催化剂上可发生以下反应: 更优异。
2
反应i. CO g)+H (g) HCOOH(g) ΔH
2( 2 1
反应ii. CO(g)+H(g) HO(g)+CO(g) ΔH >0
2 2 2 2
反应iii.……
可能的反应机理如下(M为催化剂);
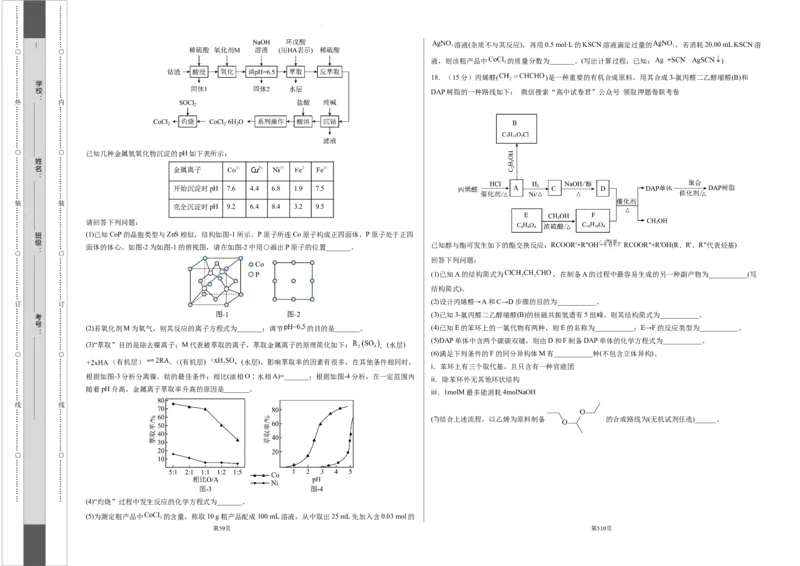
17.(15分)无水氯化钴可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量
NiO、CuO、FeO和 等)为原料制备无水氯化钴的流程如图所示:
回答下列问题:
第47页 第48页………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
…
学
校
:
______________
姓
名
:
_____________
班
级
:
_______________
考
号
:
______________________
溶液(杂质不与其反应),再用0.5 molL的KSCN溶液滴定过量的 ,若消耗20.00 mL KSCN溶
液,则该粗产品中 的质量分数为_____⋅__。(写出计算过程,已知: )
18.(15分)丙烯醛( )是一种重要的有机合成原料,用其合成3-氯丙醛二乙醇缩醛(B)和
DAP树脂的一种路线如下: 微信搜索“高中试卷君”公众号 领取押题卷联考卷
已知几种金属氢氧化物沉淀的pH如下表所示:
金属离子
开始沉淀时pH 7.6 4.4 6.8 1.9 7.5
完全沉淀时pH 9.2 6.4 8.4 3.2 9.5
请回答下列问题:
(1)已知CoP的晶胞类型与ZnS相似,结构如图-1所示。P原子所连Co原子构成正四面体,P原子处于正四
已知醇与酯可发生如下的酯交换反应:RCOOR′+R″OH RCOOR″+R′OH(R、R'、R″代表烃基)
面体的体心。如图-2为如图-1的俯视图,请在如图-2中用○画出P原子的位置_______。
回答下列问题:
(1)已知A的结构简式为 ,在制备A的过程中最容易生成的另一种副产物为___________(写
结构简式)。
(2)设计丙烯醛→A和C→D步骤的目的为___________。
(3)已知3-氯丙醛二乙醇缩醛(B)的核磁共振氢谱有5组峰,则其结构简式为___________。
(2)若氧化剂M为氧气,则其反应的离子方程式为_______;调节 的目的是_______。 (4)已知E的苯环上的一氯代物有两种,则E的名称为___________;E→F的反应类型为___________。
(5)DAP单体中含两个碳碳双键,则由D和F制备DAP单体的化学方程式为___________。
(3)“萃取”目的是除去镍离子;M代表被萃取的离子,萃取金属离子的原理简化如下: (水层)
(6)满足下列条件的F的同分异构体M有___________种(不包含立体异构)。
(有机层) ((有机层) (水层),影响萃取率的因素有很多,在其他条件相同时,
i.苯环上有三个取代基,且只含有一种官能团
根据如图-3分析分离镍、钴的最佳条件:相比(油相O∶水相A)=_______;根据如图-4分析,在一定范围内
ii.除苯环外无其他环状结构
随着pH升高,金属离子萃取率升高的原因是_______。
iii.1molM最多能消耗4molNaOH
(7)结合上述流程,以乙烯为原料制备 的合成路线为(无机试剂任选)______。
(4)“灼烧”过程中发生反应的化学方程式为_______。
(5)为测定粗产品中 的含量,称取10 g粗产品配成100 mL溶液,从中取出25 mL先加入含0.03 mol的
第59页 第510页
学科网(北京)股份有限公司………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
此
卷
只
装
订
不
密
封
第67页 第68页