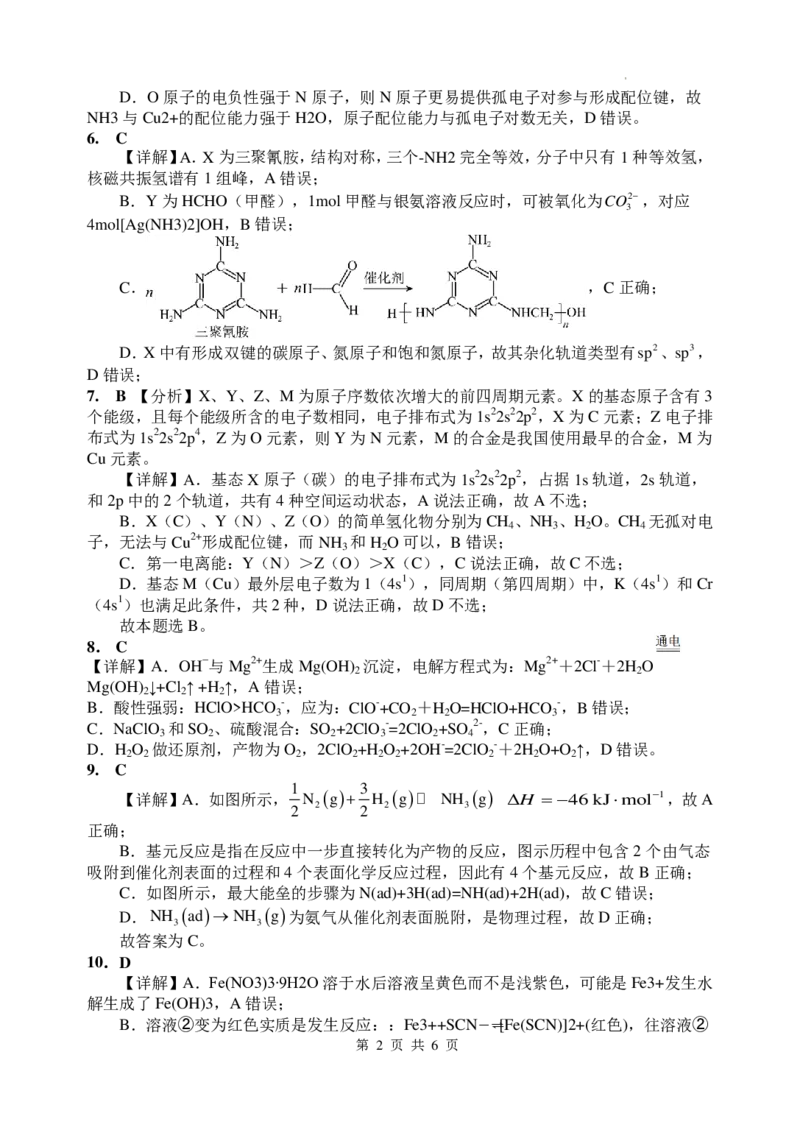
文档内容
广西2026届高三年级秋季学期11月阶段性联合测试
化 学 参 考 答 案
一、选择题:
1.D
【解析】A.碳陶瓷属于新型无机非金属材料,传统无机非金属材料主要指硅酸盐材
料(如陶瓷、玻璃),A错误;
B.芯片材料主要成分为晶体硅,光导纤维为二氧化硅,二者不同,B错误;
C.石墨烯与金刚石均为碳元素组成的单质,互为同素异形体,C错误;
D.聚酰亚胺是聚合物,属于有机高分子材料,D正确;
2.C
【详解】A.滴定管能精确到两位小数,量取10.00mLK2Cr2O7溶液,要选择酸式滴
定管,实验装置正确,A正确;
B.油和水是互不相溶液体,可用分液的方式分离,B正确;
C.给坩埚加热时不需要使用石棉网或陶土网,需在泥三角上加热,C错误;
D.制备乙酸乙酯,导管末端不伸入液面下,利用饱和碳酸钠收集乙酸乙酯,D正确。
3.C
【详解】A.在标准状态下,溴单质呈液态,不能用气体摩尔体积数据来计算,A错
误;
B.0.1 mol/L的 Na2CO3溶液的体积未知,无法求出CO2−、HCO−、H CO 的微
3 3 2 3
粒总数,B错误;
C.每消耗3mol Br2,其中有0.5mol Br2被氧化成NaBrO3,有2.5mol Br2被还原成
NaBr,整个过程中转移电子的物质的量为5mol,数目约为5N ,C正确;
A
D.在1L0.1mol⋅L−1NaBrO 溶液中除NaBrO 含O原子外,还有作为溶剂的H O分子
3 3 2
中也含O原子,则含有的氧原子数远大于0.3N ,D错误;
A
故答案为C。
4. D
【详解】A.在羟胺分子中,1个N原子与2个H原子、1个O原子形成三个共价键
后,还剩余1对孤对电子,所以羟胺的电子式为 ,A错误;
选项中为氨分子的球棍模型,不是空间填充模型,B错误;
C.由已知液氨可以微弱的电离,故应使用可逆符号,C错误;
D.CO(NH2)2的结构简式为: ,D正确。
5. B
【详解】A.电负性O>N>H,则NH2OH中N原子的电子云密度小于NH3中N原子,
故碱性NH2OH HCO -,应为:ClO-+CO +H O=HClO+HCO -,B错误;
3 2 2 3
C.NaClO 和SO 、硫酸混合:SO +2ClO -=2ClO +SO 2-,C正确;
3 2 2 3 2 4
D.H O 做还原剂,产物为O ,2ClO +H O +2OH-=2ClO -+2H O+O ↑,D错误。
2 2 2 2 2 2 2 2 2
9. C
1 3
【详解】A.如图所示, N (g)+ H (g)� NH (g) ΔH = −46kJ⋅mol−1,故A
2 2 2 2 3
正确;
B.基元反应是指在反应中一步直接转化为产物的反应,图示历程中包含2个由气态
吸附到催化剂表面的过程和4个表面化学反应过程,因此有4个基元反应,故B正确;
C.如图所示,最大能垒的步骤为N(ad)+3H(ad)=NH(ad)+2H(ad),故C错误;
D.NH (ad)→NH (g)为氨气从催化剂表面脱附,是物理过程,故D正确;
3 3
故答案为C。
10.D
【详解】A.Fe(NO3)3∙9H2O溶于水后溶液呈黄色而不是浅紫色,可能是Fe3+发生水
解生成了Fe(OH)3,A错误;
B.溶液②变为红色实质是发生反应::Fe3++SCN−⇌[Fe(SCN)]2+(红色),往溶液②
第 2 页 共 6 页
学科网(北京)股份有限公司加入少量KNO3固体,平衡不移动,溶液颜色不变,B错误;
C.②、③溶液中,均存在平衡Fe3++SCN−⇌[Fe(SCN)]2+,由于温度不变,故该反应
的平衡常数不变,③溶液中生成[FeF6]3-使溶液变为无色,导致③溶液中SCN−浓度大于②,
所以②溶液中Fe3+浓度更大,即c
( Fe3+)
:②>③,C错误;
D.为了观察到浅紫色,需要除去红褐色,即抑制铁离子的水解,所以可向溶液中加
稀硝酸,D正确。
11.B
【详解】A.该电池负极是金属锂,锂是较活泼金属,乙醇会与锂反应生成氢气,不
能用乙醇代替有机电解质,A错误;
B.由电极反应可知,Li电极为负极,石墨烯电极为正极,放电时,Li+移向正极,B
正确;
C.放电时总反应中CO 被还原生成C,C是还原产物而非氧化产物,C错误;
2
D.由题意可知,充电时阳极电极反应为2Li CO +C−4e− =3CO +4Li+,理论上充电时
2 3 2
每转移4mol电子,阳极消耗2mol Li2CO3和1mol C,质量减少2×74g+12g=160g,D错误。
12.D
【解析】A.由晶胞结构可知,Ti位于顶点,周围等距且最近的O位于面心,每个Ti周
围等距且最近的O有12个,故A正确;
B.根据图中已知的两个Ti的坐标(0,0,0)和(1,1,1),A点O在左侧面心位置,分数
坐标为
0 ,
1
,
1
,故B正确;
2 2 1 1
C.根据晶胞结构示意图,晶胞中Fe个数为1,O个数为6 × =3,Ti的个数为8× =1,
2 8
152
晶胞的质量为 g,晶胞的体积为( a×10−7)3 cm3,晶体的密度为
N
A
152 1.52×1023
g/cm3 = g/cm3 ,C正确;
N A ( a×10−7)3 N A a3
1 3
D.Fe和Ti之间的距离为体对角线的 ,即为 anm,Fe和O之间的距离为棱长的一半,
2 2
1
即为 a nm,则两者的比值为 ,故D错误。
2 3:1
13.C
【详解】A.随着温度的升高,反应①正向移动,CO含量增大,反应②逆向移动,甲
烷含量减小,所以曲线c表示的物质为CO;Y点时,曲线b表示的物质体积分数为0,所
以曲线b表示的物质为CH ,曲线a表示的物质为CO ,A错误;
4 2
B.Y点没有CH ,且CO 、CO含量相等,投料n(CO ):n(H )=1:1,则此时反应①
4 2 2 2
平衡时CO 、H 、CO、H O的物质的量相等,所以CO 转化率为50%,B错误;
2 2 2 2
C.若起始按n(CO ):n(H )=1:2投料,反应①、②平衡均向右移动,CO和CH 体
2 2 4
积分数均增大,则曲线交点X应向d点方向移动,C正确;
D.500℃时,容器中v (H )为反应①、②总消耗量,而v逆(CO)仅为反应①消耗量,
正 2
所以当容器中v (H )=v (CO)时,不能说明反应①达到平衡状态,D错误。
正 2 逆
14.C
【详解】A.CO2-的水解以第一步为主,水解方程式为CO2-+H O� HCO-+OH-,根
3 3 2 3
第 3 页 共 6 页
学科网(北京)股份有限公司c(H+)⋅c(CO2-)
据图1可知pH=10.25时,c(CO2-)=c(HCO-),故K = 3 =c(H+)=10−10.25,
3 3 a2 c(HCO-)
3
K 10−14
常温下CO2-的水解常数K = w = =10−3.75,A正确;
3 h K 10−10.25
a2
B.由图1可知,在pH为8~12范围内,CO2-的物质的量分数逐渐增大。由Ksp(MgCO )=
3 3
c(Mg2+)×c(CO2-)可知lg[Ksp(MgCO )]=lg[c(Mg2+)]+lg[c(CO2-)],故lg[c(Mg2+)]=
3 3 3
lg[Ksp(MgCO )]-lg[c(CO2-)],lg[c(CO2-)]逐渐增大,则lg[c(Mg2+)]逐渐减小,且二者之和
3 3 3
为常数。同理,对于Mg(OH) 沉淀,lg[c(Mg2+)]= lg[Ksp{Mg(OH) }]-2lg[c(OH-)]=
2 2
lg[Ksp{Mg(OH) }]-2[-14-lgc(H+)],故lg[c(Mg2+)]~lgc(H+)曲线是一条关于pH的一次函
2
数曲线。故曲线Ⅱ代表MgCO 的溶解平衡曲线,曲线Ⅰ代表Mg(OH) 的溶解平衡曲线,B
3 2
正确;
C.当pH=9、lgc ( Mg2+) =-2时,图2中(9,−2)位于曲线Ⅰ的下方、曲线II的上方,属
于MgCO 的过饱和溶液,生成MgCO 沉淀,导致溶液中含碳微粒总浓度小于0.1mol/L,
3 3
C错误;
D.NaHCO 溶液pH较低,OH-浓度小,可减少Mg(OH) 生成,更利于MgCO 沉淀,
3 2 3
D正确。
二、非选择题
15.(1)3d54s1 (2)适当升温、搅拌、增大盐酸的浓度(任写一条)
(3)10-5.9 mol/L ;Mg2+(1分) (4)3:2
(5)2BaCrO +2H+ +2SO2− =2BaSO +CrO2−+H O
4 4 4 2 7 2
2
(6)共价(1分) ; c
4
【分析】
高铝铬铁矿(主要含CrO ,还含Al O 、Fe O 、MgO、SiO )加稀盐酸进行酸浸,
2 3 2 3 2 3 2
CrO 、Al O 、Fe O 、MgO转化为盐酸盐溶液,SiO 不溶于盐酸,过滤除去,滤渣1为
2 3 2 3 2 3 2
SiO ;滤液加氨水调pH=6将铁离子、铝离子、铬离子转化为氢氧化物,过滤得到含氢氧
2
化铁、氢氧化铝、氢氧化铬的滤渣,进行碱浸、过滤得到含[Al(OH) ]- 、[Cr(OH) ]-的溶液,
4 4
向溶液中加H O 、BaCl 沉铬得到BaCrO 沉淀,加硫酸发生沉淀转化、系列操作得到产
2 2 2 4
品。
【详解】
(1)提高酸浸取率除粉碎矿石外还可以适当升温、搅拌、增大盐酸的浓度。
(2)基态 Cr的价层电子排布式为3d54s1;
24
(3)根据已知③,Ksp[Fe(OH) ]=10-5×(10-10.8)3 =1×10-37.4;当Al3+开始沉淀,此时pH=3.5
3
则c(OH-)=10-10.5mol/L,
c(Fe3+)=(1×10-37.4)/(10-10.5)3=10-5.9 mol/L;由分析可知滤液1中含量最高的金属阳离子是
Mg2+
(4)氧化剂:H O →H O~2e-;还原剂:Cr(OH) − →CrO2−~3e-;则根据氧化还原反
2 2 2 4 4
应中得失电子守恒,氧化剂和还原剂的物质的量之比为3:2
(5)“沉淀转化”后溶液呈橙色,该“沉淀转化”的离子方程式为
2BaCrO +2H+ +2SO2− =2BaSO + CrO2−+H O;
4 4 4 2 7 2
(6)①硼化铬化学稳定性好,耐高温,耐磨,可作抗高温氧化涂层,抗冲击能力强,则
第 4 页 共 6 页
学科网(北京)股份有限公司CrB属于共价晶体。
2
②硼化铬(CrB)晶胞中,设晶胞棱长为c nm,设Cr原子半径为r nm,则4r= 2c nm,r= c
4
2
nm,所以Cr原子的半径为 c nm。
4
16.【答案】(1)④①③② (2)饱和NaHS溶液
(3)500mL容量瓶 胶头滴管 (4) H S+2NH +NiCl =NiS↓+2NH Cl
2 3 2 4
(5)防止倒吸 (6)b(1分) (7)91%(0.91) (8)AB
【分析】由装置图可以知道,整个装置通入氮气使反应都处在氮气氛围下,防止产物被氧
气氧化,装置Ⅰ是浓盐酸和FeS反应生成H S气体和FeCl ,然后经过装置Ⅱ除去HCl杂质
2 2
气体,最后H S进入装置Ⅲ 和NiCl、NH 反应生成NiS,装置Ⅳ吸收多余H S、NH ,
2 2 3 2 3
通过浮子缓冲气流,防止倒吸。
【详解】(1)检查装置气密性并加入药品。打开K 、K ,关闭K 、K ,并通入N ;一
1 4 2 3 2
段时间后,关闭K 并打开a活塞加入浓盐酸,同时打开K ,通入NH ,观察Ⅲ中产生浑
1 2 3
浊,继续反应一段时间。所以实验操作顺序为:④①③②;
(2)由分析可知,浓盐酸具有挥发性,装置Ⅱ除去H S中的HCl杂质气体,其中适宜的
2
试剂可以为饱和NaHS溶液,可以将HCl气体转化为H S气体;
2
(3)配制500mLNiCl 和NH Cl混合溶液时,需要用到的玻璃仪器有:烧杯、量筒、玻璃
2 4
棒、500 mL容量瓶,定容时还需要胶头滴管;
(4)根据分析,装置Ⅲ中H S、NiCl、NH 反应生成NiS沉淀,化学方程式为:
2 2 3
H S+2NH +NiCl =NiS↓+2NH Cl;
2 3 2 4
(5)根据分析,装置Ⅳ吸收多余H S、NH ,通过浮子缓冲气流,防止倒吸。
2 3
(6)如图可知,装置甲是抽滤装置,装置乙是洗涤沉淀的装置,b口导管与装置Ⅲ中液体
相连通,故b口接甲抽滤装置,c口接乙洗涤沉淀装置;
(7)已知滴定反应:Ni2++EDTA=EDTA-Ni2+,Cu2++EDTA=EDTA-Cu2+,并且过量的EDTA
溶液可以被Cu2+滴定来计算用量,所以过量的n(EDTA)=n(Cu2+)=0.1mol/L×10×10-3L
=1×10-3mol,n(Ni2+)=n(EDTA) - n(过量EDTA)=(30-10)×10-3×0.1mol=2×10-3mol,则该镍样
品纯度为: 250mL
2×10−3mol×91g/mol×
20mL
×100%=91%
2.5g
(8)A.在配制CuSO 溶液时,容量瓶中液面超过刻度线,会使溶液体积偏大,配制溶液
4
的浓度偏低,会使滴定过程中消耗的CuSO 溶液体积偏高,导致测定结果偏低,A正确;
4
B.滴定管水洗后未用CuSO 溶液润洗,会导致CuSO 溶液浓度偏低,会使滴定过程中消
4 4
耗的CuSO 溶液体积偏高,导致测定结果偏低,B正确;
4
C.滴定过程中,待测液有可能会溅到锥形瓶内壁,滴定近终点时,为了使结果更精确,
可用洗瓶冲洗锥形瓶内壁,对测定结果无影响,C不符合题意;
D.若滴定前滴定管尖嘴处无气泡,滴定后有气泡,测得消耗CuSO 溶液体积偏小,导致
4
测定结果偏高,D不符合题意。
17.【答案】(1) -49.5 低温 (2)AB
(3)①该条件下,主反应的反应速率大于副反应的反应速率(或答主反应的活化能小于
副反应的活化能),单位时间内生成甲醇的量比生成一氧化碳的量多
② 0.33
第 5 页 共 6 页
学科网(北京)股份有限公司4
(4) H 2 O+CH 3 OH-4e-=HCOOH+4H+ 3
【详解】(1)反应焓变等于生成物能量总和减去反应物能量总和,则
ΔH =[(-200.5)+(-242)-(-393)] kJ/mol=-49.5 kJ/mol,ΔG=ΔH-TΔS<0的反应能自发进行,反
1
应Ⅰ为放热的熵减反应,在低温下能自发进行;
(2)A.H O与CH OH均为极性分子且能形成分子间氢键,等物质的量的H O中氢键比
2 3 2
甲醇多;CO 与H 均为非极性分子,CO 相对分子质量较大,范德华力较大,故A正确;
2 2 2
B.反应Ⅱ的ΔH =+41.0 kJ/mol,ΔH等于正反应活化能减去逆反应活化能,则活化能:
2
E (正)>E (逆),B正确;
a a
CO
C.体系达平衡后,若压缩体积,相当于增大压强,反应Ⅰ平衡正向移动,会使反应Ⅰ中 2
H H O
和 2量减小, 2 量增大,反应Ⅱ的化学平衡逆向移动,故C错误;
D.加入反应Ⅰ的催化剂,反应Ⅰ的平衡不会发生移动,不可提高平衡时甲醇的产率,故 D
错误;
(3)①该条件下,主反应的反应速率大于副反应的反应速率,单位时间内生成甲醇的量
比生成一氧化碳的量多,所以温度相同时CH OH的选择性的实验值略高于平衡值。
3
②260℃时,CO 的平衡转化率为25%,CH OH的选择性的平衡值为50%,CO 和H 的初
2 3 2 2
始 浓度 均为 1.00 mol·L-1, 可 以 得出各 物质 浓度 分别是 c(CO )=0.75mol/L;
2
c(CO)=c(CH OH)=0.125mol/L ; c(H O)=0.125mol/L+0.125mol/L=0.25mol/L ;
3 2
c(H )=1mol/L-0.125mol/L×3-0.125mol/L=0.5mol/L ; 反 应Ⅰ 的 平 衡 常 数 K=
2
c(H O)×c(CH OH) 0.25×0.125
2 3 = =0.33
c(CO )×c3(H ) 0.75×0.53
2 2 。
(4)阳极发生氧化反应,甲醇在CuONS/CF电极上被氧化为甲酸。根据元素守恒和电荷
CH OH+H O-4e-=HCOOH+4H+
守恒,电极反应式为 3 2 。
电解
2CO +CH OH+H O 3HCOOH
总反应为 2 3 2 ,电路中转移4 mol电子时,生成3 mol HCOOH,
4
则制备1mol HCOOH,在电路中转移3mol电子。
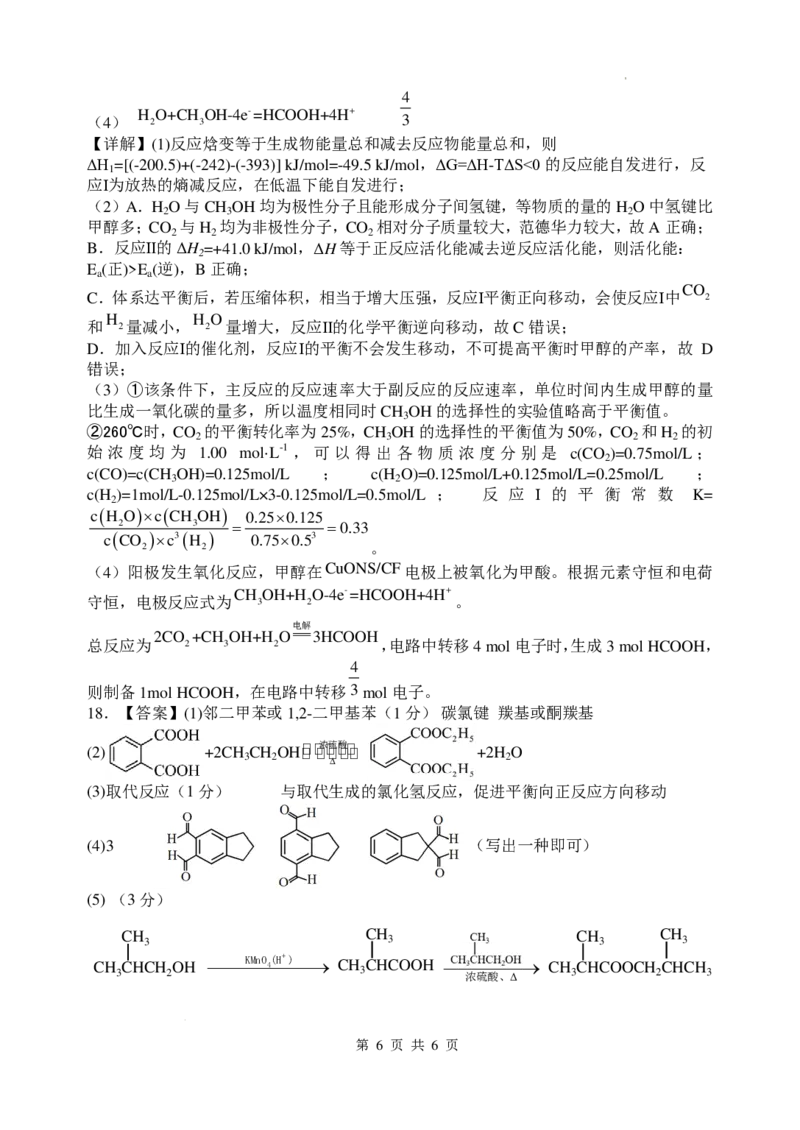
18.【答案】(1)邻二甲苯或1,2-二甲基苯(1分) 碳氯键 羰基或酮羰基
(2) +2CH CH OH���� 浓�硫 � 酸���� +2H O
3 2 ∆ 2
(3)取代反应(1分) 与取代生成的氯化氢反应,促进平衡向正反应方向移动
(4)3 (写出一种即可)
(5) (3分)
CH 3 CH 3 CH 3 CH 3
CH 3 CHCH 2 OH KMnO4 (H+ ) → CH 3 CHCOOH C 浓 H 硫 3 C 酸 H 、 2 O Δ H→ CH 3 CHCOOCH 2 CHCH 3
第 6 页 共 6 页
学科网(北京)股份有限公司CH CH CH
3 3 3
或者
CH
3
CHCH
2
OH Cu、
Δ
O 2→ CH
3
CHCHO 催化剂
Δ
、O 2→ CH
3
CHCOOH
CH CH
3 3
CH
3
CH
2
OH→
CH CHCOOCH CHCH
浓硫酸、Δ 3 2 3
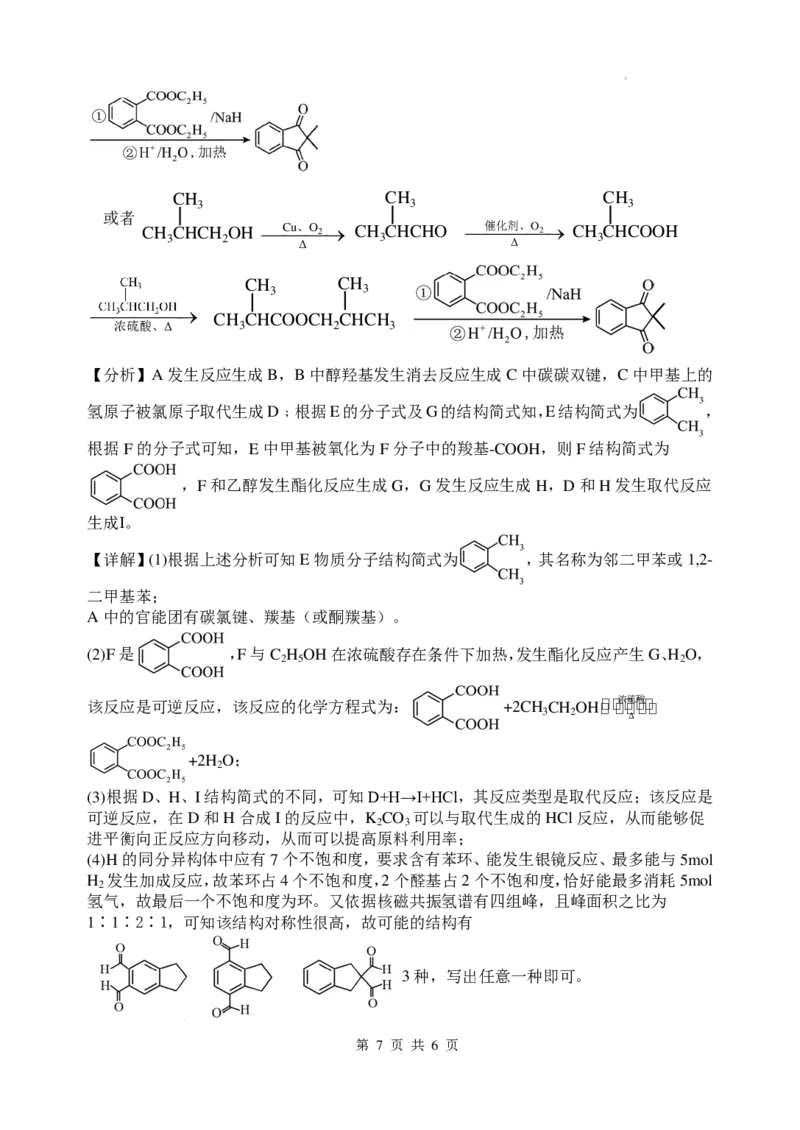
【分析】A发生反应生成B,B中醇羟基发生消去反应生成C中碳碳双键,C中甲基上的
氢原子被氯原子取代生成D﹔根据E的分子式及G的结构简式知,E结构简式为 ,
根据F的分子式可知,E中甲基被氧化为F分子中的羧基-COOH,则F结构简式为
,F和乙醇发生酯化反应生成G,G发生反应生成H,D和H发生取代反应
生成Ⅰ。
【详解】(1)根据上述分析可知E物质分子结构简式为 ,其名称为邻二甲苯或1,2-
二甲基苯;
A中的官能团有碳氯键、羰基(或酮羰基)。
(2)F是 ,F与C H OH在浓硫酸存在条件下加热,发生酯化反应产生G、H O,
2 5 2
该反应是可逆反应,该反应的化学方程式为: +2CH CH OH���� 浓�硫 � 酸����
3 2 ∆
+2H O;
2
(3)根据D、H、I结构简式的不同,可知D+H→I+HCl,其反应类型是取代反应;该反应是
可逆反应,在D和H合成I的反应中,K CO 可以与取代生成的HCl反应,从而能够促
2 3
进平衡向正反应方向移动,从而可以提高原料利用率;
(4)H的同分异构体中应有7个不饱和度,要求含有苯环、能发生银镜反应、最多能与5mol
H 发生加成反应,故苯环占4个不饱和度,2个醛基占2个不饱和度,恰好能最多消耗5mol
2
氢气,故最后一个不饱和度为环。又依据核磁共振氢谱有四组峰,且峰面积之比为
1∶1∶2∶1,可知该结构对称性很高,故可能的结构有
3种,写出任意一种即可。
第 7 页 共 6 页
学科网(北京)股份有限公司CH CH
3 3
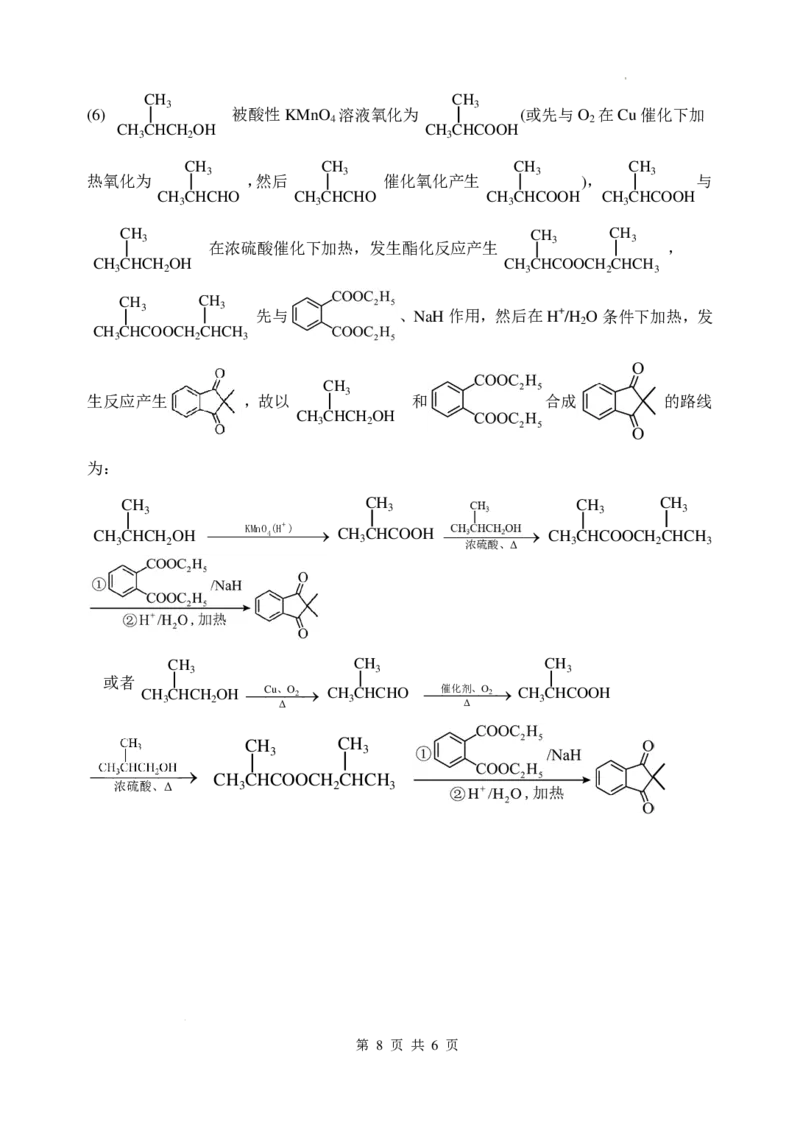
(6) 被酸性KMnO 溶液氧化为 (或先与O 在Cu催化下加
4 2
CH CHCH OH CH CHCOOH
3 2 3
CH CH CH CH
3 3 3 3
热氧化为 ,然后 催化氧化产生 ), 与
CH CHCHO CH CHCHO CH CHCOOH CH CHCOOH
3 3 3 3
CH CH CH
3 3 3
在浓硫酸催化下加热,发生酯化反应产生 ,
CH CHCH OH CH CHCOOCH CHCH
3 2 3 2 3
CH CH
3 3 先与 、NaH作用,然后在H+/H O条件下加热,发
2
CH CHCOOCH CHCH
3 2 3
CH
3
生反应产生 ,故以 和 合成 的路线
CH CHCH OH
3 2
为:
CH 3 CH 3 CH 3 CH 3
CH 3 CHCH 2 OH KMnO4 (H+ ) → CH 3 CHCOOH C 浓 H 硫 3 C 酸 H 、 2 O Δ H→ CH 3 CHCOOCH 2 CHCH 3
CH CH CH
3 3 3
或者
CH
3
CHCH
2
OH Cu、
Δ
O 2→ CH
3
CHCHO 催化剂
Δ
、O2→ CH
3
CHCOOH
CH CH
3 3
CH
3
CH
2
OH→
CH CHCOOCH CHCH
浓硫酸、Δ 3 2 3
第 8 页 共 6 页
学科网(北京)股份有限公司