文档内容
2024 年 6 月高考浙江卷化学试题
一、单选题
1.按物质组成分类, 属于
A.酸 B.碱 C.盐 D.混合物
KAl(SO4)2⋅12H2O
【答案】C
【解析】KAl(SO ) ∙12H O是结晶水合物,属于纯净物;是由金属阳离子K+、Al3+和酸根阴离子 组成的复盐;
4 2 2
故选C。 2-
SO4
2.下列说法不
.
正
.
确
.
的是
A. 呈两性,不能用于治疗胃酸过多
B. 能与 反应产生 ,可作供氧剂
Al(OH)3
C. 有还原性,能被氧化成
Na2O2 CO2 O2
D. 见光易分解,应保存在棕色试剂瓶中
FeO Fe3O4
【答案】A
HNO3
【解析】A. 呈两性,不溶于水,但可以与胃酸反应生成无毒物质,因此其能用于治疗胃酸过多,A错误;
B. 能与 反应产生 ,该反应能安全发生且不生成有毒气体,故 可作供氧剂,B正确;
Al(OH)3
C. 有还原性,其中Fe元素的化合价为+2,用适当的氧化剂可以将其氧化成更高价态的 ,C正确;
Na2O2 CO2 O2 Na2O2
D.见光易分解的物质应保存在棕色试剂瓶中; 见光易分解,故其应保存在棕色试剂瓶中,D正确;
FeO Fe3O4
故选A。
HNO3
3.下列表示不
.
正
.
确
.
的是
A. 的电子式: B. 中共价键的电子云图:
CO2 Cl2
C. 的空间填充模型: D.3,3-二甲基戊烷的键线式:
【答案】
NH
A3
【解析】A. 的电子式: ,A错误;
B.Cl 中的共价键是由2个氯原子各提供1个未成对电子的3p原子轨道重叠形成的,共价键电子云图为: ,
2 CO2
B正确;
C. 的中心原子N形成3个σ键和1个孤电子对,为sp3杂化, 为三角锥形,空间填充模型: ,C正确;
NH3 NH3
D.3,3-二甲基戊烷的主链上有5个C,3号碳上连接有2个甲基,键线式为: ,D正确;
故选A。
4.下列说法不
.
正
.
确
.
的是
A.装置①可用于铜与浓硫酸反应并检验气态产物 B.图②标识表示易燃类物质
C.装置③可用于制取并收集氨气 D.装置④可用于从碘水中萃取碘
【答案】C【解析】A.铜与浓硫酸反应方程式为: + 浓 + + ,可用装置①制取,气态产物为
Δ
SO ,可利用SO 的漂白性进行检验,A正Cu确;2H 2SO4( ) CuSO4 2H2O SO2 ↑
2 2
B.图②标识表示易燃类物质,B正确;
C.NH 的密度比空气小,应用向下排空气法进行收集,C错误;
3
D.萃取是利用物质在不同溶剂中溶解性的差异进行分离混合物,装置④可用于从碘水中萃取碘,D正确;
故选C。
5.化学与人类社会可持续发展息息相关。下列说法不
.
正
.
确
.
的是
A.部分金属可在高温下用焦炭、一氧化碳、氢气等还原金属矿物得到
B.煤的气化是通过物理变化将煤转化为可燃性气体的过程
C.制作水果罐头时加入抗氧化剂维生素C,可延长保质期
D.加入混凝剂聚合氯化铝,可使污水中细小悬浮物聚集成大颗粒
【答案】B
【解析】A.根据金属活泼性的不同,可以采用不同的方法冶炼金属,大部分金属(主要是中等活泼的金属)的冶
炼是通过高温下发生氧化还原反应来完成的,即热还原法,常用的还原剂有焦炭、CO、H 等,A正确;
2
高温
B.煤的气化是将煤转化为可燃性气体的过程,主要发生的反应为C+H O(g) CO+H ,该过程属于化学变化,B
2 2
错误;
C.维生素C(即抗坏血酸)具有还原性,能被氧化成脱氢抗坏血酸,故制作水果罐头时加入维生素C作抗氧化剂,
可延长保质期,C正确;
D.混凝剂聚合氯化铝在污水中能水解成Al(OH) 胶体,Al(OH) 胶体能吸附污水中细小悬浮物,使其聚集成较大颗
3 3
粒而沉降下来,D正确;
故选B。
6.利用 可将废水中的 转化为对环境无害的物质后排放。反应原理为: (未
配平)。下列说法正确的是 - + -
CH3OH NO3 H +CH3OH+NO3 →X+CO2+H2O
A.X表示
B.可用 替换
NO2
C.氧化剂与还原剂物质的量之比为
O3 CH3OH
D.若生成标准状况下的 气体 ,则反应转移的电子数为 ( 表示阿伏加德罗常数的值)
6:5
【答案】C
CO2 11.2L 2NA NA
【解析】A.利用 可将废水中的 转化为对环境无害的物质X后排放,则X表示 , 仍然是大气污染
物,A错误; -
CH3OH NO3 N2 NO2
B. 中C元素的化合价由-2价升高到+4价, 是该反应的还原剂, 有强氧化性,通常不能用作还原
剂,故不可用 替换 ,B错误;
CH3OH CH3OH O3
C.该反应中,还原剂 中C元素的化合价由-2价升高到+4价,升高了6个价位,氧化剂 中N元素的化合
O3 CH3OH
价由+5价降低到0价,降低了5个价位,由电子转移守恒可知,氧化剂与还原剂的物质的量之比-为 ,C正确;
CH3OH NO3
D. 中C元素的化合价由-2价升高到+4价,升高了6个价位,若生成标准状况下的 气体 ,即生成
6:5
0.5mol ,反应转移的电子数为0.5×6= ,D错误;
CH3OH CO2 11.2L
故选C。
CO2 3NA
7.物质微观结构决定宏观性质,进而影响用途。下列结构或性质不
.
能
.
解
.
释
.
其用途的是
选
结构或性质 用途
项
A 石墨呈层状结构,层间以范德华力结合 石墨可用作润滑剂
B 具有氧化性 可用作漂白剂
SO2 SO2C 聚丙烯酸钠可用于制备高吸水性树脂
聚丙烯酸钠( )中含有亲水基团
冠醚18-冠-6空腔直径( )与 直径 冠醚18-冠-6可识别 ,能增大 在有机溶剂中
D
( )接近 + 的溶解度 +
260~320pm K K KMnO4
A.A27
6pm
B.B C.C D.D
【答案】B
【解析】A. 石墨呈层状结构,层间以范德华力结合,该作用力较小,层与层容易滑动,石墨可用作润滑剂,A正
确;
B. 具有漂白性,可用作漂白剂,B错误;
SO2
C. 聚丙烯酸钠( )中含有亲水基团-COO-,聚丙烯酸钠可用于制备高吸水性树脂,C正确;
D. 冠醚18-冠-6空腔直径( )与 直径( )接近,可识别 ,使K+存在于其空腔中,进而能增大
在有机溶剂中的溶解度,D正确; + +
260~320pm K 276pm K
故选B。
KMnO4
8.下列离子方程式正确的是
A.用 溶液除 气体:
B. 溶液中滴加 溶2液+ :2-
CuSO4 H2S Cu +S =CuS↓
C. 溶液中通入少量 : 2+ +
H2SO3 Ba(NO3)2 H2SO3+Ba =BaSO3 ↓+2H
D.用 溶液刻蚀覆铜板制作印刷电-路板: - -
NaHCO3 Cl2 2HCO3+Cl2 =2CO2+Cl+ClO+H2O
【答案】D 3+ 2+ 2+
FeCl3 2Fe +Cu=2Fe +Cu
【解析】A.H S在离子方程式中应以化学式保留,正确的离子方程式为Cu2++H S=CuS↓+2H+,A错误;
2 2
B.酸性条件下 会将H SO 氧化成H SO ,Ba2+与 形成BaSO 沉淀,滴加少量Ba(NO ) 时的离子方程式为
2 3 2 4 4 3 2
Ba2++2 +3H SO-=BaSO ↓+2NO↑+2 +4H++H O,滴2加- 足量Ba(NO ) 时的离子方程式为
2 NO33 4 2 SO4 3 2
3Ba2++2 - +3H SO =3BaSO ↓+2NO↑+4H2-++H O,B错误;
NO3 2 3 4 SO4 2
C.电离平衡- 常数:K (H CO ) >K (HClO) >K (H CO ),Cl 与水反应生成的HClO与NaHCO 不反应,正确的
NO3 a1 2 3 a a2 2 3 2 3
离子方程式为Cl + =Cl-+HClO+CO ,C错误;
2 2
D.Cu与FeCl 溶液反应- 生成CuCl 、FeCl ,反应的离子方程式为Cu+2Fe3+=Cu2++2Fe2+,D正确;
3 HCO3 2 2
故选D。
9.有机物A经元素分析仪测得只含碳、氢、氧3种元素,红外光谱显示A分子中没有醚键,质谱和核磁共振氢谱
示意图如下。下列关于A的说法正确的是
A.能发生水解反应 B.能与 溶液反应生成
C.能与 反应生成丙酮 D.能与 反应生成
NaHCO3 CO2
【答案】D
O2 Na H2
【分析】根据质谱图可知,有机物A相对分子质量为60,A只含C、H、O三种元素,因此A的分子式为C H O
3 8
或C H O ,由核磁共振氢谱可知,A有4种等效氢,个数比等于峰面积之比为3:2:2:1,因此A为CH CH CH OH。
2 4 2 3 2 2
【解析】A.A为CH CH CH OH,不能发生水解反应,A错误;
3 2 2B.A中官能团为羟基,不能与 溶液反应生成 ,B错误;
C.CH CH CH OH的羟基位于末端C上,与 反应生成丙醛,无法生成丙酮,C错误;
3 2 2 NaHCO3 CO2
D.CH CH CH OH中含有羟基,能与Na反应生成H ,D正确;
3 2 2 O2 2
故选D。
10.X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同主族,Y与Z核电荷
数相差2,Z的原子最外层电子数是内层电子数的3倍。下列说法不
.
正
.
确
.
的是
A.键角: B.分子的极性:
C.共价晶体熔+点:- D.热稳定性:
YX3>YX3 Y2X2>X2Z2
【答案】B
Y>M YX4>MX4
【分析】X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Y与M同主族,Y与Z核
电荷数相差2,Z的原子最外层电子数是内层电子数的3倍,则Z为O元素,Y为C元素,X为H元素,M为Si
元素。
【解析】A. 为 ,其中C原子的杂化类型为 , 的空间构型为平面正三角形,键角为120°; 为 ,
其中C原子的杂+化类型+ 为 , 的空间构型为三角2锥形+,由于C原子还有1个孤电子对,故键角小于-109°2-8´,
YX3 CH3 sp CH3 YX3 CH3
因此,键角的大小关系为 3 -,A正确;
sp CH3
B. 为 ,其为直线形+分子-,分子结构对称,分子中正负电荷的重心是重合的,故其为百极性分子; 分
YX3>YX3
子结构不对称,分子中正负电荷的重心是不重合的,故其为极性分子,因此,两者极性的大小关系为 ,
Y2X2 C2H2 H2O2
B错误;
Y2X20
向容积为 的密闭容器中投入 和 ,不同温度下,测得 时(反应均未平衡)的相关数据见下表,
C2H6(g)+2CO2(g)⇌4CO(g)+3H2(g) ΔH2>0
下列说法不
1 . 0
正
L .
确
.
的是
2mol C2H6 3mol CO2 5min
温度( ) 400 500 600
乙烷转°C化率( ) 2.2 9.0 17.8
乙烯选择性(%) 92.6 80.0 61.8
% 转化为乙烯的乙烷的物质的量
注:乙烯选择性
转化的乙烷的总物质的量
A.反应活化=能: Ⅱ ×100%
B. 时, 反应I的平均速率为:
I<
C.其他条件不变,平衡后及时移除 ,可提高乙烯的产率 -3 -1 -1
500℃ 0~5𝑚𝑚𝑚𝑚𝑚𝑚 v(C2H4)=2.88×10 mol⋅L ⋅min
D.其他条件不变,增大投料比 投料,平衡后可提高乙烷转化率
H2O(g)
【答案】D
[n(C2H6)/n(CO2)]
【解析】A.相同温度下,乙烷在发生转化时,反应Ⅰ更易发生,则反应活化能:Ⅰ<Ⅱ,A正确;
B.500℃时,乙烷的转化率为9.0%,可得转化的乙烷的总物质的量为2mol×9.0%=0.18mol,而此温度下乙烯的选
择性为80%,则转化为乙烯的乙烷的物质的量为0.18mol×80%=0.144mol,根据方程式可得,生成乙烯的物质的量
为0.144mol,则 反应I的平均速率为: ,B正确;
0.144mol
10L -3 -1 -1
C.其他条件不变 0~ , 5 平 𝑚𝑚 衡 𝑚𝑚𝑚𝑚 后及时移除 ,反 v 应 (CⅠ2正 H4向 )= 进行 5m , in 可 = 提 2.8 高 8 乙 × 烯 10 的 m 产 o 率 l⋅ , LC⋅ 正 m 确 in ;
D.其他条件不变,增大投料比 投料,平衡后CO 转化率提高,C H 转化率降低,D错误;
H2O(g) 2 2 6
故选D。
[n(C2H6)/n(CO2)]
12.丙烯可发生如下转化(反应条件略):下列说法不
.
正
.
确
.
的是
A.产物M有2种且互为同分异构体(不考虑立体异构)
B. 可提高Y→Z转化的反应速率
C.Y+→Z过程中,a处碳氧键比b处更易断裂
H
D.Y→P是缩聚反应,该工艺有利于减轻温室效应
【答案】D
【分析】
丙烯与HOCl发生加成反应得到M,M有CH -CHCl-CH OH和CH -CHOH-CH Cl两种可能的结构,在Ca(OH) 环
3 2 3 2 2
境下脱去HCl生成物质Y( ),Y在H+环境水解引入羟基再脱H+得到主产物Z;Y与CO 可发生反应得到
2
物质P( )。
【解析】A. 据分析,产物M有2种且互为同分异构体(不考虑立体异构),A正确;
B. 据分析, 促进Y中醚键的水解,后又脱离,使Z成为主产物,故其可提高Y→Z转化的反应速率,B正确;
+
H
C.从题干 部分可看出,是a处碳氧键断裂,故a处碳氧键比b处更易断裂,C正确;
D. Y→P是CO 与Y发生加聚反应,没有小分子生成,不是缩聚反应,该工艺有利于消耗CO ,减轻温室效应,
2 2
D错误;
故选D。
13.金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关。下图为两种对海水中钢闸门的防腐措
施示意图:
下列说法正确的是
A.图1、图2中,阳极材料本身均失去电子
B.图2中,外加电压偏高时,钢闸门表面可发生反应:
C.图2中,外加电压保持恒定不变,有利于提高对钢闸门的防-护效果 -
O2+4e+2H2O=4OH
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
【答案】B【解析】A.图1为牺牲阳极的阴极瓮中保护法,牺牲阳极一般为较活泼金属,其作为原电池的负极,其失去电子
被氧化;图2为外加电流的阴极保护法,阳极材料为辅助阳极,其通常是惰性电极,其本身不失去电子,电解质溶
液中的阴离子在其表面失去电子,如海水中的 ,A错误;
B.图2中,外加电压偏高时,钢闸门表面积累的−电子很多,除了海水中的 放电外,海水中溶解的 也会竞争放
Cl
电,故可发生 ,B正确; +
H O2
C.图2为外加电流的- 阴极保护法,-理论上只要能对抗钢闸门表面的腐蚀电流即可,当钢闸门表面的腐蚀电流为零
O2+4e+2H2O=4OH
时保护效果最好;腐蚀电流会随着环境的变化而变化,若外加电压保持恒定不变,则不能保证抵消腐蚀电流,不利
于提高对钢闸门的防护效果,C错误;
D.图1、图2中,当钢闸门表面的腐蚀电流为零时,说明从牺牲阳极或外加电源传递过来的电子阻止了
的发生,钢闸门不发生化学反应,但是牺牲阳极和发生了氧化反应,辅助阳极上也发生了氧化反应,D错误-; 2+
Fe-2e=Fe
故选B。
14. 中的 原子均通过 杂化轨道成键,与 溶液反应 元素均转化成 。下列说法不
.
正
.
确
.
的是
3
Si5Cl10 Si sp NaOH Si Na2SiO3
A. 分子结构可能是 B. 与水反应可生成一种强酸
C. 与 溶液反应会产生 D. 沸点低于相同结构的
Si5Cl10 Si5Cl10
【答案】A
Si5Cl10 NaOH H2 Si5Cl10 Si5Br10
【详解】A.该结构中,如图 所示的两个Cl,Cl最外层有7个电子,形成了两个共价键,因此其中
1个应为配位键,而Si不具备空轨道来接受孤电子对,因此 结构是错误的,A错误;
B. 与水反应可生成HCl,HCl是一种强酸,B正确;
C. 与 溶液反应 元素均转化成 ,Si的化合价升高,根据得失电子守恒可知,H元素的化合价
Si5Cl10
降低,会有H 生成,C正确;
Si5Cl10 N 2 aOH Si Na2SiO3
D. 的相对分子质量大于 ,因此 的范德华力更大,沸点更高,D正确;
故选A。
Si5Br10 Si5Cl10 Si5Br10
15.室温下, 水溶液中各含硫微粒物质的量分数 随 变化关系如下图[例如 ]。已知:
c(H2S)
H2S δ pH δ(H2S)=c(H2S)+c(HS - )+c(S 2- )
, 。
-18 -17
𝐾𝐾sp(FeS)=6.3×10 𝐾𝐾sp[Fe(OH)2]=4.9×10
下列说法正确的是
A.溶解度: 大于
B.以酚酞为指示剂(变色的 范围8.2~10.0),用 标准溶液可滴定 水溶液的浓度
FeS Fe(OH)2
C.忽略 的第二步水解, 的 溶液中 水解率约为
pH NaOH H2S
D. 2- 的 溶液中加入等体积 的2- 溶液,反应初始生成的沉淀是
S 0.10mol/L Na2S S 62%
【答案】C
0.010mol/L FeCl2 0.20mol/L Na2S FeS【分析】在H S溶液中存在电离平衡:H S H++HS-、HS- H++S2-,随着pH的增大,H S的物质的量分数逐渐减
2 2 2
⇌ ⇌
小,HS-的物质的量分数先增大后减小,S2-的物质的量分数逐渐增大,图 中线①、②、
③依次代表H S、HS-、S2-的物质的量分数随pH的变化,由①和②交点的pH=7可知K (H S)=1×10-7,由②和③交
2 a1 2
点的pH=13.0可知K (H S)=1×10-13。
a2 2
【解析】A.FeS的溶解平衡为FeS(s) Fe2+(aq)+S2-(aq),饱和FeS溶液物质的量浓度为
= mol/L= ×1⇌0-9mol/L,Fe(OH) 的溶解平衡为Fe(OH) Fe2+(aq)+2OH-(aq),饱和Fe(OH)
2 2 2
−18
�𝐾𝐾sp(FeS) √6.3×10 √6.3 ⇌
溶液物质的量浓度为 = mol/L= ×10-6mol/L> ×10-9mol/L,故溶解度:FeS小于Fe(OH) ,
2
3 𝐾𝐾sp[Fe(OH)2] 3 4.9×10 −17 3
A错误; � 4 � 4 √12.25 √6.3
B.酚酞的变色范围为8.2~10,若以酚酞为指示剂,用NaOH标准溶液滴定H S水溶液,由图可知当酚酞发生明显
2
颜色变化时,反应没有完全,即不能用酚酞作指示剂判断滴定终点,B错误;
C.Na S溶液中存在水解平衡S2-+H O HS-+OH-、HS-+H O H S+OH-(忽略第二步水解),第一步水解平衡常数
2 2 2 2
K (S2-)= = = ⇌= =0.1,设水解⇌的S2-的浓度为x mol/L,则 =0.1,解得x≈0.062,
h
- - - - + −14 2
𝑐𝑐(HS)𝑐𝑐(OH) 𝑐𝑐(HS)𝑐𝑐(OH)𝑐𝑐(H ) 𝐾𝐾w 1×10 x
2- 2- + −13
𝑐𝑐(S ) 𝑐𝑐(S )𝑐𝑐(H ) 𝐾𝐾a2(H2S) 1×10 0.1-x
S2-的水解率约为 ×100%=62%,C正确;
0.062mol/L
D.0.01mol/L FeC0l.1m溶ol液/L中加入等体积0.2mol/L Na S溶液,瞬间得到0.005mol/L FeCl 和0.1mol/L Na S的混合液,
2 2 2 2
结合C项,瞬时c(Fe2+)c(S2-)=0.005mol/L×(0.1mol/L-0.062mol/L)=1.9×10-4>K (FeS),
sp
c(Fe2+)c2(OH-)=0.005mol/L×(0.062mol/L)2=1.922×10-5>K [Fe(OH) ],故反应初始生成的沉淀是FeS和Fe(OH) ,D
sp 2 2
错误;
故选C。
16.为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计和结论都正确的是
选 影响
方案设计 现象 结论
项 因素
向 溶液中加入 黄色溶液 增大反应物浓度,平衡向正反应方
A 浓度
溶液 变橙色 向移动
1mL 0.1mol/L K2CrO4
1向m恒L1温.0恒m容ol/密L 闭HB玻r璃容器中充入 气体,分 气体颜色 对于反应前后气体总体积不变的
B 压强
解达到平衡后再充入 不变 可逆反应,改变压强平衡不移动
100mL HI
100mL Ar 气体颜色 升高温度,平衡向吸热反应方向移
C 温度 将封装有 和 混合气体的烧瓶浸泡在热水中
变深 动
NO2 N2O4
催化 向 乙酸乙酯中加入 溶液, 上层液体 使用合适的催化剂可使平衡向正
D
剂 水浴加热 逐渐减少 反应方向移动
1mL 1mL 0.3mol/L H2SO4
A.A B.B C.C D.D
【答案】C
【解析】A. 黄色 橙色 ,向 溶液中加入 溶
2- + 2-
液,H+浓度增大Cr,O4平�衡正�向+移2H动,⇌实Cr验2O现7象� 应为�+溶H液2O橙色加1深m,L A0.1错m误ol;/L K2CrO4 1mL1.0mol/L HBr
B.反应2HI H +I 为反应前后气体总体积不变的可逆反应,向恒温恒容密闭玻璃容器中充入 气体,分解
2 2
达到平衡后再⇌充入 ,平衡不发生移动,气体颜色不变,应得到的结论是:对于反应前1后00气m体L 总HI体积不变的
可逆反应,恒温恒容时,改变压强平衡不移动,B错误;
100mL ArC.反应 为放热反应,升高温度,气体颜色变深,说明平衡逆向移动,即向吸热反应方向移动,C正
确; 2NO2 ⇌N2O4
D.催化剂只会改变化学反应速率,不影响平衡移动,D错误;
故选C。
二、解答题
17.氧是构建化合物的重要元素。请回答:
(1)某化合物的晶胞如图1, 的配位数(紧邻的阳离子数)为 ;写出该化合物的化学式 ,写出该化合物与
足量 溶液反应的化学方-程式 。
Cl
NH4Cl
(2)下列有关单核微粒的描述正确的是_______。
A. 的基态原子电子排布方式只有一种
B. 的第二电离能 的第一电离能
Ar
C. 的基态原子简化电子排布式为
Na >Ne
D. 原子变成 ,优先失去 轨道上的电2 子2
Ge [Ar]4s 4p
(3)化合物 、 、 +和 的结构如图2。
Fe Fe 3d
HA HB HC HD
① 、 和 中羟基与水均可形成氢键( ),按照氢键由强到弱对三种酸排序 ,请说明理由 。
②已知 、 钠盐的碱性 ,请从结构角度说明理由 。
HA HB HC -O-H…OH2
【答案】(1) 12 K ClO K ClO+2NH Cl+H O=3KCl+2NH ∙H O
3 3 4 2 3 2
HC HD NaC>NaD
(2)AB
(3) HC>HB>HA O、S、Se的电负性逐渐减小,键的极性:C=O>C=S>C=Se,使得HA、HB、HC中羟
基的极性逐渐增大,其中羟基与H O形成的氢键逐渐增强 S的原子半径大于O的原子半径,S—H键的键长大
2
于O—H键,S—H键的键能小于O—H键,同时HC可形成分子间氢键,使得HD比HC更易电离出H+,酸性HD
>HC,C-的水解能力大于D-,碱性NaC>NaD
【详解】(1)根据晶胞结构知,Cl位于8个顶点,O位于体心,K位于面心,1个晶胞中含Cl:8× =1个、含O:
1
8
1个、含K:6× =3个,该化合物的化学式为K ClO;由图可知,Cl-的配位数为 =12;该化合物可看成KCl∙K O,
3 2
1 8×3
故该化合物与足2量NH Cl溶液反应生成KCl和NH ∙H O,反应的化学方程式为2
4 3 2
K ClO+2NH Cl+H O=3KCl+2NH ∙H O。
3 4 2 3 2
(2)A.根据原子核外电子排布规律,基态Ar原子的电子排布方式只有1s22s22p63s23p6一种,A正确;
B.Na的第二电离能指气态基态Na+失去一个电子转化为气态基态正离子所需的最低能量,Na+和Ne具有相同的电
子层结构,Na+的核电荷数大于Ne,Na+的原子核对外层电子的引力大于Ne的,故Na的第二电离能>Ne的第一电
离能,B正确;
C.Ge的原子序数为32,基态Ge原子的简化电子排布式为[Ar]3d104s24p2,C错误;
D.基态Fe原子的价电子排布式为3d64s2,Fe原子变成Fe+,优先失去4s轨道上的电子,D错误;
故选AB。
(3)①O、S、Se的电负性逐渐减小,键的极性:C=O>C=S>C=Se,使得HA、HB、HC中羟基的极性逐渐增大,
从而其中羟基与水形成的氢键由强到弱的顺序为HC>HB>HA;②HC、HD钠盐的碱性NaC>NaD,说明酸性HC<HD,原因是:S的原子半径大于O的原子半径,S—H键的键
长大于O—H键,S—H键的键能小于O—H键,同时HC可形成分子间氢键,使得HD比HC更易电离出H+,酸
性HD>HC,C-的水解能力大于D-,钠盐的碱性NaC>NaD。
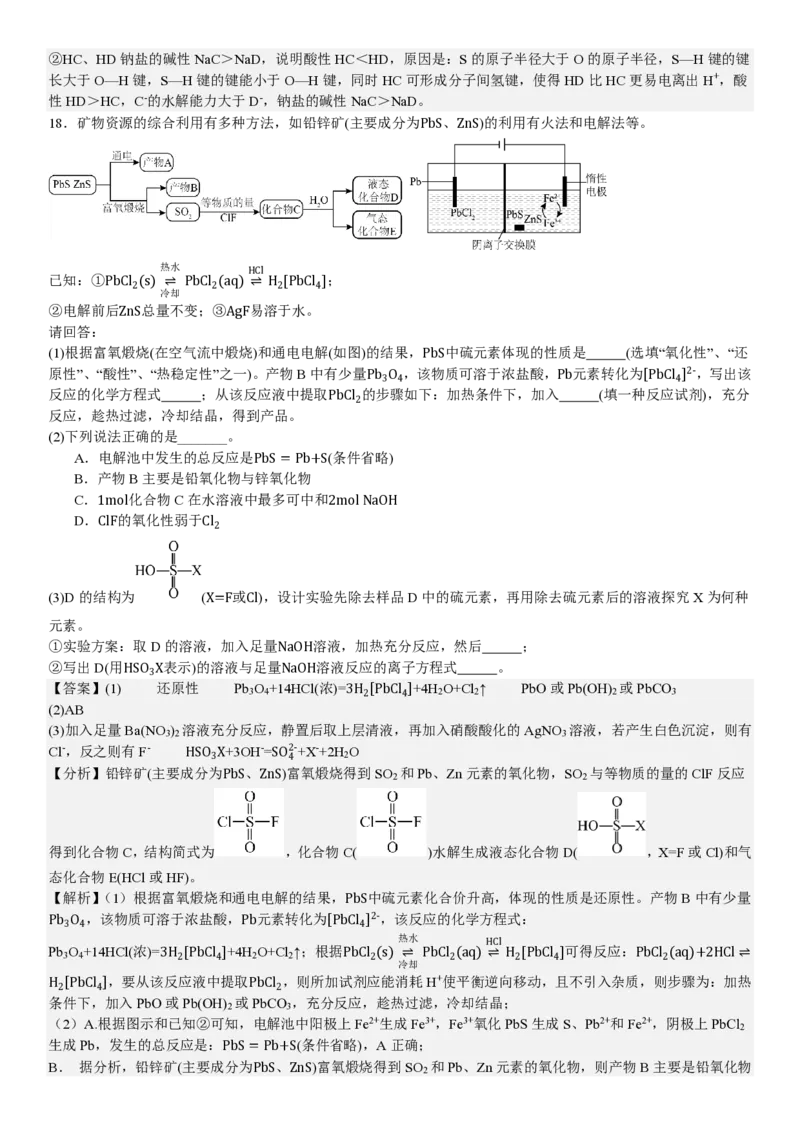
18.矿物资源的综合利用有多种方法,如铅锌矿(主要成分为 、 )的利用有火法和电解法等。
PbS ZnS
热水
已知:① ;
冷却 HCl
②电解前P后bCl2(总s)量⇌不变Pb;Cl2③(aq) 易⇌溶H2于[P水bC。l4 ]
请回答:
ZnS AgF
(1)根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果, 中硫元素体现的性质是 (选填“氧化性”、“还
原性”、“酸性”、“热稳定性”之一)。产物B中有少量 ,该物质可溶于浓盐酸, 元素转化为 ,写出该
PbS
反应的化学方程式 ;从该反应液中提取 的步骤如下:加热条件下,加入 (填一种反应试2剂- ),充分
Pb3O4 Pb [PbCl4]
反应,趁热过滤,冷却结晶,得到产品。
PbCl2
(2)下列说法正确的是_______。
A.电解池中发生的总反应是 (条件省略)
B.产物B主要是铅氧化物与锌氧化物
PbS=Pb+S
C. 化合物C在水溶液中最多可中和
D. 的氧化性弱于
1mol 2mol NaOH
ClF Cl2
(3)D的结构为 ( 或 ),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种
元素。
X=F Cl
①实验方案:取D的溶液,加入足量 溶液,加热充分反应,然后 ;
②写出D(用 表示)的溶液与足量 溶液反应的离子方程式 。
NaOH
【答案】(1) 还原性 Pb O +14HCl(浓)= +4H O+Cl ↑ PbO或Pb(OH) 或PbCO
HSO3X 3 4 NaOH 2 2 2 3
(2)AB
3H2[PbCl4]
(3)加入足量Ba(NO ) 溶液充分反应,静置后取上层清液,再加入硝酸酸化的AgNO 溶液,若产生白色沉淀,则有
3 2 3
Cl-,反之则有F- +3OH-= +X-+2H O
2
【分析】铅锌矿(主要成分为 、 )富2-氧煅烧得到SO 和Pb、Zn元素的氧化物,SO 与等物质的量的ClF反应
HSO3X SO4 2 2
PbS ZnS
得到化合物C,结构简式为 ,化合物C( )水解生成液态化合物D( ,X=F或Cl)和气
态化合物E(HCl或HF)。
【解析】(1)根据富氧煅烧和通电电解的结果, 中硫元素化合价升高,体现的性质是还原性。产物B中有少量
,该物质可溶于浓盐酸, 元素转化为 ,该反应的化学方程式:
PbS
2- 热水
PPbb3 OO4 +14HCl(浓)= +4PHbO+Cl ↑;根[据PbCl4] 可得反应:
3 4 2 2
冷却 HCl
,要从该3反H2应[P液bC中l4提] 取 ,则所加试Pb剂Cl应2(能s)消⇌耗PHb+C使l2(平aq衡)逆⇌向H移2[P动b,Cl4且] 不引入杂质P,bC则l2步(a骤q)+为2:HC加l热⇌
条件下,加入PbO或Pb(OH) 或PbCO ,充分反应,趁热过滤,冷却结晶;
H2[PbCl4] 2 PbCl2 3
(2)A.根据图示和已知②可知,电解池中阳极上Fe2+生成Fe3+,Fe3+氧化PbS生成S、Pb2+和Fe2+,阴极上PbCl
2
生成Pb,发生的总反应是: (条件省略),A正确;
B. 据分析,铅锌矿(主要成分为 、 )富氧煅烧得到SO 和Pb、Zn元素的氧化物,则产物B主要是铅氧化物
PbS=Pb+S 2
PbS ZnS与锌氧化物,B正确;
C. 据分析,化合物C是 ,卤素原子被-OH取代后生成H SO 和HCl、HF,则 化合物C在水溶液
2 4
中最多可中和 ,C错误;
1mol
D. 的氧化性由+1价的Cl表现,Cl 的氧化性由0价的Cl表现,则ClF的氧化锌强于 ,D错误;
2
4molNaOH
故选AB。
ClF Cl2
(3)①D的结构为 (X=F或Cl),加入足量NaOH溶液,加热充分反应,生成Na SO 和NaX,则实验方
2 4
案为:取D的溶液,加入足量NaOH溶液,加热充分反应,然后加入足量Ba(NO ) 溶液充分反应,静置后取上层
3 2
清液,再加入硝酸酸化的AgNO 溶液,若产生白色沉淀,则有Cl-,反之则有F-;②D(用HSO X表示)的溶液与足
3 3
量NaOH溶液反应生成Na SO 和NaX,发生反应的离子方程式为:HSO X+3OH-= +X-+2H O。
2 4 3 2
19.氢是清洁能源,硼氢化钠( )是一种环境友好的固体储氢材料,其水解生氢反2应− 方程式如下:(除非特别说
SO4
明,本题中反应条件均为 , )
NaBH4
25℃ 101kPa
请回答:
NaBH4(s)+2H2O(l)=NaBO2(aq)+4H2(g) ΔH<0
(1)该反应能自发进行的条件是_______。
A.高温 B.低温 C.任意温度 D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是_______。
A.升高溶液温度 B.加入少量异丙胺
C.加入少量固体硼酸 D.增大体系压强
[(CH3)2CHNH2]
(3)为加速 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应
[B(OH)3]
开始时生氢速率v与投料比 之间的关系,结果如图1所示。请解释ab段变化的原因 。
NaBH4
[n(NaBH4)/n(H2O)]
(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如图2所示,
正极上的电极反应式是 。该电池以 恒定电流工作14分钟,消耗 体积为 ,故可测得该电池将化学
能转化为电能的转化率为 。[已知:该条件下 的摩尔体积为 ;电荷量 电流 时间 ;
3.2A H2 0.49L
; 。]
H2 24.5L/mol q(C)= I(A)× (s)
23 -1 -19
NA=6.0×10 mol e=1.60×10 C(5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方法,将反
应副产物偏硼酸钠( )再生为 。(已知: 是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比
计算方法;当 时,反应能自发进行。)
NaBO2 NaBH4 ΔG
I.
Δ𝐻𝐻 ΔG<0
II.NaBH4(s)+2H2O(l)=NaBO2(s)+4H2(g) Δ G1=-320kJ/mol
1
H2(g)+2O2(g)=H2O(l) ΔG2=-240kJ/mol
III.
1
请书M写g一(s个)+方2程O2式(g表)=示MgO(s) 再 Δ生G3为=-570kJ/的m一ol种制备方法,并注明 。(要求:反应物不超过三种物质;氢
原子利用率为 。)
NaBO2 NaBH4 ΔG
【答案】(1)C
100%
(2)A
(3)随着投料比 增大,NaBH 的水解转化率降低
4
(4) O +4e-+2CO =2 70%
2 [n(NaB 2 H4)/n(H2O)]
(5) 2-
CO3
【解析】(1)反应 , > ,由 可知,任意温度下,
NaBO2(s)+2H2(g)+2Mg(s)=NaBH4(s)+2MgO(s) ΔG=-340kJ/mol
该反应均能自发进行;
NaBH4(s)+2H2O(l)=NaBO2(aq)+4H2(g) ΔH<0 ΔS 0 ΔG=ΔH-TΔS
故选C;
(2)A.升高温度,活化分子数增多,有效碰撞几率增大,反应速率加快,A正确;
B.加入少量异丙胺 ,H O的量减少,化学反应速率降低,B错误;
2
C. 加入少量固体硼酸 ,H O的量减少,化学反应速率降低,C错误;
[(CH3)2CHNH2] 2
D.增大体系压强,忽略体积变化,则气体浓度不变,化学反应速率不变,D错误;
[B(OH)3]
故选A。
(3)随着投料比 增大,NaBH 的水解转化率降低,因此生成氢气的速率不断减小。
4
(4)该燃料电池中H 为负极,O 为正极,熔融碳酸盐为电解质溶液,故正极的电极反应式为:O +4e-+2CO =2 ,
[n(N 2 aBH4)/n(H 22O)] 2 2
2-
该条件下,0.49L H 的物质的量为 ,工作时,H 失去电子:H -2e-=2H+,所带电荷量CO为3:
2 2 2
0.49L
2×0.02mol×6.0×1023mol-1×1.60×10-1n9=(H 3 2 8)4=0C24,.5L工/m作ol=电0荷.02量m为ol:3.2×14×60=2688C,则该电池将化学能转化为电能的
转化率为: ;
2688C
(5)要使得38氢40原C×子1利00用%率=为701%00%,可由(2×反应3)-(2×反应Ⅱ+反应Ⅰ)得
, 。
NaBO2(s)+2H2(g)+2Mg(s)=
20.某小组采用如下实验流程制备 :
NaBH4(s)+2MgO(s) ΔG=2ΔG3-(2ΔG2+ΔG1)=2×(-570kJ/mol)-[2×(-240kJ/mol)+(-320kJ/mol)]=-340kJ/mol
AlI3
已知: 是一种无色晶体,吸湿性极强,可溶于热的正己烷,在空气中受热易被氧化。
请回答:
AlI3
(1)如图为步骤I的实验装置图(夹持仪器和尾气处理装置已省略),图中仪器A的名称是 ,判断步骤I反应结
束的实验现象是 。(2)下列做法不
.
正
.
确
.
的是_______。
A.步骤I中,反应物和溶剂在使用前除水
B.步骤I中,若控温加热器发生故障,改用酒精灯(配石棉网)加热
C.步骤Ⅲ中,在通风橱中浓缩至蒸发皿内出现晶膜
D.步骤Ⅳ中,使用冷的正己烷洗涤
(3)所得粗产品呈浅棕黄色,小组成员认为其中混有碘单质,请设计实验方案验证 。
(4)纯化与分析:对粗产品纯化处理后得到产品,再采用银量法测定产品中 含量以确定纯度。滴定原理为:先用过
量 标准溶液沉淀 ,再以 标准溶液回滴剩余的 。已知: -
I
- +
难 A 溶 g 电 NO 解3质 (黄 I 色) NH4SC(N 白色) (红色)A g
溶度积常数 AgI AgSCN Ag2CrO4
-17 -12 -12
①从下列选
K
项sp中选
8
择
.5
合
×
适
10
的操作
1.
补
0×
全
1
测
0
定步骤
1 .1 × 1
。
0
称取产品 ,用少量稀酸A溶解后转移至 容量瓶,加水定容得待测溶液。取滴定管检漏、水洗
→_______→装液、赶气泡、调液面、读数→用移液管准确移取 待测溶液加入锥形瓶→_______→_______→
1.0200g 250mL
加入稀酸B→用 标准溶液滴定→_______→读数。
25.00mL
a.润洗,从滴定管尖嘴放出-2液体
1.000×10 mol/LNH4SCN
b.润洗,从滴定管上口倒出液体
c.滴加指示剂 溶液
d.滴加指示剂硫酸铁铵 溶液
K2CrO4
e.准确移取 标准溶液加入锥形瓶
[NH4Fe(SO4)2]
f.滴定至溶液呈浅红色 -2
25.00mL4.000×10 mol/LAgNO3
g.滴定至沉淀变白色
②加入稀酸B的作用是 。
③三次滴定消耗 标准溶液的平均体积为 ,则产品纯度为 。
【答案】(1) 球形冷凝管 溶液由紫红色恰好变为无色(或溶液褪为无色)
NH4SCN 25.60mL [M(AlI3)=408g/mol]
(2)BC
(3)取少量粗产品置于少量冷的正己烷中充分搅拌,静置后,取少量上层清液,向其中滴加淀粉溶液,观察液体是否
变蓝,若变蓝则其中混有碘单质,否则没有
(4) a e d f 抑制 发生水解反应,保证滴定终点的准确判断
【解析】(1)由实验装置图3中+仪器的结构可知,图中仪器A的名称是球形冷凝管,其用于冷凝回流;碘溶于正己烷
Fe 99.20%
使溶液显紫红色, 是无色晶体,当碘反应完全后,溶液变为无色,因此,判断步骤I反应结束的实验现象是:
溶液由紫红色恰好变为无色(或溶液褪为无色)。
AlI3
(2)A. 吸湿性极强,因此在步骤I中,反应物和溶剂在使用前必须除水,A正确;
B.使用到易烯的有机溶剂时,禁止使用明火加热,因此在步骤I中,若控温加热器发生故障,不能改用酒精灯(配
AlI3
石棉网)加热,B错误;
C. 在空气中受热易被氧化,因此在步骤Ⅲ中蒸发浓缩时,要注意使用有保护气(如持续通入氮气的蒸馏烧瓶等)
的装置中进行,不能直接在蒸发皿浓缩,C错误;
AlI3
D. 在空气中受热易被氧化、可溶于热的正己烷因此,为了减少溶解损失,在步骤Ⅳ中要使用冷的正己烷洗涤,
D正确;
AlI3
故选BC。
(3)碘易溶于正己烷,而 可溶于热的正己烷、不易溶于冷的正己烷,因此,可以取少量粗产品置于少量冷的正
己烷中充分搅拌,静置后,取少量上层清液,向其中滴加淀粉溶液,观察液体是否变蓝,若变蓝则其中混有碘单质,
AlI3
否则没有。
(4)①润洗时,滴定管尖嘴部分也需要润洗;先加 待测溶液,后加 标准
溶液,两者充分分反应后,剩余的 浓度较小,然后滴加指示剂硫酸铁铵 溶液作-2指示剂,可以防止
25.00mL 25.00mL4.000×10 mol/LAgNO3
生成 沉淀; 的溶度积+常数与 非常接近,因此, 溶液不能用作指示剂,应该选用
Ag [NH4Fe(SO4)2]
溶液,其中的 可以与过量的半滴 溶液中的 反应生成溶液呈红色的配合物,故
Ag2SO4 Ag2CrO4 AgSCN K2CrO4
滴定至溶液呈浅红色;综上所述3+,需要补全的操作步骤依次是:a e d f。 −
[NH4Fe(SO4)2] Fe [NH4Fe(SO4)2] SCN
② 和 均易发生水解, 溶液中含有 ,为防止影响滴定终点的判断,必须抑制其发生水解,
3+ 3+ 3+
Fe Al [NH4Fe(SO4)2] Fe因此加入稀酸B的作用是:抑制 发生水解反应,保证滴定终点的准确判断。
③根据滴定步骤可知, 3+ 标准溶液分别与 溶液中的 、
Fe
标准溶液中的 发生反应生成 和 -2 ;由 守恒可知, - ,则-2
25.00mL4.000×10 mol/LAgNO3 AlI3 I 1.000×10 mol/LNH4SCN
− ;+ 三次滴定消耗 标准溶液的平均体积为 ,则
SCN AgI AgSCN Ag n(AgI)+n(AgSCN)=n(AgNO3)
n(AgI)=n(AgNO3)-n(AgSCN)=n(AgNO3)-n(NH4SCN) NH4SCN 25.60mL
−3 −1 -2
n(AgI)=n(AgNO3)-n(AgSCN)=n(Ag=NO3)-n(NH4SCN),=由25I.守00恒m可L×知10 L⋅mL ×4.000×10 mol/L-25.60mL×
−3 −1 -2 -4 1 -4 1
10 L⋅mL ×1.000×10 mol/L 7.440×10 mol n(AlI3)=3n(AgI)=7.440×10 mol×3=
,因此,纯度为 。
-4
-4 2.480×10 mol×408g/mol
25.00mL
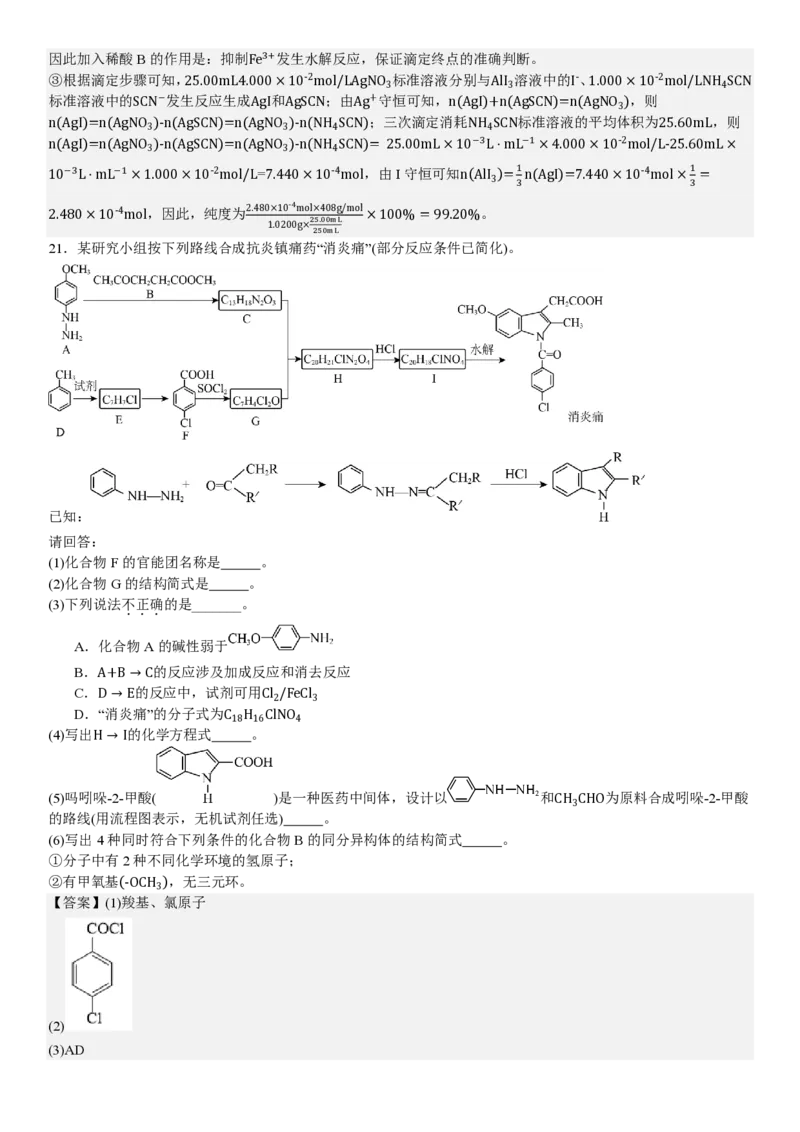
221.4.80某×研1究0 小m组ol按下列路线合成抗炎1.镇020痛0g药×2“50消mL炎痛”×(部10分0%反应=条99件.20已%简化)。
已知:
请回答:
(1)化合物F的官能团名称是 。
(2)化合物G的结构简式是 。
(3)下列说法不
.
正
.
确
.
的是_______。
A.化合物A的碱性弱于
B. 的反应涉及加成反应和消去反应
C. 的反应中,试剂可用
A+B→C
D.“消炎痛”的分子式为
D→E Cl2/FeCl3
(4)写出 的化学方程式 。
C18H16ClNO4
H→I
(5)吗吲哚-2-甲酸( )是一种医药中间体,设计以 和 为原料合成吲哚-2-甲酸
的路线(用流程图表示,无机试剂任选) 。
CH3CHO
(6)写出4种同时符合下列条件的化合物B的同分异构体的结构简式 。
①分子中有2种不同化学环境的氢原子;
②有甲氧基 ,无三元环。
【答案】(1)羧基、氯原子
(-OCH3)
(2)
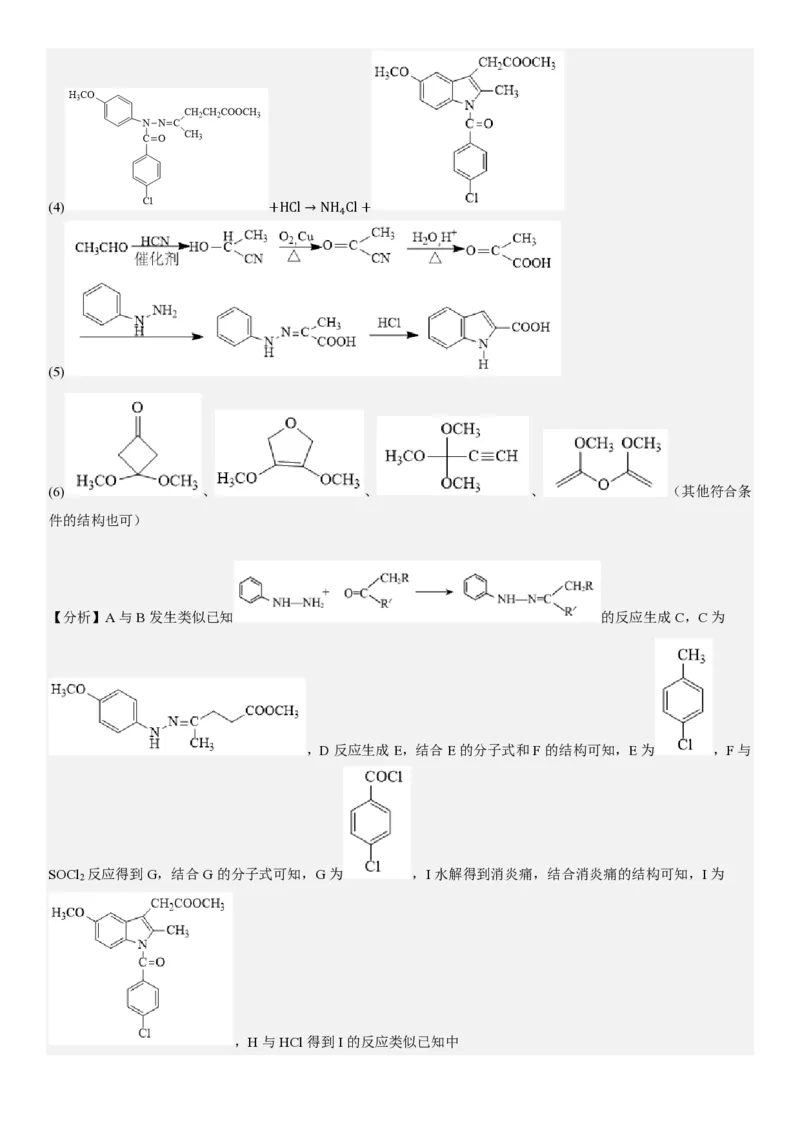
(3)AD(4)
+HCl→NH4Cl+
(5)
(6) 、 、 、 (其他符合条
件的结构也可)
【分析】A与B发生类似已知 的反应生成C,C为
,D反应生成E,结合E的分子式和F的结构可知,E为 ,F与
SOCl 反应得到G,结合G的分子式可知,G为 ,I水解得到消炎痛,结合消炎痛的结构可知,I为
2
,H与HCl得到I的反应类似已知中的反应,由此可知H为 ,C与
G反应得到H。
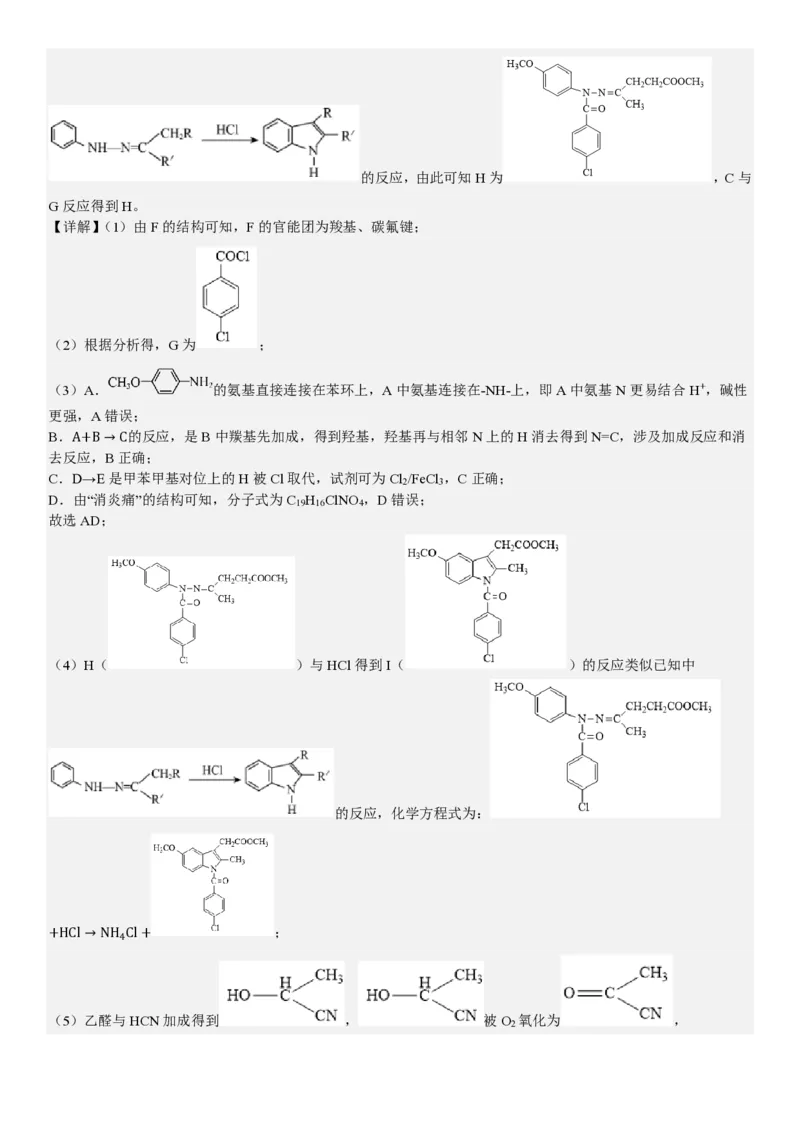
【详解】(1)由F的结构可知,F的官能团为羧基、碳氟键;
(2)根据分析得,G为 ;
(3)A. 的氨基直接连接在苯环上,A中氨基连接在-NH-上,即A中氨基N更易结合H+,碱性
更强,A错误;
B. 的反应,是B中羰基先加成,得到羟基,羟基再与相邻N上的H消去得到N=C,涉及加成反应和消
去反应,B正确;
A+B→C
C.D→E是甲苯甲基对位上的H被Cl取代,试剂可为Cl /FeCl ,C正确;
2 3
D.由“消炎痛”的结构可知,分子式为C H ClNO ,D错误;
19 16 4
故选AD;
(4)H( )与HCl得到I( )的反应类似已知中
的反应,化学方程式为:
;
+HCl→NH4Cl+
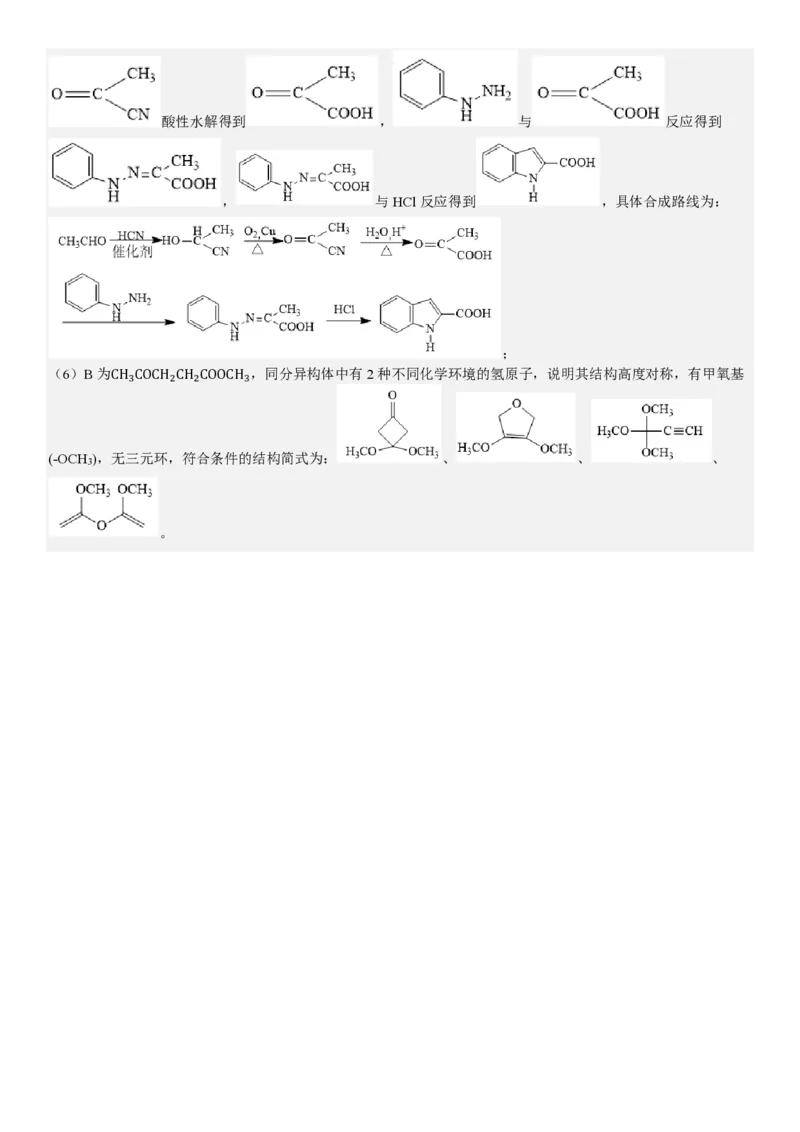
(5)乙醛与HCN加成得到 , 被O 氧化为 ,
2酸性水解得到 , 与 反应得到
, 与HCl反应得到 ,具体合成路线为:
;
(6)B为 ,同分异构体中有2种不同化学环境的氢原子,说明其结构高度对称,有甲氧基
CH3COCH2CH2COOCH3
(-OCH ),无三元环,符合条件的结构简式为: 、 、 、
3
。