文档内容
2024 届高三年级第二次调研测试化学试题
出题人:刘烁 审题人:战丽娜
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:
32 Cl:35.5 K:39 Co:59
第I卷(选择题 共50分)
一、选择题(每题只有一个正确选项,2×10=20分)
1.下列应用中涉及到氧化还原反应的是( )
A.使用明矾对水进行净化 B.雪天道路上撒盐融雪
C.暖贴中的铁粉遇空气放热 D.荧光指示牌被照发光
2.考古中出土的锡青铜(铜锡合金)文物常有 覆盖其表面。下列说法正确的是( )
A.锡青铜的熔点比纯铜高
B.锡青铜文物在潮湿环境中的腐蚀比干燥环境中快
C.锡青铜中的锡加速了铜的腐蚀速度
D.生成 覆盖物是电化学腐蚀过程,但不是化学反应过程
3.下列说法正确的是( )
A.用丁达尔效应区分溶液与胶体 B.用浓硫酸干燥碘化氢气体
C.用乙醇萃取碘水中的碘 D.用分液漏斗可分离溴苯和溴的混合物
4. 为阿伏加德罗常数的值。下列叙述正确的是( )
A. 与 的混合物中所含中子数为
B.标准状况下,11.2L丙烷具有的共价键数为
C.电解精炼铜时,若电路中转移0.2mol电子,阳极质量减少6.4g
D.常温下,0.5molFe投入浓硫酸中,反应转移的电子数为
5.海洋是巨大的资源宝库,从海水中提取的氯化钠是一种重要的化工原料。下列说法正确的是( )
A.利用日光和风力使海水蒸干,可以获得大量纯净氯化钠
B.工业上通过电解饱和氯化钠溶液来制取金属钠
C.氯化钠在日常生活中可用作调味剂,也可用作防腐剂
D.向饱和氯化钠溶液先通入过量 ,再通入氨气,会析出大量 固体
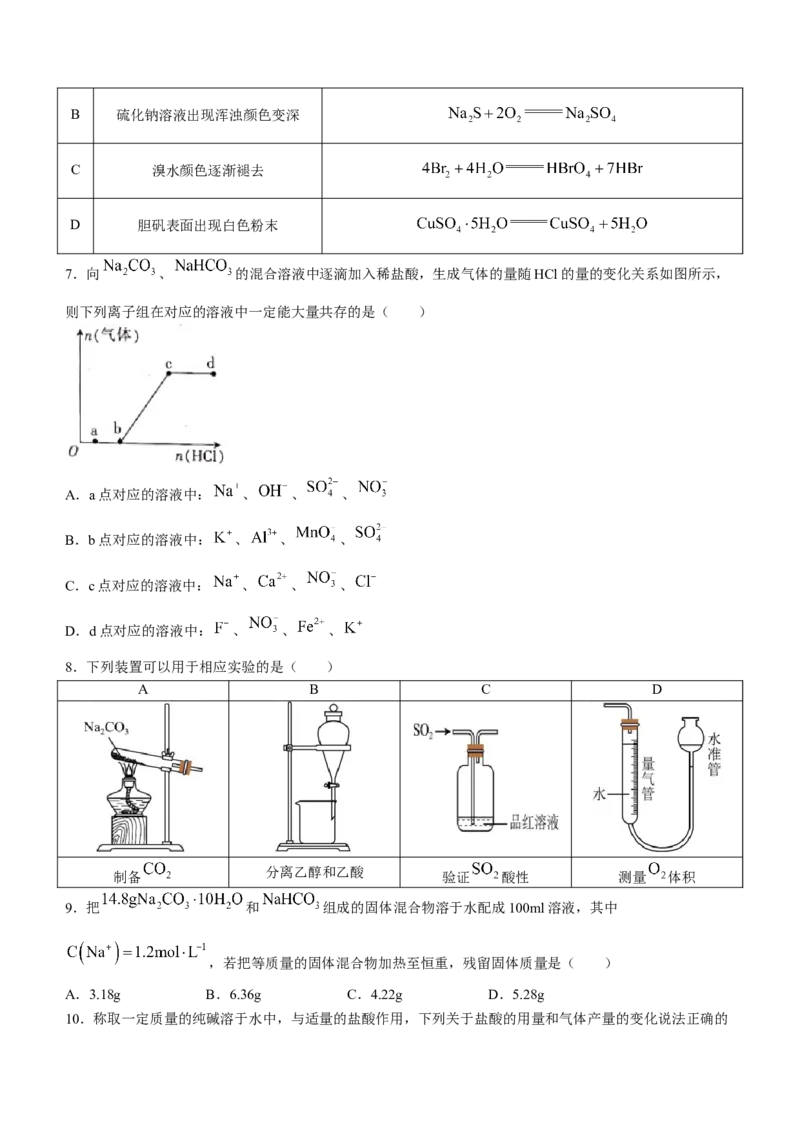
6.一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是( )
A 硫酸亚铁溶液出现棕黄色沉淀B 硫化钠溶液出现浑浊颜色变深
C 溴水颜色逐渐褪去
D 胆矾表面出现白色粉末
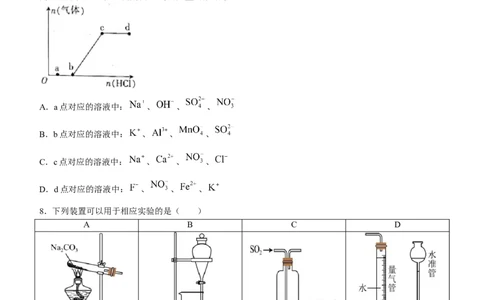
7.向 、 的混合溶液中逐滴加入稀盐酸,生成气体的量随HCl的量的变化关系如图所示,
则下列离子组在对应的溶液中一定能大量共存的是( )
A.a点对应的溶液中: 、 、 、
B.b点对应的溶液中: 、 、 、
C.c点对应的溶液中: 、 、 、
D.d点对应的溶液中: 、 、 、
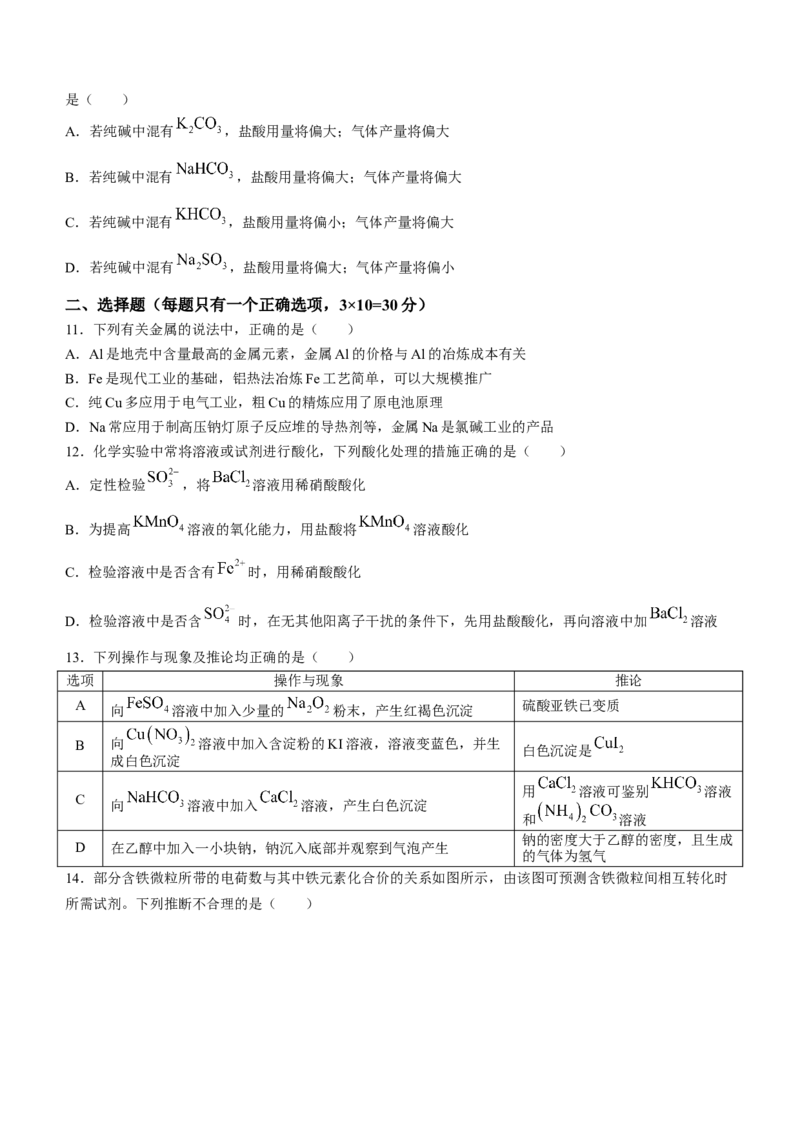
8.下列装置可以用于相应实验的是( )
A B C D
分离乙醇和乙酸
制备 验证 酸性 测量 体积
9.把 和 组成的固体混合物溶于水配成100ml溶液,其中
,若把等质量的固体混合物加热至恒重,残留固体质量是( )
A.3.18g B.6.36g C.4.22g D.5.28g
10.称取一定质量的纯碱溶于水中,与适量的盐酸作用,下列关于盐酸的用量和气体产量的变化说法正确的是( )
A.若纯碱中混有 ,盐酸用量将偏大;气体产量将偏大
B.若纯碱中混有 ,盐酸用量将偏大;气体产量将偏大
C.若纯碱中混有 ,盐酸用量将偏小;气体产量将偏大
D.若纯碱中混有 ,盐酸用量将偏大;气体产量将偏小
二、选择题(每题只有一个正确选项,3×10=30分)
11.下列有关金属的说法中,正确的是( )
A.Al是地壳中含量最高的金属元素,金属Al的价格与Al的冶炼成本有关
B.Fe是现代工业的基础,铝热法冶炼Fe工艺简单,可以大规模推广
C.纯Cu多应用于电气工业,粗Cu的精炼应用了原电池原理
D.Na常应用于制高压钠灯原子反应堆的导热剂等,金属Na是氯碱工业的产品
12.化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是( )
A.定性检验 ,将 溶液用稀硝酸酸化
B.为提高 溶液的氧化能力,用盐酸将 溶液酸化
C.检验溶液中是否含有 时,用稀硝酸酸化
D.检验溶液中是否含 时,在无其他阳离子干扰的条件下,先用盐酸酸化,再向溶液中加 溶液
13.下列操作与现象及推论均正确的是( )
选项 操作与现象 推论
A 硫酸亚铁已变质
向 溶液中加入少量的 粉末,产生红褐色沉淀
B 向 溶液中加入含淀粉的KI溶液,溶液变蓝色,并生
白色沉淀是
成白色沉淀
用 溶液可鉴别 溶液
C
向 溶液中加入 溶液,产生白色沉淀
和 溶液
钠的密度大于乙醇的密度,且生成
D 在乙醇中加入一小块钠,钠沉入底部并观察到气泡产生
的气体为氢气
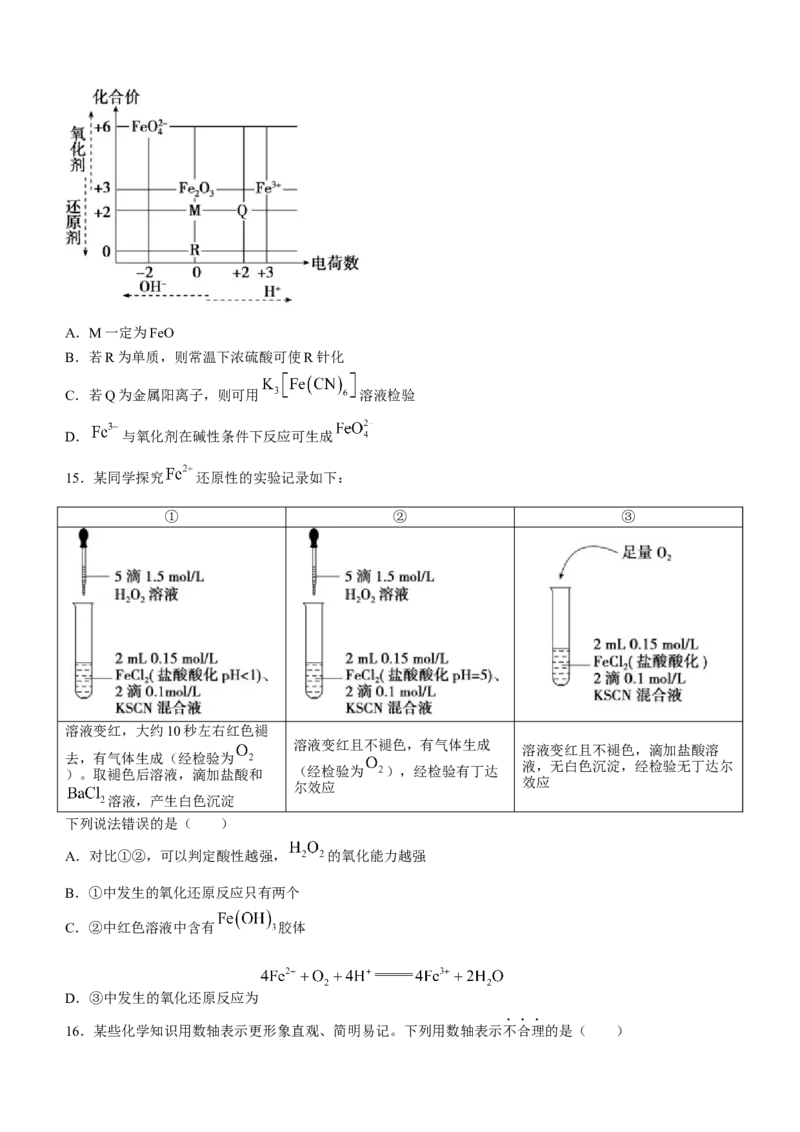
14.部分含铁微粒所带的电荷数与其中铁元素化合价的关系如图所示,由该图可预测含铁微粒间相互转化时
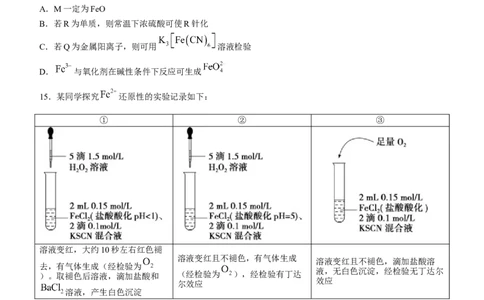
所需试剂。下列推断不合理的是( )A.M一定为FeO
B.若R为单质,则常温下浓硫酸可使R针化
C.若Q为金属阳离子,则可用 溶液检验
D. 与氧化剂在碱性条件下反应可生成
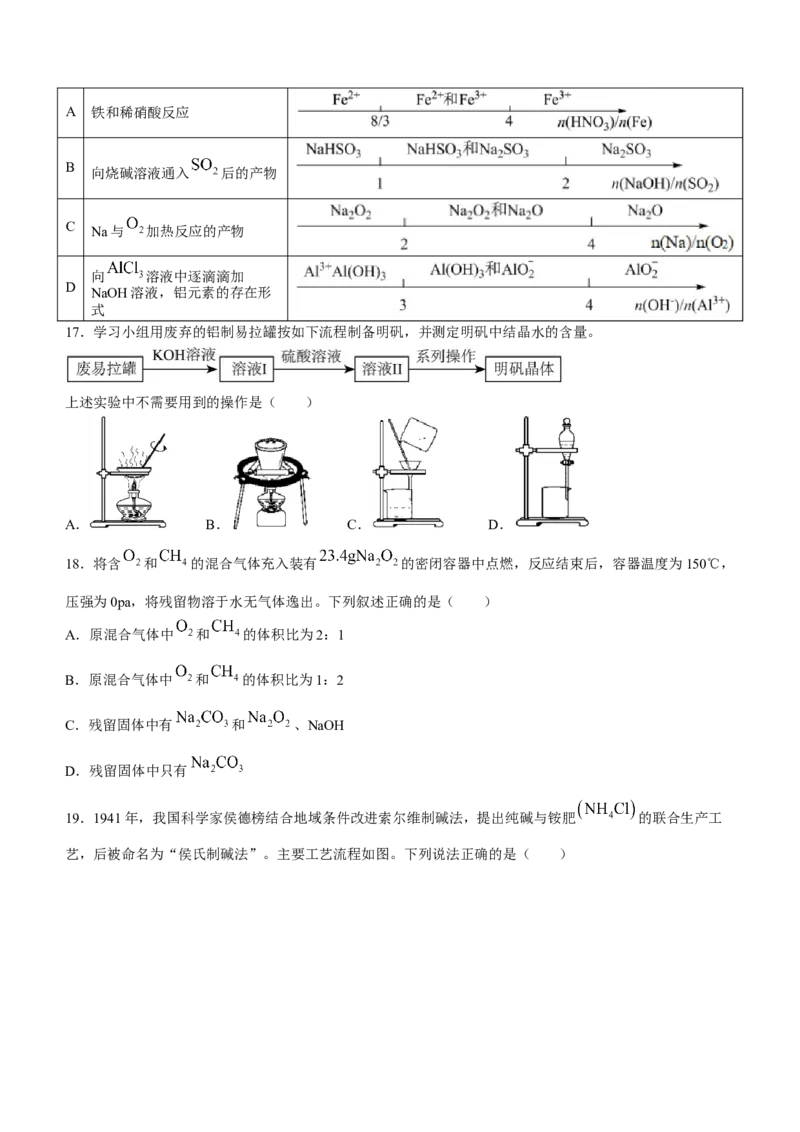
15.某同学探究 还原性的实验记录如下:
① ② ③
溶液变红,大约10秒左右红色褪
溶液变红且不褪色,有气体生成
溶液变红且不褪色,滴加盐酸溶
去,有气体生成(经检验为
液,无白色沉淀,经检验无丁达尔
)。取褪色后溶液,滴加盐酸和 (经检验为 ),经检验有丁达
效应
尔效应
溶液,产生白色沉淀
下列说法错误的是( )
A.对比①②,可以判定酸性越强, 的氧化能力越强
B.①中发生的氧化还原反应只有两个
C.②中红色溶液中含有 胶体
D.③中发生的氧化还原反应为
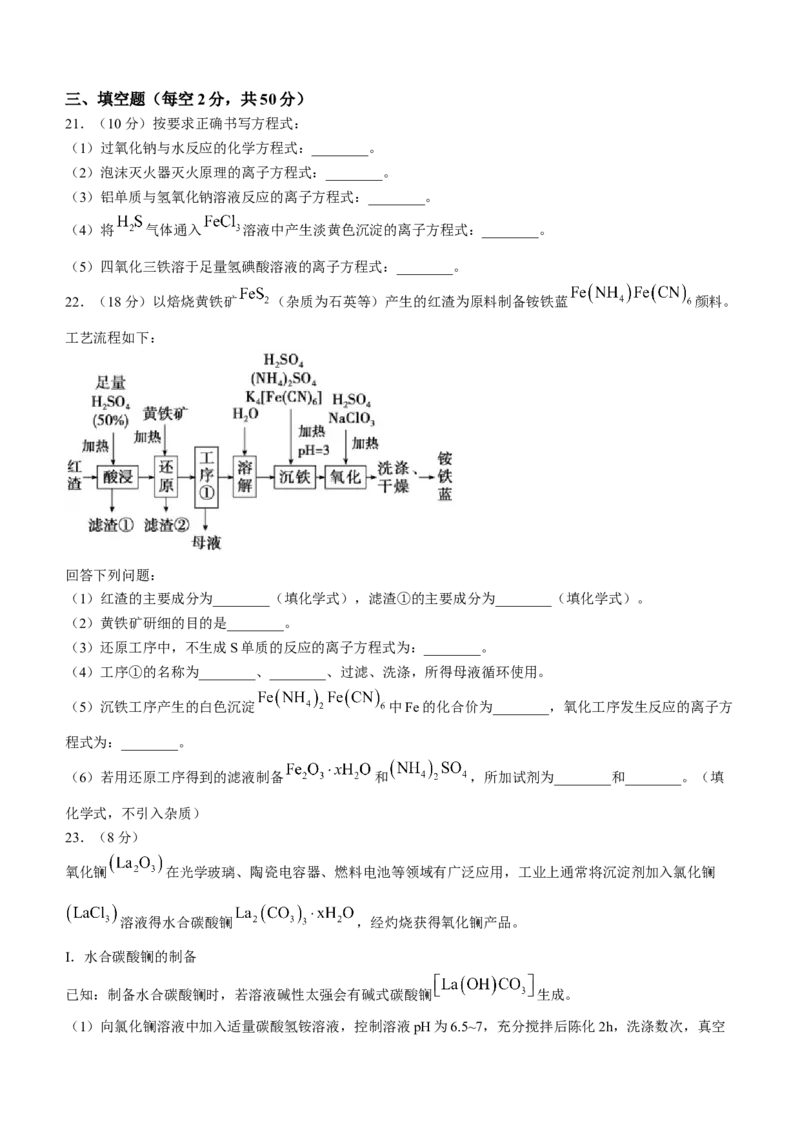
16.某些化学知识用数轴表示更形象直观、简明易记。下列用数轴表示不合理的是( )A 铁和稀硝酸反应
B
向烧碱溶液通入 后的产物
C
Na与 加热反应的产物
向 溶液中逐滴滴加
D
NaOH溶液,铝元素的存在形
式
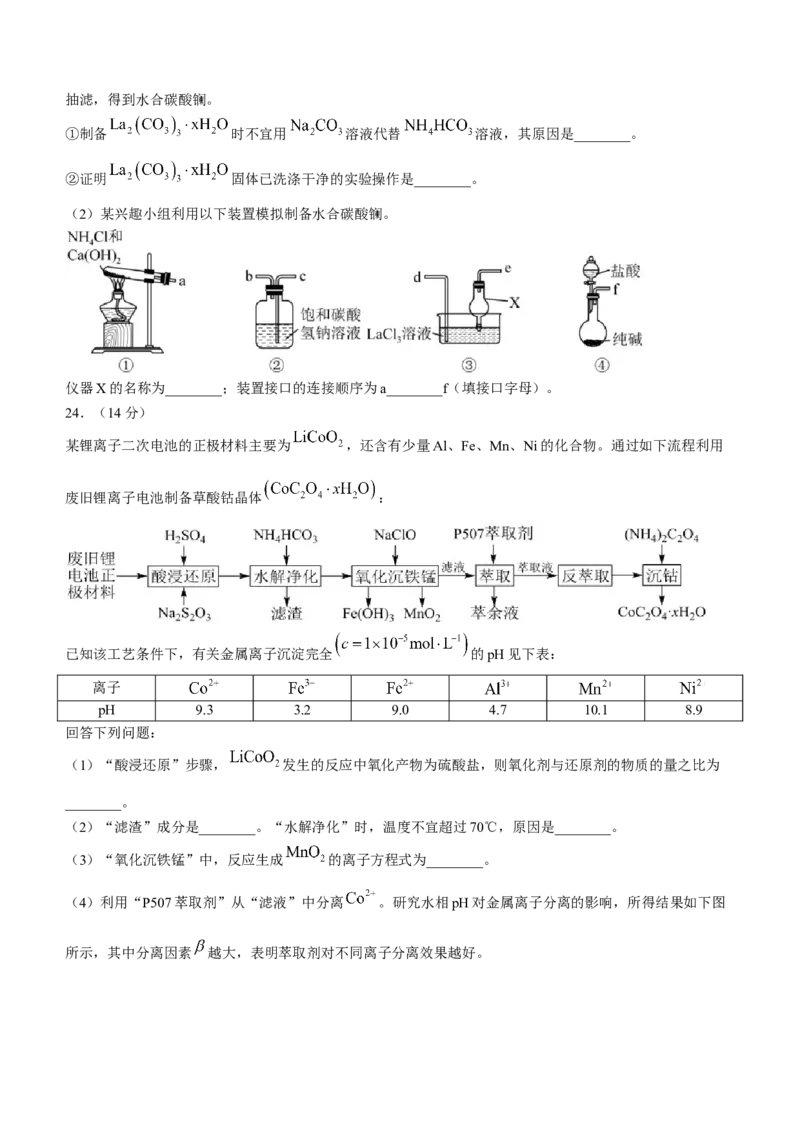
17.学习小组用废弃的铝制易拉罐按如下流程制备明矾,并测定明矾中结晶水的含量。
上述实验中不需要用到的操作是( )
A. B. C. D.
18.将含 和 的混合气体充入装有 的密闭容器中点燃,反应结束后,容器温度为150℃,
压强为0pa,将残留物溶于水无气体逸出。下列叙述正确的是( )
A.原混合气体中 和 的体积比为2:1
B.原混合气体中 和 的体积比为1:2
C.残留固体中有 和 、NaOH
D.残留固体中只有
19.1941年,我国科学家侯德榜结合地域条件改进索尔维制碱法,提出纯碱与铵肥 的联合生产工
艺,后被命名为“侯氏制碱法”。主要工艺流程如图。下列说法正确的是( )已知:侯氏制碱法总反应:
索尔维制碱法总反应: ( 作为废液排放)
A.气体1、气体2均为
B.溶液2中,含碳微粒主要是
C.侯氏制碱法和索尔维制碱法中原料NaCl的原子利用率相同
D.盐析池中加入NaCl, 增大, 的平衡逆向移动, 析出
20.某固体混合物可能由Al、 、 、 、 中的一种或几种组成,现对该混合物
做如下实验,所得现象和有关数据如下图所示(气体体积数据已换算成标准状况下的体积),则关于该固体
混合物,下列说法中正确的是( )
A.一定含 、 且物质的量相等
B.一定含有Al,其质量为4.05g
C.一定不含 ,可能含有 和
D.一定含有 、 和
第II卷(非选择题 共50分)三、填空题(每空2分,共50分)
21.(10分)按要求正确书写方程式:
(1)过氧化钠与水反应的化学方程式:________。
(2)泡沫灭火器灭火原理的离子方程式:________。
(3)铝单质与氢氧化钠溶液反应的离子方程式:________。
(4)将 气体通入 溶液中产生淡黄色沉淀的离子方程式:________。
(5)四氧化三铁溶于足量氢碘酸溶液的离子方程式:________。
22.(18分)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。
工艺流程如下:
回答下列问题:
(1)红渣的主要成分为________(填化学式),滤渣①的主要成分为________(填化学式)。
(2)黄铁矿研细的目的是________。
(3)还原工序中,不生成S单质的反应的离子方程式为:________。
(4)工序①的名称为________、________、过滤、洗涤,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中Fe的化合价为________,氧化工序发生反应的离子方
程式为:________。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为________和________。(填
化学式,不引入杂质)
23.(8分)
氧化镧 在光学玻璃、陶瓷电容器、燃料电池等领域有广泛应用,工业上通常将沉淀剂加入氯化镧
溶液得水合碳酸镧 ,经灼烧获得氧化镧产品。
I.水合碳酸镧的制备
已知:制备水合碳酸镧时,若溶液碱性太强会有碱式碳酸镧 生成。
(1)向氯化镧溶液中加入适量碳酸氢铵溶液,控制溶液pH为6.5~7,充分搅拌后陈化2h,洗涤数次,真空抽滤,得到水合碳酸镧。
①制备 时不宜用 溶液代替 溶液,其原因是________。
②证明 固体已洗涤干净的实验操作是________。
(2)某兴趣小组利用以下装置模拟制备水合碳酸镧。
仪器X的名称为________;装置接口的连接顺序为a________f(填接口字母)。
24.(14分)
某锂离子二次电池的正极材料主要为 ,还含有少量Al、Fe、Mn、Ni的化合物。通过如下流程利用
废旧锂离子电池制备草酸钴晶体 :
已知该工艺条件下,有关金属离子沉淀完全 的pH见下表:
离子
pH 9.3 3.2 9.0 4.7 10.1 8.9
回答下列问题:
(1)“酸浸还原”步骤, 发生的反应中氧化产物为硫酸盐,则氧化剂与还原剂的物质的量之比为
________。
(2)“滤渣”成分是________。“水解净化”时,温度不宜超过70℃,原因是________。
(3)“氧化沉铁锰”中,反应生成 的离子方程式为________。
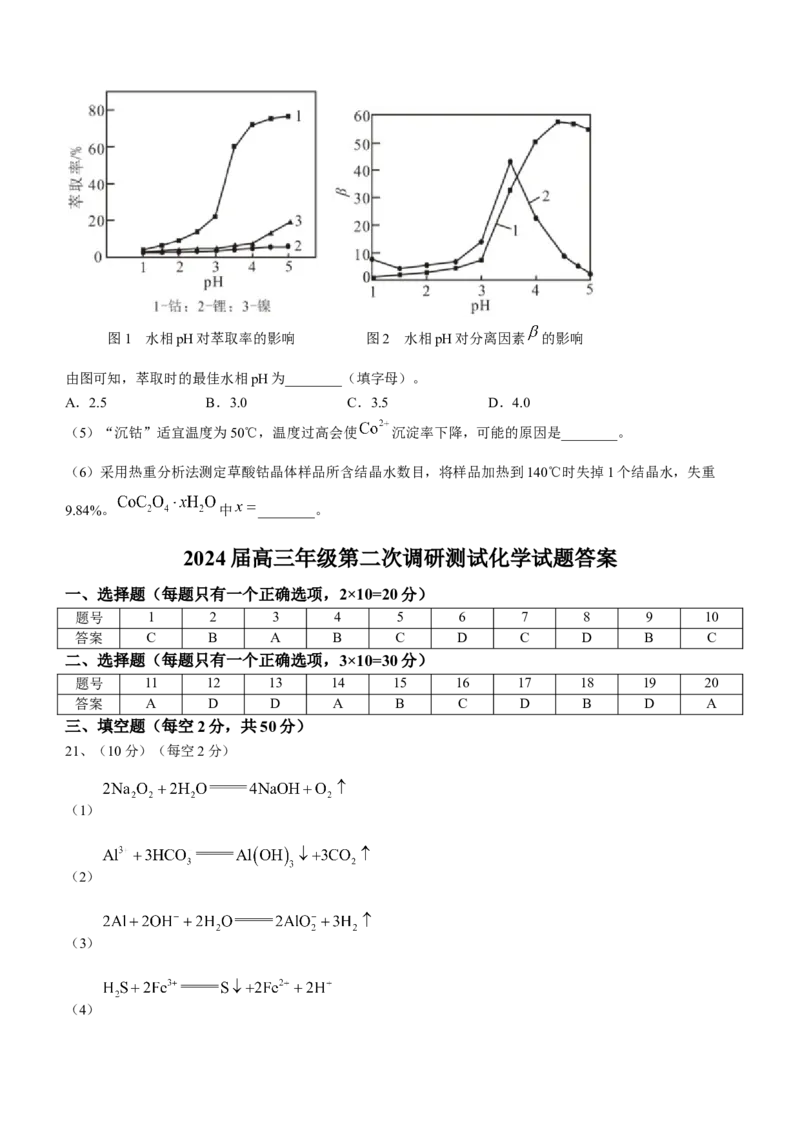
(4)利用“P507萃取剂”从“滤液”中分离 。研究水相pH对金属离子分离的影响,所得结果如下图
所示,其中分离因素 越大,表明萃取剂对不同离子分离效果越好。图1 水相pH对萃取率的影响 图2 水相pH对分离因素 的影响
由图可知,萃取时的最佳水相pH为________(填字母)。
A.2.5 B.3.0 C.3.5 D.4.0
(5)“沉钴”适宜温度为50℃,温度过高会使 沉淀率下降,可能的原因是________。
(6)采用热重分析法测定草酸钴晶体样品所含结晶水数目,将样品加热到140℃时失掉1个结晶水,失重
9.84%。 中 ________。
2024 届高三年级第二次调研测试化学试题答案
一、选择题(每题只有一个正确选项,2×10=20分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C B A B C D C D B C
二、选择题(每题只有一个正确选项,3×10=30分)
题号 11 12 13 14 15 16 17 18 19 20
答案 A D D A B C D B D A
三、填空题(每空2分,共50分)
21、(10分)(每空2分)
(1)
(2)
(3)
(4)(5)
22、(18分)(除标注外,每空2分)
(1)
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(3)
(4)蒸发浓缩(1分)、冷却结晶(1分)
(5)
(6) (无先后顺序)
23.(8分)(每空2分)
(1)①防止溶液碱性太强时生成碱式碳酸钵[或 ]
②取最后一次洗涤液于试管中,加入硝酸酸化的硝酸银,若无白色沉淀生成,证明已洗涤干净
(2)(球形)干燥管 edbc
24.(14分)(每空2分)
(1)8:1
(2) 避免 受热分解
(3)
(4)C