文档内容
专题18 钠及其化合物
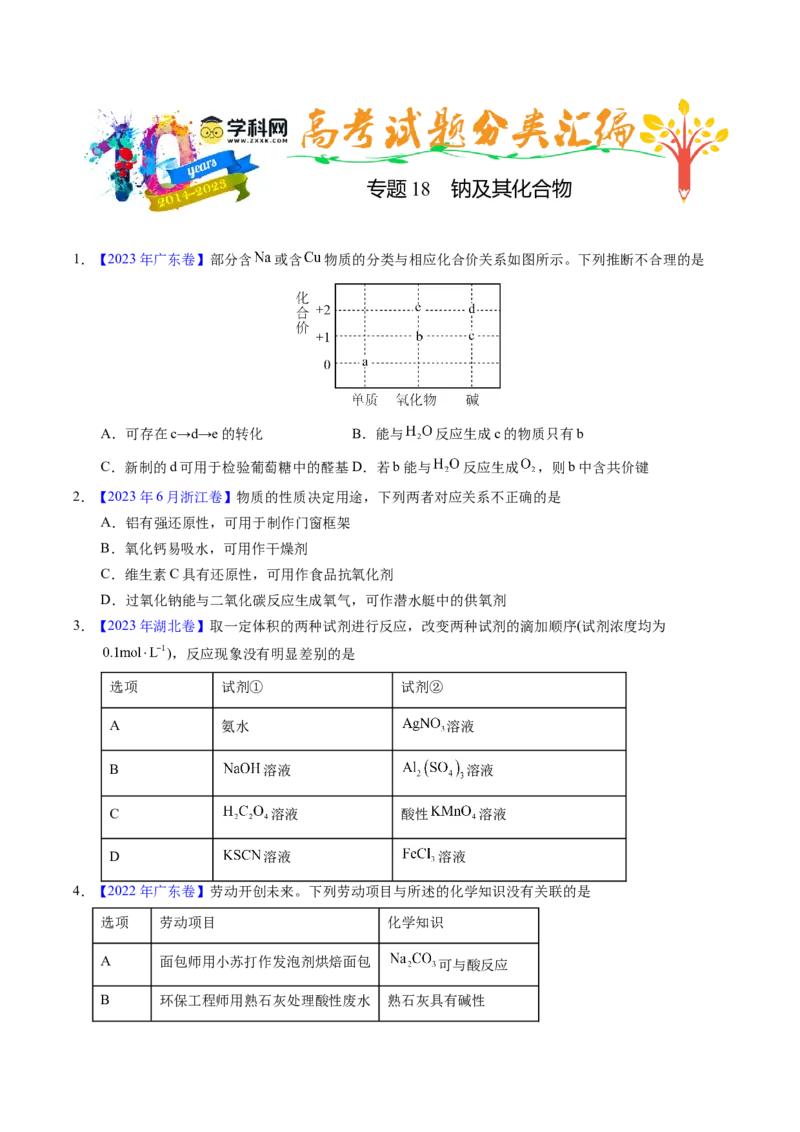
1.【2023年广东卷】部分含 或含 物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.可存在c→d→e的转化 B.能与 反应生成c的物质只有b
C.新制的d可用于检验葡萄糖中的醛基D.若b能与 反应生成 ,则b中含共价键
2.【2023年6月浙江卷】物质的性质决定用途,下列两者对应关系不正确的是
A.铝有强还原性,可用于制作门窗框架
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
3.【2023年湖北卷】取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为
),反应现象没有明显差别的是
选项 试剂① 试剂②
A 氨水 溶液
B 溶液 溶液
C 溶液 酸性 溶液
D 溶液 溶液
4.【2022年广东卷】劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 面包师用小苏打作发泡剂烘焙面包 可与酸反应
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性C 工人将模具干燥后再注入熔融钢水 铁与 高温下会反应
D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
5.【2022年广东卷】下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:
B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
6.【2022年海南卷】钠和钾是两种常见金属,下列说法正确的是
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差18
7.【2022年6月浙江卷】亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将
适量某样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列
方案设计、现象和结论都正确的是
方案设计 现象和结论
先加入少量 溶液,再加 溶液和足量稀硝酸,振 若产生白色沉淀,则样品为亚硝酸
A
荡 钠
B 加到少量 溶液中,再加硫酸酸化,振荡 若溶液褪色,则样品为亚硝酸钠
C 先加到少量 溶液中,再加入稀盐酸酸化,振荡 若溶液变黄色,则样品为亚硝酸钠
若产生白色沉淀,则样品为亚硝酸
D 先加入少量 溶液,再加入 溶液和稀硝酸,振荡
钠
8.(2021.1·浙江真题)下列“类比”合理的是
A.Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B.NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO 和HClO
2 3 2 3
C.NaN与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D.NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应生成Ag O
3 2 3 3 2
和NH NO
4 3
9.【2020年7月浙江选考】下列说法不正确的是( )
A.Cl-会破坏铝表面的氧化膜
B.NaHCO 的热稳定性比Na CO 强
3 2 3C.KMnO 具有氧化性,其稀溶液可用于消毒
4
D.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
10.【2020年7月浙江选考】下列说法不正确的是( )
A.高压钠灯可用于道路照明
B.SiO 可用来制造光导纤维
2
C.工业上可采用高温冶炼黄铜矿的方法获得粗铜
D.BaCO 不溶于水,可用作医疗上检查肠胃的钡餐
3
11.【2020年7月浙江选考】下列说法正确的是( )
A.Na O在空气中加热可得固体Na O
2 2 2
B.Mg加入到过量FeCl 溶液中可得Fe
3
C.FeS 在沸腾炉中与O 反应主要生成SO
2 2 3
D.H O 溶液中加入少量MnO 粉末生成H 和O
2 2 2 2 2
12.(2016·浙江高考真题)下列有关钠及其化合物的说法不正确的是
A.电解饱和食盐水可制取金属钠 B.钠与氧气反应的产物与反应条件有关
C.氧化钠与水反应生成氢氧化钠 D.钠可以从四氯化钛中置换出钛
13.(2020·全国高考真题)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实
4 3
验:① 混合物溶于水,得到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液
中加碱,产生白色沉淀。根据实验现象可判断其组成为
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
14.(2018·全国高考真题)化学与生活密切相关。下列说法错误的是
A.碳酸钠可用于去除餐具的油污 B.漂白粉可用于生活用水的消毒
C.氢氧化铝可用于中和过多胃酸 D.碳酸钡可用于胃肠X射线造影检查
15.【2014年高考上海卷第 19题】下列反应与 NaO +SO →NaSO 相比较,NaO 的作用相同的是
2 2 2 2 4 2 2
( )
A.2NaO+2CO→2NaCO+O B.2NaO+2SO →2NaSO +O
2 2 2 2 3 2 2 2 3 2 4 2
C.2NaO+HSO →NaSO +HO D.3NaO+Cr O→2NaCrO+NaO
2 2 2 4 2 4 2 2 2 2 2 3 2 4 2
16.【2016年高考新课标Ⅱ卷】某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为
A.NaHCO 、Al(OH) B.AgCl、NaHCO C.NaSO 、BaCO D.NaCO、CuSO
3 3 3 2 3 3 2 3 4
17.【2014年高考福建卷第6题】下列有关物质应用的说法正确的是( )
A.生石灰用作食品抗氧剂 B.盐类都可作调味品
C.铝罐可久盛食醋 D.小苏打是面包发酵粉的主要成分
18.【2016年高考新课标Ⅲ卷】化学在生活中有着广泛的应用,下列对应关系错误的是( )化学性质 实际应用
A. Al (SO ) 和小苏打反应 泡沫灭火器灭火
2 4 3
B. 铁比铜金属性强 FeCl 腐蚀Cu刻制印刷电路板
3
C. 次氯酸盐具有氧化性 漂白粉漂白织物
D. HF与SiO 反应 氢氟酸在玻璃器皿上刻蚀标记
2
19.(2010·安徽高考真题)将0.01mol下列物质分别加入100mL蒸馏水中,恢复至室温,所得溶液中阴离
子浓度的大小顺序是(溶液体积变化忽略不计)
①NaO ②NaO ③NaCO ④NaCl
2 2 2 2 3
A.①>②>③>④ B.①>②>④>③
C.①=②>③>④ D.①=②>③=④
20.【2022年6月浙江卷】回答下列问题:
(1)乙醇的挥发性比水的强,原因是_______。
(2)金属氢化物是应用广泛的还原剂。KH的还原性比NaH的强,原因是_______。