文档内容
河南省中原名校联盟2024届高三上学期9月调研考试
化 学
全卷满分100分,考试时间90分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答
题卡上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上
的非答题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答
题卡上作答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
5.本卷主要考查内容:物质及其变化,物质的量,金属及其化合物。
可能用到的相对原子质量:H 1 Li 7 C 12 O 16 Na 23 Mg 24 Al 27 P 31
S 32 Fe 56
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与人类生活、社会可持续发展密切相关,下列说法错误的是
A.神舟飞船的轨道舱壳体采用了铝合金材料,铝合金具有密度小、抗腐蚀性能好等特
性
B.利用CO 合成淀粉有助于实现“碳达峰”和“碳中和”
2
C.燃煤中加入CaO主要是为了减少温室气体的排放和酸雨的形成
D.丝绸的主要原料为蚕丝,其主要成分是蛋白质
2.分类是科学研究的重要方法,下列物质分类错误的是
A.化合物:干冰、烧碱、小苏打
B.碱性氧化物:氧化钙、氧化铁、过氧化钠
C.同素异形体:C 、石墨、金刚石
60
D.混合物:空气、硫酸铜溶液、汽油
3.构建知识网络是一种重要的学习方法。如图是关于盐酸化
学性质的知识网络图,“-”表示相连的两种物质能发生
反应,“→”表示一种物质能转化为另一种物质。若A、
B、C分别属于不同类别的化合物,则A、B、C可能是
A.CuO、Ba(OH)、CuSO
2 4
B.KOH、FeCl 、NaCO
3 2 3
C.NaOH、HNO、KCO
3 2 3
D.NaOH、Ba(NO )、HSO
3 2 2 4
4.电导率可用于衡量电解质溶液导电能力的大小。室温下,用
学科网(北京)股份有限公司0.100 mol·L-1NH ·H O溶液滴定10 mL浓度均为0.100 mol·L-1HCl和CHCOOH
3 2 3
的混合液,电导率曲线如图所示。下列说法正确的是
A.①点溶液中,c(H+)为0.200 mol·L-1
B.溶液温度高低为①点>③点>②点
C.③点后溶液的电导率逐渐降低,是因为溶液中离子数目逐渐减小
D.③点溶液中有c(Cl-)>c(CHCOO-)
3
5.能正确表示下列反应的离子方程式为
A.向Ca(HCO ) 溶液中滴入少量NaOH溶液: +Ca2++OH- CaCO ↓
3 2 3
+HO
2
B.明矾溶于水产生Al(OH) 胶体:Al3++3HO Al(OH)↓+3H+
3 2 3
C.NaO 溶于水产生O:NaO+HO 2Na++2OH-+O↑
2 2 2 2 2 2 2
△
D.向MnO 中滴入浓盐酸并加热:MnO +4HCl(浓) Mn2++2Cl-+Cl↑+
2 2 2
2HO
2
6.高铜酸钾(KCuO )是一种难溶于水的黑色粉末状固体,与高铁酸钾(KFeO )性质相
2 2 4
似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:① K[Cu(OH) ]+HBrO
2 4
KCuO +KBr+KBrO+HO(未配平)。高铜酸钾在酸性条件下不稳定:
2 2
②KCuO +HSO O↑+CuSO +H O+KSO (未配平)。下列说法错误的是
2 2 4 2 4 2 2 4
A.①中还原剂和氧化剂的物质的量之比为2 :1
B.②若有标准状况下5.6 L O 生成,则转移电子0.5 mol
2
C.②中KCuO 既表现氧化性,又表现还原性
2
D.由①、②可知氧化性强弱顺序为HBrO>KCuO >O
2 2
7.设N 为阿伏加德罗常数的值。下列说法错误的是
A
A.3.9 g NaO 晶体中阴离子的数目为0.05N
2 2 A
B.标准状况下,2.24 L HO中含有的原子数目为0.3N
2 A
C.18 g C 和石墨的混合物中含有的碳原子数目为1.5N
60 A
D.1 L 0.2 mol·L-1 NaOH溶液与足量的Al反应,生成的H 分子数为0.3N
2 A
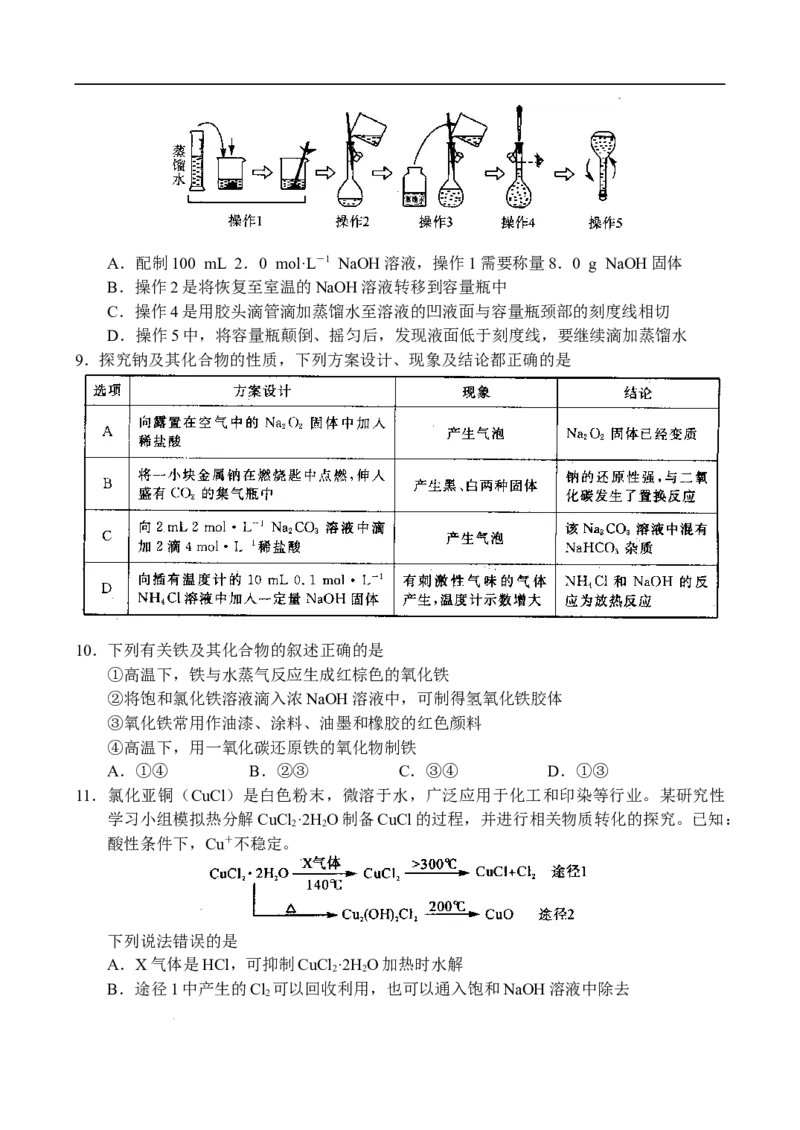
8.下图是配制一定物质的量浓度溶液的过程示意图。下列说法错误的是
学科网(北京)股份有限公司A.配制100 mL 2.0 mol·L-1 NaOH溶液,操作1需要称量8.0 g NaOH固体
B.操作2是将恢复至室温的NaOH溶液转移到容量瓶中
C.操作4是用胶头滴管滴加蒸馏水至溶液的凹液面与容量瓶颈部的刻度线相切
D.操作5中,将容量瓶颠倒、摇匀后,发现液面低于刻度线,要继续滴加蒸馏水
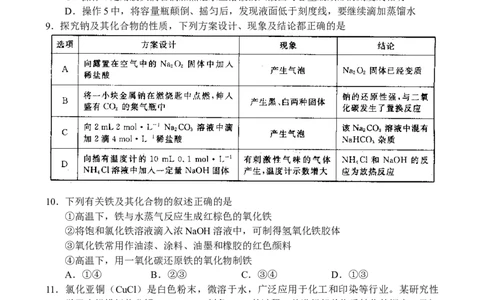
9.探究钠及其化合物的性质,下列方案设计、现象及结论都正确的是
10.下列有关铁及其化合物的叙述正确的是
①高温下,铁与水蒸气反应生成红棕色的氧化铁
②将饱和氯化铁溶液滴入浓NaOH溶液中,可制得氢氧化铁胶体
③氧化铁常用作油漆、涂料、油墨和橡胶的红色颜料
④高温下,用一氧化碳还原铁的氧化物制铁
A.①④ B.②③ C.③④ D.①③
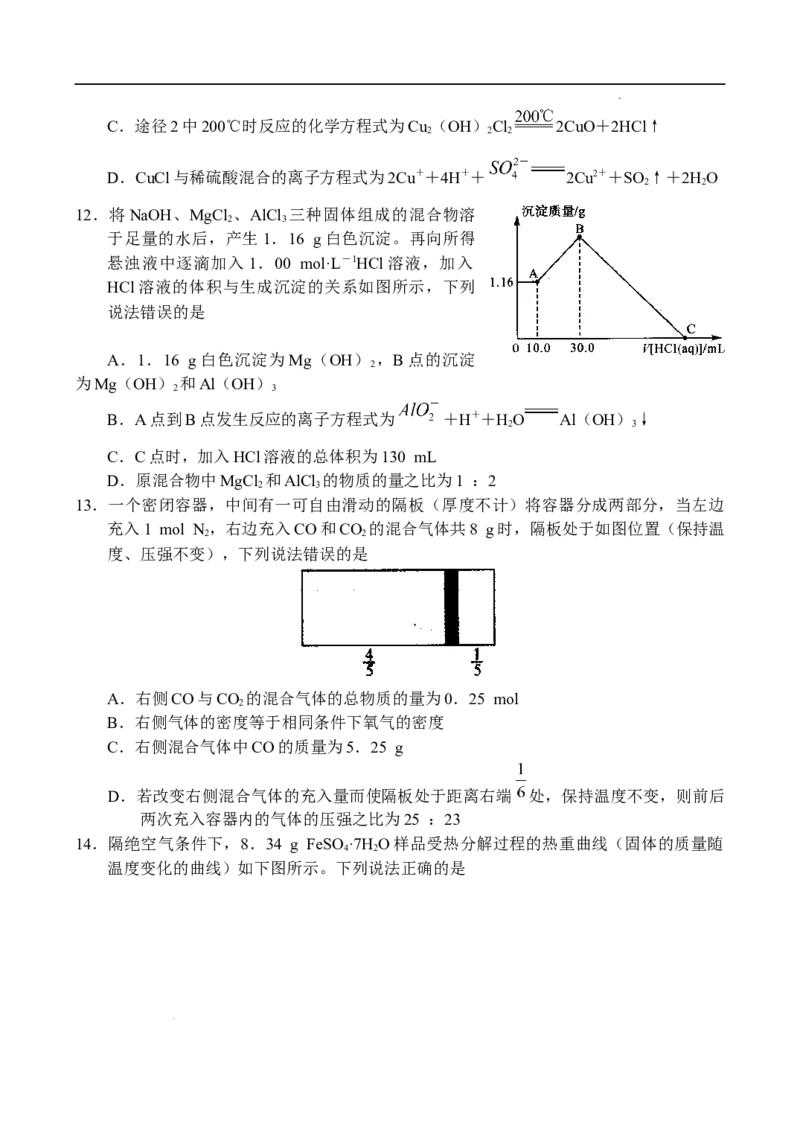
11.氯化亚铜(CuCl)是白色粉末,微溶于水,广泛应用于化工和印染等行业。某研究性
学习小组模拟热分解CuCl ·2H O制备CuCl的过程,并进行相关物质转化的探究。已知:
2 2
酸性条件下,Cu+不稳定。
下列说法错误的是
A.X气体是HCl,可抑制CuCl ·2H O加热时水解
2 2
B.途径1中产生的Cl 可以回收利用,也可以通入饱和NaOH溶液中除去
2
学科网(北京)股份有限公司C.途径2中200℃时反应的化学方程式为Cu (OH)Cl 2CuO+2HCl↑
2 2 2
D.CuCl与稀硫酸混合的离子方程式为2Cu++4H++ 2Cu2++SO ↑+2HO
2 2
12.将NaOH、MgCl 、AlCl 三种固体组成的混合物溶
2 3
于足量的水后,产生1.16 g白色沉淀。再向所得
悬浊液中逐滴加入1.00 mol·L-1HCl溶液,加入
HCl溶液的体积与生成沉淀的关系如图所示,下列
说法错误的是
A.1.16 g白色沉淀为Mg(OH) ,B点的沉淀
2
为Mg(OH) 和Al(OH)
2 3
B.A点到B点发生反应的离子方程式为 +H++HO Al(OH)↓
2 3
C.C点时,加入HCl溶液的总体积为130 mL
D.原混合物中MgCl 和AlCl 的物质的量之比为1 :2
2 3
13.一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边
充入1 mol N,右边充入CO和CO 的混合气体共8 g时,隔板处于如图位置(保持温
2 2
度、压强不变),下列说法错误的是
A.右侧CO与CO 的混合气体的总物质的量为0.25 mol
2
B.右侧气体的密度等于相同条件下氧气的密度
C.右侧混合气体中CO的质量为5.25 g
D.若改变右侧混合气体的充入量而使隔板处于距离右端 处,保持温度不变,则前后
两次充入容器内的气体的压强之比为25 :23
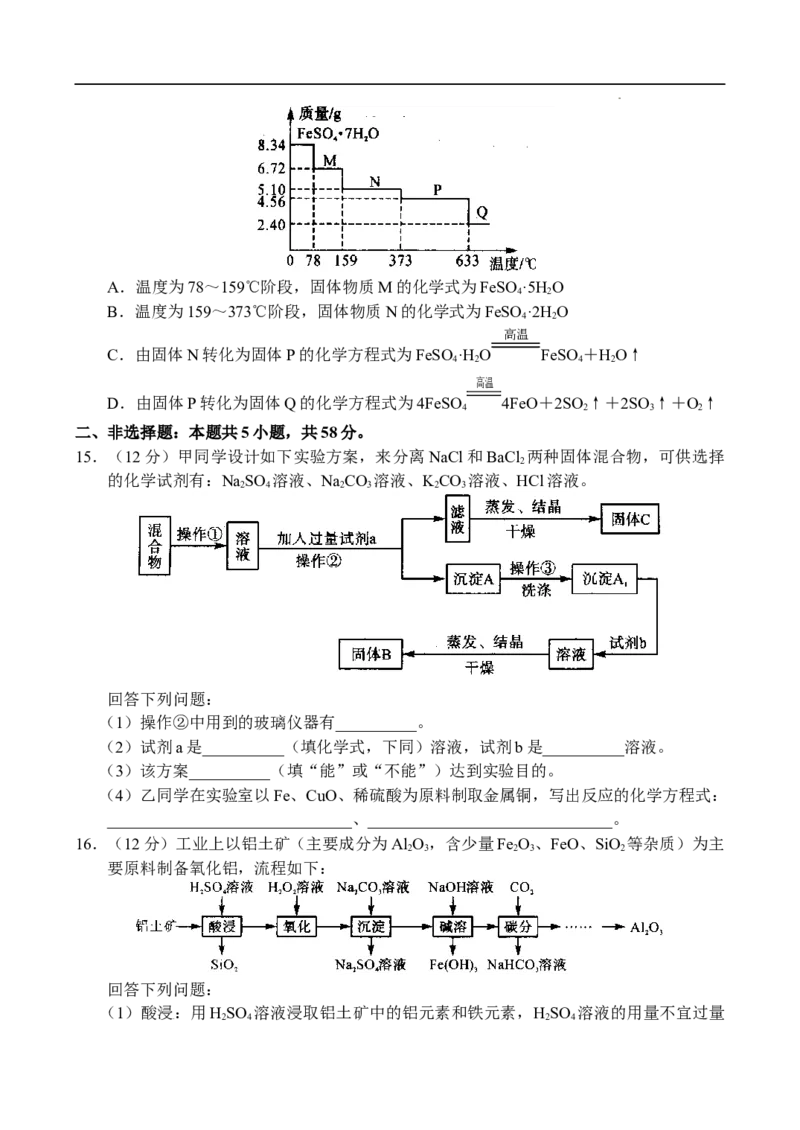
14.隔绝空气条件下,8.34 g FeSO ·7H O样品受热分解过程的热重曲线(固体的质量随
4 2
温度变化的曲线)如下图所示。下列说法正确的是
学科网(北京)股份有限公司A.温度为78~159℃阶段,固体物质M的化学式为FeSO ·5H O
4 2
B.温度为159~373℃阶段,固体物质N的化学式为FeSO ·2H O
4 2
高温
C.由固体N转化为固体P的化学方程式为FeSO
4
·H
2
O FeSO
4
+H
2
O↑
高温
D.由固体P转化为固体Q的化学方程式为4FeSO
4
4FeO+2SO
2
↑+2SO
3
↑+O
2
↑
二、非选择题:本题共5小题,共58分。
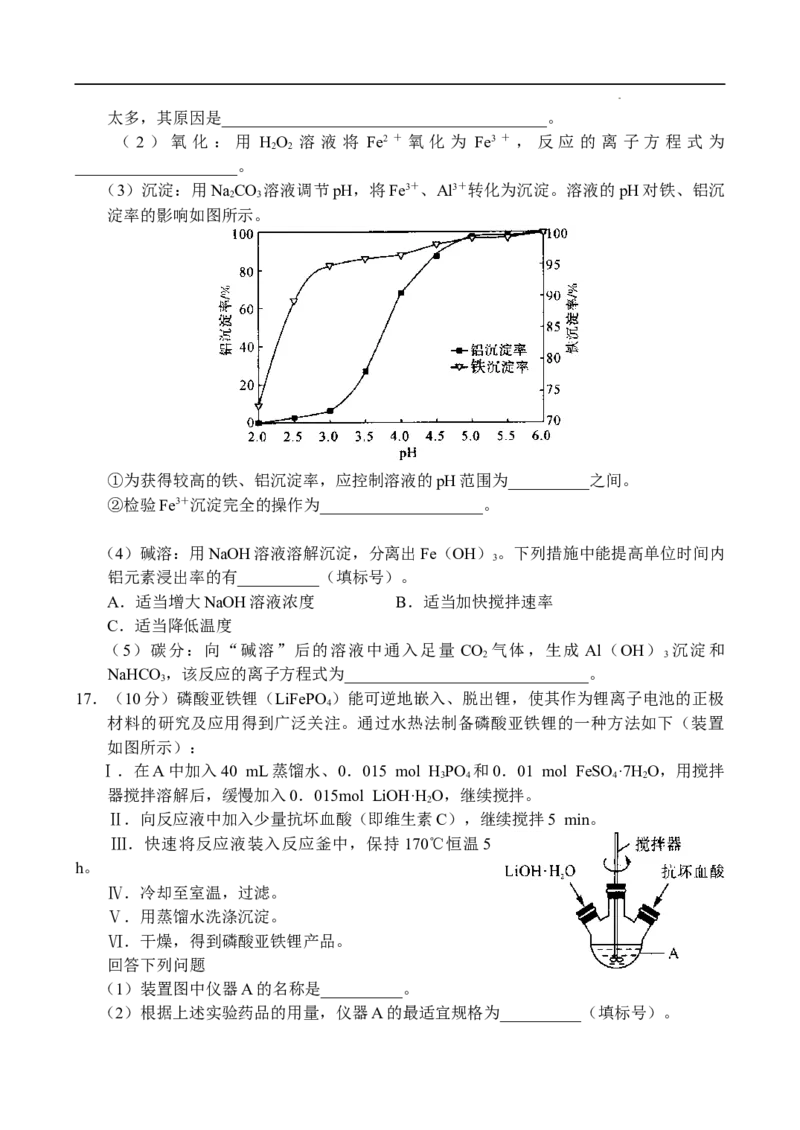
15.(12分)甲同学设计如下实验方案,来分离NaCl和BaCl 两种固体混合物,可供选择
2
的化学试剂有:NaSO 溶液、NaCO 溶液、KCO 溶液、HCl溶液。
2 4 2 3 2 3
回答下列问题:
(1)操作②中用到的玻璃仪器有__________。
(2)试剂a是__________(填化学式,下同)溶液,试剂b是__________溶液。
(3)该方案__________(填“能”或“不能”)达到实验目的。
(4)乙同学在实验室以Fe、CuO、稀硫酸为原料制取金属铜,写出反应的化学方程式:
______________________________、______________________________。
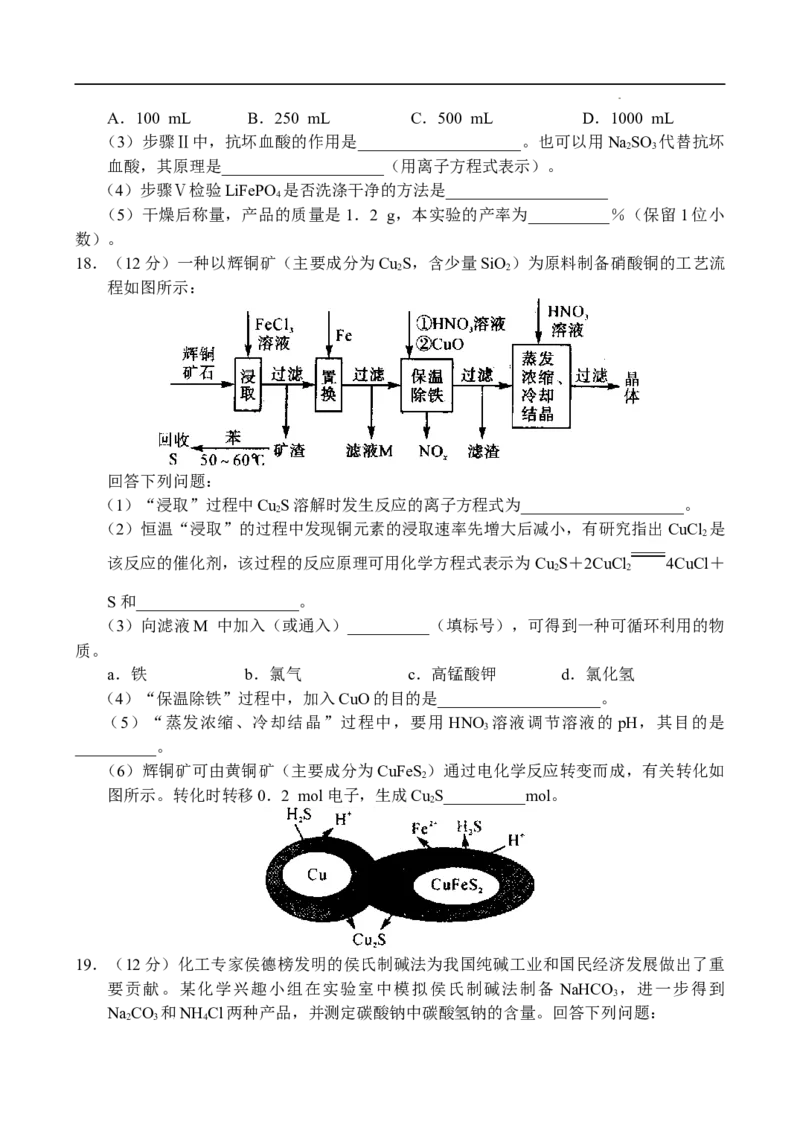
16.(12分)工业上以铝土矿(主要成分为Al O,含少量Fe O、FeO、SiO 等杂质)为主
2 3 2 3 2
要原料制备氧化铝,流程如下:
回答下列问题:
(1)酸浸:用HSO 溶液浸取铝土矿中的铝元素和铁元素,HSO 溶液的用量不宜过量
2 4 2 4
学科网(北京)股份有限公司太多,其原因是________________________________________。
( 2 ) 氧 化 : 用 HO 溶 液 将 Fe2 + 氧 化 为 Fe3 + , 反 应 的 离 子 方 程 式 为
2 2
____________________。
(3)沉淀:用NaCO 溶液调节pH,将Fe3+、Al3+转化为沉淀。溶液的pH对铁、铝沉
2 3
淀率的影响如图所示。
①为获得较高的铁、铝沉淀率,应控制溶液的pH范围为__________之间。
②检验Fe3+沉淀完全的操作为____________________。
(4)碱溶:用NaOH溶液溶解沉淀,分离出Fe(OH)。下列措施中能提高单位时间内
3
铝元素浸出率的有__________(填标号)。
A.适当增大NaOH溶液浓度 B.适当加快搅拌速率
C.适当降低温度
(5)碳分:向“碱溶”后的溶液中通入足量 CO 气体,生成 Al(OH) 沉淀和
2 3
NaHCO ,该反应的离子方程式为______________________________。
3
17.(10分)磷酸亚铁锂(LiFePO )能可逆地嵌入、脱出锂,使其作为锂离子电池的正极
4
材料的研究及应用得到广泛关注。通过水热法制备磷酸亚铁锂的一种方法如下(装置
如图所示):
Ⅰ.在A中加入40 mL蒸馏水、0.015 mol HPO 和0.01 mol FeSO ·7H O,用搅拌
3 4 4 2
器搅拌溶解后,缓慢加入0.015mol LiOH·H O,继续搅拌。
2
Ⅱ.向反应液中加入少量抗坏血酸(即维生素C),继续搅拌5 min。
Ⅲ.快速将反应液装入反应釜中,保持170℃恒温5
h。
Ⅳ.冷却至室温,过滤。
Ⅴ.用蒸馏水洗涤沉淀。
Ⅵ.干燥,得到磷酸亚铁锂产品。
回答下列问题
(1)装置图中仪器A的名称是__________。
(2)根据上述实验药品的用量,仪器A的最适宜规格为__________(填标号)。
学科网(北京)股份有限公司A.100 mL B.250 mL C.500 mL D.1000 mL
(3)步骤Ⅱ中,抗坏血酸的作用是____________________。也可以用NaSO 代替抗坏
2 3
血酸,其原理是____________________(用离子方程式表示)。
(4)步骤Ⅴ检验LiFePO 是否洗涤干净的方法是____________________
4
(5)干燥后称量,产品的质量是1.2 g,本实验的产率为__________%(保留1位小
数)。
18.(12分)一种以辉铜矿(主要成分为Cu S,含少量SiO )为原料制备硝酸铜的工艺流
2 2
程如图所示:
回答下列问题:
(1)“浸取”过程中Cu S溶解时发生反应的离子方程式为____________________。
2
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减小,有研究指出CuCl 是
2
该反应的催化剂,该过程的反应原理可用化学方程式表示为Cu S+2CuCl 4CuCl+
2 2
S和____________________。
(3)向滤液M 中加入(或通入)__________(填标号),可得到一种可循环利用的物
质。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(4)“保温除铁”过程中,加入CuO的目的是____________________。
(5)“蒸发浓缩、冷却结晶”过程中,要用 HNO 溶液调节溶液的pH,其目的是
3
__________。
(6)辉铜矿可由黄铜矿(主要成分为CuFeS )通过电化学反应转变而成,有关转化如
2
图所示。转化时转移0.2 mol电子,生成Cu S__________mol。
2
19.(12分)化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重
要贡献。某化学兴趣小组在实验室中模拟侯氏制碱法制备 NaHCO ,进一步得到
3
NaCO 和NH Cl两种产品,并测定碳酸钠中碳酸氢钠的含量。回答下列问题:
2 3 4
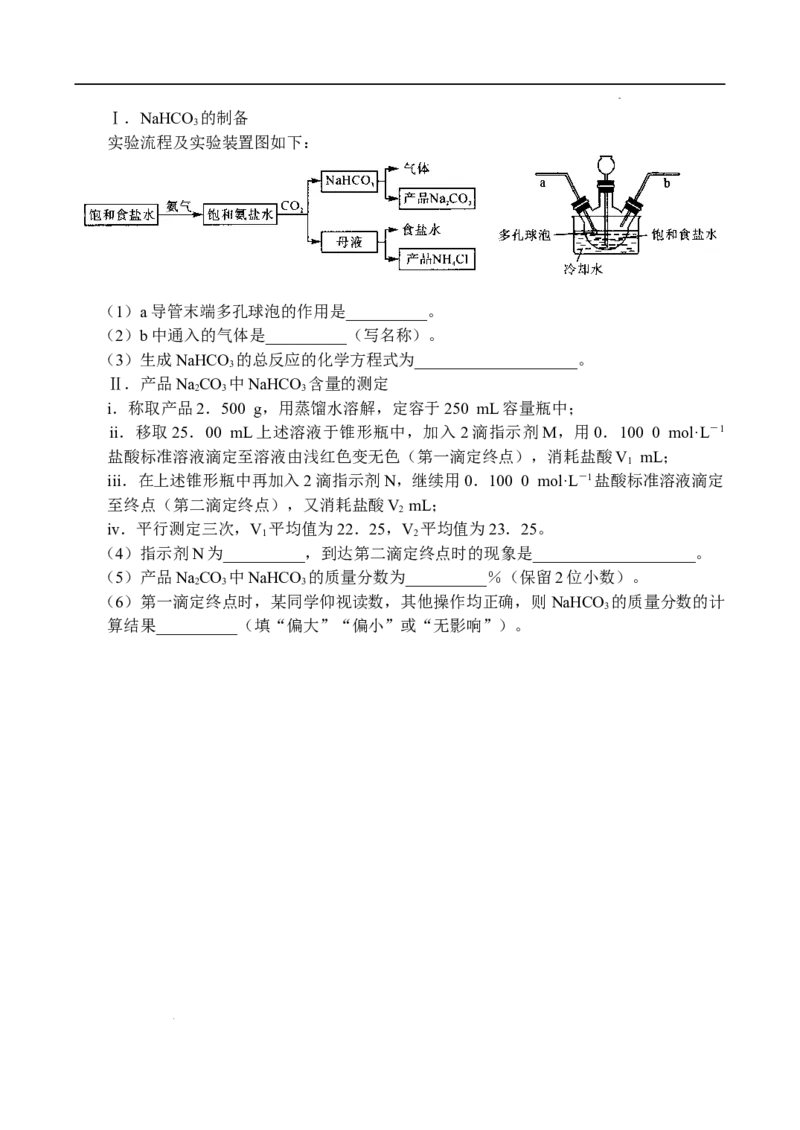
学科网(北京)股份有限公司Ⅰ.NaHCO 的制备
3
实验流程及实验装置图如下:
(1)a导管末端多孔球泡的作用是__________。
(2)b中通入的气体是__________(写名称)。
(3)生成NaHCO 的总反应的化学方程式为____________________。
3
Ⅱ.产品NaCO 中NaHCO 含量的测定
2 3 3
i.称取产品2.500 g,用蒸馏水溶解,定容于250 mL容量瓶中;
ii.移取25.00 mL上述溶液于锥形瓶中,加入2滴指示剂M,用0.100 0 mol·L-1
盐酸标准溶液滴定至溶液由浅红色变无色(第一滴定终点),消耗盐酸V mL;
1
iii.在上述锥形瓶中再加入2滴指示剂N,继续用0.100 0 mol·L-1盐酸标准溶液滴定
至终点(第二滴定终点),又消耗盐酸V mL;
2
iv.平行测定三次,V 平均值为22.25,V 平均值为23.25。
1 2
(4)指示剂N为__________,到达第二滴定终点时的现象是____________________。
(5)产品NaCO 中NaHCO 的质量分数为__________%(保留2位小数)。
2 3 3
(6)第一滴定终点时,某同学仰视读数,其他操作均正确,则NaHCO 的质量分数的计
3
算结果__________(填“偏大”“偏小”或“无影响”)。
学科网(北京)股份有限公司学科网(北京)股份有限公司