文档内容
姓名______ 座位号______
(在此卷上答题无效)
化 学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2B铅笔把答题卡上
对应题目的答案标号涂黑;非选择题请用直径 0.5毫米黑色墨水签字笔在答题卡上各题的答
题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:H 1 Li 7 Mg 24 Al 27 Cl 35.5 Cr 52 Zr 91
一、单项选择题:共14小题,每题3分,共42分。每题只有一个选项符合题意。
1.“福建号”航母下水、“太空之家”遨游苍穹、“神州飞船”接力腾飞、国产“C919”大飞机正式交
付都彰显了中国科技力量。下列成果所涉及的材料为金属材料的是( )
A.“福建号”航母使用的高强度甲板材料——合金钢
B.“天宫”空间站使用的太阳能电池板材料——砷化镓
C.“神州十五”号飞船使用的耐辐照光学窗材料——石英玻璃
D.“C919”大飞机使用的机身复合材料——碳纤维和环氧树脂
2.化学与生活息息相关,下列说法错误的是( )
A.漂粉精可用于游泳池的消毒
B.葡萄糖在酒化酶的作用下发生水解反应生成乙醇
C.将 还原为甲醇,有利于实现“碳中和”
D.“复方氯乙烷”气雾剂可用于运动中急性损伤的镇痛
3.科学家发现了铝的“超级原子”结构 和 。已知这类“超级原子”最外层电子数之和为40时处
于相对稳定状态。下列说法正确的是( )
A. 和 互为同位素
B.镁能与 反应生成
C. 中Al原子之间通过离子键结合
D.等质量的 和 中含有的铝原子个数比为14∶13
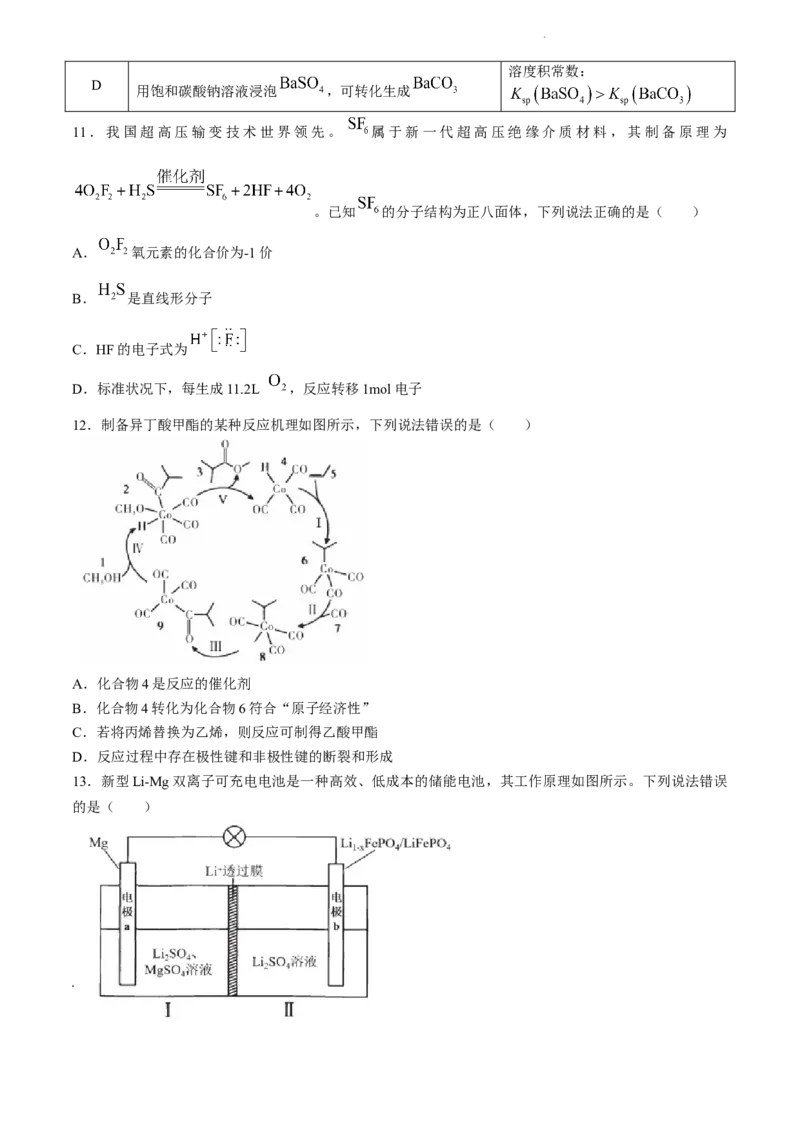
4.常用于治疗心律失常药物的有效成分为 ,合成该有机物的主要过程:
学科网(北京)股份有限公司下列叙述正确的是( )
A.X中所有原子一定共平面 B.Y中碳原子只有一种杂化方式
C.Z存在顺式异构体 D.1mol Z最多可以和6mol氢气发生加成反应
阅读下列材料,回答5—6小题。
卤族元素形成物质种类众多,溴化碘(IBr)的化学性质与卤素相似。已知常温下,几种酸的电离常数:
, ;HClO 。
5.下列化学反应表示正确的是( )
A.IBr与水反应:
B. 溶液中加入过量NaOH溶液:
C.AgCl悬浊液中加入 溶液:
D.向NaClO溶液中通入少量 :
6. 和 均是化工中重要的化合物。已知 的熔点是-107℃, 的熔点是-40℃。下列说法
正确的是( )
A.键角:
B.两者均为极性分子
C.两者在液态时均具有良好的导电性
D. 键能比 键能大, 的熔点高于-40℃
7.下列实验装置、试剂选用或操作正确的是( )
学科网(北京)股份有限公司A.用图甲装置收集 B.用图乙装置制备、干燥并收集
C.用图丙装置制备 固体 D.用图丁装置探究浓度对反应速率的影响
8.TFMT因具有成本低廉及反应性质多样等优点被用作有机合成的缩合试剂,其结构如图所示,其中
W、X、Y、Z为原子半径依次增大的短周期非金属元素,W位于元素周期表的p区。下列说法错误的是(
)
A.元素电负性:W>X>Y B.基态原子未成对电子数:Y=Z>W
C.所有原子都满足8电子结构 D.简单氢化物沸点:X>W>Y
9.汽车尾气的排放会对环境造成污染。利用高效催化剂处理汽车尾气中的 NO 与 CO 的反应为
。一定温度下,在 1L恒容密闭容器中加入 1mol
CO和1mol NO发生上述反应,部分物质的体积分数( )随时间(t)的变化如图所示。下列说法正确的
是( )
A.曲线Ⅱ表示的是 随时间的变化
B. min时,反应达到化学平衡状态
C.增大压强,该平衡右移,平衡常数增大
D.0~t4时间段内的平均反应速率为:
10.根据下列实验事实能得出相应结论的是( )
选项 实验事实 结论
A
向 溶液中通入 气体,生成CuS和 酸性:
相同条件下Na分别与水和乙醇反应,前者产生气体的速
B 羟基氢原子的活泼性:水>乙醇
率更快
C 分子的键能比 分子的键能小 键长:
学科网(北京)股份有限公司溶度积常数:
D
用饱和碳酸钠溶液浸泡 ,可转化生成
11.我国超高压输变技术世界领先。 属于新一代超高压绝缘介质材料,其制备原理为
。已知 的分子结构为正八面体,下列说法正确的是( )
A. 氧元素的化合价为-1价
B. 是直线形分子
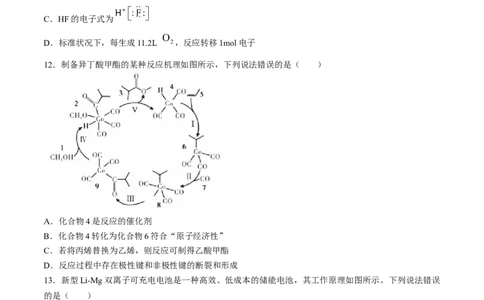
C.HF的电子式为
D.标准状况下,每生成11.2L ,反应转移1mol电子
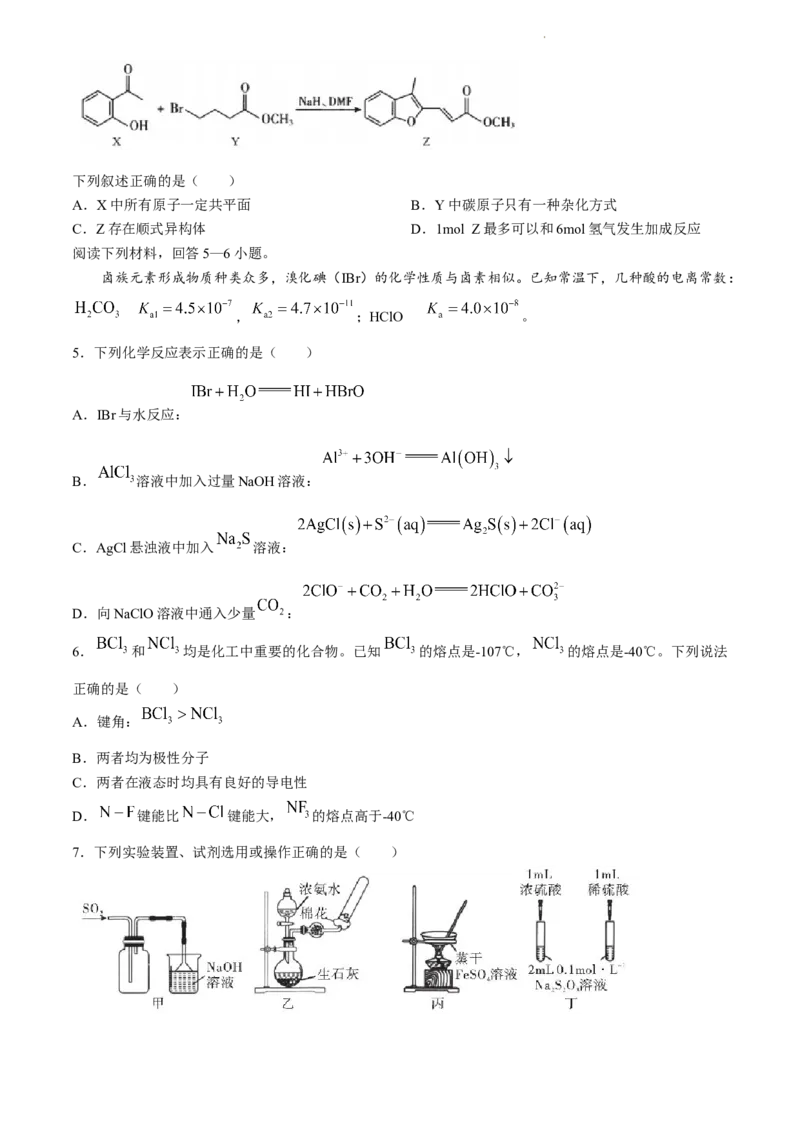
12.制备异丁酸甲酯的某种反应机理如图所示,下列说法错误的是( )
A.化合物4是反应的催化剂
B.化合物4转化为化合物6符合“原子经济性”
C.若将丙烯替换为乙烯,则反应可制得乙酸甲酯
D.反应过程中存在极性键和非极性键的断裂和形成
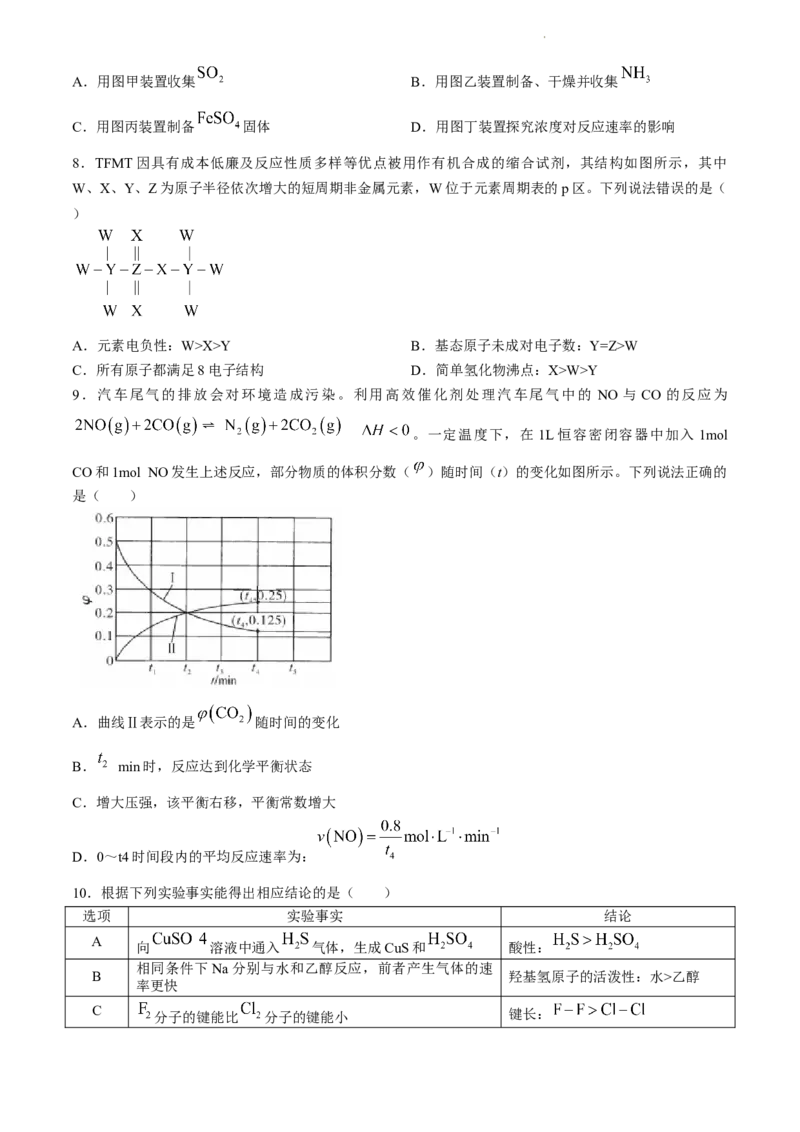
13.新型Li-Mg双离子可充电电池是一种高效、低成本的储能电池,其工作原理如图所示。下列说法错误
的是( )
学科网(北京)股份有限公司A.放电时,电极a发生氧化反应
B.放电时,电极b反应为:
C.充电时,Ⅱ室 溶液的浓度不变
D.充电时,电极a质量增加24g,电极b质量理论上减少7g
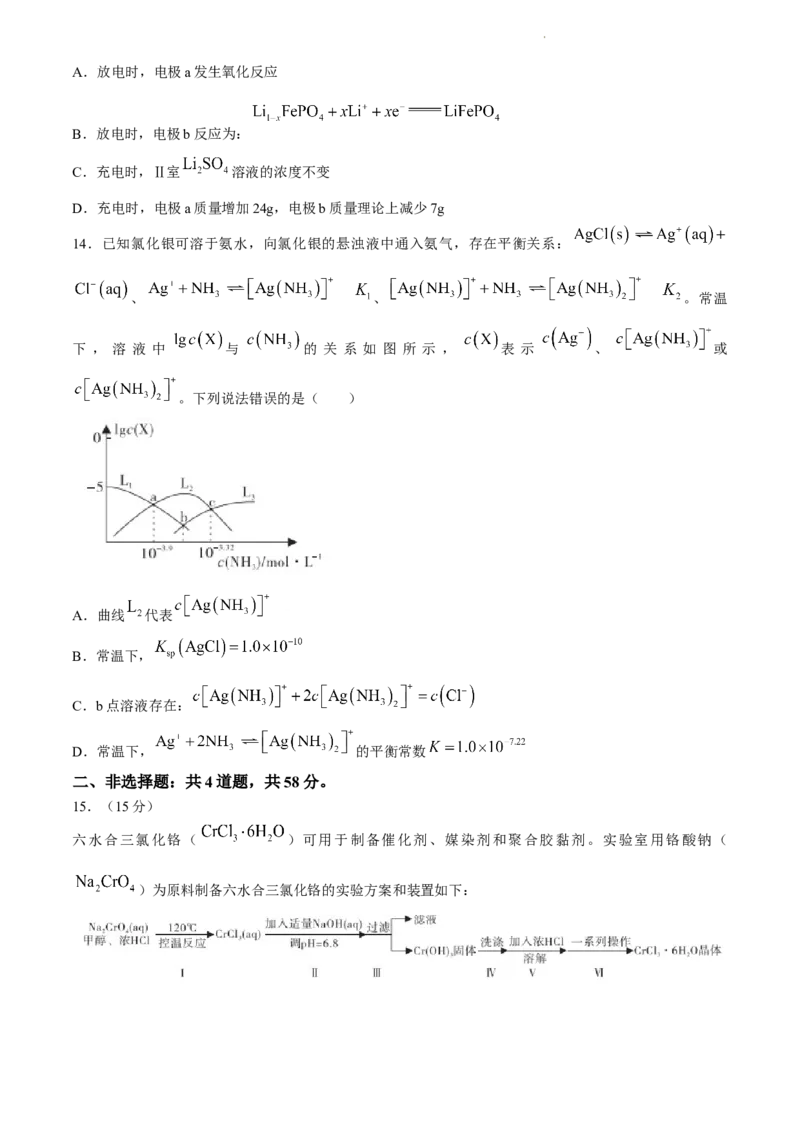
14.已知氯化银可溶于氨水,向氯化银的悬浊液中通入氨气,存在平衡关系:
、 、 。常温
下 , 溶 液 中 与 的 关 系 如 图 所 示 , 表 示 、 或
。下列说法错误的是( )
A.曲线 代表
B.常温下,
C.b点溶液存在:
D.常温下, 的平衡常数
二、非选择题:共4道题,共58分。
15.(15分)
六水合三氯化铬( )可用于制备催化剂、媒染剂和聚合胶黏剂。实验室用铬酸钠(
)为原料制备六水合三氯化铬的实验方案和装置如下:
学科网(北京)股份有限公司已知:①甲醇沸点61.7℃。②六水合三氯化铬易溶于水、可溶于乙醇、不溶于乙醚。③ 的性质
与 类似。
回答下列问题:
(1)仪器a的名称为______;步骤Ⅰ中使用该仪器的作用是______。
(2)步骤Ⅰ反应生成 的同时有 气体逸出,反应的化学方程式为______。
(3)步骤Ⅱ中调节溶液pH不能加入过量NaOH的原因是______(用离子方程式解释)。
(4)步骤Ⅳ中洗涤 固体的方法是______。
(5)步骤Ⅵ中“一系列操作”包括加热浓缩、冷却结晶、过滤、用少量______洗涤、低温烘干。
(6)用碘量法测定产品纯度。称取6.0g产品,在强碱性条件下,加入过量 溶液,小火加热使
完全转化为 ,再继续加热煮沸一段时间。冷却至室温后,滴入适量稀硫酸使 转化为 ,
再加入蒸馏水将溶液稀释至250mL。取25.00mL溶液,加入过量KI溶液,滴加2-3滴淀粉溶液,用0.3000
标准溶液滴定,发生反应: ,三次平行实验测得消耗
标准溶液体积的数据如下:
第1次 第2次 第3次
20.05mL 20.30mL 19.95mL
①“继续加热煮沸一段时间”的目的是______。
②滴定终点的现象为______。
③该产品的纯度为______%(结果保留1位小数)。
16.(14分)
锂离子电池给生活带来了便利,但数量巨大的废旧锂电池的处理问题也日益显现。对废旧锂离子电池的有
效回收,不仅具有巨大的社会、经济效益,而且还可以缓解我国钴和锂等矿产资源紧缺的压力。以某废旧
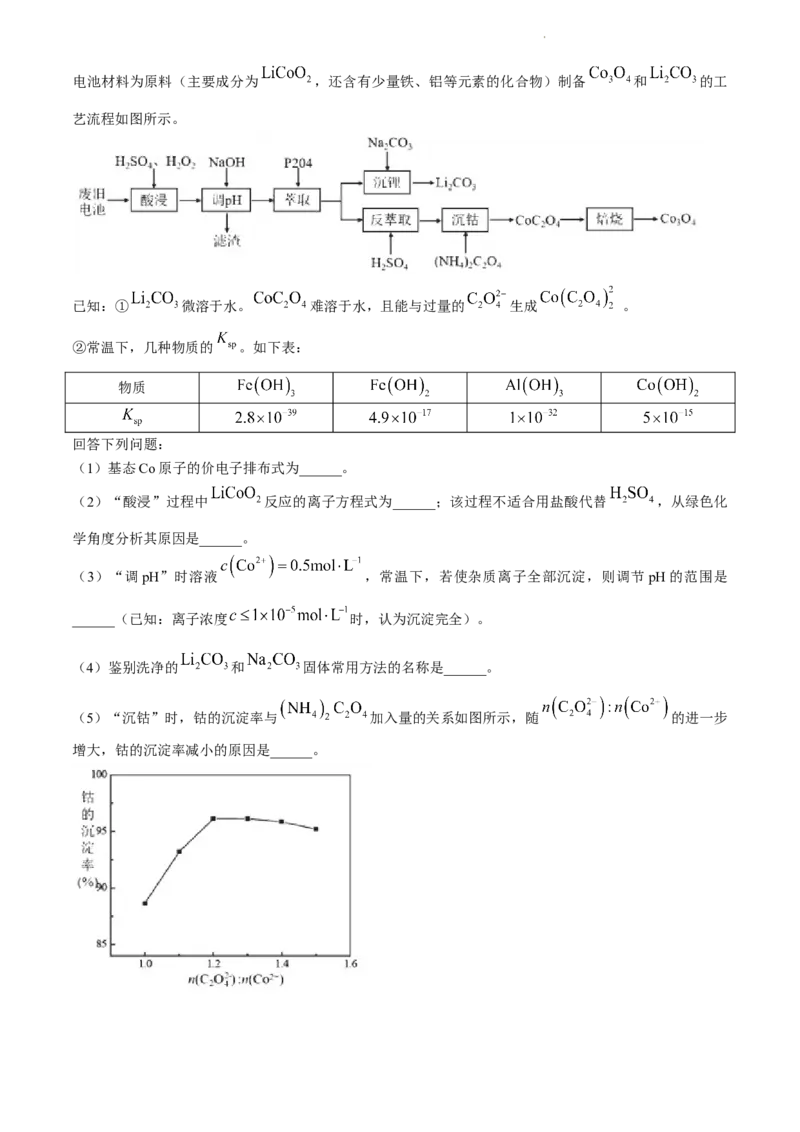
学科网(北京)股份有限公司电池材料为原料(主要成分为 ,还含有少量铁、铝等元素的化合物)制备 和 的工
艺流程如图所示。
已知:① 微溶于水。 难溶于水,且能与过量的 生成 。
②常温下,几种物质的 。如下表:
物质
回答下列问题:
(1)基态Co原子的价电子排布式为______。
(2)“酸浸”过程中 反应的离子方程式为______;该过程不适合用盐酸代替 ,从绿色化
学角度分析其原因是______。
(3)“调pH”时溶液 ,常温下,若使杂质离子全部沉淀,则调节pH的范围是
______(已知:离子浓度 时,认为沉淀完全)。
(4)鉴别洗净的 和 固体常用方法的名称是______。
(5)“沉钴”时,钴的沉淀率与 加入量的关系如图所示,随 的进一步
增大,钴的沉淀率减小的原因是______。
学科网(北京)股份有限公司(6) 在空气中“焙烧”转化为 的化学方程式为______。
17.(14分)
异丁烯是一种重要的化工原料,主要用于生产橡胶、催化剂、汽油添加剂和润滑油等。工业上常用异丁烷
为原料制备异丁烯。回答下列问题:
(1)异丁烷直接脱氢制备异丁烯,反应为
根据下列键能数据,计算该反应的 ______ 。
化学键
键能/(
348 615 413 436
)
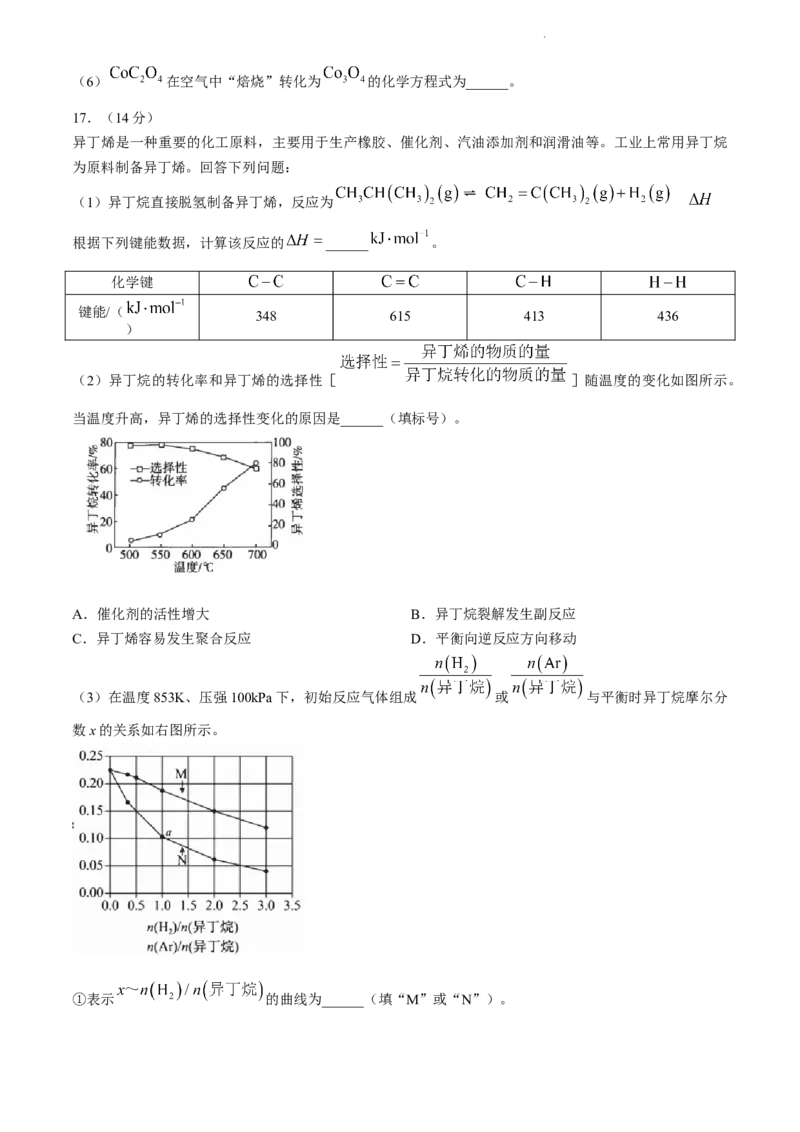
(2)异丁烷的转化率和异丁烯的选择性[ ]随温度的变化如图所示。
当温度升高,异丁烯的选择性变化的原因是______(填标号)。
A.催化剂的活性增大 B.异丁烷裂解发生副反应
C.异丁烯容易发生聚合反应 D.平衡向逆反应方向移动
(3)在温度853K、压强100kPa下,初始反应气体组成 或 与平衡时异丁烷摩尔分
数x的关系如右图所示。
①表示 的曲线为______(填“M”或“N”)。
学科网(北京)股份有限公司②a点反应的平衡常数 ______kPa(列出计算式,分压=总压×物质的量分数)。
( 4 ) 有 人 提 出 加 入 适 量 空 气 , 采 用 异 丁 烷 氧 化 脱 氢 制 备 异 丁 烯 , 反 应 为
,与异丁烷
直接脱氢制备异丁烯相比,该方法的优缺点有______。
(5)一种 基催化剂可高效催化异丁烷直接脱氢制备异丁烯。四方 晶胞如图所示,晶胞参数为
a pm、a pm、c pm。 离子在晶胞中的配位数是______,该晶体的密度为______ (列出计算
式,阿伏加德罗常数的值为 )。
18.(15分)
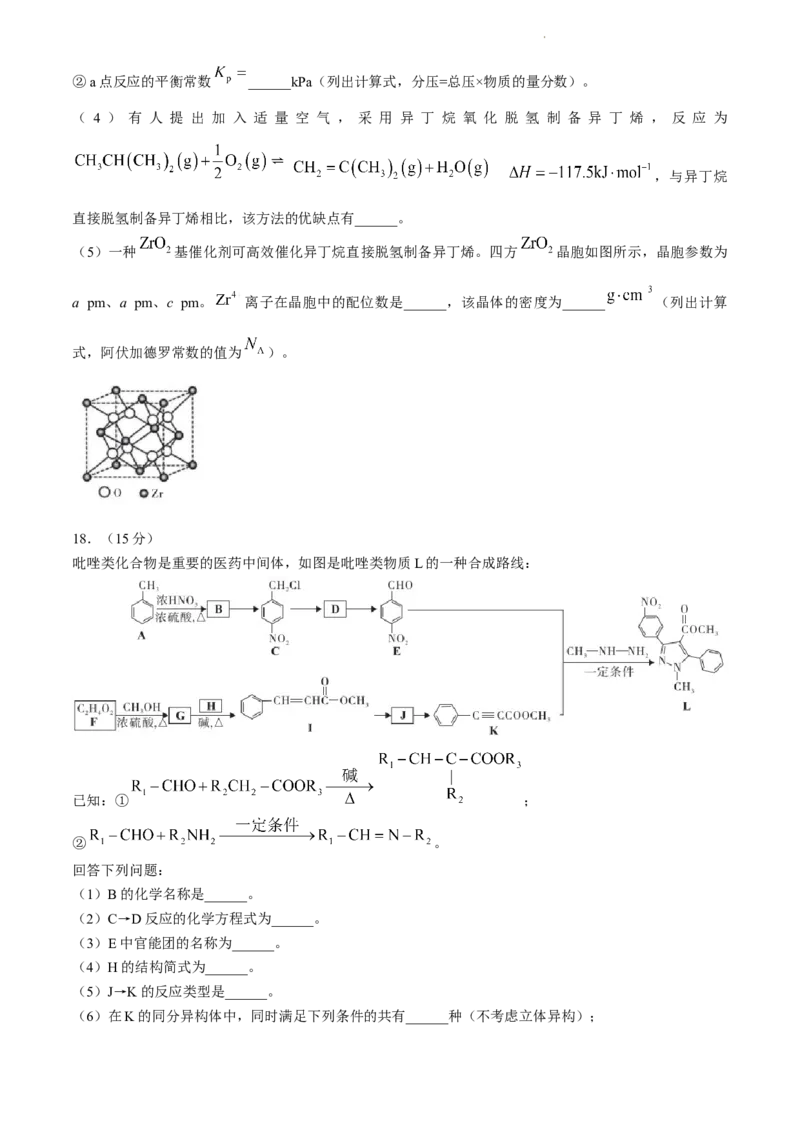
吡唑类化合物是重要的医药中间体,如图是吡唑类物质L的一种合成路线:
已知:① ;
② 。
回答下列问题:
(1)B的化学名称是______。
(2)C→D反应的化学方程式为______。
(3)E中官能团的名称为______。
(4)H的结构简式为______。
(5)J→K的反应类型是______。
(6)在K的同分异构体中,同时满足下列条件的共有______种(不考虑立体异构);
学科网(北京)股份有限公司①含有苯环,且有两个取代基;②含有碳碳三键;③既能发生水解反应又能发生银镜反应。
其中,核磁共振氢谱显示为四组峰,且峰面积比为3∶2∶2∶1的同分异构体的结构简式为______。
(7)参照上述合成路线,以乙酸和 为原料,设计合成 的路线:______(无
机试剂任选)。
学科网(北京)股份有限公司化学参考答案
1.【答案】A 【解析】合金钢里面除了铁、碳外,还加入其他金属元素,属于合金材料,A项正确;砷
化镓是一种无机化合物,属于半导体材料,B项错误;石英玻璃主要成分 是无机非金属材料,不属于
金属材料,C项错误;碳纤维是一种无机高分子材料,环氧树脂是一种有机高分子材料,D项错误。
2.【答案】B 【解析】漂粉精的有效成分是次氯酸钙,在水中生成次氯酸,可用于游泳池消毒,A项正
确;葡萄糖不能发生水解反应,B项错误;将 还原为甲醇,可减少 的排放,有利于实现“碳中
和”,C项正确;氯乙烷沸点低,可迅速气化局部降温,减轻疼痛,D项正确。
3.【答案】B 【解析】同位素是指同种元素的不同原子,A项错误;“超级原子”最外层电子数之和为
40时处于相对稳定状态,故 反应时失去2个电子,生成 ,B项正确;离子键是阴阳离子间
的相互作用,C项错误;等质量的 和 中含有的铝原子个数比1∶1,D项错误。
4.【答案】C 【解析】X中含有甲基,所有原子一定不会共平面,A项错误;Y中碳原子有 、
两种杂化方式,B项错误;根据Z的结构可知,存在顺式异构体,C项正确;Z中的酯基不能和氢气发生
加成反应,1mol Z最多可以和5mol氢气发生加成反应,D项错误。
5.【答案】C 【解析】IBr与水反应: ,A项错误; 溶液中加入过量
NaOH溶液: ,B项错误;AgCl悬浊液中加入 溶液发生沉淀转化:
,C项正确;酸性: ,故向NaClO溶液中通入少量 :
,D项错误。
6.【答案】A 【解析】 的空间构型为平面三角形, 的空间构型为是三角锥形,故键角:
,A项正确; 是非极性分子,B项错误;两者的熔点较低,属于分子晶体,故液态时
导电性较差,C项错误; 和 均是分子晶体,熔点与分子间作用力、极性有关,与键能无关,D项
错误。
7.【答案】A 【解析】 的密度大于空气,可用向上排空气法进行收集,多余的 可用氢氧化钠
学科网(北京)股份有限公司溶液吸收,且做防倒吸处理,A项正确;图乙装置导气管应该伸到试管底部,B项错误; 溶液在加
热时会被空气中的氧气氧化,C项错误;图丁装置浓硫酸、稀硫酸发生的氧化还原反应发生了变化,D项
错误。
8.【答案】C 【解析】W位于元素周期表的p区,形成一个共价键,故为F元素。根据X、Y、Z的成
键情况可知,X为O元素、Y为C元素、Z为S元素。元素电负性:F>O>C,A项正确。基态原子未成对
电子数:C=S>F,B项正确;S形成6个共价键,不满足 8电子结构,C项错误;简单氢化物沸点:
O>F>C,D项正确。
9.【答案】D 【解析】根据题意列三段式,计算可得平衡时 、 ,故曲线
Ⅱ表示的是 随时间的变化,A项错误; min时,反应达到化学平衡状态,B项错误;增大压强,
该平衡右移,平衡常数不变,C 项错误;计算可得 时间段内, ,故
。
10.【答案】B 【解析】酸性: ,A项错误;相同条件下Na与水反应的速率更快,羟基
氢原子的活泼性更大,B项正确;键长: ,正因为F半径小离的近,故其原子核外孤对电
子之间斥力大,键能反而小,C项错误;用饱和碳酸钠溶液浸泡 ,部分 因较高浓度的
可转化生成 ,但是溶度积常数: ,D项错误。
11.【答案】D 【解析】F元素的电负性较O元素大,故氧元素的化合价为+1价,A项错误; 的S
元素为 杂化,略去两对孤对电子,分子构型为V形,B项错误;HF是共价化合物,C项错误;标准状
况下,每生成0.5mol的 ,反应转移1mol的电子,D项正确。
12.【答案】C 【解析】由反应机理图可知,化合物4是反应的催化剂,A正确;化合物4转化为化合物
6发生加成反应,符合“原子经济性”,B正确;若将丙烯替换为乙烯,则反应可制得丙酸甲酯,C错误;
反应Ⅰ有碳碳键的断裂,反应Ⅲ有碳碳键的形成,反应Ⅳ有极性键的断裂,反应Ⅴ有极性键的形成,D正
确。
13.【答案】D 【解析】放电时,电极a是负极,发生氧化反应,A项正确;电极b是正极,反应为:
,B项正确;充电时,Ⅱ室生成的 和向Ⅰ室迁移的 数目相
学科网(北京)股份有限公司同, 溶液的浓度不变,C项正确;充电时,电极a质量增加24g,生成1mol Mg,转移2mol ,
电极b理论上减少2mol ,质量减少14g,D项错误。
14.D 【解析】随着 增大, 不断减小, 先增大后减小,
不 断 增 大 , 故 曲 线 代 表 , A 项 正 确 ;
, B 项 正 确 ; 根 据 物 料 守 恒 可 知 ,
,b点溶液中 ,C项正
确 ; ,
,D项错误。
二、非选择题:本题共4小题,共58分。
15.(15分,除标注外,每空2分)
(1)球形冷凝管(1分) 将甲醇、盐酸冷凝回流,提高原料利用率
(2)
(3)
(4)向漏斗中加入蒸馏水至刚好浸没沉淀,待蒸馏水自然流下,重复操作2-3次
(5)乙醚(1分)
(6)①除去过量的 ,防止将KI氧化为 (1分)
②当滴入最后半滴 标准溶液,溶液恰好由蓝色褪为无色,且半分钟不恢复原来的颜色
③88.8%
【解析】(1)由装置图可知,仪器a为冷凝管;因为甲醇沸点为64.7℃,为减少反应过程中甲醇和盐酸的
大量挥发,故使用冷凝管对其冷凝回流,提高原料利用率。(2)由信息可知,甲醇转变为 ,
被 还 原 为 , 根 据 元 素 守 恒 和 得 失 电 子 守 恒 可 写 出 反 应 的 化 学 方 程 式 为
学科网(北京)股份有限公司。(3)因为 的性质与
类似具有两性,故如果加入过量 NaOH 溶液, 会反应生成 ,离子方程式为
。(4)洗涤 固体的方法是向漏斗中加入蒸馏水至刚好浸
没沉淀,待蒸馏水自然流下,重复操作 2-3 次。(5) 不溶于乙醚,由 溶液得到
晶体的一系列操作为加热浓缩、冷却结晶、过滤、用少量乙醚洗涤、低温烘干。(6)①继
续加热煮沸一段时间的目的是除去过量的 溶液,防止将KI氧化为 。②滴定终点的现象为当滴入
最后半滴 标准溶液,溶液恰好由蓝色褪为无色,且半分钟不恢复原来的颜色。③根据元素守恒和
电子得失守恒可得出关系: ,又第二次滴定时的误差较大,因此
消 耗 标 准 溶 液 的 体 积 为 , 故 滴 定 产 品 的 纯 度 为
。
16.(14分,每空2分)
(1)
(2)
会将盐酸氧化生成氯气,污染环境
(3)5≤pH<7
(4)焰色试验
(5) 与过量的 生成 而溶解
(6)
学科网(北京)股份有限公司【解析】(1)基态Co原子的价电子排布式为 。(2) 中+3价的Co元素被 还原为
+2 价的 ,故反应的离子方程式为 。
中+3价的Co元素具有较强的氧化性,会将盐酸氧化生成氯气,污染环境。(3)“调pH”将溶
液中的杂质离子 和 转化为沉淀, ,即pH≥5;同时不能沉淀 ,故
,即pH<7。(4) 和 所含金属元素不同,可通过焰色试验鉴别,
其中Li元素焰色为紫红色,Na元素焰色为黄色。(5)随 的进一步增大,
与过量的 生成 导致钴的沉淀率减小。(6)根据元素守恒和电子得失守恒可写出反应
的化学方程式为 。
17.(14分,每空2分)
(1)+123 (2)BC
(3)①M ②
(4)优点:该反应为熵增的放热反应,可以在较低温度下自发进行,节约能源。缺点:异丁烷和异丁烯
容易被氧气氧化,导致原料浪费和目标产物的选择性降低
(5)8
17. 【解析】(1) 反应物键能之和-生成物键能之和,除去异丁烷和异丁烯中相同的化学键,则
反应的 。
(2)由图可知,当温度升高时,异丁烯的选择性降低,有可能是催化剂失活,A项错误;也可能是异丁烷
在温度较高时,发生了裂解反应,B项正确;异丁烯中存在碳碳双键,可以发生聚会反应,也会导致异丁
烯的选择性降低,C项正确;异丁烷直接脱氢生成异丁烯的反应为吸热反应,升高温度,平衡向反应方向
学科网(北京)股份有限公司移动,D项错误。(3)①对于一定量的异丁烷,起始加入等物质的量的 与Ar时,由于 为生成物,
故平衡左移,气体总物质的量减小且异丁烷的物质的量增加;Ar为稀有气体,不参与反应,相当于减小压
强,平衡右移,气体总物质的量增加且异丁烷物质的量减小,故投入 时对应的x值更大,曲线M为
。②根据题意可列三段式:
平衡时异丁烷摩尔分数 ,解得 , 。
(4)异丁烷氧化脱氢法的优点:该反应为熵增的放热反应,可以在较低温度下自发进行,节约能源。缺
点:异丁烷和异丁烯容易被氧气氧化,导致原料浪费和目标产物的选择性降低。(5)由图可知,与
离子距离最近且等距的 数目为 8,故 离子在晶胞中的配位数是 8,该晶体的密度为
。
18.(15分,除标注外,每空2分)
(1)对硝基甲苯(1分)
(2)
(3)硝基、醛基
(4)
(5)消去反应(1分)
(6)12 、
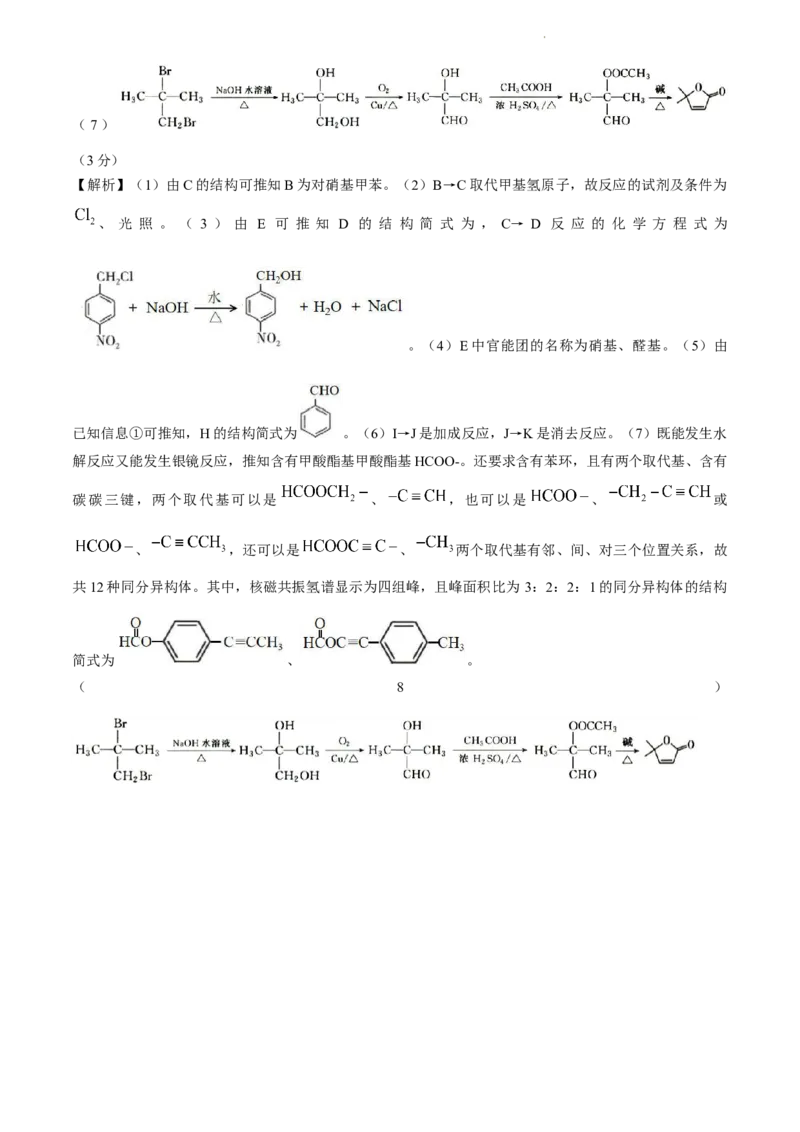
学科网(北京)股份有限公司(7)
(3分)
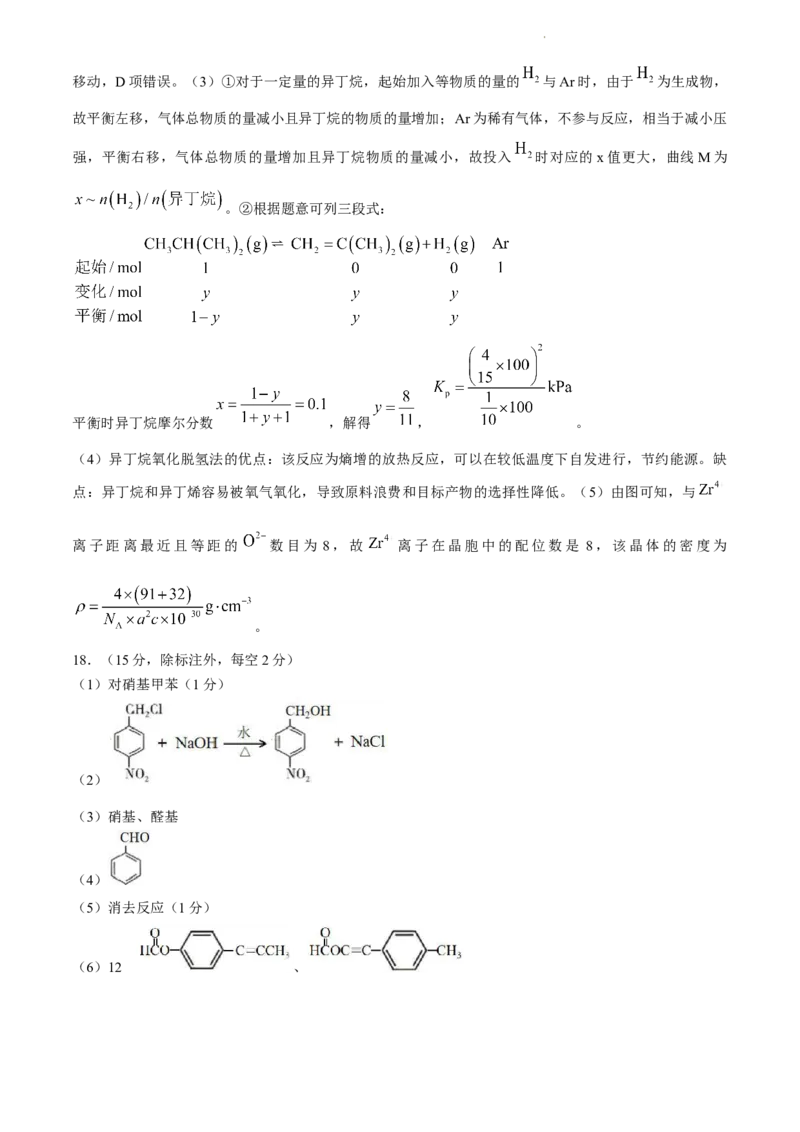
【解析】(1)由C的结构可推知B为对硝基甲苯。(2)B→C取代甲基氢原子,故反应的试剂及条件为
、 光 照 。 ( 3 ) 由 E 可 推 知 D 的 结 构 简 式 为 , C→ D 反 应 的 化 学 方 程 式 为
。(4)E中官能团的名称为硝基、醛基。(5)由
已知信息①可推知,H的结构简式为 。(6)I→J是加成反应,J→K是消去反应。(7)既能发生水
解反应又能发生银镜反应,推知含有甲酸酯基甲酸酯基HCOO-。还要求含有苯环,且有两个取代基、含有
碳碳三键,两个取代基可以是 、 ,也可以是 、 或
、 ,还可以是 、 两个取代基有邻、间、对三个位置关系,故
共12种同分异构体。其中,核磁共振氢谱显示为四组峰,且峰面积比为 3:2:2:1的同分异构体的结构
简式为 、 。
( 8 )
学科网(北京)股份有限公司