文档内容
2023--2024 学年度上学期 9 月份开学考试
化 学 试 卷
时间:75 分钟 满分 100 出题人 冯秀丽
可能用到的相对原子质量 H 1 O 16 Na 23 Bi 209
一、单选题
1.2022年我国科技创新成果丰硕,下列有关说法正确的是
A.量子通信的光纤和超算“天河一号”的芯片主要材料均为SiO
2
B.“深海一号”母船海水浸泡区的铝基可保障船体不易腐蚀
C.“北斗卫星”授时系统的“星载铷钟”含铷元素,其单质遇水能缓慢反应放出H
2
D.C919民航客机机身材料中的复合纤维属于天然有机高分子
2.下列过程中,颜色变化与氧化还原反应无
.
关
.
的是
A.浓硝酸长时间放置,溶液变为黄色
B.放置时间较长的苯酚固体,变为粉红色
C.氯化铁溶液遇硫氰化钾溶液变红色
D.酸性K Cr O 溶液滴入乙醇,溶液变为绿色
2 2 7
3.N 是阿伏加德罗常数的数值。下列说法正确的是
A
A.标准状况下,2.24LHF中含有的分子数为0.1N
A
B.2gD O和H 18O的混合物含有质子数为N
2 2 A
C.pH=3的H PO 溶液中氢离子数目为10-3N
3 4 A
D.1molCl 通入水中反应转移的电子数为N
2 A
4.下列关于元素及其化合物的性质说法不
.
正
.
确
.
的是
A.工业上利用二氧化氮与水反应生产硝酸
B.将Cl 通入冷的Ca(OH) 溶液中,制得以Ca(ClO) 为有效成分的漂白粉
2 2 2
C.工业上用98.3%的浓硫酸吸收SO 制备硫酸
3
D.Al和氢氧化钠溶液反应可生成H
2
1
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}5.化学与生活密切相关,下列关于劳动项目涉及的化学知识正确的是
选项 劳动项目 化学知识
A 用葡萄酿酒 葡萄糖在酶作用下发生水解生成乙醇
B FeCl 溶液可用于刻蚀铜电路板 FeCl 溶液显酸性
3 3
C 葡萄酒中适量添加少量二氧化硫 二氧化硫用于杀菌、抗氧化
D 用小苏打作发泡剂烘焙面包 Na CO 可与发酵时产生的酸反应生成二氧化碳
2 3
6.下列各组离子在指定条件下一定能大量共存的是
A.c(H+)=0.1mol/L的溶液中:K+ AlO - HCO - Cl-
2 3
B.c(OH-)=0.1mo/L的溶液中:S2-、SO2、I-、ClO-、K+
3
C.某透明溶液中: SO2、H+、 Cu2+、Na+
4
D.加铝生成氢气的溶液中: NH+、 Mg2+、Br-、NO
4 3
7.对于下列实验,能正确描述其反应的离子方程式的是
A.向漂白粉水溶液中通入少量SO :Ca2++2ClO-+H O+SO =CaSO ↓+2HClO
2 2 2 3
B.Na S溶液长期露淔在空气中:2S22H OO 2S4OH
2 2 2
C.在CaHCO 溶液中加入过量的NaOH溶液:Ca2 HCOOH CaCO H O
3 2 3 3 2
D.向饱和碳酸钠溶液中通入足量CO :CO2+H O+CO =2HCO -
2 3 2 2 3
8.具有美白功效的化合物乙的合成反应如图所示。下列说法错误的是
A.该反应为加成反应
B.可用酸性KMnO 溶液检验乙中是否混有苯乙烯
4
C.乙的苯环上一氯代物有5种
D.1mol甲与足量溴水反应,最多消耗3molBr
2
2
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}9.下列实验操作能达到相应实验目的是
实验目的 实验操作
检验淀粉已经 取少量水解液加适量氢氧化钠溶液使其呈碱性,加入银氨溶液混合加
A
完全水解 热,观察是否有有光亮的银镜生成
证明Y中是否 向1mL1%的NaOH溶液中加入2mL2%的CuSO 溶液,振荡后再加
4
B
含有醛基
入0.5mL有机物Y,加热,观察是否出现砖红色沉淀
除去苯中混有
C 加入NaOH溶液,振荡,静置分层后,用分液漏斗可分离出苯
的少量苯酚
检验RX是溴 将RX与NaOH水溶液共热,经充分反应后冷却,向冷却液中加AgNO
3
D
代烷
溶液,观察沉淀颜色
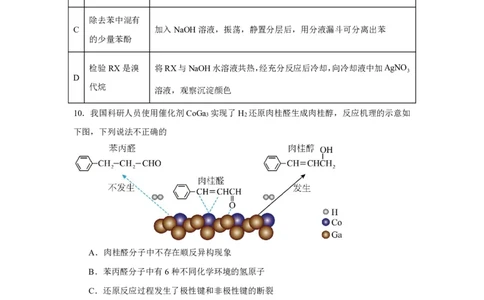
10.我国科研人员使用催化剂CoGa 实现了H 还原肉桂醛生成肉桂醇,反应机理的示意如
3 2
下图,下列说法不正确的
A.肉桂醛分子中不存在顺反异构现象
B.苯丙醛分子中有6种不同化学环境的氢原子
C.还原反应过程发生了极性键和非极性键的断裂
D.该催化剂实现了选择性还原肉桂醛中的醛基
11.某溶液只可能大量含有下列离子:NH、Na、Mg2、Fe2、NO、CO2、I中的几
4 3 3
种(忽略水的电离),且各离子的物质的量浓度相等,现进行如下实验:
(1)取少量该溶液加过量稀硫酸溶液共热,观察到红棕色气体;
(2)取少量(1)所得的溶液,向溶液中加入过量氢氧化钠溶液,微热,生成刺激性气体,无沉
淀生成。
3
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}根据上述实验,下列说法正确的是
A.不需要焰色试验检验Na的存在
B.取实验(2)后的溶液滴加淀粉溶液一定变蓝
C.原溶液中可能含有CO2,一定不含Fe2
3
D.取少量原溶液加新制氯水,原溶液中可能有两种离子被氧化
12.有关金属冶炼或其原理的说法正确的是( )
A.给定条件下,Mg(OH) MgCl (aq) Mg,物质间转化能一步实
2 2
现
B.工业上,常用电解熔融AlCl 的方法冶炼金属铝,加入冰晶石作助熔剂
3
高温
C.火法炼铜:Cu SO 2CuSO ,其中Cu S既作氧化剂又作还原剂
2 2 2 2
D.铝热法炼铁:2Al+Fe O =2Fe+Al O ,反应物刚好完全反应,反应后固体质量增加
2 3 2 3
13.某同学通过如下流程制备Cu O,已知CuCl难溶于水和稀硫酸。
2
下列说法错误的是
A.步骤⑤可以用HNO 酸化的AgNO 溶液检验沉淀是否洗涤干净
3 3
B.步骤③中为防止CuCl被氧化,可用Na SO 溶液洗涤
2 3
C.步骤④发生反应的离子方程式为2CuCl+2OH Cu O+2Cl+H O
2 2
D.步骤②中氧化剂和还原剂物质的量之比为1:2
14.以水泥厂的废料(主要成分为MgO,含少量MnO、Fe O、FeO、Al O、SiO 等杂质)
2 3 2 3 2
为原料制备MgSO 7H O 的工艺流程如下:
4 2
已知:MnO+H SO =MnSO +H O ,氧化性:ClO-大于MnO 下列说法正确的是
2 4 4 2 2
4
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}A.为提高酸浸速率,可使用98%浓硫酸 B.试剂X可以是MgSO
4
C.滤渣为Al(OH)、Fe(OH)、SiO D.操作a所得滤液经处理后可循环利用
3 3 2
15.有机物XY的异构化反应如图所示,下列说法错误的是
A.依据红外光谱可确证X、Y存在不同的官能团
B.除氢原子外,X中其他原子可能共平面
C.含醛基和碳碳双键且有手性碳原子的Y的同分异构体有4种(不考虑立体异构)
D.类比上述反应, 的异构化产物可发生银镜反应和加聚反应
二、填空题
16.某小组同学探究铁离子与苯酚的反应。
已知:Fe3++6C H O [Fe(C H O) ]3 ;[Fe(C H O) ]3 为紫色配合物。
6 5 6 5 6 6 5 6
(1)配制100mL0.1mol·L-1苯酚溶液,需要用到的玻璃仪器有:烧杯、玻璃棒、胶头滴
管、 。
(2)氯化铁溶液呈酸性,用离子方程式表示原因 。
(3)进行如下实验。
实验1:
实验2:
5
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}
【提出猜想】i.Cl 对铁离子与苯酚的反应有促进作用;
ii.SO2对铁离子与苯酚的反应有抑制作用。
4
①向实验2反应后溶液中加入 ,溶液颜色无变化,证明猜想i不成立。
②实验证明猜想ii成立,请写出实验操作和现象 。
(4)实验证明,H+对Fe3+与苯酚反应生成的配合物有抑制作用,请从平衡角度结合化学用语
进行解释 。
(5)有同学提出,溶液pH越大,越利于铁离子与苯酚发生显色反应。你认为是否合理,并说
明理由 。
(6)由以上研究可知,影响铁离子与苯酚反应的因素有 。
17.硫酸亚铁铵晶体[(NH ) Fe(SO ) ·6H O]是分析化学中的重要试剂,是一种复盐,与其他复
4 2 4 2 2
盐一样,硫酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,利用这一性质可以
用等物质的量的(NH ) SO 和FeSO 混合制备。请回答以下问题:
4 2 4 4
I.硫酸亚铁铵晶体的制备
步骤一:称取一定质量铁屑,加入15mL10%Na CO 溶液,小火加热30分钟,过滤洗涤、
2 3
干燥、称量得固体mg。
步骤二:将步骤一中的mg固体转移至锥形瓶,加入一定体积3mol·L-1H SO 充分溶解,将
2 4
溶液转移入蒸发皿
步骤三:计算所得FeSO 的物质的量,计算等物质的量的(NH ) SO 固体的质量,准确取
4 4 2 4
(NH ) SO
4 2 4。
步骤四:将(NH ) SO 固体加入步骤二蒸发皿中,缓慢加热浓缩至表面出现结晶薄膜为止,
4 2 4
放置冷却。
步骤五:经过一系列操作,最终得到较纯净的(NH ) FeSO ·6H O。
4 2 4 2
(1)步骤一中加入10%Na CO 溶液,小火加热30分钟的目的是
2 3
(2)关于步骤五中的一系列操作的相关表述,错误的是___________(填字母)。
6
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}A.过滤时可使用玻璃棒搅拌的方式来缩短时间
B.过滤和洗涤的速度都要尽可能的快,可以减少产品的氧化
C.洗涤时使用无水乙醇既可以洗去晶体表面的杂质离子,又可以起到干燥作用
D.所得的产品可以采取电热炉烘干的方式彻底干燥
II.硫酸亚铁铵的分解
已知硫酸亚铁铵在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物的成分。
(3)B装置的作用是
(4)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定分解产物中含有
气体,写出D中发生反应的离子方程式 ;若去掉C,是否能得出同样结论,并
解释其原因 。
(5) A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe O 而不
2 3
含FeO。其预期实验现象为: 。
实验步骤 预期现象 结论
①取少量A中残留物于试管中,加入适量稀硫酸,充分
振荡便其完全溶解; 固体残留物仅为
___________
②将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶 Fe O
2 3
液
7
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}18.铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为Bi S ,含FeS 、
2 3 2
CuO、SiO 等杂质)制备NaBiO 的工艺流程如下:
2 3
已知:
i.Bi3易水解。NaBiO 难溶于冷水。
3
ii.“氧化浸取”时,铋元素转化为Bi3,硫元素转化为硫单质。
iii.CuOH 2 s4NH 3 g Cu NH 3 4 2aq 2OH aq K 4.4107。
回答下列问题:
(1)为提高“浸取”速率,采取的措施有:升高温度、 (写出一条)。辉铋矿浸取率
随温度的变化曲线如图,高于40℃时浸取率快速下降,其可能的原因是 。
(2)“氧化浸取”时,H O 和FeS 发生反应的物质的量之比为 。
2 2 2
(3)“除铜”时发生反应:
Cu2aq4NH 3 g Cu NH 3 4 2aq K 21013,则K sp CuOH 2 。
(4)“转化”时,生成NaBiO 的离子方程式为 。
3
(5)已知酸性环境下,NaBiO 可以将Mn2氧化成MnO(BiO被还原成Bi3)。
3 4 3
取NaBiO 产品wg,加入足量稀硫酸和MnSO 稀溶液使其完全反应,再用amol·L1
3 4
H C O 标准溶液滴定生成的MnO,当溶液紫红色恰好褪去时,消耗bmL标准溶液。该产
2 2 4 4
品的纯度为 (用含w、a、b的代数式表示)。
8
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}19.化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线
如下:
已知:RCHO+CH CHONaOH/H2O RCH=CHCHO+H O
3 Δ 2
回答下列问题:
(1)A的结构简式为 。
(2)往D中加KOH/C H OH发生的反应类型为 。
2 5
(3)F中所含官能团名称为 。
(4)写B与新制Cu(OH) 反应的化学方程式 。
2
(5)G的结构简式 。
(6)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO ,其核磁共振
2
氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1,写出符合要求的X的结构简
式 。
9
{#{QQABDYCUogCAAgAAABhCEQEwCgOQkAGCACgOgBAAoAABCBNABAA=}#}