文档内容
第一课时 反应热 焓变基础练习题解析版
1.某试管中盛有Al粉和稀盐酸,下列有关说法不正确的是( )
A.试管、Al粉、稀盐酸及发生的反应可看作一个体系
B.除反应物、生成物及相关反应外,其他均看作环境
C.Al与稀盐酸反应导致体系温度升高,且向环境中释放热量
D.Al与稀盐酸反应的反应热可以通过量热计测量
2.关于中和反应反应热的测定实验,下列说法正确的是( )
A. 为了使反应进行得更完全,可以使酸或碱适当过量
B.为了使反应均匀进行,可以向酸(碱)溶液中分几次加入碱(酸)溶液
C.中和反应反应热的测定结果与所用酸(碱)的种类无关
D.测完酸溶液的温度后,未冲洗温度计并擦干就直接测碱溶液的温度,会使测得的反应热数值的绝对值偏大
3.下列有关中和反应反应热测定实验的说法正确的是( )
A. 温度计能代替玻璃搅拌器,用于搅拌反应物
B.强酸与强碱反应生成1molH O(l)释放的热量都约为57.3kJ
2
C.测定中和反应反应热实验中,读取混合溶液不再变化的温度为终止温度
D.某同学通过实验测得盐酸和NaOH溶液反应生成1molH O(1)放出的热量为52.3kJ,造成这结果的原因不可能是所用酸、
2
碱溶液浓度过大
4.下列说法正确的是( )
A. 反应热是1mol物质参加反应时的能量变化
B.当反应放热时△H>0,反应吸热时△H<0
C.任何条件下,化学反应的焓变都等于化学反应的反应热
D.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差决定
5.下列反应中,生成物的总焓大于反应物的总焓,但不属于氧化还原反应的是( )
A.焦炭在高温下与水蒸气反应
B.Ba(OH) ·8H O与NH Cl的反应
2 2 4
C.NaOH溶液与HSO 溶液混合
2 4
D.铝热反应
6.下列说法中正确的是( )
A.焓变是指1mol物质参加反应时的能量变化
B.反应放热时,△H>0;反应吸热时,△H<0
C.在一个确定的化学反应关系中,反应物的总焓与生成物的总焓一定不同
D.在一个确定的化学反应关系中,反应物的总焓总是高于生成物的总焓
7.下列反应属于吸热反应的是( )
A.甲烷在空气中燃烧
B.葡萄糖在人体内氧化分解
C.碳与水蒸气的反应
D.锌粒与稀HSO 反应制取H
2 4 2
8.下列反应中△H<0的是( )
A.氯酸钾分解制氧气
B.氯化铵加热制备氨气
C.碳与二氧化碳高温生成一氧化碳
D.实验室制备氢气
9.已知强酸稀溶液与强碱的稀溶液发生中和反应生成1molH O时的反应热△H=-57.3kJ·mol-1,下列反应放热为57.3kJ的
2
是( )
A.含1molH SO 的稀硫酸与足量稀NaOH溶液反应
2 4
B.稀盐酸与稀氨水反应生成1molH O
2
C.稀盐酸与稀Ba(OH)2溶液反应生成1molH O
2
D.稀NaOH溶液与95%浓硫酸反应生成1molH O
210.对于放热反应H+Cl 2HCl,下列说法正确的是( )
2 2
A.该反应涉及离子键和共价键的断裂与形成
B.该反应中,化学能只转变为热能
C.断开1moHH键和1 mol Cl-Cl键所吸收的总能量小于形成1molH-C1键所放出的能量
D.反应物所具有的总能量高于生成物所具有的总能量
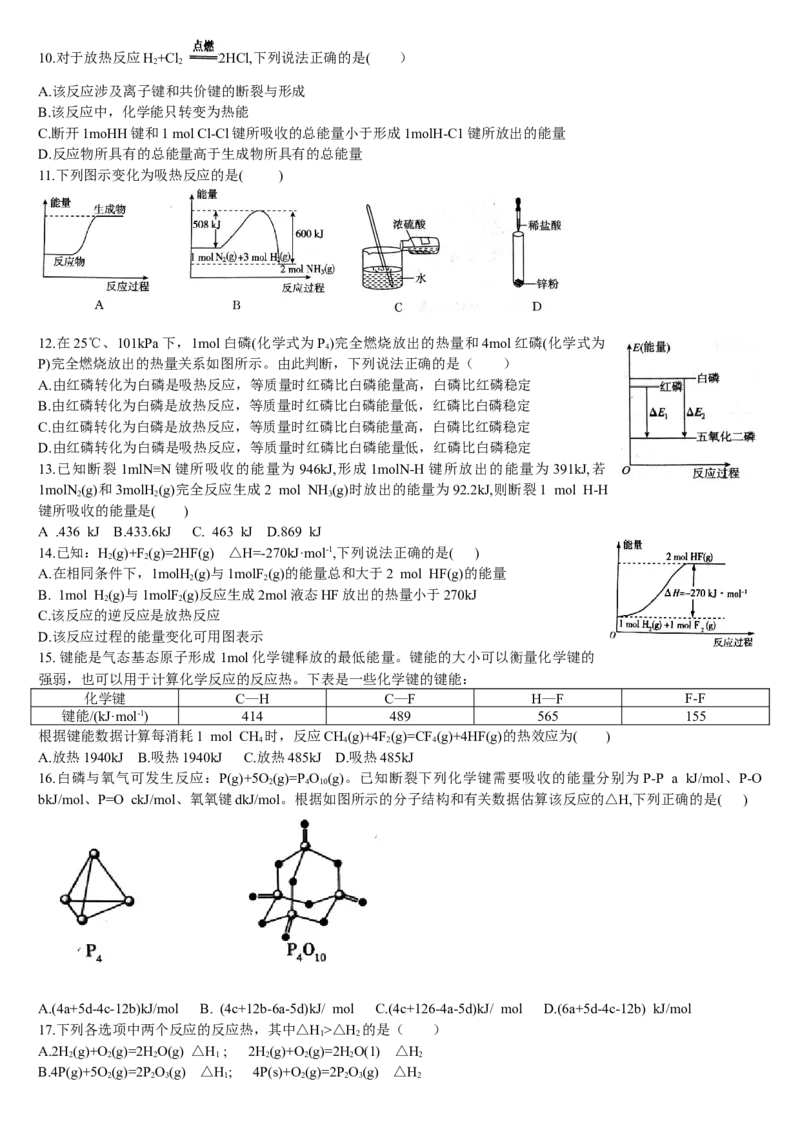
11.下列图示变化为吸热反应的是( )
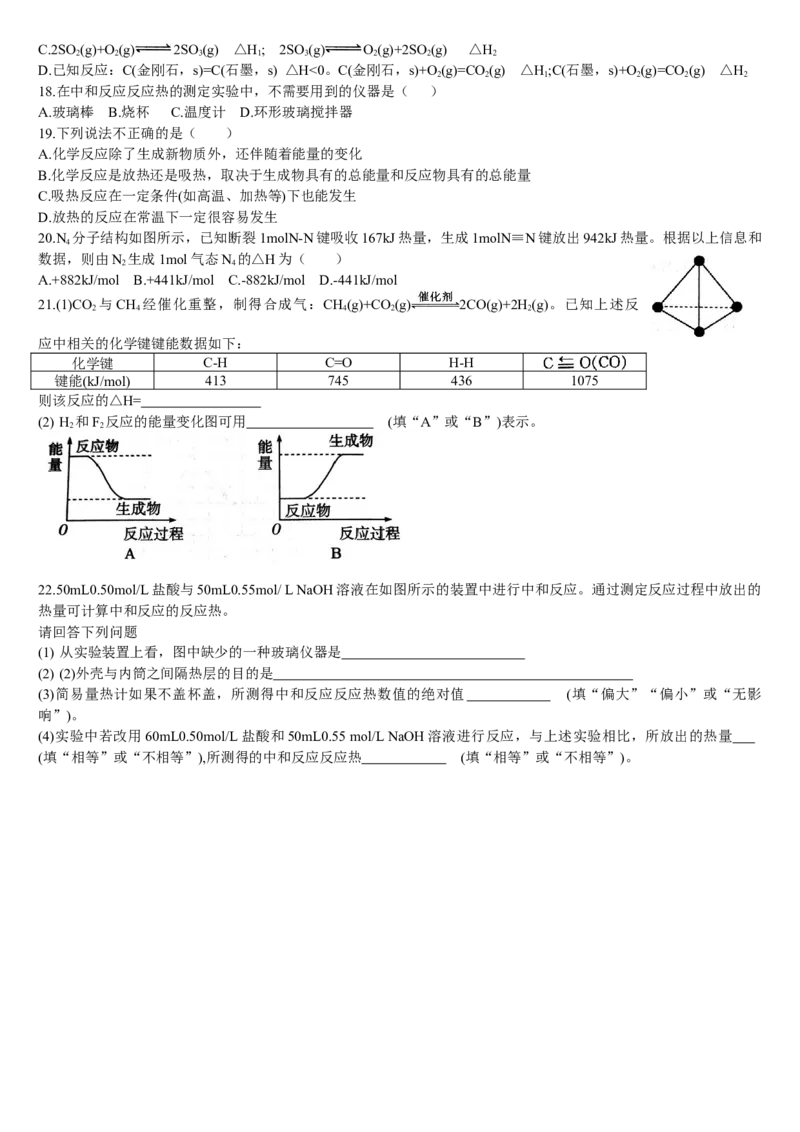
12.在25℃、101kPa下,1mol白磷(化学式为P)完全燃烧放出的热量和4mol红磷(化学式为
4
P)完全燃烧放出的热量关系如图所示。由此判断,下列说法正确的是( )
A.由红磷转化为白磷是吸热反应,等质量时红磷比白磷能量高,白磷比红磷稳定
B.由红磷转化为白磷是放热反应,等质量时红磷比白磷能量低,红磷比白磷稳定
C.由红磷转化为白磷是放热反应,等质量时红磷比白磷能量高,白磷比红磷稳定
D.由红磷转化为白磷是吸热反应,等质量时红磷比白磷能量低,红磷比白磷稳定
13.已知断裂1mlN≡N键所吸收的能量为 946kJ,形成1molN-H键所放出的能量为 391kJ,若
1molN (g)和3molH (g)完全反应生成2 mol NH (g)时放出的能量为92.2kJ,则断裂1 mol H-H
2 2 3
键所吸收的能量是( )
A .436 kJ B.433.6kJ C. 463 kJ D.869 kJ
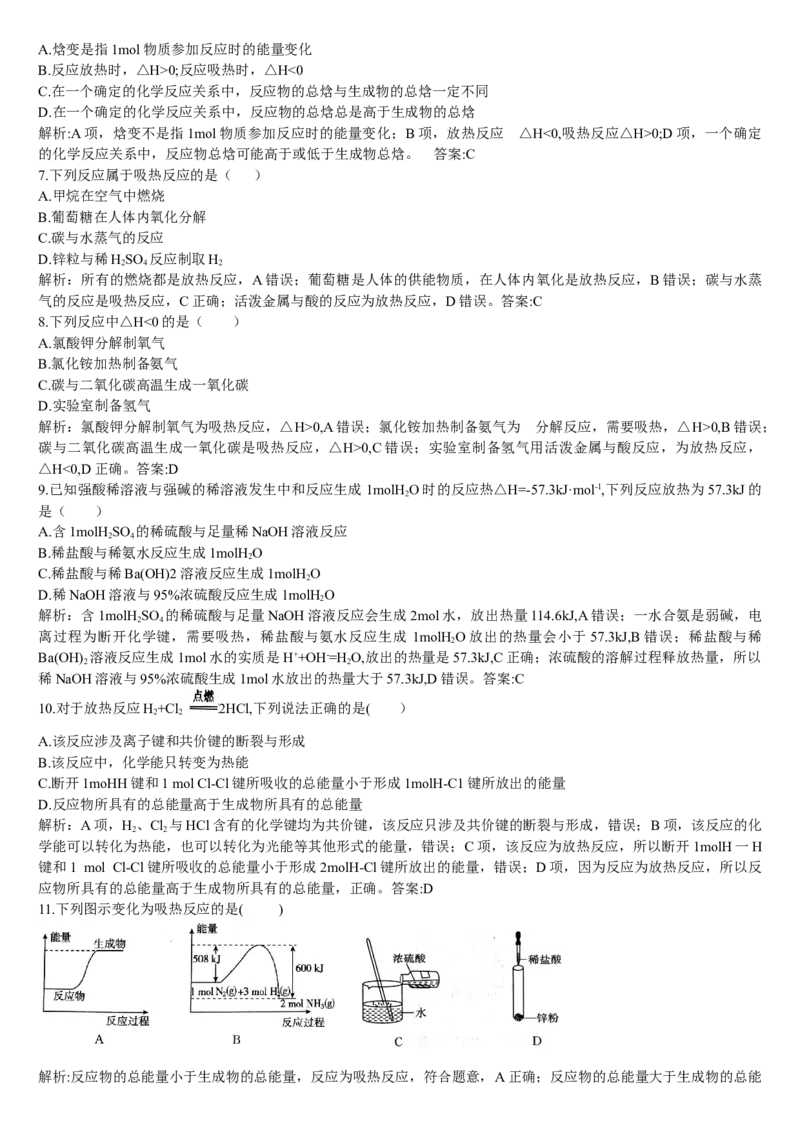
14.已知:H(g)+F (g)=2HF(g) △H=-270kJ·mol-1,下列说法正确的是( )
2 2
A.在相同条件下,1molH (g)与1molF (g)的能量总和大于2 mol HF(g)的能量
2 2
B. 1mol H(g)与1molF (g)反应生成2mol液态HF放出的热量小于270kJ
2 2
C.该反应的逆反应是放热反应
D.该反应过程的能量变化可用图表示
15.键能是气态基态原子形成1mol化学键释放的最低能量。键能的大小可以衡量化学键的
强弱,也可以用于计算化学反应的反应热。下表是一些化学键的键能:
化学键 C—H C—F H—F F-F
键能/(kJ·mol-1) 414 489 565 155
根据键能数据计算每消耗1 mol CH 时,反应CH(g)+4F (g)=CF (g)+4HF(g)的热效应为( )
4 4 2 4
A.放热1940kJ B.吸热1940kJ C.放热485kJ D.吸热485kJ
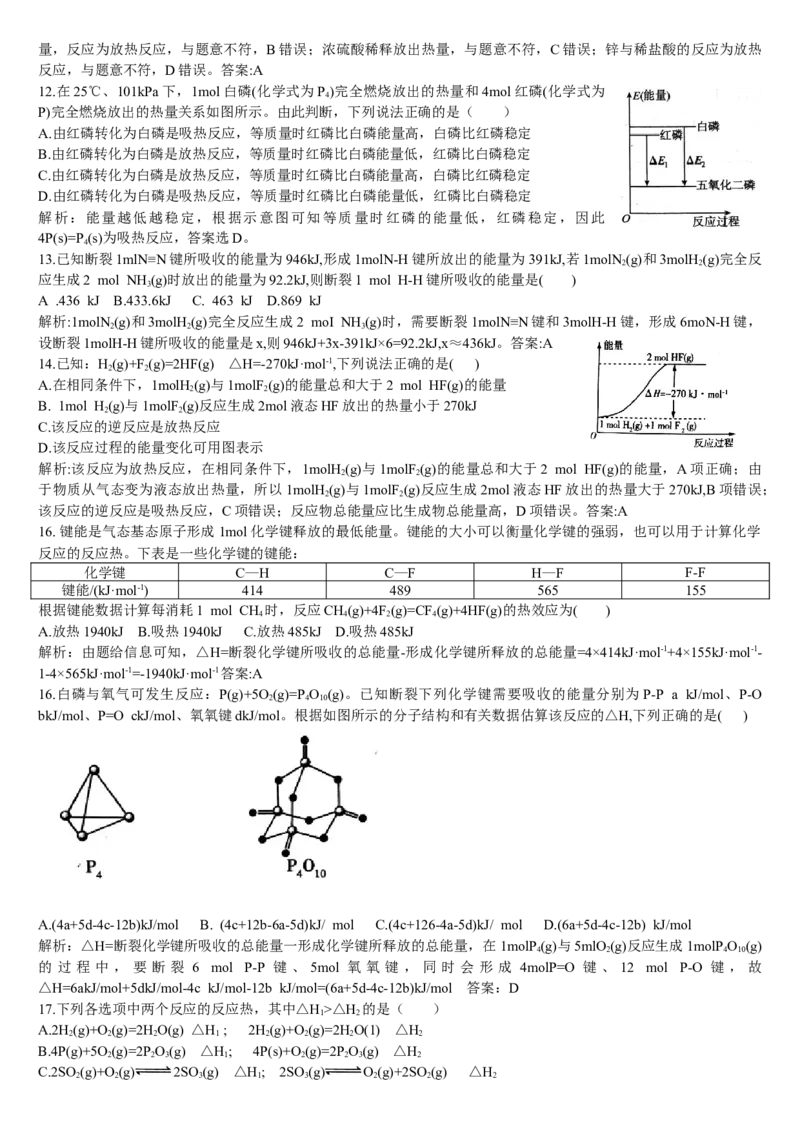
16.白磷与氧气可发生反应:P(g)+5O(g)=P O (g)。已知断裂下列化学键需要吸收的能量分别为P-P a kJ/mol、P-O
2 4 10
bkJ/mol、P=O ckJ/mol、氧氧键dkJ/mol。根据如图所示的分子结构和有关数据估算该反应的△H,下列正确的是( )
A.(4a+5d-4c-12b)kJ/mol B. (4c+12b-6a-5d)kJ/ mol C.(4c+126-4a-5d)kJ/ mol D.(6a+5d-4c-12b) kJ/mol
17.下列各选项中两个反应的反应热,其中△H>△H 的是( )
1 2
A.2H(g)+O(g)=2HO(g) △H ; 2H(g)+O(g)=2HO(1) △H
2 2 2 1 2 2 2 2
B.4P(g)+5O (g)=2P O(g) △H; 4P(s)+O (g)=2P O(g) △H
2 2 3 1 2 2 3 2C.2SO (g)+O(g) 2SO (g) △H; 2SO (g) O(g)+2SO(g) △H
2 2 3 1 3 2 2 2
D.已知反应:C(金刚石,s)=C(石墨,s) △H<0。C(金刚石,s)+O(g)=CO (g) △H;C(石墨,s)+O(g)=CO (g) △H
2 2 1 2 2 2
18.在中和反应反应热的测定实验中,不需要用到的仪器是( )
A.玻璃棒 B.烧杯 C.温度计 D.环形玻璃搅拌器
19.下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能量的变化
B.化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量
C.吸热反应在一定条件(如高温、加热等)下也能发生
D.放热的反应在常温下一定很容易发生
20.N 分子结构如图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量。根据以上信息和
4
数据,则由N 生成1mol气态N 的△H为( )
2 4
A.+882kJ/mol B.+441kJ/mol C.-882kJ/mol D.-441kJ/mol
21.(1)CO 与CH 经催化重整,制得合成气:CH(g)+CO (g) 2CO(g)+2H(g)。已知上述反
2 4 4 2 2
应中相关的化学键键能数据如下:
化学键 C-H C=O H-H
键能(kJ/mol) 413 745 436 1075
则该反应的△H=
(2) H 和F 反应的能量变化图可用 (填“A”或“B”)表示。
2 2
22.50mL0.50mol/L盐酸与50mL0.55mol/ L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中放出的
热量可计算中和反应的反应热。
请回答下列问题
(1) 从实验装置上看,图中缺少的一种玻璃仪器是
(2) (2)外壳与内筒之间隔热层的目的是
(3)简易量热计如果不盖杯盖,所测得中和反应反应热数值的绝对值 (填“偏大”“偏小”或“无影
响”)。
(4)实验中若改用60mL0.50mol/L盐酸和50mL0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
(填“相等”或“不相等”),所测得的中和反应反应热 (填“相等”或“不相等”)。第二课时 反应热 焓变基础练习题解析版
1.某试管中盛有Al粉和稀盐酸,下列有关说法不正确的是( )
A.试管、Al粉、稀盐酸及发生的反应可看作一个体系
B.除反应物、生成物及相关反应外,其他均看作环境
C.Al与稀盐酸反应导致体系温度升高,且向环境中释放热量
D.Al与稀盐酸反应的反应热可以通过量热计测量
解析:
反应2Al+6HCl=2ACl +3H ↑放出热量,体系温度升高,热量由温度高的体系释放到环境中,C项正确;通过量热计中
3 2
的温度计可测量反应前后体系的温度变化,根据有关物质的比热容及反应物的量来计算反应热,D项正确。答案:A
2.关于中和反应反应热的测定实验,下列说法正确的是( )
B. 为了使反应进行得更完全,可以使酸或碱适当过量
B.为了使反应均匀进行,可以向酸(碱)溶液中分几次加入碱(酸)溶液
C.中和反应反应热的测定结果与所用酸(碱)的种类无关
D.测完酸溶液的温度后,未冲洗温度计并擦干就直接测碱溶液的温度,会使测得的反应热数值的绝对值偏大
解析:中和反应反应热测定实验中,为保证反应完全,可以使酸或碱适当过量,A项正确;分几次加入酸溶液或碱溶液,
会导致部分热量散失,B项错误;中和反应反应热的测定结果与所用酸(碱)的种类有关,C项错误;测完酸溶液的温
度计表面附着有酸,未冲洗温度计并擦干就直接测量碱溶液的温度,会导致测量的碱溶液温度偏高,从而使测得的温
度差值偏小,测得的反应热数值的绝对值偏小D项错误。答案:A
3.下列有关中和反应反应热测定实验的说法正确的是( )
B. 温度计能代替玻璃搅拌器,用于搅拌反应物
B.强酸与强碱反应生成1molH O(l)释放的热量都约为57.3kJ
2
C.测定中和反应反应热实验中,读取混合溶液不再变化的温度为终止温度
D.某同学通过实验测得盐酸和NaOH溶液反应生成1molH O(1)放出的热量为52.3kJ,造成这结果的原因不可能是所用酸、
2
碱溶液浓度过大
解析:温度计不能代替玻璃搅拌器,只能用于测量溶液的温度,A项错误;强酸与强碱发生中和反生成1molH O(l)时,
2
放出的热量不一定等于57.3kJ,如浓硫酸与NaOH溶液反应生成1molH O(l)时,放出的热量大于57.3kJ,B项错误;测定
2
中和反应反应热时,应读取混合溶液的最高温度,C项错误;浓酸或浓碱溶于水时会放热,则生成1mol H O(l)时放出
2
的热量大于57.3kJ,D项正确。答案:D
4.下列说法正确的是( )
B. 反应热是1mol物质参加反应时的能量变化
B.当反应放热时△H>0,反应吸热时△H<0
C.任何条件下,化学反应的焓变都等于化学反应的反应热
D.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差决定
解析:在等温条件下,化学反应体系向环境释放或从环境吸收的热量叫反应热,此时参加反应的物质的物质的量不一定
是mol,故A错误;当反应放热时△H<0,反应吸热时△H>0,故B错误;在等压条件下,反应的ΔH(焓变)等于反应热,
故C错误;对于一个化学反应,生成物与反应物的焓值差即焓变决定了反应是吸热还是放热,故D正确。答案:D
5.下列反应中,生成物的总焓大于反应物的总焓,但不属于氧化还原反应的是( )
A.焦炭在高温下与水蒸气反应
B.Ba(OH) ·8H O与NH Cl的反应
2 2 4
C.NaOH溶液与HSO 溶液混合
2 4
D.铝热反应
解析:生成物的总焓大于反应物的总焓,说明反应为吸热反应。A项,是吸热反应,但属于氧化还原反应,错误;B项,
是吸热反应,且不属于氧化还原反应,正确;C项,是放热反应,且不属于氧化还原反应,错误;D项,是放热反应,
且属于氧化还原反应,错误。答案:B
6.下列说法中正确的是( )A.焓变是指1mol物质参加反应时的能量变化
B.反应放热时,△H>0;反应吸热时,△H<0
C.在一个确定的化学反应关系中,反应物的总焓与生成物的总焓一定不同
D.在一个确定的化学反应关系中,反应物的总焓总是高于生成物的总焓
解析:A项,焓变不是指1mol物质参加反应时的能量变化;B项,放热反应 △H<0,吸热反应△H>0;D项,一个确定
的化学反应关系中,反应物总焓可能高于或低于生成物总焓。 答案:C
7.下列反应属于吸热反应的是( )
A.甲烷在空气中燃烧
B.葡萄糖在人体内氧化分解
C.碳与水蒸气的反应
D.锌粒与稀HSO 反应制取H
2 4 2
解析:所有的燃烧都是放热反应,A错误;葡萄糖是人体的供能物质,在人体内氧化是放热反应,B错误;碳与水蒸
气的反应是吸热反应,C正确;活泼金属与酸的反应为放热反应,D错误。答案:C
8.下列反应中△H<0的是( )
A.氯酸钾分解制氧气
B.氯化铵加热制备氨气
C.碳与二氧化碳高温生成一氧化碳
D.实验室制备氢气
解析:氯酸钾分解制氧气为吸热反应,△H>0,A错误;氯化铵加热制备氨气为 分解反应,需要吸热,△H>0,B错误;
碳与二氧化碳高温生成一氧化碳是吸热反应,△H>0,C错误;实验室制备氢气用活泼金属与酸反应,为放热反应,
△H<0,D正确。答案:D
9.已知强酸稀溶液与强碱的稀溶液发生中和反应生成1molH O时的反应热△H=-57.3kJ·mol-1,下列反应放热为57.3kJ的
2
是( )
A.含1molH SO 的稀硫酸与足量稀NaOH溶液反应
2 4
B.稀盐酸与稀氨水反应生成1molH O
2
C.稀盐酸与稀Ba(OH)2溶液反应生成1molH O
2
D.稀NaOH溶液与95%浓硫酸反应生成1molH O
2
解析:含1molHSO 的稀硫酸与足量NaOH溶液反应会生成2mol水,放出热量114.6kJ,A错误;一水合氨是弱碱,电
2 4
离过程为断开化学键,需要吸热,稀盐酸与氨水反应生成 1molHO放出的热量会小于57.3kJ,B错误;稀盐酸与稀
2
Ba(OH) 溶液反应生成1mol水的实质是H++OH-=H O,放出的热量是57.3kJ,C正确;浓硫酸的溶解过程释放热量,所以
2 2
稀NaOH溶液与95%浓硫酸生成1mol水放出的热量大于57.3kJ,D错误。答案:C
10.对于放热反应H+Cl 2HCl,下列说法正确的是( )
2 2
A.该反应涉及离子键和共价键的断裂与形成
B.该反应中,化学能只转变为热能
C.断开1moHH键和1 mol Cl-Cl键所吸收的总能量小于形成1molH-C1键所放出的能量
D.反应物所具有的总能量高于生成物所具有的总能量
解析:A项,H、Cl 与HCl含有的化学键均为共价键,该反应只涉及共价键的断裂与形成,错误;B项,该反应的化
2 2
学能可以转化为热能,也可以转化为光能等其他形式的能量,错误;C项,该反应为放热反应,所以断开1molH一H
键和1 mol Cl-Cl键所吸收的总能量小于形成2molH-Cl键所放出的能量,错误;D项,因为反应为放热反应,所以反
应物所具有的总能量高于生成物所具有的总能量,正确。答案:D
11.下列图示变化为吸热反应的是( )
解析:反应物的总能量小于生成物的总能量,反应为吸热反应,符合题意,A正确;反应物的总能量大于生成物的总能量,反应为放热反应,与题意不符,B错误;浓硫酸稀释放出热量,与题意不符,C错误;锌与稀盐酸的反应为放热
反应,与题意不符,D错误。答案:A
12.在25℃、101kPa下,1mol白磷(化学式为P)完全燃烧放出的热量和4mol红磷(化学式为
4
P)完全燃烧放出的热量关系如图所示。由此判断,下列说法正确的是( )
A.由红磷转化为白磷是吸热反应,等质量时红磷比白磷能量高,白磷比红磷稳定
B.由红磷转化为白磷是放热反应,等质量时红磷比白磷能量低,红磷比白磷稳定
C.由红磷转化为白磷是放热反应,等质量时红磷比白磷能量高,白磷比红磷稳定
D.由红磷转化为白磷是吸热反应,等质量时红磷比白磷能量低,红磷比白磷稳定
解析:能量越低越稳定,根据示意图可知等质量时红磷的能量低,红磷稳定,因此
4P(s)=P (s)为吸热反应,答案选D。
4
13.已知断裂1mlN≡N键所吸收的能量为946kJ,形成1molN-H键所放出的能量为391kJ,若1molN (g)和3molH (g)完全反
2 2
应生成2 mol NH (g)时放出的能量为92.2kJ,则断裂1 mol H-H键所吸收的能量是( )
3
A .436 kJ B.433.6kJ C. 463 kJ D.869 kJ
解析:1molN(g)和3molH (g)完全反应生成2 moI NH (g)时,需要断裂1molN≡N键和3molH-H键,形成6moN-H键,
2 2 3
设断裂1molH-H键所吸收的能量是x,则946kJ+3x-391kJ×6=92.2kJ,x≈436kJ。答案:A
14.已知:H(g)+F (g)=2HF(g) △H=-270kJ·mol-1,下列说法正确的是( )
2 2
A.在相同条件下,1molH (g)与1molF (g)的能量总和大于2 mol HF(g)的能量
2 2
B. 1mol H(g)与1molF (g)反应生成2mol液态HF放出的热量小于270kJ
2 2
C.该反应的逆反应是放热反应
D.该反应过程的能量变化可用图表示
解析:该反应为放热反应,在相同条件下,1molH (g)与1molF (g)的能量总和大于2 mol HF(g)的能量,A项正确;由
2 2
于物质从气态变为液态放出热量,所以1molH (g)与1molF (g)反应生成2mol液态HF放出的热量大于270kJ,B项错误;
2 2
该反应的逆反应是吸热反应,C项错误;反应物总能量应比生成物总能量高,D项错误。答案:A
16.键能是气态基态原子形成1mol化学键释放的最低能量。键能的大小可以衡量化学键的强弱,也可以用于计算化学
反应的反应热。下表是一些化学键的键能:
化学键 C—H C—F H—F F-F
键能/(kJ·mol-1) 414 489 565 155
根据键能数据计算每消耗1 mol CH 时,反应CH(g)+4F (g)=CF (g)+4HF(g)的热效应为( )
4 4 2 4
A.放热1940kJ B.吸热1940kJ C.放热485kJ D.吸热485kJ
解析:由题给信息可知,△H=断裂化学键所吸收的总能量-形成化学键所释放的总能量=4×414kJ·mol-1+4×155kJ·mol-1-
1-4×565kJ·mol-1=-1940kJ·mol-1答案:A
16.白磷与氧气可发生反应:P(g)+5O(g)=P O (g)。已知断裂下列化学键需要吸收的能量分别为P-P a kJ/mol、P-O
2 4 10
bkJ/mol、P=O ckJ/mol、氧氧键dkJ/mol。根据如图所示的分子结构和有关数据估算该反应的△H,下列正确的是( )
A.(4a+5d-4c-12b)kJ/mol B. (4c+12b-6a-5d)kJ/ mol C.(4c+126-4a-5d)kJ/ mol D.(6a+5d-4c-12b) kJ/mol
解析:△H=断裂化学键所吸收的总能量一形成化学键所释放的总能量,在 1molP (g)与5mlO (g)反应生成1molP O (g)
4 2 4 10
的 过 程 中 , 要 断 裂 6 mol P-P 键 、 5mol 氧 氧 键 , 同 时 会 形 成 4molP=O 键 、 12 mol P-O 键 , 故
△H=6akJ/mol+5dkJ/mol-4c kJ/mol-12b kJ/mol=(6a+5d-4c-12b)kJ/mol 答案:D
17.下列各选项中两个反应的反应热,其中△H>△H 的是( )
1 2
A.2H(g)+O(g)=2HO(g) △H ; 2H(g)+O(g)=2HO(1) △H
2 2 2 1 2 2 2 2
B.4P(g)+5O (g)=2P O(g) △H; 4P(s)+O (g)=2P O(g) △H
2 2 3 1 2 2 3 2
C.2SO (g)+O(g) 2SO (g) △H; 2SO (g) O(g)+2SO(g) △H
2 2 3 1 3 2 2 2D.已知反应:C(金刚石,s)=C(石墨,s) △H<0。C(金刚石,s)+O(g)=CO (g) △H;C(石墨,s)+O(g)=CO (g) △H
2 2 1 2 2 2
解析:气态水转化为液态水放出热量,故|△H|>|△H|,且 这两个反应均为放热反应,△H为负值,所以△H>△H,A
2 1 1 2
项正确;气态P比固态P的能量高,气态P燃烧放出的热量更多 故|△H|<|△H|,且这两个反应均为放热反应,所以
2 1
△H>△H,B项错误;第一个反应为放热反应,第二个反应为吸热反应,故ΔH>ΔH ,C项错误;金刚石的能量高,燃
2 1 2 1
烧放出的热量多,故|△H|<|△H|,且这两个反应均为放热反应,所以△H<△H,D项错误。答案:A
2 1 1 2
18.在中和反应反应热的测定实验中,不需要用到的仪器是( )
A.玻璃棒 B.烧杯 C.温度计 D.环形玻璃搅拌器
解析:中和热的测定实验中,一定需要的仪器是烧杯、温度计和环形玻璃搅拌器,一定不需要的仪器是玻璃棒。答案:
A
19.下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能量的变化
B.化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量
C.吸热反应在一定条件(如高温、加热等)下也能发生
D.放热的反应在常温下一定很容易发生
解析:任何化学反应都伴随着能量的变化,A项正确;反应物的总能量大于生成物的总能量的反应是放热反应,反之
为吸热反应,B项正确;某些吸热反应可能在高温或加热时进行,如CO 和C的反应,C项正确;并不是所有的放热
2
反应在常温下都能发生,如碳的燃烧,D项不正确。答案:D
20.N 分子结构如图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量。根据以上信息和
4
数据,则由N 生成1mol气态N 的△H为( )
2 4
A.+882kJ/mol B.+441kJ/mol C.-882kJ/mol D.-441kJ/mol
解析:1molN 分子可转化为2molN ,1molN 中含6molN一N键,断开6 moI N-N键吸收的热量
4 2 4
为 167kJ·mol-1×6mol=1002kJ,生成 2molN 时放出热量为 942k·mol-1×2mol=1884kJ,则 1molN 生成
2 4
2molN 放出热量为 1884kJ-1002kJ=882k,则由 N 生成 1mo1气态 N 需要吸收的热量为 882kJ,即
2 2 4
△H=+882kJ·mol-1,A项正确。答案:A
21.(1)CO 与CH 经催化重整,制得合成气:CH(g)+CO (g) 2CO(g)+2H(g)。已知上述反应中相关的化学键键能
2 4 4 2 2
数据如下:
化学键 C-H C=O H-H
键能(kJ/mol) 413 745 436 1075
则该反应的△H=
(3) H 和F 反应的能量变化图可用 (填“A”或“B”)表示。
2 2
参考答案:(1)+120kJ/mol (2)A
解析:(1)该反应中△H=断开旧化学键的键能总和一形成新化学键的键能总和,即△H=(413kJ/mol×4+745kJ/mol×2)-
(1075kJ/mol×2+436kJ/mol×2)=+120kJ/mol。(2)H 和F 的反应是放热反应,反应物的总能量大于生成物的总能量,即 A
2 2
图像正确。
22.50mL0.50mol/L盐酸与50mL0.55mol/ L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中放出的
热量可计算中和反应的反应热。
请回答下列问题
(3) 从实验装置上看,图中缺少的一种玻璃仪器是
(4) (2)外壳与内筒之间隔热层的目的是
(3)简易量热计如果不盖杯盖,所测得中和反应反应热数值的绝对值 (填“偏大”“偏小”或“无影
响”)。
(4)实验中若改用60mL0.50mol/L盐酸和50mL0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”或“不相等”),所测得的中和反应反应热 (填“相等”或“不相等”)。
参考答案:(1)玻璃搅拌器 (2)减少实验过程中的热量损失 (3)偏小 (4)不相等 相等
解析:在测定中和反应反应热时,需使用玻璃搅拌器搅拌,加快酸与碱的反应。实验中要尽可能减少热量损失,否则会
使测得的中和反应反应热数值的绝对值偏小。实验中反应的酸和碱增多,放出的热量也增多,但测得的中和反应反应
热不变,因为对于同一反应来说,|中和反应反应热|与所用酸、碱溶液的体积无关,根据公式|中和反应反应热|=
,可算出中和反应反应热。