文档内容
第一章 有机化合物的结构特点与研究方法
第一节 研究有机化合物的一般方法
第1课时 有机化合物的分离提纯
1.(2020·昆明市官渡区第一中学高二月考)下列实验操作能达到目的的是( )
实验目的 实验操作
A 除去乙醇中的水 加入生石灰,蒸馏
B 除去乙烷中的乙烯 将混合气体通入酸性高锰酸钾溶液
C 鉴别苯和环己烷 加入溴水振荡,静置后观察分层及颜色差异
D 分离苯和溴苯 加水后分液
2.(2020·北方民族大学附属中学高二月考)下列实验操作正确且能达到对应实验目的的是( )
A.石油的分馏 B.煤的干馏
C.除去乙烷中的乙烯 D.提纯乙酸乙酯
3.(2020·浙江高三其他模拟)分离常温下苯酚与水混合物的操作中所用主要仪器是
A. B. C. D.
4.(2020·深圳市高级中学高一期中)2015年10月,我国科学家屠呦呦获得诺贝尔奖生理学或医学奖,
以表彰她发现青蒿素(C H O),显著降低了疟疾患者的死亡率。右下图为青蒿素的分子结构模型和结构简
15 22 5
式,则下列相关说法正确的是( )A.受“青蒿一握,以水二升渍,绞取汁”启发,屠呦呦使用乙醚提取青蒿素属于化学变化
B.青蒿素分子中氧元素化合价均为+2价
C.青蒿素的发现、提纯、合成及修饰过程中体现了化学学科的重要特征
D.282 g的青蒿素中含碳原子数目为14N
A
5.(2020·北方民族大学附属中学高二月考)除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方
法错误的是( )
选
含杂质的物质 试剂 除杂方法
项
A 乙烯(SO ) NaOH溶液 洗气
2
B 苯(Br) Fe粉 蒸馏
2
C 乙醇(水) 生石灰 蒸馏
D KNO 固体(NaCl) 水 重结晶
3
6.(2020·汉中市龙岗学校高三月考)下列有机物的除杂方法正确的是(括号中的是杂质)
A.乙酸(乙醛):加入新制的氢氧化铜悬浊液.加热
B.苯(苯酚):加入溴水,过滤
C.乙醇(水):加入氧化钙,蒸馏
D.乙酸乙酯(乙酸):加入氢氧化钠溶液洗涤,分液
7.将溴水分别与酒精、己烯、己烷和四氯化碳四种试剂混合,充分振荡后静置,下列现象与所加试剂不
相吻合的是( )
A B C D
与溴水混合
酒精 己烯 己烷 四氯化碳
的试剂
现象8.下列关于物质的分离、提纯实验中的一些操作或做法,不正确的是( )
A.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤
B.在组装蒸馏装置时,温度计的水银球应在蒸馏烧瓶支管口
C.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加入少量蒸馏水
D.96% 的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏
9.(2020·宁夏银川一中高一期中)下列各组混合物中,不能用分液漏斗进行分离的是( )
A.碘和四氯化碳 B.四氯化碳和饱和碳酸钠溶液
C.水和汽油 D.苯和水
10.(2020·浙江温州·高二期中)下列图示与操作名称不对应的是( )
A.过滤 B.洗气
C.分液 D.蒸馏
11.(2020·浙江温州·高三月考)实验室用95%乙醇溶液制备无水乙醇,通常需要用到的仪器是
A. B. C. D.
12.(2020·陕西西安市西光中学高一月考)甲、乙两种有机物的物理性质如下,将甲、乙混合物分离应采
取的方法是
物质 密度/(g·cm-3) 沸点/℃ 水溶性 溶解性
甲 0.7893 68.5 溶 溶于乙
乙 1.220 100.7 溶 溶于甲
A.蒸馏 B.分液 C.蒸发 D.萃取13.(2020·济南市历城第二中学高三期中)乙酸异戊酯是组成蜜蜂信息素质的成分之一,具有香蕉的香味,
实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:
+ +H O
2
相对分子质量 密度/(g·cm-3) 沸点/℃ 水中溶解性
异戊醇 88 0.8123 131 微溶
乙酸 60 1.0492 118 溶
乙酸异戊酯 130 0.8670 142 难溶
(实验步骤)
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50分钟,
反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量
无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯
3.9 g 。回答下列问题:
(1)装置B的名称是_____。
(2)①在洗涤操作中,第一次水洗的主要目的是_____
②在洗涤、分液操作中,应充分振荡,然后静置,待分层后_____(填标号)。
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
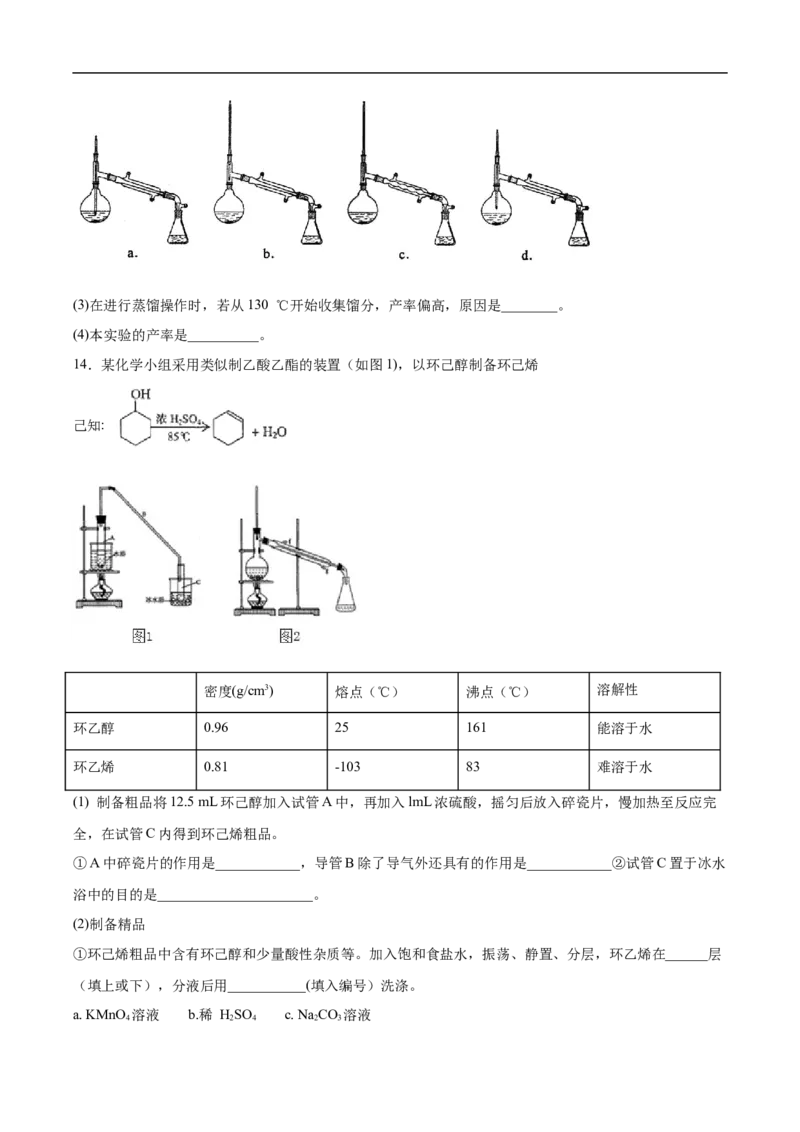
③在蒸馏操作中,仪器选择及安装都正确的是_____(填标号)。(3)在进行蒸馏操作时,若从130 ℃开始收集馏分,产率偏高,原因是________。
(4)本实验的产率是__________。
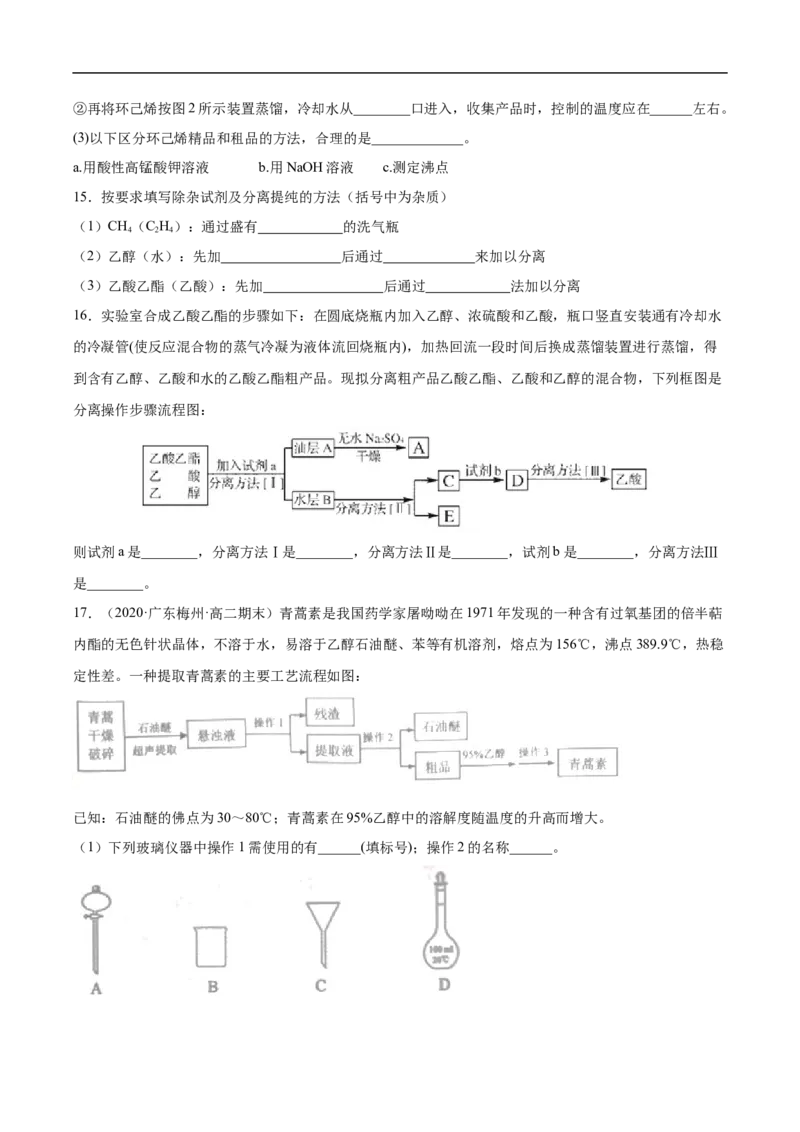
14.某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
己知:
密度(g/cm3) 熔点(℃) 沸点(℃) 溶解性
环乙醇 0.96 25 161 能溶于水
环乙烯 0.81 -103 83 难溶于水
(1) 制备粗品将12.5 mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,慢加热至反应完
全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________②试管C置于冰水
浴中的目的是______________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环乙烯在______层
(填上或下),分液后用___________(填入编号)洗涤。
a. KMnO 溶液 b.稀 HSO c. Na CO 溶液
4 2 4 2 3②再将环己烯按图2所示装置蒸馏,冷却水从________口进入,收集产品时,控制的温度应在______左右。
(3)以下区分环己烯精品和租品的方法,合理的是_____________。
a.用酸性高锰酸钾溶液 b.用NaOH溶液 c.测定沸点
15.按要求填写除杂试剂及分离提纯的方法(括号中为杂质)
(1)CH(C H):通过盛有 的洗气瓶
4 2 4
(2)乙醇(水):先加 后通过 来加以分离
(3)乙酸乙酯(乙酸):先加 后通过 法加以分离
16.实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水
的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得
到含有乙醇、乙酸和水的乙酸乙酯粗产品。现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下列框图是
分离操作步骤流程图:
则试剂a是________,分离方法Ⅰ是________,分离方法Ⅱ是________,试剂b是________,分离方法Ⅲ
是________。
17.(2020·广东梅州·高二期末)青蒿素是我国药学家屠呦呦在1971年发现的一种含有过氧基团的倍半萜
内酯的无色针状晶体,不溶于水,易溶于乙醇石油醚、苯等有机溶剂,熔点为156℃,沸点389.9℃,热稳
定性差。一种提取青蒿素的主要工艺流程如图:
已知:石油醚的佛点为30~80℃;青蒿素在95%乙醇中的溶解度随温度的升高而增大。
(1)下列玻璃仪器中操作1需使用的有______(填标号);操作2的名称______。(2)操作3的步骤是蒸发浓缩、_______、过滤洗涤、干燥。
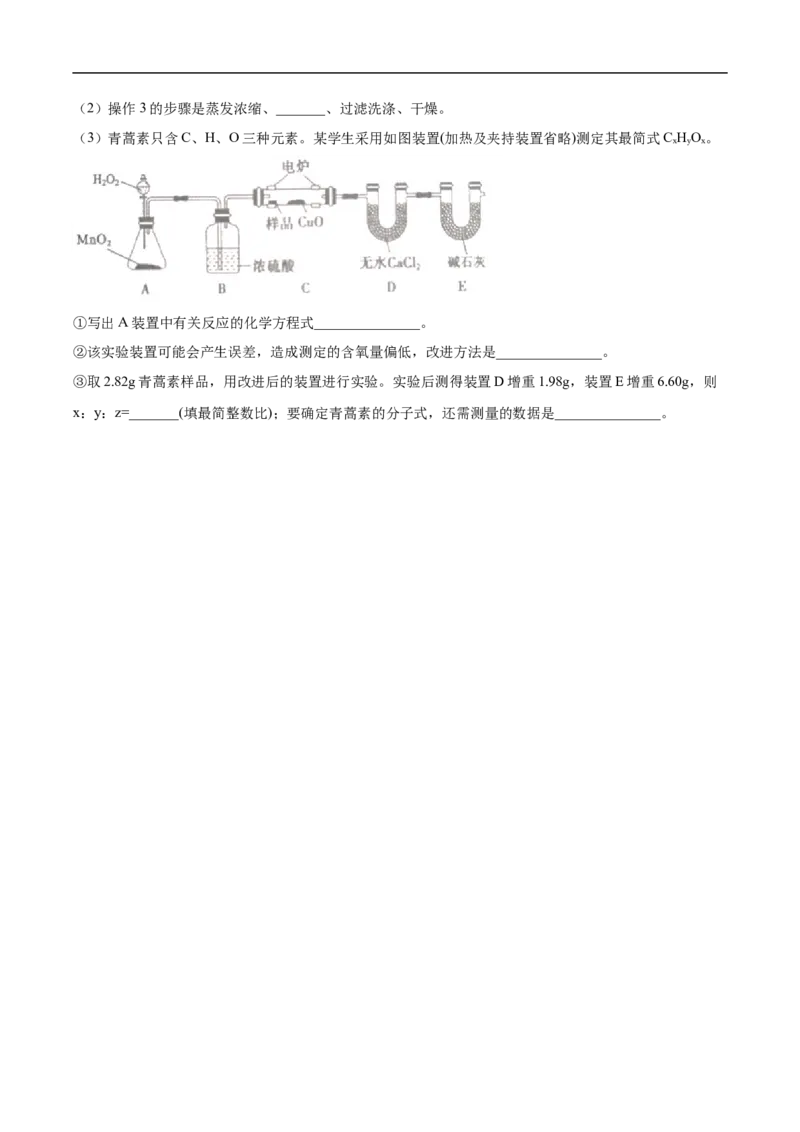
(3)青蒿素只含C、H、O三种元素。某学生采用如图装置(加热及夹持装置省略)测定其最简式C HO。
x y x
①写出A装置中有关反应的化学方程式_______________。
②该实验装置可能会产生误差,造成测定的含氧量偏低,改进方法是_______________。
③取2.82g青蒿素样品,用改进后的装置进行实验。实验后测得装置D增重1.98g,装置E增重6.60g,则
x:y:z=_______(填最简整数比);要确定青蒿素的分子式,还需测量的数据是_______________。