文档内容
第五章 化工生产中的重要非金属元素
第2节 氮及其化合物
(第2课时 氨和铵盐)
一、选择题
1.在NO 与水的反应中( )
2
A.氮元素的化合价不发生变化 B.NO 只是氧化剂
2
C.NO 只是还原剂 D.NO 既是氧化剂又是还原剂
2 2
2.用下面实验方案进行离子检验,方案设计不严密的是
A.检验试液中的 :试液 无色无味气体 先变浑浊后澄清
B.检验试液中的 :试液 无沉淀 白色沉淀
C.检验试液中的 :试液 火焰颜色为黄色
D.检验试液中的 :试液 刺激性气味气体 试纸变蓝
色
3.下列说法正确的是
A.浓硫酸具有强氧化性,常温下可与铁单质剧烈反应
B.SO 能杀菌消毒防腐,常用作食品添加剂
2
C.氨气因有刺激性气味,因此不用来作制冷剂
D.所有铵盐受热均可以分解,产物均有NH
3
4.将导出的氨气接近下列物质时,不会产生白烟的是
A.氯气 B.浓 HSO C.浓 HCl D.浓 HNO
2 4 3
5.下列有关NH 两个实验说法中正确的是
3
学科网(北京)股份有限公司A.两个实验均表现了NH 易溶于水 B.两个实验均表现了NH 易挥发
3 3
C.两个实验均表现了NH 是碱性气体 D.两个实验均表现了NH 是还原性气体
3 3
6.下列关于铵盐的叙述中正确的是
①所有铵盐中,氮元素化合价都是-3价
②所有铵盐都溶于水
③铵态氮肥不宜与碱性物质混合使用
④铵盐都是离子化合物
⑤铵盐都能与碱反应,不能与酸反应
A.①③④ B.②③④
C.①②③④ D.①②③④⑤
7.为检验一种氮肥的成分,某学习小组同学进行了以下实验:①加热氮肥样品生成气体,
其中一种气体能使湿润的红色石蕊试纸变蓝,另一种无色无味气体能使澄清石灰水变浑浊。
②取少量该氮肥样品溶于水,并加入少量BaCl 溶液,没有明显变化。由此可知该氮肥的
2
主要成分是
A.NH HCO B.NH Cl C.(NH)CO D.NH NO
4 3 4 4 2 3 4 3
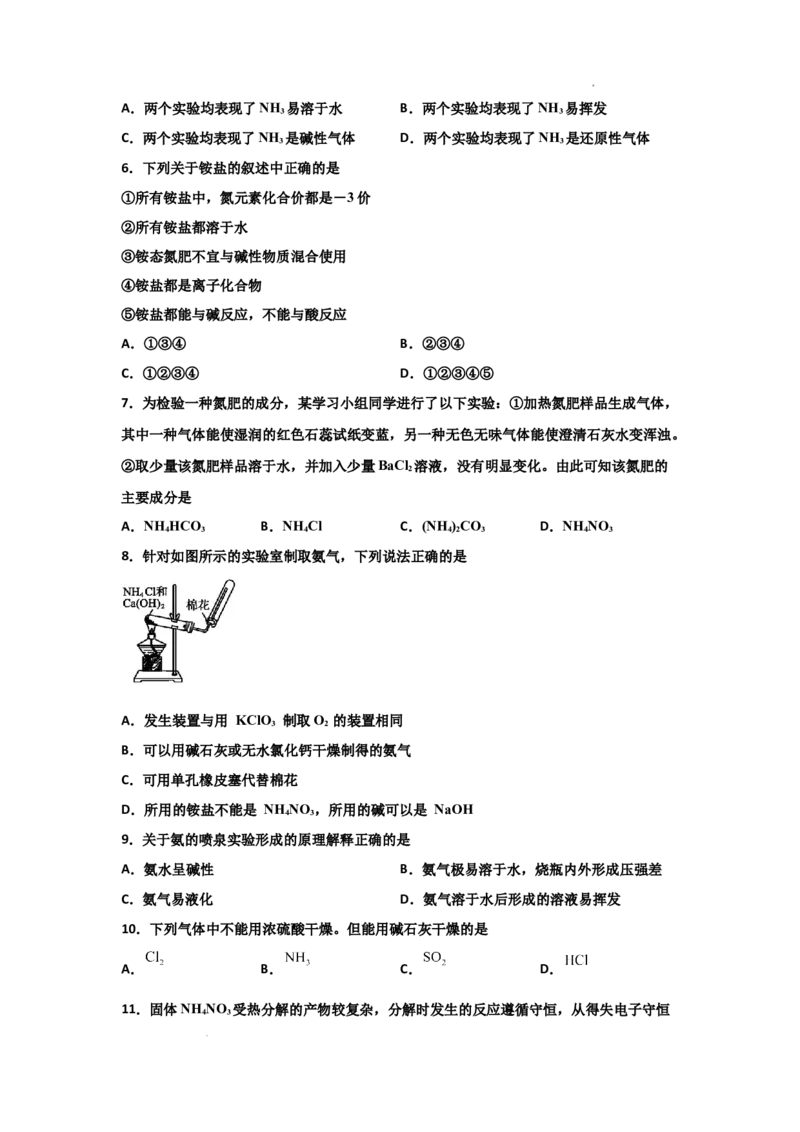
8.针对如图所示的实验室制取氨气,下列说法正确的是
A.发生装置与用 KClO 制取O 的装置相同
3 2
B.可以用碱石灰或无水氯化钙干燥制得的氨气
C.可用单孔橡皮塞代替棉花
D.所用的铵盐不能是 NH NO ,所用的碱可以是 NaOH
4 3
9.关于氨的喷泉实验形成的原理解释正确的是
A.氨水呈碱性 B.氨气极易溶于水,烧瓶内外形成压强差
C.氨气易液化 D.氨气溶于水后形成的溶液易挥发
10.下列气体中不能用浓硫酸干燥。但能用碱石灰干燥的是
A. B. C. D.
11.固体NH NO 受热分解的产物较复杂,分解时发生的反应遵循守恒,从得失电子守恒
4 3
学科网(北京)股份有限公司和元素守恒方面分析,对NH NO 热分解的产物猜想不正确的是( )
4 3
A.N、HNO 、HO B.NO、HO
2 3 2 2 2
C.NO 、NO、HO D.NH 、HNO
2 2 2 3 3
12.氢化铵(NHH)与氯化铵结构相似,又已知NH H与水反应有氢气产生,下列叙述中不
4 4
正确的是( )
A.NH H是由NH +和H-构成的
4 4
B.NH H固体投入少量水中,有两种气体产生
4
C.NH H中的H-半径比锂离子半径大
4
D.NH H溶于水后,形成的溶液显酸性
4
二、非选择题
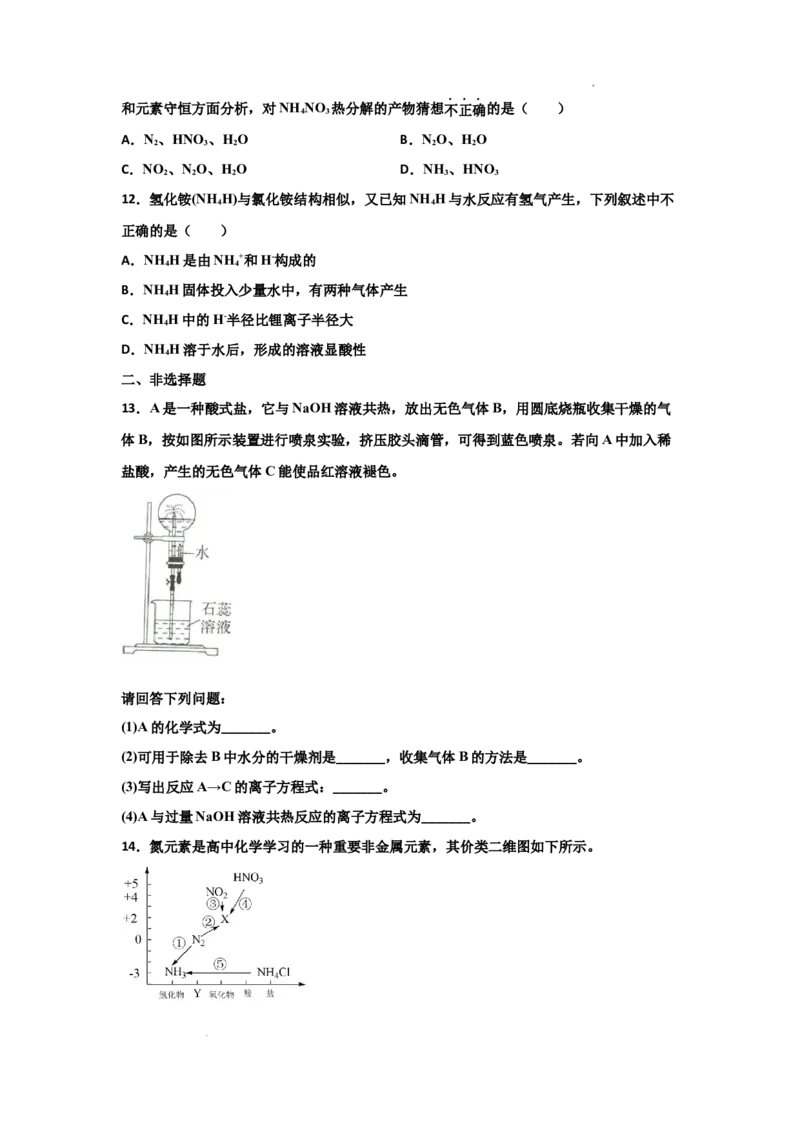
13.A是一种酸式盐,它与NaOH溶液共热,放出无色气体B,用圆底烧瓶收集干燥的气
体B,按如图所示装置进行喷泉实验,挤压胶头滴管,可得到蓝色喷泉。若向A中加入稀
盐酸,产生的无色气体C能使品红溶液褪色。
请回答下列问题:
(1)A的化学式为_______。
(2)可用于除去B中水分的干燥剂是_______,收集气体B的方法是_______。
(3)写出反应A→C的离子方程式:_______。
(4)A与过量NaOH溶液共热反应的离子方程式为_______。
14.氮元素是高中化学学习的一种重要非金属元素,其价类二维图如下所示。
学科网(北京)股份有限公司(1)图中物质“X”的化学式是___________;“Y”代表的物质类别是___________。
(2)工业上可利用反应① 实现氮的固定,用双线桥标出该反
应的电子转移方向和数目___________;自然界在雷电作用下通过反应___________(填图中
编号)也能将氮固定。
(3) 溶于水可发生反应③,其离子方程式为___________;铜与足量稀硝酸反应能实
现反应④的转化,其中硝酸表现出的性质是___________。
(4)实验室利用反应⑤制备 。写出其化学方程式_______; 在工业上的用途
_______(任填一个)。
学科网(北京)股份有限公司学科网(北京)股份有限公司