文档内容
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 B A B B A B B
题号 8 9 10 11 12 13 14
答案 B D A D B D C
【解析】
1.维生素C具有还原性,常添加在水果罐头中防止食品被氧化腐败,A正确。六六六等有机
氯杀虫剂广泛使用会对环境及人类健康造成危害,B 错误。使用氮肥可以提高作物产量,
同时科学合理使用氮肥可以有效防止污染,C 正确。燃料脱硫、脱硝的目的是减少空气污
染和酸雨的产生,D正确。
2.氯乙烯分子中碳原子的杂化方式为sp2杂化,分子中碳氯键采用的成键轨道是sp2−p,A正
确。同系物必须是结构相似,相差一个或若干个CH 原子团的同类物质, 属于
2
酚类, 属于芳香醇,不是同类物质,不互为同系物,B错误。同素异形体是
指同种元素组成的不同种单质,而单晶硅为硅单质,而石英是SiO ,两者不属于同素异形
2
体,C 错误。2p 的电子云图为哑铃形: ,其中的黑点不代表核外电子的运
y
动轨迹,表示电子出现的几率的多少,小黑点越密集的地方,电子出现的几率越高,小黑
点越稀薄的地方,电子出现的几率越小,D错误。
3.氢氟酸能与二氧化硅反应生成氟化硅和水,氟化钙与浓硫酸反应生成硫酸钙和氟化氢,则
糊状混合物中的氢氟酸能与玻璃中的二氧化硅反应,可用于刻蚀玻璃,A 正确。SO 可用
2
于丝织品漂白是由于其能与丝织品中有色成分化合为不稳定的无色物质,B 错误。清洗附
有银镜的试管用稀硝酸,反应原理为3Ag+4HNO (稀)=3AgNO +NO↑+2H O,C正确。
3 3 2
通入 CO 后,发生反应 NaClO+CO +H O=NaHCO +HClO,漂白液消毒能力增强,D
2 2 2 3
正确。
4.根据H S的组成解答,A不正确。H 18O和2H O的相对分子质量均为20,质子数均为10,
2 2 2
2g 该混合物的物质的量为 0.1mol,含有的质子数为 N ,B 正确。17g H S 与足量 CuSO
A 2 4
溶液充分反应后,将生成48g难溶物,C不正确。未给体积,D不正确。
化学参考答案·第1页(共6页)5.苯环上连接的叔丁基碳为sp3杂化,不可能所有碳原子共平面。
6.乙酸乙酯的制备演示实验如图所示,A正确。由于CCl 不溶于水,故向硫酸四氨合铜溶液
4
中加入CCl 不能起到减弱水分子极性的作用,不能制得硫酸四氨合铜晶体,B符合题意。
4
制备检验醛基用的 Cu(OH) ,氢氧化钠溶液需过量,C 正确。将闸门与电源的负极相连,
2
属于外加电源阴极保护法,D正确。
7.CH COONH 溶液为中性,浓度越小,水解程度越大,不能比较pH判断水的电离程度,A
3 4
错误。灼烧铜丝至其表面变黑、灼热,伸入盛有某有机物的试管中,铜丝恢复亮红色,可
能是因为该有机物含有醇羟基,和黑色的CuO反应生成亮红色的铜,也可能是因为该有机
物含有羧基,将黑色的CuO反应掉剩余亮红色的铜,B正确。试管里出现凝胶,说明生成
硅酸,根据强酸制备弱酸的原理可知酸性:盐酸>硅酸,但盐酸不是最高价氧化物对应的
水化物,不能判断非金属性的强弱,C 错误。麦芽糖是还原性糖,加热麦芽糖和稀 H SO
2 4
混合溶液,冷却后的溶液也有还原性,无法证明麦芽糖是否发生了水解,D错误。
8.甲既能与酸反应又能与碱反应,应为Al O 或Al(OH) ,甲由单质A和B反应生成,应为
2 3 3
Al O ,则A为Al,B为O ,C为H ,乙为NaAlO ,丁为AlCl ,丙为H O,戊为Al(OH) ,
2 3 2 2 2 3 2 3
往AlCl 溶液中滴加氨水得Al(OH) ,A错误。甲为Al O ,硬度大,熔点高,可做手表轴
3 3 2 3
承或耐火材料,B正确。甲→乙+丙反应的离子方程式为Al O +2OH-=2AlO+H O,
2 3 2 2
C错误。A→乙+C反应的化学方程式为2Al+2NaOH+6H O=2Na[Al(OH) ] +3H ↑,D
2 4 2
错误。
9.分子式为C H N O ,A错误。光照下不能发生苯环上氢原子的取代,B错误。酚的酸性
11 12 2 3
比碳酸弱,不能与碳酸氢钠反应,C错误。环上的碳原子、氮原子的杂化类型都为sp2,D
正确。
10.四氨合铜离子的配位体 NH 的 N 原子与中心 Cu2+之间以配位键结合,在配位体 NH 中
3 3
H—N键为极性共价键,不存在离子键,A错误。FeS 的电子式为 ,存在离子
2
键、非极性共价键,B正确。根据图乙可知距离Fe2+最近且等距离的Fe2+在12个棱心,
1 1 1
C 正确。根据均摊法,Fe2+: 1214,S2: 8 64,一个晶胞中有 4 个
4 2 8 2
4Mg/mol
FeS 2 ,其密度为 (a N 1 A 0 / m 7c o m l )3 4M N a 1 3 021 g/cm3;晶胞中Fe2+位于S2 2 所形成的正八面体
A
2 2
a a 2a
的体心,该正八面体的边为两个面心相连,其距离为 nm nm,D正确。
2 2 2
化学参考答案·第2页(共6页)11.电负性为F > Cl > P,A错误。HZO是HClO,为弱酸,中心原子O为sp3杂化,分子空
间构型为V型,B错误。元素W(N)最高价含氧酸为硝酸, Y(P)最高价含氧酸为磷
酸,C错误。X(F)、W(N)和氢三种元素可形成氟化铵,铵根和氟离子皆为10电子离
子,D正确。
12.Ca (PO ) F的K 更小,使用含氟牙膏时,Ca (PO ) (OH)可转化为Ca (PO ) F,A不正确。
5 4 3 sp 5 4 3 5 4 3
牙 釉 质 的 主 要 成 分 是 Ca (PO ) (OH) , 根 据 元 素 守 恒 c(Ca2+) ∶
5 4 3
[c(H PO)+c(HPO2)+c(PO3)]=5∶3,因此 c(Ca2+)>c(H PO)+c(HPO2)+c(PO3),B
2 4 4 4 2 4 4 4
正确。由磷酸二氢钠溶液呈酸性可知,磷酸二氢根离子在溶液中的电离程度大于水解程
度,C 不正确。糖附着在牙齿上发酵时,会产生 H+,根据 Ca (PO ) OH(s)
5 4 3
5Ca2+(aq)+3PO3(aq)+OH-(aq) ,氢离子消耗氢氧根离子,使平衡正向移动,导致羟磷灰
4
石溶解,加重龋齿,D错误。
13.在原电池中,阳离子向正极移动,则钠离子可以通过交换膜X,A正确。放电时负极反应
为 Zn+4OH-−2e-=Zn(OH)2,正极反应为 Fe3++e-=Fe2+,当反应转移 1mol 电
4
子时,左侧负极附近的溶液中阴离子负电荷数目减少 1mol,右侧正极附近溶液中阳离子
的正电荷数目减少1mol,为维持电荷守恒,就会有1mol Na+通过阳离子交换膜进入中间
腔室内;右侧有 1mol Cl-通过阴离子交换膜进入中间腔室内,导致中间腔室内的溶液中
将增加1mol NaCl,B正确。充电时,阳极反应式为Fe2+−e-=Fe3+,每转移2mol电
子,参与反应的铁元素质量为 112g,C 正确。根据分析可知,充电时③区溶液的酸性不
变,D错误。
10
14.开始时,总压强为 560kPa ,CH 的分压 p(CH )=560kPa 280kPa,A 正确。50min
4 4
20
280kPa40%
后反应到达平衡,v(CH )= 2.24kPa/min,B正确。保持温度不变,若增大
4
50min
压强,CO+H O=CO +H 平衡不移动,CH +H O=CO+3H 平衡逆向移动,CH
2 2 2 4 2 2 4
转化率降低,同时压强增大,反应速率加快,应为曲线丁,C错误。保持压强不变,若降
低温度,CO+H O=CO +H 平衡正向移动,CH +H O=CO+3H 平衡逆向移动,
2 2 2 4 2 2
CO转化率增大,同时降低温度,反应速率减慢,应为曲线戊,D正确。
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共15分)
(1)V O +2OH-=2VO+H O
2 5 3 2
(2)加热、不断搅拌等(1分)
化学参考答案·第3页(共6页)(3)是
(4)酸性(1分)
(5)90
(6)利用同离子效应,促进NH VO 尽可能析出完全,提高V元素的利用率
4 3
(7)①<(1分) ②2H O−4e-=4H++O ↑ ③10.8
2 2
【解析】(1)“碱浸”时V O 转化为VO,反应的离子方程式为V O +2OH-=2VO+
2 5 3 2 5 3
H O。
2
(2)通常采取加热、不断搅拌等措施防止胶体的生成、易于沉淀分离。
c{[Al(OH) ]}
(3)该反应的平衡常数K 4 100.63,当 pH 为 8.37 时,c{[Al(OH) ]-}=
c(OH) 4
10−5mol·L−1,故[Al(OH) ] -此时刚好沉淀完全。
4
(4)根据其作用机理可表示为VO2++2HR(有机层) VOR (有机层)+2H+,欲反萃取
2
操作需增大H+浓度,故加入的反萃取剂为酸性溶液。
(5)萃取、反萃取前后V的化合价都是+5价,则根据得失电子守恒可知,还原剂失去电
子的物质的量等于氧化剂得到电子的物质的量,设V的总回收率为α,则2×10×α=6×3,
则α=0.90,即90%。
(6)利用同离子效应,促进NH VO 尽可能析出完全,提高V元素的利用率。
4 3
(7)①泡沫 Ni 网电极为阴极,FTO@BiVO 电极为阳极,因此电势:泡沫 Ni 网电极<
4
FTO@BiVO 电极;
4
②FTO@BiVO 电极为阳极,发生的电极反应式应为2H O−4e-=4H++O ↑。
4 2 2
③当电解电压为U V时,电解生成的HCHO和HCOOH的物质的量之比为5∶3,生成
3
1mol HCHO转移4mol电子,生成1mol HCOOH转移2mol电子,图中可以读出生成甲醛
Q 36% Q m%
的 FE%为 36%, 总 ∶ 总 =5∶3,m=10.8,图中生成 HCOOH 的法拉第效
4 2
率为10.8%。
16.(每空2分,共14分)
(1)水浴加热
(2)恒压滴液漏斗 提供还原剂
(3)洗去产品表面的(绿茶提取液)剩余附着的黄酮、多酚等有机物
(4)取最后一次洗涤液少许于试管中,加入盐酸酸化后加入BaCl 溶液,若无白色沉淀产
2
生,则证明已洗净
化学参考答案·第4页(共6页)(5)①xCr3++(1−x)Fe3++2H O=Cr Fe OOH↓+3H+
2 x (1−x)
②纳米铁分散附着在FeO 表面,增大表面积;纳米铁将FeO 还原为Fe2+,Fe2+与CrO2反
3 4 3 4 2 7
应(答对1点得两分)
【解析】(1)操作(b)中,需维持55~60℃,故最适宜采用水浴加热。
(2)盛装绿茶提取液的仪器名称为恒压滴液漏斗;加入的绿茶提取液中含较多黄酮、多
酚等还原性物质,是获得纳米铁的还原剂。
(3)因绿茶提取液中含较多黄酮、多酚等有机物,均易溶于乙醇、丙酮等有机溶剂。故
用乙醇洗去产品表面的绿茶提取液剩余附着的黄酮、多酚等有机物。
(4)判断产品洗涤干净的实质是检验最后一次洗涤液中是否含有SO2或 Fe2+。即:取最
4
后一次洗涤液少许于试管中,加入盐酸酸化后加入BaCl 溶液。若无白色沉淀产生,则证
2
明已洗净。
(5)①根据反应过程描述可知,Fe3+和 Cr3+共沉为 Cr Fe OOH 的离子方程式为
x (1−x)
xCr3++(1−x)Fe3++2H O=Cr Fe OOH↓+3H+。
2 x (1−x)
②结合图示信息和实验结论可知,实验 3 降解CrO2效率显著增大的原因是Fe O 有磁
2 7 3 4
性,吸引生物炭负载纳米铁颗粒,使其分散附着在Fe O 表面,增大表面积;纳米铁能将
3 4
含三价铁元素的物质(Fe O 、Fe3)还原为含二价铁元素的物质(Fe O 、Fe2),含二
3 4 3 4
价铁元素的物质能继续与CrO2反应,降解效率显著增大。
2 7
17.(除特殊标注外,每空2分,共14分)
(1)CO(g)+NO (g)=NO(g)+CO (g) ΔH=−227kJ/mol
2 2
(2)AD
(3)①未达到(1分) ②温度升高催化剂活性降低
(4)①N ②102
2
(5)①La3+(1分) ②
18.(除特殊标注外,每空2分,共15分)
(1)2−溴苯酚(邻溴苯酚)(1分)
(2)
(3)保护羟基(1分)
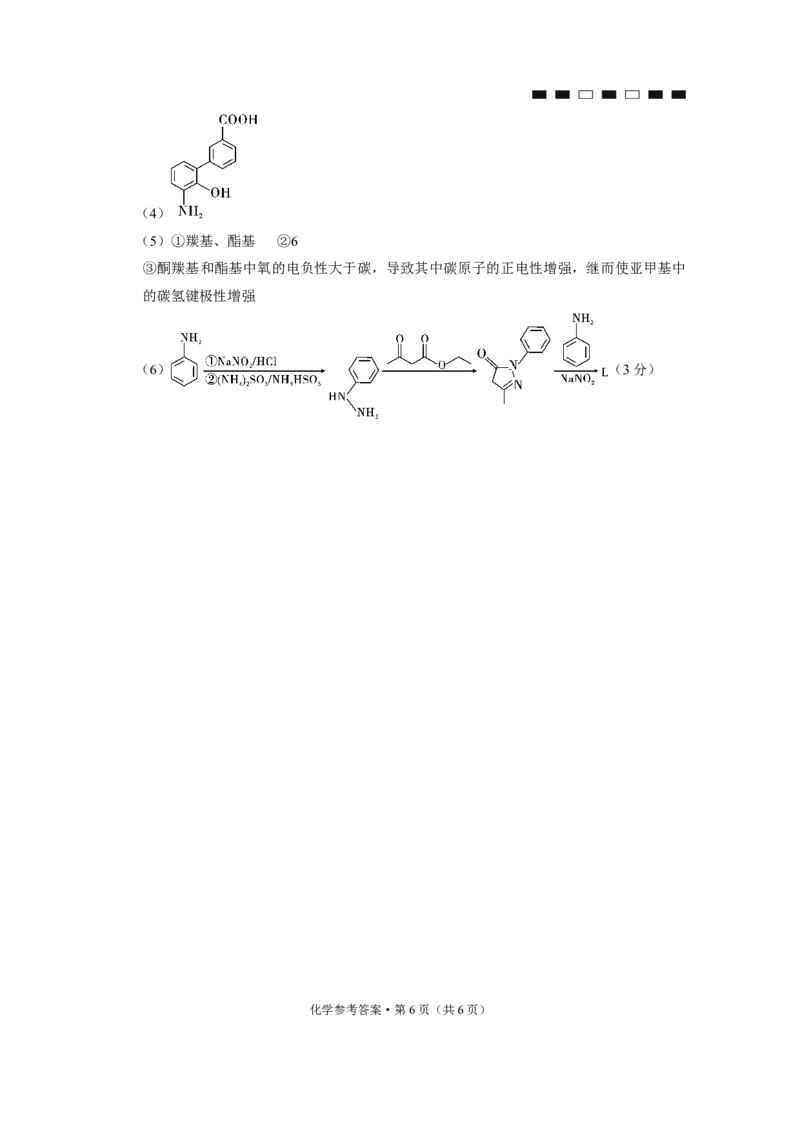
化学参考答案·第5页(共6页)(4)
(5)①羰基、酯基 ②6
③酮羰基和酯基中氧的电负性大于碳,导致其中碳原子的正电性增强,继而使亚甲基中
的碳氢键极性增强
(6) (3分)
化学参考答案·第6页(共6页)