文档内容
广西桂林市部分学校2024-2025学年高一下学期5月联考
化学试题
一、单选题
1.化学与生活密切相关,下列叙述正确的是
A.电车出行促环保,电车中的锂离子电池属于一次电池
B.铝锅不易生锈,可用来长时间存放酸性、碱性食物
C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果,其作用是吸收水果释放出的乙烷
D.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用
2.下列化学用语表示正确的是
A.甲烷分子的空间填充模型: B.HF的电子式:
C.二氧化碳的结构式: D.硫原子结构示意图:
3.在工业生产或实验中,下列做法与调控化学反应速率无关的是
A.煅烧矿石时,向炉膛中鼓入空气增强火势
B.将Fe与稀 反应中的稀 换成稀
C.食品抽真空包装
D.实验室制氢气时,用锌粉代替锌块
4.信息技术离不开芯片,现代芯片离不开高纯度的硅,工业上生产高纯硅的工艺流程如下:
则下列说法正确的是
A.工业上用焦炭还原石英砂制硅的反应为
B.光导纤维的成分为高纯硅
C.上述流程②③需在无氧条件下进行
D.上述流程中能循环利用的物质只有5.某华人科学家和他的团队研发出“纸电池”(如图)。这种一面镀锌、一面镀二氧化锰的超薄电池在使用
印刷与压层技术后,厚度仅为0.5毫米。纸内的离子“流过”水和氧化锌组成电解液,电池总反应式为
Zn+2MnO +H O=ZnO+2MnO(OH)。下列说法正确的是
2 2
A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生氧化反应
C.电池的正极反应式为MnO +H O+e-=MnO(OH)+OH-
2 2
D.当有0.1mol锌溶解时,流经电解液的电子数为1.204×1023
6.有机物 的结构如图所示,下列说法正确的是
A. 分子中含有4种官能团
B. 最多能消耗
C. 的分子式为
D.X既可以与乙醇发生酯化反应,也可以与乙酸发生酯化反应
7.图中实验装置或操作能达到相应实验目的的是
A.装置甲可用于验证反应是否有 生成 B.装置乙可以完成“喷泉”实验
C.装置丙可除去甲烷中的乙烯 D.装置丁可用于制备乙酸乙酯
8.设 为阿伏加德罗常数的值。下列说法正确的是A. 甲基中含电子数为
B.标准状况下 所含的氧原子数为
C. 聚乙烯中含碳碳双键数目为
D.在锌铜原电池中,负极减少 时理论上转移电子数为
9.下列离子方程式正确的是
A.氯化铁溶液溶解铜片:
B.用醋酸溶液除水垢中的 :
C.少量 通入 溶液中:
D.金属钠与水反应:
10.由下列实验操作和现象得出的结论不正确的是
选
实验操作 现象 结论
项
将稀硝酸中加入少量铁粉,充分反应后滴加 有气体生成,溶液呈血 稀硝酸将Fe氧化为
A
KSCN溶液 红色
B 向 中滴加浓盐酸 产生黄绿色气体 氧化性:
C 蘸有浓氨水的玻璃棒靠近溶液X 有白烟 X可能是浓盐酸
D 将 通入酸性高锰酸钾溶液中 溶液褪色 具有漂白性
A.A B.B C.C D.D
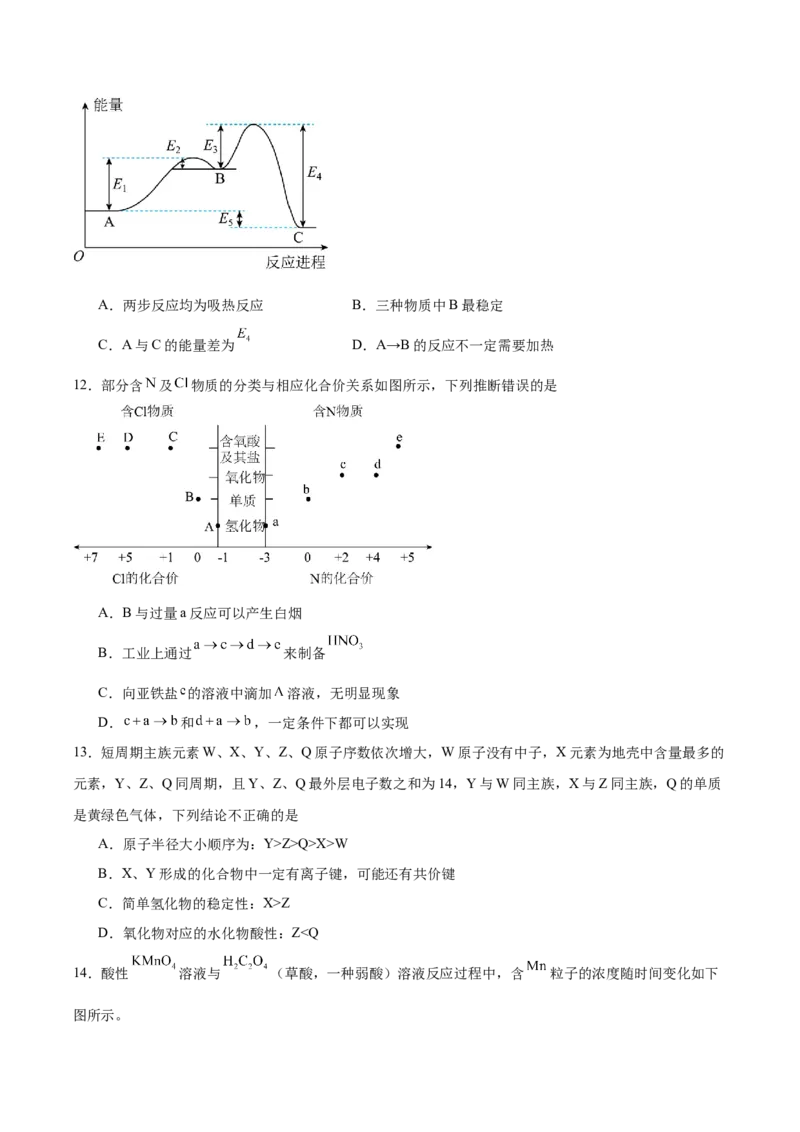
11.某反应由两步反应A→B→C构成,其反应能量曲线如图所示,下列叙述正确的是A.两步反应均为吸热反应 B.三种物质中B最稳定
C.A与C的能量差为 D.A→B的反应不一定需要加热
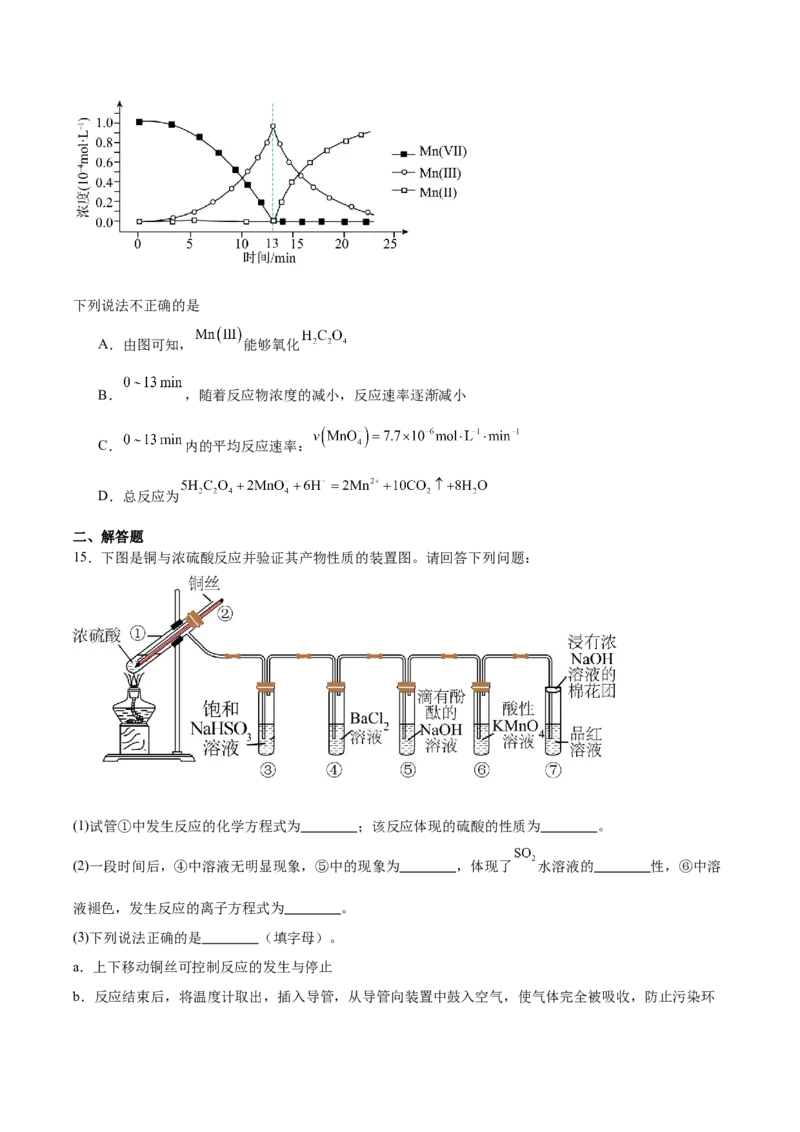
12.部分含 及 物质的分类与相应化合价关系如图所示,下列推断错误的是
A.B与过量a反应可以产生白烟
B.工业上通过 来制备
C.向亚铁盐 的溶液中滴加 溶液,无明显现象
D. 和 ,一定条件下都可以实现
13.短周期主族元素W、X、Y、Z、Q原子序数依次增大,W原子没有中子,X元素为地壳中含量最多的
元素,Y、Z、Q同周期,且Y、Z、Q最外层电子数之和为14,Y与W同主族,X与Z同主族,Q的单质
是黄绿色气体,下列结论不正确的是
A.原子半径大小顺序为:Y>Z>Q>X>W
B.X、Y形成的化合物中一定有离子键,可能还有共价键
C.简单氢化物的稳定性:X>Z
D.氧化物对应的水化物酸性:Z
”“=”或“<”) ;若升高温度,则 (填 “增大”“减小”或“不变”)。 ② 时,生成 的物质的量为 ,在第 时, 的转化率为 。 ③已知图中曲线分别代表 、 、 浓度变化,则无关曲线为 (填字母)。 ④下列能说明该反应已达到平衡状态的是 (填字母)。 a.容器内同时存在 、 和 b.混合气体颜色不再改变 c.混合气体的平均相对分子质量不变 d.容器内密度保持不变 (2)氮氧化物 能引起雾霾、光化学烟雾、酸雨等环境问题。某科研机构设计方案利用原电池原理处理 氮氧化合物( ),其原理如图所示。①在电池工作时,电子流入电极 (填“A”或“B”)。 ②电极B的电极方程式: 。 18.A是一种重要的有机化工原料,其产量通常用来衡量一个国家的石油化学工业发展水平,通过一系列 化学反应,可以制得成千上万种有用的物质。结合下图物质间转化关系回答问题: (1)A的结构简式为 。 (2)③的反应类型为 ,E中的官能团名称是 。 (3)高分子化合物G是由丙烯通过加聚反应制得的,G的结构简式为 。 (4) 的化学方程式为 。 (5)写出反应②的化学方程式: 。 (6) 与足量的金属 完全反应,生成标准状况下氢气的体积为 。 (7)写出E与HBr发生加成反应可能会生成的产物的结构简式: 。题号 1 2 3 4 5 6 7 8 9 10 答案 D C B C C D B A D D 题号 11 12 13 14 答案 D C D B 15.(1) 强氧化性和酸性 (2) 溶液褪色 酸性 (3)ab (4)bc 16.(1)第三周期第IVA族 (2) 搅拌[或适当提高硫酸(或 )浓度] 受热易分解 (3) (4) 和 ② (5) 17.(1) = 增大 0.012 65% bc (2) B 18.(1) (2) 取代反应 酯基、碳碳双键 (3) (4) (5) (6)4.48