文档内容
班级 姓名 学号 分数
第 07 单元 有机化合物
(B 卷•提升能力)
(时间:75分钟,满分:100分)
一、选择题(本题共16小题,每小题3分,共48分)
1.有关有机化合物中碳原子的成键特点,下列说法错误的是
A.碳原子最外层有4个电子,每个碳原子形成4个价键
B.碳原子间只能形成碳链,不能形成碳环
C.在CH 分子中,四个碳氢共价键的长度和强度均相同
4
D.在正丁烷分子中,4个碳原子形成的碳链为锯齿形,不为直线形
【答案】B
【解析】A.碳的原子序数为6,碳原子最外层有4个电子,每个碳原子可形成4个价键,A正确;
B.碳原子间不但能形成碳链,还可以形成碳环,如环丁烷( ),B错误;
C.在CH 分子中,形成4个碳氢键,四个碳氢键的键长与键能均相同,C正确;
4
D.饱和碳与周围四个原子形成四面体结构,因此正丁烷分子中,4个碳原子形成的碳链为锯齿形,不为
直线形,D正确;
答案选B。
2.下列有关甲烷的取代反应的叙述正确的是
A.甲烷与氯气以物质的量之比为1∶4混合时只生成CCl
4
B.甲烷与氯气反应生成的产物中CHCl的量最多
3
C.甲烷与氯气的取代反应生成的产物为混合物
D.1mol甲烷生成CHCl 最多消耗1mol氯气
2 2
【答案】C
【解析】A.甲烷与氯气一旦发生取代反应就不会停止在某一步,四种有机物都会产生,故得不到纯净的
CHCl,A错误;
3
B.甲烷与氯气的反应中每取代1 mol氢原子,消耗1 mol氯气,生成1 mol HCl,故产物中HCl最多,B
错误;
1 / 16
学科网(北京)股份有限公司C.由A分析可知,甲烷与氯气的取代反应生成的产物为混合物,C正确;
D.1 mol甲烷生成CHCl 最多消耗2mol氯气,D错误。
2 2
故选C。
3.下列说法错误的是( )
A.烷烃的通式为C H ,随n值的增大,碳元素的质量分数逐渐增大
n 2n+2
B.分子式为C H 和分子式为C H 的烷烃的一氯代物的数目不可能相同
2 6 5 12
C.丙烷的球棍模型为
D. 和 属于同种物质
【答案】B
6
【详解】A.由烷烃中碳元素的质量分数计算式 12n = 1 可知,随着碳原子数逐渐增多碳元素的质量
7+
14n+2 n
分数逐渐增大,A正确;
B.C H 的一氯代物只有一种,C H 中的新戊烷的一氯代物也只有一种,因此可能相同,B错误;
2 6 5 12
C.符合丙烷球棍模型的表示方式,C正确;
D.二者的分子式相同,结构相同,属于同种物质,D正确;
故选B。
4.下列有关烷烃(C H )的叙述不正确的是
4 10
A.分子中碳原子不在同一直线上
B.分子中所有原子不可能在同一平面内
C.符合该分子式的烷烃的一氯代物共有4种
D.不能发生氧化反应
【答案】D
【解析】A.烷烃(C H )中的C原子具有甲烷的四面体结构,分子中四个C原子不可能在同一直线上,A
4 10
正确;
B.烷烃(C H )中的C原子具有甲烷的四面体结构,分子中所有原子不可能在同一平面上,B正确;
4 10
C.烷烃(C H )有CHCHCHCH 和CHCH(CH ) 两种结构,每种结构中都含有2种不同的H原子,故符
4 10 3 2 2 3 3 3 2
合该分子式的烷烃的一氯代物共有4种,C正确;
D.该物质是烃,属于可燃物,其能够完全燃烧产生CO、HO,燃烧反应属于氧化反应,D错误;
2 2
故合理选项是D。
5.下列化学用语不正确的是
2 / 16
学科网(北京)股份有限公司A.丙烷分子的球棍模型:
B.乙烯分子的电子式:
C.CH(CH)CH 与CHCH(CH ) 互为同分异构体
3 2 2 3 3 3 2
D.CCl 是正四面体空间结构
4
【答案】B
【解析】A.丙烷分子中有三个碳原子,碳原子间以单键相连,端点碳原子各连3个氢原子,中间碳原子
连有2个氢原子,碳原子半径大于氢原子的半径,所以 是表示丙烷分子的球棍模型,故A正
确;
B. 乙烯分子的两个碳原子间以双键相连,故B错误;
C.CH(CH)CH 与CHCH(CH ) 分子式相同,均为C H ,结构不同,互为同分异构体,故C正确;
3 2 2 3 3 3 2 4 10
D.CCl 可以看做是甲烷中的4个H被Cl代替,甲烷是正四面体结构,所以CCl 也正四面体结构,故D
4 4
正确;
故选B。
6.欲除去甲烷中混有的乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶
A.澄清石灰水,溴水 B.酸性高锰酸钾溶液,浓硫酸
C.溴水,碱石灰 D.浓硫酸,酸性高锰酸钾溶液
【答案】C
【解析】A.乙烯与澄清石灰水不反应,乙烯含有碳碳双键,可与溴水发生加成反应除去乙烯,但甲烷气
体中混有水蒸气,不能得到纯净的甲烷,故A错误;
B.乙烯可与酸性高锰酸钾发生氧化还原反应生成二氧化碳气体,引入新的杂质,故B错误;
C.乙烯含有碳碳双键,可与溴水发生加成反应,然后用碱石灰干燥可得纯净、干燥的甲烷,故C正确;
D.乙烯可与酸性高锰酸钾发生氧化还原反应生成二氧化碳气体,引入新的杂质,故D错误;
故选:C。
7.下列关于乙烯和环丙烷( )的说法中,正确的是
3 / 16
学科网(北京)股份有限公司A.二者都为不饱和烃 B.二者互为同分异构体
C.二者互为同系物 D.二者碳、氢元素的质量比相同
【答案】D
【详解】A.环丙烷属于饱和烃,A错误;
B.二者的分子式不相同,因此不互为同分异构体,B错误;
C.二者的结构不相似,因此不互为同系物,C错误;
D.乙烯分子式为C H,环丙烷分子式为C H,它们的分子中碳、氢原子个数比相同,碳、氢元素的质量
2 4 3 6
比相同,D正确;
故选D。
CH CHCH CH
8.根据乙烯的性质可以推测丁烯( 2 2 3)的性质,下列说法不正确的是
A.丁烯能使酸性高锰酸钾溶液褪色
B.聚丁烯的结构可以表示为
C.丁烯能在空气中燃烧
CH BrCH CH CH Br
D.丁烯与溴发生加成反应的产物是 2 2 2 2
【答案】D
CH CHCH CH
【解析】A.乙烯中含碳碳双键,能使酸性高锰酸钾溶液褪色,丁烯( 2 2 3)中也含碳碳双键,
也能使酸性高锰酸钾溶液褪色,A正确;
CH CHCH CH
B.乙烯中含碳碳双键,能发生加聚反应生成聚乙烯,丁烯( 2 2 3)中也含碳碳双键,也能发生
加聚反应生成聚丁烯,其结构简式为: ,B正确;
C.乙烯在空气中能燃烧生成二氧化碳和水,丁烯也能在空气中能燃烧生成二氧化碳和水,C正确;
CH BrCHBrCH CH
D.乙烯与溴发生加成反应生成BrCHCHBr,丁烯与溴发生加成反应的产物为: 2 2 3,D
2 2
错误;
答案选D。
4 / 16
学科网(北京)股份有限公司9.在下列物质中,不能与 发生化学反应的是
①CHCHOH(酸催化) ②CHCHCHCH ③Na ④CHCOOH(酸催化)
3 2 3 2 2 3 3
A.①② B.①④ C.只有② D.③④
【答案】C
【解析】根据有机物的结构简式可知,含有的官能团为醇羟基、羧基,含有苯环;
①含有羧基,可与CHCHOH(酸催化)发生酯化反应,不符合题意;
3 2
②有机物不与CHCHCHCH 发生化学反应,符合题意;
3 2 2 3
③含有的羟基与羧基均可与Na发生化学反应,不符合题意;
④含有羟基可与CHCOOH(酸催化)发生酯化反应,不符合题意;
3
答案选C。
10.某单烯烃与 加成后的产物为 ,则该烯烃可能的结构简式有
H
2
A.1种 B.2种 C.3种 D.4种
【答案】C
【详解】将相邻的两个含有氢原子的碳原子之间的单键变双键即可,如 在
①②③④处均可使碳碳单键变为碳碳双键,但①②处位置是等效的,所以该烯烃可能的结构简式有3种。
答案选C。
11.聚苯乙烯是一种无毒、无臭的热塑性材料,被广泛应用于食品包装材料、电器绝缘外壳、光学仪器以
及日用产品等。工业以苯和乙烯为原料制备聚苯乙烯的流程如下图所示(部分条件略去),下列说法错误
的是( )
5 / 16
学科网(北京)股份有限公司A.过程①生成乙苯,反应类型为加成反应
B.过程②生成苯乙烯,苯乙烯分子中最多有16个原子共平面
C.过程③原子利用率为100%,反应类型为加聚反应
D.上述流程中涉及的五种有机物均可使酸性高锰酸钾溶液褪色
【答案】D
【详解】A.过程①中苯分子断裂C—H键,乙烯分子断裂碳碳双键中的较活泼的键,然后二者结合生成
乙苯,反应类型为加成反应,A正确;
—CH CH
B.苯乙烯可看作苯分子中的1个氢原子被 2取代产生的物质,由于苯分子、乙烯分子都是平
—CH CH
面结构, 和 2之间的单键可以通过旋转使所有原子都在同一平面上,所以最多有16个
原子共平面,B正确;
C.过程③为苯乙烯加聚生成聚苯乙烯,C正确;
D.在题述流程涉及的物质中,苯、聚苯乙烯不能使酸性高锰酸钾溶液褪色,D错误;
故选D。
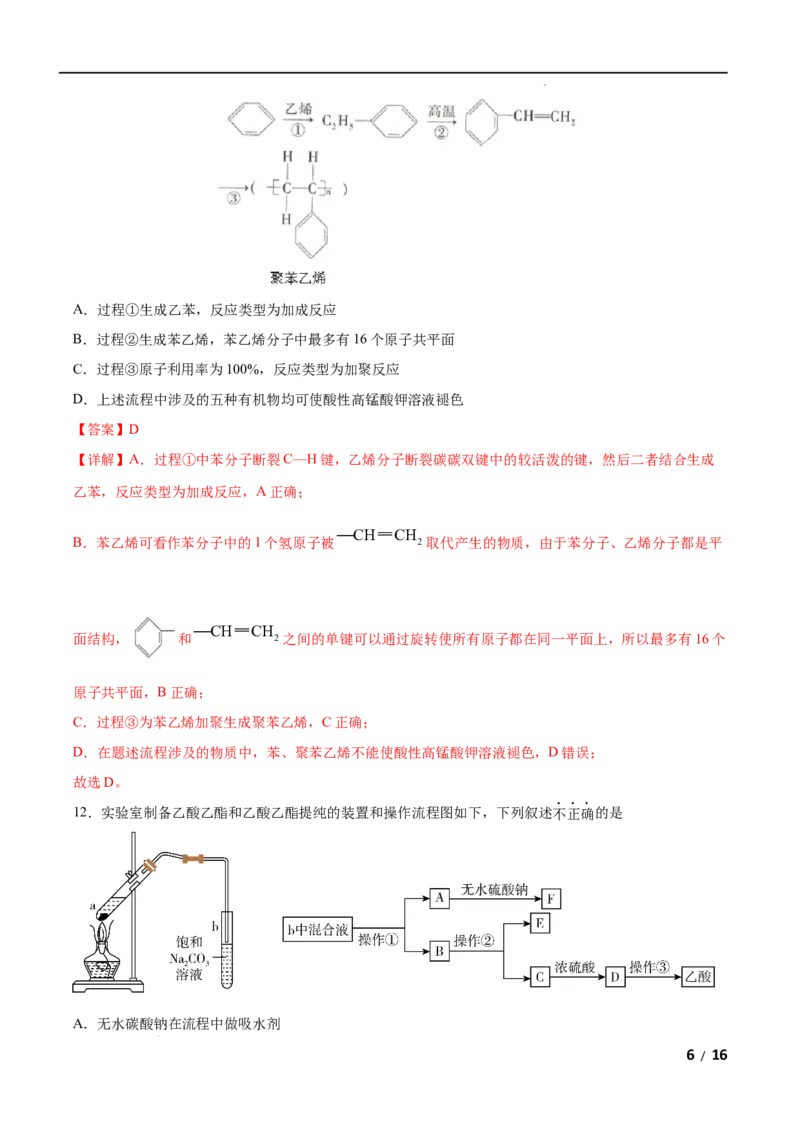
12.实验室制备乙酸乙酯和乙酸乙酯提纯的装置和操作流程图如下,下列叙述不正确的是
A.无水碳酸钠在流程中做吸水剂
6 / 16
学科网(北京)股份有限公司B.操作①为分液
C.向试管中先加入浓硫酸,然后边振荡试管边慢慢加入乙醇,再加入冰醋酸
Na CO
D.试管b中饱和 3 3溶液的作用是吸收蒸出的少量乙酸和乙醇,减小乙酸乙酯的溶解
【答案】C
【解析】实验室制备乙酸乙酯时,向试管中先加无水乙醇,再缓慢加入浓硫酸,冷却后再加入无水乙酸,
加热,用饱和碳酸钠溶液接受,将b中混合液分液得到乙酸乙酯和乙酸钠和乙醇混合溶液,用无水硫酸钠
干燥乙酸乙酯,将乙酸钠和乙醇混合溶液蒸馏得到乙醇和乙酸钠,向乙酸钠溶液中加入硫酸得到乙酸和硫
酸钠,再蒸馏得到乙酸。
A.A是乙酸乙酯,乙酸乙酯中有水分,因此无水碳酸钠在流程中做吸水剂,起干燥作用,故A正确;
B.b中是不相溶的两种液体分离,因此操作①为分液,故B正确;
C.向试管中先加入乙醇,然后边振荡试管边慢慢加入浓硫酸,冷却后再加入冰醋酸,故C错误;
Na CO
D.试管b中饱和 3 3溶液的作用是吸收蒸出的少量乙酸,溶解乙醇,降低乙酸乙酯溶解度,减小乙酸
乙酯的溶解,故D正确。
综上所述,答案为C。
13.二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式如
下:
HO—CH CH—O—CH CH—OH
2 2 2 2
下列有关二甘醇的叙述中不正确的是( )
A.符合通式C H O
n 2n 3
B.和乙醇中化学键类型相同
C.能和金属钠反应
D.能使酸性KMnO 溶液褪色
4
【答案】A
【解析】二甘醇分子式为C H O ,不符合通式C H O ,A错误;二甘醇和乙醇中的化学键都是共价键,
4 10 3 n 2n 3
C—H、C—O、O—H,B正确;分子中含有羟基,可以与Na反应,C正确;分子中含有羟基,能被酸性
高锰酸钾氧化,D正确。
14.下列说法中正确的是 ( )
A.淀粉和纤维素都是多糖,它们是由许多单糖混合而成的
B.蔗糖是重要的双糖,它的相对分子质量小于葡萄糖相对分子质量的2倍
C.蔗糖、淀粉和纤维素水解的最终产物都是葡萄糖
D.含葡萄糖1 mol的水溶液与足量金属钠反应,得到2.5 mol H
2
7 / 16
学科网(北京)股份有限公司【答案】B
【解析】淀粉和纤维素都是多糖,它们是由许多单糖缩聚而成的,故A错;蔗糖的水解产物是果糖和葡萄
糖,故C错;葡萄糖溶液中的水也与Na反应生成H,故D错。
2
15.下列说法正确的是
A.可用碘水检验淀粉是否水解完全
B.人体摄入的油脂、淀粉、葡萄糖、蛋白质必须经过水解才能吸收
C.利用乙酸乙酯或油脂在碱性条件下的水解反应来制取肥皂
D.加热、紫外线、酒精、福尔马林、饱和硫酸钠溶液会使蛋白质发生盐析,具有可逆性
【答案】A
【解析】A.若淀粉水解完全,则加入碘水后不变蓝,可用碘水检验淀粉是否水解完全,故A正确;
B.人体摄入的油脂、淀粉、蛋白质必须经过水解才能吸收,但葡萄糖不需要水解即可被人体吸收利用,
故B错误;
C.油脂在碱性条件下的水解反应又称皂化反应,用于制取肥皂,生成的高级脂肪酸盐是肥皂的主要成分,
而乙酸乙酯的碱性水解不能生成高级脂肪酸盐,不能用于制取肥皂,故C错误;
D.加热、紫外线、酒精、福尔马林都会使蛋白质发生变性,不可逆,饱和硫酸钠溶液会使蛋白质发生盐
析,具有可逆性,故D错误;
故选A。
16.某有机物的结构简式如图所示,下列关于这种有机物的说法不正确的是
①分子中含有苯环,属于芳香烃
②既能使溴水褪色,又能使酸性KMnO 溶液褪色
4
③既能和乙酸发生酯化反应,又能和乙醇发生酯化反应
④1mol该有机物分别与足量的Na、NaHCO 反应,产生气体的物质的量之比是2∶1
3
A.1种 B.2种 C.3种 D.4种
【答案】B
【解析】①分子中含有苯环,还含有羧基和羟基,则该物质不属于芳香烃,①项错误;
②该分子含有碳碳双键,则既能使溴水褪色,又能使酸性KMnO 溶液褪色,②项正确;
4
③该分子含有羧基和羟基,则既能和乙酸发生酯化反应,又能和乙醇发生酯化反应,③项正确;
8 / 16
学科网(北京)股份有限公司④1mol该有机物分别与足量的Na、NaHCO 反应,分别产生1mol氢气和1mol二氧化碳,则产生气体的物
3
质的量之比是1∶1,④项错误;
答案选B。
二、非选择题(本题共5小题,共52分)
17.(12分)写出下列各烷烃的分子式。
(1)烷烃A在同温同压下蒸气的密度是H 的50倍____。
2
(2)烷烃B的分子中含有200个氢原子____。
(3)1L烷烃C的蒸气完全燃烧时,生成同温同压下16L的水蒸气____。
(4)分子中含有22个共价键的烷烃D____。
(5)0.1mol烷烃E完全燃烧,消耗标准状况下的O11.2L____。
2
(6)室温下相对分子质量最大的气态直链烷烃F____。
【答案】(1)C H
7 16
(2)C H
99 200
(3)C H
15 32
(4)C H
7 16
(5)C H
3 8
(6)C H
4 10
【解析】烷烃的通式为C H ;
n 2n+2
(1)烷烃A在同温同压下蒸气的密度是H 的50倍,则A的相对分子质量为50×2=100,则12n+(2n+2)=10,
2
n=7,化学式为C H ;
7 16
(2)烷烃B的分子中含有200个氢原子,则2n+2=200,n=99,化学式为C H ;
99 200
(3)1L烷烃C的蒸气完全燃烧时,生成同温同压下16L的水蒸气,相同条件下气体体积比等于物质的量比,
则1个C分子中含有氢原子的数目为16×2=32,则n=15,化学式为C H ;
15 32
(4)烷烃C H 中共价键的数目为3n+1,分子中含有22个共价键的烷烃D,则n=7,化学式为C H ;
n 2n+2 7 16
n+1
n+ mol
(5)1mol烷烃C H 完全燃烧消耗O 的物质的量为 2 ,0.1mol烷烃E完全燃烧,消耗标准状况
n 2n+2 2
下的O11.2L,O 的物质的量11.2L÷22.4L/mol=0.5mol,则1molE完全燃烧消耗O 的物质的量为5mol,
2 2 2
n+1
n+ =5,n=3,化学式为C H;
2 3 8
(6)室温下相对分子质量最大的气态直链烷烃F为正丁烷,化学式为C H 。
4 10
9 / 16
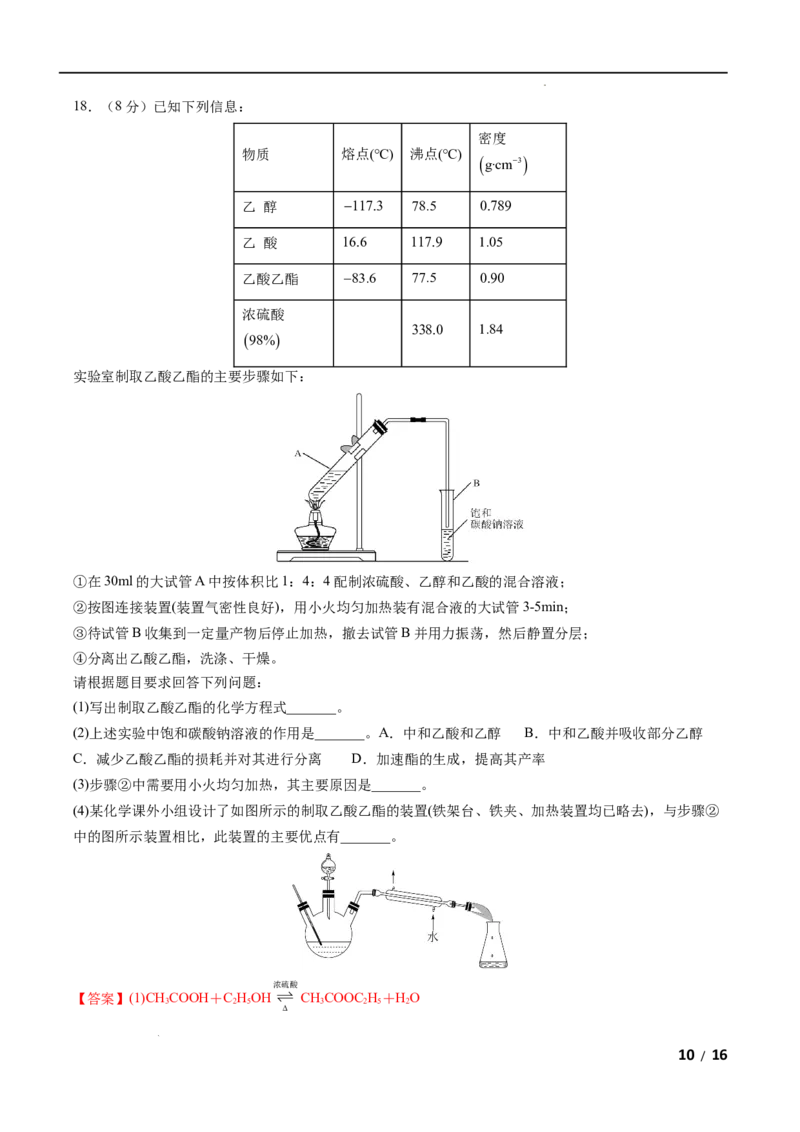
学科网(北京)股份有限公司18.(8分)已知下列信息:
密度
物质 熔点(℃) 沸点(℃)
g·cm3
乙 醇 117.3 78.5 0.789
乙 酸 16.6 117.9 1.05
乙酸乙酯 83.6 77.5 0.90
浓硫酸
338.0 1.84
98%
实验室制取乙酸乙酯的主要步骤如下:
①在30ml的大试管A中按体积比1:4:4配制浓硫酸、乙醇和乙酸的混合溶液;
②按图连接装置(装置气密性良好),用小火均匀加热装有混合液的大试管3-5min;
③待试管B收集到一定量产物后停止加热,撤去试管B并用力振荡,然后静置分层;
④分离出乙酸乙酯,洗涤、干燥。
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式_______。
(2)上述实验中饱和碳酸钠溶液的作用是_______。A.中和乙酸和乙醇 B.中和乙酸并吸收部分乙醇
C.减少乙酸乙酯的损耗并对其进行分离 D.加速酯的生成,提高其产率
(3)步骤②中需要用小火均匀加热,其主要原因是_______。
(4)某化学课外小组设计了如图所示的制取乙酸乙酯的装置(铁架台、铁夹、加热装置均已略去),与步骤②
中的图所示装置相比,此装置的主要优点有_______。
浓硫酸
【答案】(1)CH 3 COOH+C 2 H 5 OH CH 3 COOC 2 H 5 +H 2 O
10 / 16
学科网(北京)股份有限公司(2)BC
(3)减少原料损失,减少副产物
(4)①增加了温度计,有利于控制发生装置中反应液的温度;②增加了分液漏斗,有利于及时补充反应混合
液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙酯
【解析】利用乙醇和乙酸发生酯化反应生成乙酸乙酯,且用饱和碳酸钠分离除杂,得到纯净的乙酸乙酯。
(1)实验室利用无水乙醇和乙酸在浓硫酸的催化下加热制得乙酸乙酯,制取乙酸乙酯的化学方程式为:
浓硫酸
CH 3 COOH+C 2 H 5 OH CH 3 COOC 2 H 5 +H 2 O;
(2)饱和碳酸钠溶液的作用主要有3个:①使混入乙酸乙酯中的乙酸与NaCO 反应而除去,②使混入的乙
2 3
醇溶解.③使乙酸乙酯的溶解度减小,减少其损耗及有利于它的分层和提纯.答案选BC;
(3)由题中给出的各物质的主要物理性质,根据各物质的沸点数据可知,乙酸(117.9℃)、乙醇(78.0℃)的沸
点都比较低,且与乙酸乙酯的沸点(77.5℃)比较接近,若用大火加热,反应物容易随生成物(乙酸乙酯)一起
蒸出来,导致原料的大量损失;另一个方面,温度太高,可能发生其他副反应;
(4)图2与图1所示装置相比,此装置的主要优点有①增加了温度计,有利于控制发生装置中反应液的温度;
②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收
集产物乙酸乙酯。
19.(10分)有机化合物与人类的生活、健康密不可分,糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综
合症,以高血糖为主要标志。长期摄入高糖食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖(C H O),下列说法不正确的是___________。
6 12 6
a.葡萄糖属于碳水化合物,其分子式可表示为C (H O) ,则每个葡萄糖分子中含6个HO
6 2 6 2
b.糖尿病人尿糖高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
c.葡萄糖为人体提供能量
d.淀粉水解的最终产物是葡萄糖
(2)木糖醇[CHOH(CHOH) CHOH]是一种甜味剂,糖尿病人食用后血糖不会升高,请预测木糖醇的一种化
2 3 2
学性质:___________。
(3)糖尿病人宜多吃蔬菜和豆类食品等低糖食物,蔬菜中富含维生素,豆类食品中富含蛋白质。下列说法错
误的是___________(填序号)。
a.蛋白质都属于天然有机高分子化合物,且都不溶于水
b.误服可溶性重金属盐时,可以吃熟鸡蛋、生牛奶等解救
c.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
d.用天然彩棉和丝织品均不可用加酶洗衣粉洗涤
(4)在日常生活中,下列做法错误的是___________。
a.用燃烧法鉴别毛织品和棉织品、合成纤维和羊毛
b.用纯碱洗涤锅盖上的油渍
11 / 16
学科网(北京)股份有限公司c.用闻气味的方法鉴别白酒和米醋
d.用淀粉溶液鉴别加碘盐与非加碘盐
(5)淀粉溶液和蛋白质溶液都是胶体,用一束光通过其溶液,都有___________ ,若检验它们可选用的试剂
是___________。
【答案】(1)a
(2)能与羧酸发生酯化反应(或其他合理的答案)
(3)abcd
(4)d
(5)丁达尔效应 碘水
【解析】(1)a.葡萄糖分子中不含水,a错误;
b.葡萄糖在碱性条件下与新制的氢氧化铜悬浊液共热生成砖红色沉淀,新制氢氧化铜悬浊液可用于检测
糖尿病病人尿液中的葡萄糖,b正确;
c.葡萄糖是人体的供能物质,可为人体提供能量,c正确;
d.淀粉、纤维素水解的最终产物都是葡萄糖,d正确;
答案选a。
(2)木糖醇结构中含醇羟基,所以可以发生酯化反应、氧化反应、与金属钠反应等。
(3)a.蛋白质是天然高分子化合物,但有些蛋白质溶于水,a错误;
b.误服可溶性重金属盐时,可以吃生鸡蛋、生牛奶等解救,熟鸡蛋的蛋清已经变性,不能解救,b错误;
c.纤维素虽然不能被人消化,但可以促进肠胃的蠕动,加强消化和排泄,c错误;
d.天然彩棉的成分是纤维素,可以用加酶洗衣粉洗涤,丝织品的成分是蛋白质,不能用加酶洗衣粉洗涤,
d错误;
答案选abcd。
(4)a.毛织品和羊毛的主要成分为蛋白质,灼烧会有烧焦羽毛气味,棉织品主要成分为纤维素,灼烧会有
烧纸气味,合成纤维灼烧会有特殊气味,a正确;
b.纯碱水解使溶液呈碱性,油渍在碱性条件下可水解,b正确;
c.白酒中有乙醇,米醋中含乙酸,乙醇和乙酸气味不同,因此可用闻气味的方法鉴别白酒和米醋,c正确;
d.加碘盐中含的是碘酸钾,不是碘单质,用淀粉溶液无法鉴别加碘盐与非加碘盐,d错误;
答案选d。
(5)当一束光线透过胶体,从垂直入射光方向可以观察到胶体里出现的一条光亮的“通路”,为胶体的丁达
尔效应;淀粉遇碘变蓝,蛋白质没有这个性质,因此可用碘水检验。
20.(10分)某氨基酸中含有C、N、H、O四种元素,已知除氢原子外,其他原子均达到最外层8电子的
12 / 16
学科网(北京)股份有限公司稳定结构。如图为该氨基酸分子的球棍模型:
(1)氨基酸是________(填“淀粉”“纤维素”“蛋白质”或“油脂”)完全水解的产物,该氨基酸的结构简
式为__________________________________。
(2)该氨基酸中含氧官能团的名称是________。
(3)已知R—NO 为硝基化合物(R—表示烃基),碳原子数相同而结构相似的一元氨基酸与一元硝基化合物互
2
为 同 分 异 构 体 , 写 出 该 氨 基 酸 的 所 有 硝 基 化 合 物 类 同 分 异 构 体 的 结 构 简 式 :
____________________________________。
(4)一定条件下,该氨基酸能与乙醇发生反应,此反应类似于乙酸与乙醇的反应,写出此反应的化学方程式:
_________________________________。
(5)互为同系物的有机物具有相同的官能团,与该氨基酸互为同系物且分子中少一个碳原子的氨基酸的结构
简式为_______________________________。
【答案】(1)蛋白质
(2)羧基
(3)CH CHCHNO 、
3 2 2 2
(4) +CHCHOH +HO
3 2 2
(5)H N—CH —COOH
2 2
【解析】(1)氨基酸是蛋白质完全水解的产物。根据球棍模型及C、H、O、N原子的成键特点可知,表示氢
原子,表示碳原子,◎表示氮原子,○表示氧原子,据此即可得出题给氨基酸的结构简式。
(3)该氨基酸分子中含有3个碳原子,先写出碳链C—C—C,再考虑硝基的位置,据此可知共有两种同分异
构体。
(4)根据乙酸与乙醇反应的化学方程式即可写出该氨基酸与乙醇反应的化学方程式。
(5)氨基酸分子中含有羧基和氨基,分子中比该氨基酸分子少一个碳原子的氨基酸只能是 HN—CH —
2 2
13 / 16
学科网(北京)股份有限公司COOH。
21.(12分)已知A是一种气态烃,其密度在标准状况下是H 的14倍。下列关系图中部分产物可能略去,
2
试回答下列问题:
Δ
已知反应:R—X+NaOH R—OH+NaX(R代表烃基,X代表卤素原子)
(1)C分子的官能团的名称为_______。
(2)反应①~⑦中属于取代反应的是_______。
(3)C与F以物质的量之比2:1反应生成G,反应④的化学方程式为_______。
(4)B物质可在催化剂作用下被空气中的氧气氧化为具有刺激性气味的物质,写出反应的化学方程式
_______。
(5)聚苯乙烯的结构简式为_______。
(6)下列说法正确的是_______。
a.D在一定条件下可能会和水反应生成B和C
b.B和F属于同系物
c.A、B、F和I都能使酸性高锰酸钾溶液褪色
d.与E互为同分异构体的有机物只有1种
【答案】(1)羧基
(2)③④⑤
浓硫酸
(3)HOCHCHOH+2CHCOOH
Δ
CHCOOCH
CHOOCCH + 2H O
2 2 3 3 2 2 3 2
Cu
(4)2CH CHOH + O Δ 2CHCHO + 2H O
3 2 2 3 2
14 / 16
学科网(北京)股份有限公司(5)
(6)acd
【解析】
【分析】
A是一种气态烃,其密度在标准状况下是H 的14倍,A的相对分子质量是28,因此A是乙烯;A和水发
2
生加成反应生成B是乙醇,乙醇被酸性高锰酸钾溶液氧化生成C是乙酸,乙酸和乙醇发生酯化反应生成D
是乙酸乙酯,乙烯和溴单质发生加成反应生成E是BrCHCHBr,根据已知信息E发生水解反应生成F是
2 2
乙二醇,乙二醇和乙酸发生酯化反应生成G为CHCOOCH CHOOCCH ,E和苯发生取代反应生成H,H
3 2 2 3
发生消去反应生成I,I分子中含有碳碳双键,可发生加聚反应生成聚苯乙烯,据此解答。
(1)C是乙酸,分子的官能团的名称为羧基。
(2)酯化反应和水解反应均属于取代反应,根据以上分析可知反应①~⑦中属于取代反应的是③④⑤。
(3)C与F以物质的量之比2:1发生酯化反应生成G,反应④的化学方程式为HOCH CHOH+2CHCOOH
2 2 3
浓硫酸
Δ
CHCOOCH
CHOOCCH + 2H O。
3 2 2 3 2
(4)乙醇可在催化剂作用下被空气中的氧气氧化为具有刺激性气味的物质乙醛,反应的化学方程式为
Cu
2CHCHOH + O Δ 2CHCHO + 2H O。
3 2 2 3 2
(5)聚苯乙烯的结构简式为 。
(6)a.D是乙酸乙酯,在一定条件下能和水发生水解反应生成乙醇和乙酸,a正确;
b.B和F含有的羟基个数不同,二者不属于同系物,b错误;
c.A和I都含有碳碳双键,B、F都含有羟基,因此都能使酸性高锰酸钾溶液褪色,c正确;
d.与E互为同分异构体的有机物只有1种,即CHCHCl ,d正确;
3 2
答案选acd。
15 / 16
学科网(北京)股份有限公司16 / 16
学科网(北京)股份有限公司