文档内容
课时作业
A篇·知识对点训练
1.瓦斯爆炸往往与矿坑中的甲烷有关,下列叙述中错误的是( )
A.点燃甲烷不必事先进行验纯
B.甲烷燃烧放出大量的热,所以是一种很好的气体燃料
C.煤矿的矿井要注意通风并严禁烟火,以防爆炸事故的发生
D.点燃混有空气的甲烷不一定会爆炸
答案 A
解析 A项,甲烷是可燃性气体,点燃前必须先验纯,错误;B项,甲烷燃
烧放热,是很好的气体燃料,正确;C项,煤矿的矿井中有很多的甲烷气体,容
易燃烧爆炸,所以要注意通风并严禁烟火,正确;D项,空气中甲烷含量在5%
~15.4%(体积)范围内遇火将会爆炸,所以点燃混有空气的甲烷不一定爆炸,正
确。
2.等体积的甲烷与氯气混合于一集气瓶中,加盖后置于光亮处,下列有关
实验现象和结论中,正确的是( )
①反应后Cl 完全反应而CH 有剩余
2 4
②瓶内壁有油状液滴生成
③最后有CH 、Cl 、CH Cl、CH Cl 、CHCl 、CCl 、HCl七种物质共存
4 2 3 2 2 3 4
④只有CH Cl和HCl两种产物
3
A.①② B.②③ C.③④ D.①④
答案 B
解析 有机化学反应进行不彻底,故反应后有 CH 和 Cl 剩余,产物有
4 2
CH Cl、CH Cl 、CHCl 、CCl 和HCl。
3 2 2 3 4
3.下列反应属于取代反应的是( )
A.CH ――→C+2H
4 2
B.2HI+Cl ===2HCl+I
2 2
C.CH +2O ――→CO +2H O
4 2 2 2
D.CH +Cl ――→CH Cl+HCl
4 2 3
答案 D
解析 A属于分解反应,B属于置换反应,C属于氧化还原反应(燃烧),D属
于取代反应。
4.已知一些烷烃的沸点,甲烷:-164 ℃;乙烷:-89 ℃;丁烷:-1 ℃;
戊烷:36 ℃。根据以上数据推断丙烷的沸点可能是( )
A.约-40 ℃ B.低于-164 ℃
C.低于-89 ℃ D.高于36 ℃
答案 A解析 依据烷烃熔、沸点的变化规律可知,丙烷的沸点是介于乙烷和丁烷之
间,即高于-89 ℃,低于-1 ℃,A项符合上述要求。
5.美国宇航局(NASA)马里诺娃博士发现了一种比二氧化碳高 104倍的“超
级温室气体”全氟丙烷(C F ),提醒人们慎用含氟物。有关全氟丙烷的说法正确
3 8
的是( )
A.分子中3个碳原子可能处于同一直线上
B.全氟丙烷的电子式为
C.由丙烷转化为全氟丙烷的反应为取代反应
D.全氟丙烷属于烷烃
答案 C
解析 A项,3个碳原子不可能处于同一直线上,错误。B项,电子式中氟
原子周围应有8个电子,错误。C项,丙烷上的氢原子全部被氟原子取代得到全
氟丙烷,正确。D项,全氟丙烷中含有碳、氟元素,不含氢元素,不属于烷烃,
错误。
6.关于CH 和 的叙述正确的是( )
4
A.均能用组成通式C H 来表示
n 2n+2
B.与所有烷烃互为同素异形体
C.因为它们结构相似,所以它们的化学性质相似,物理性质相同
D.通常情况下它们都是气态烷烃
答案 A
解析 二者均为烷烃,互为同系物,化学性质相似,但物理性质不同,后者
通常情况下为液体。
7.有4种碳架如图所示的烃,则下列判断正确的是( )
A.a和d互为同分异构体
B.b和c不互为同系物
C.a和c都不能发生取代反应
D.只有b和c能发生取代反应答案 A
解析 A项,a和d均含4个碳原子,一个形成碳碳双键,一个形成环,所
含的氢原子数也相等,二者的分子式相同但结构不同,互为同分异构体,正确。
B项,b、c结构相似,组成上相差1个CH 原子团,互为同系物,错误。C项,
2
a、c上都有氢原子,能与Cl 等卤素单质发生取代反应,错误。D项,a、b、c、
2
d都能发生取代反应,错误。
8.下列叙述错误的是( )
A.通常情况下,甲烷跟强酸、强碱、强氧化剂不反应
B.甲烷是正四面体结构
C.甲烷跟氯气反应无论生成CH Cl、CH Cl 、CHCl ,还是CCl ,都属于取
3 2 2 3 4
代反应
D.甲烷与Cl 反应得到的四种取代物常温下均为液体
2
答案 D
解析 通常情况下甲烷较稳定,不与强酸、强碱和强氧化剂反应,A正确;
甲烷分子是以碳原子为中心的正四面体结构,B正确;甲烷与Cl 在光照时发生
2
取代反应生成CH Cl、CH Cl 、CHCl 、CCl 及HCl五种产物,其中四种有机产
3 2 2 3 4
物中CH Cl为气体,CH Cl 、CHCl 、CCl 为液体,C正确,D错误。
3 2 2 3 4
9.(1)某气态烃在标准状况下的体积为2.8 L,其质量为2 g,该烃中氢元素
的质量分数为25%,则该烃的分子式为________,电子式为________,结构式
为________,其空间构型为________。
(2)如图立方体中心的“·”表示甲烷分子中的碳原子,请在立方体的顶点用
“·”表示出与之紧邻的4个氢原子的位置。
答案 (1)CH 正四面体
4
(2)
解析 (1)该烃的物质的量为n=2.8 L÷22.4 L·mol-1=0.125 mol,该烃的摩尔
质量M=2 g÷0.125 mol=16 g·mol-1;1 mol该烃中,含氢原子的物质的量为n(H)
=16 g×25%÷1 g·mol-1=4 mol;1 mol含碳原子的物质的量为n(C) =16 g×(1-25%)÷12 g·mol-1=1 mol,所以分子式为CH 。
4
(2)CH 分子是以碳原子为中心的正四面体结构,在立方体中互不相邻的四个
4
顶点各有一个氢原子,即构成正四面体结构。
10.有①甲烷,②乙烷,③丙烷,④丁烷4种烷烃,试回答下列问题:
(1) 请 写 出 烷 烃 在 足 量 的 氧 气 中 充 分 燃 烧 的 化 学 方 程 式 :
____________________________________________________________________。
(2)相同状况下,等体积的上述气态烃,消耗 O 的量最多的是________(填序
2
号,下同)。
(3)在120 ℃、1.01×105 Pa条件下,某气态烃与足量的 O 完全反应后,测得
2
反应前后气体的体积没有发生改变,则该烃为________。
答案 (1)C H +O ――→nCO +(n+1)H O
n 2n+2 2 2 2
(2)④ (3)①
解析 (1)烷烃的燃烧通式为
C H +O ――→nCO +(n+1)H O。
n 2n+2 2 2 2
(2)1 mol上述气态烃消耗氧气的物质的量为 mol,故丁烷消耗O 的量最多。
2
(3)由反应前后气体体积不变可知:
1+=n+n+1,n=1,即为甲烷。
B篇·综合提升训练
11.下列有关烷烃的叙述中不正确的是( )
A.烷烃中除甲烷、乙烷外,其他都能使酸性KMnO 溶液褪色
4
B.所有的烷烃在光照条件下都能与Cl 发生取代反应
2
C.烷烃的分子通式为C H (n为正整数),符合该通式的烃一定是烷烃
n 2n+2
D.随着碳原子数的增加,烷烃的熔、沸点逐渐升高
答案 A
解析 烷烃在光照条件下都能与 Cl 发生取代反应,烷烃均不能使酸性
2
KMnO 溶液褪色,这是烷烃的主要特性;随着碳原子数的增加,烷烃的熔、沸
4
点逐渐升高;因分子通式C H (n为正整数)中碳原子的化合价已达饱和,故符
n 2n+2
合分子通式C H (n为正整数)的有机物只能是烷烃。
n 2n+2
12.在光照条件下,CH 与Cl 能发生取代反应。若1 mol CH 与Cl 反应,
4 2 4 2
待 反 应 完 成 后 测 得 四 种 有 机 取 代 物 的 物 质 的 量 之 比 为
n(CH Cl)∶n(CH Cl )∶n(CHCl )∶n(CCl )=1∶2∶3∶4,则消耗 Cl 的物质的量
3 2 2 3 4 2
为( )
A.1.0 mol B.2.0 mol
C.3.0 mol D.4.0 mol
答案 C
解析 在光照条件下,CH 与Cl 发生取代反应时,生成 1 mol CH Cl消耗1
4 2 3mol氯气;生成1 mol CH Cl 消耗2 mol氯气;生成1 mol CHCl 消耗3 mol氯气;
2 2 3
生成 1 mol CCl 消耗 4 mol 氯气。四种有机取代物的物质的量之比为
4
n(CH Cl)∶n(CH Cl )∶n(CHCl )∶n(CCl )=1∶2∶3∶4,根据碳原子守恒,生成
3 2 2 3 4
四种有机取代物的物质的量 n(CH Cl)、n(CH Cl )、n(CHCl )、n(CCl )分别是0.1
3 2 2 3 4
mol、0.2 mol、0.3 mol、0.4 mol,消耗的Cl 为0.1 mol+2×0.2 mol+3×0.3 mol
2
+4×0.4 mol=3.0 mol。
13.下列有关甲烷的取代反应的叙述正确的是( )
A.甲烷与氯气的物质的量之比为1∶1混合发生取代反应只生成CH Cl
3
B.甲烷与氯气的取代反应,生成的产物中CH Cl最多
3
C.甲烷与氯气的取代反应生成的产物为混合物
D.1 mol甲烷与4 mol氯气反应生成1 mol CCl
4
答案 C
解析 甲烷与氯气一旦发生取代反应就不会停止在某一步,四种有机物都会
产生,故得不到纯净的CH Cl,A错误,C正确;甲烷与氯气的反应中每取代1
3
mol氢原子,消耗1 mol氯气,生成1 mol HCl,故产物中HCl最多,B错误;甲
烷与氯气的反应为连锁反应,故 1 mol 甲烷与 4 mol 氯气反应不会得到 1 mol
CCl ,D错误。
4
14.将标准状况下11.2 L甲烷和22.4 L氧气混合点燃,恢复到原状况后,气
体的体积为( )
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
答案 A
解析 CH +2O ――→CO +2H O,因11.2 L甲烷与22.4 L氧气恰好完全反
4 2 2 2
应生成11.2 L的CO 气体,此时H O不是气体,故选A。
2 2
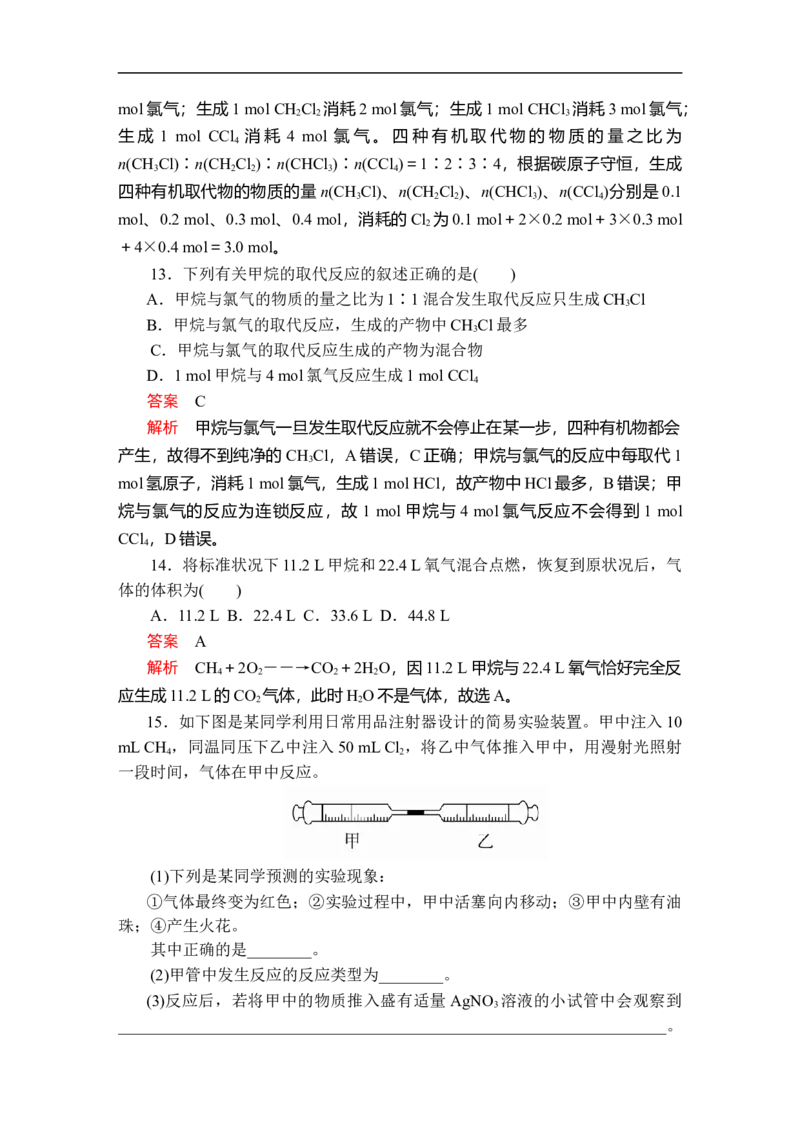
15.如下图是某同学利用日常用品注射器设计的简易实验装置。甲中注入10
mL CH ,同温同压下乙中注入50 mL Cl ,将乙中气体推入甲中,用漫射光照射
4 2
一段时间,气体在甲中反应。
(1)下列是某同学预测的实验现象:
①气体最终变为红色;②实验过程中,甲中活塞向内移动;③甲中内壁有油
珠;④产生火花。
其中正确的是________。
(2)甲管中发生反应的反应类型为________。
(3)反应后,若将甲中的物质推入盛有适量 AgNO 溶液的小试管中会观察到
3
____________________________________________________________________。若再向其中滴入几滴石蕊溶液,又观察到________。
答案 (1)②③ (2)取代反应
(3)液体分为两层,产生白色沉淀 溶液先变红后褪色
解析 在光照下,甲烷与氯气发生连锁反应:CH +Cl ――→CH Cl+HCl,
4 2 3
CH Cl+Cl ――→CH Cl +HCl,CH Cl +Cl ――→CHCl +HCl,CHCl +
3 2 2 2 2 2 2 3 3
Cl ――→CCl +HCl。
2 4
(1)理论上,甲烷与氯气体积比为 1∶4时二者恰好完全反应,而甲中氯气与
甲烷体积比为5∶1>4∶1,说明氯气过量,最终气体中仍有氯气。反应过程中
不会产生火花。产物中只有氯化氢和一氯甲烷为气体,所以气体的总物质的量减
小,内部压强减小,甲中活塞向内移动。
(2)甲烷和氯气发生的是取代反应。
(3)生成的 HCl会与AgNO 溶液反应生成 AgCl白色沉淀,同时因 CH Cl 、
3 2 2
CHCl 、CCl 难溶于水而看到液体分为两层,因 Cl 有剩余,若加入几滴石蕊溶
3 4 2
液,溶液会先变红后褪色。
16.(1)完全燃烧0.1 mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结
束后,称得浓硫酸增重 9 g,浓碱液增重17.6 g。该烃的化学式为________,并
写 出 其 所 有 可 能 的 结 构 简 式 : ______________________________
__________________________________________。
(2)某烃2.2 g,在O 中完全燃烧,生成6.6 g CO 和3.6 g H O,在标准状况下
2 2 2
其密度为1.9643 g·L-1,其化学式为________。
(3)某烷烃的相对分子质量为128,该烷烃的化学式为______________。
答案 (1)C H CH CH CH CH 、
4 10 3 2 2 3
CHCH CH CH (2)C H (3)C H
3 3 3 3 8 9 20
解析 (1)0.1 mol烃中含n(C)==0.4 mol,含n(H)=×2=1 mol,则每个烃
分子中含4个C原子、10个H原子,即分子式为C H 。该烃结构简式有两种:
4 10
(2)该烃的摩尔质量 M=22.4 L·mol-1×1.9643 g·L-1≈44 g·mol-1,烃分子中
n(C)∶n(H)=
∶×2=3∶8。最简式为 C H ,最简式相对分子质量为 44,故化学式也为
3 8
C H 。
3 8
(3)设该烷烃化学式为 C H ,则 14n+2=128,解得:n=9,化学式为
n 2n+2
C H 。
9 20