文档内容
人教版(2019)必修第一册第三章第一节 铁及其化合物
课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列离子的检验方法中合理的是
A.向某溶液中滴入 溶液呈红色,说明不含
B.用酸性 溶液检验 溶液中是否含有
C.向某溶液中加入 溶液,直接得到红褐色沉淀,说明溶液中含有
D.向某溶液中加入 溶液得到白色沉淀,又观察到颜色逐渐变为红褐色,说明
该溶液中只含有 ,不含有
2.红热的铁与水蒸气反应,产物是
A. 、 B. 、 C. 、 D. 、
3.铁元素是人体重要微量元素,参与人体血红蛋白的形成,人体内的铁大部分是
价的铁, 易被人体吸收,下列有关铁及其化合物的说法正确的是。
A.缺铁性贫血症可以服用维生素C将难吸收的 氧化为 ,促进铁元素的吸收
B.用 溶液刻蚀覆铜板是因为 的氧化性比 强
C.FeO不稳定,在空气中加热迅速被氧化成
D.铁粉与水蒸气在高温下反应,生成 和
4.纳米是长度单位,1nm=10-9m,当物质的颗粒达到纳米级时,具有特殊的性质。例
如将铁制成“纳米铁”时具有非常强的化学活性,在空气中可以燃烧。下列关于“纳
米铁”的叙述正确的是
A.常温下“纳米铁”比铁片的金属性强
B.常温下“纳米铁”比铁片更易失去电子
C.常温下“纳米铁”的还原性与铁片相同D.常温下“纳米铁”比铁片的氧化性强
5.设 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有的原子数为
B. 中含有的共价键数为
C.标准状况下, 中含有的分子数为
D. 与足量硫粉反应,转移电子数为
6.下列反应的离子方程式正确的是
A.过量铁粉加入稀硝酸中:
B.向稀硝酸中滴加 溶液:
C.向硫酸铜溶液中通入 气体:
D.向碳酸氢钠溶液中加入足量石灰水: 。
7.下面的物质不能由金属和稀酸溶液反应生成的是
A.FeSO B.MgSO C.FeCl D.ZnSO
4 4 3 4
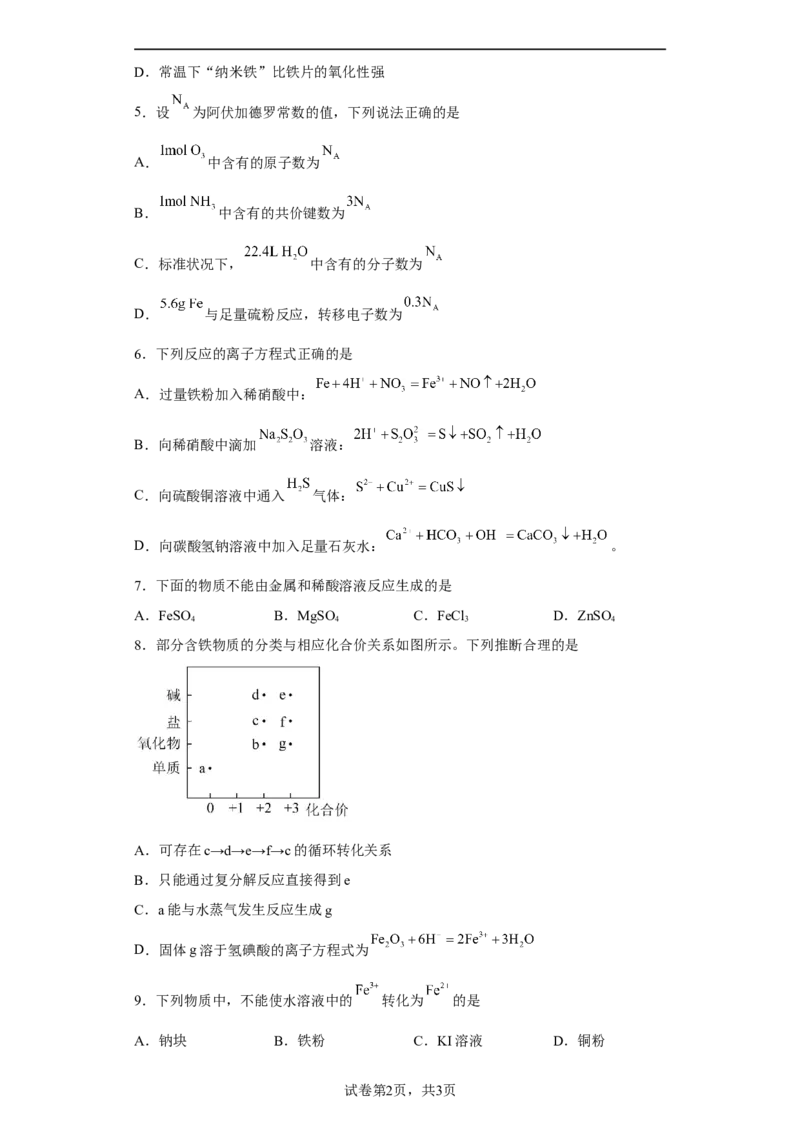
8.部分含铁物质的分类与相应化合价关系如图所示。下列推断合理的是
A.可存在c→d→e→f→c的循环转化关系
B.只能通过复分解反应直接得到e
C.a能与水蒸气发生反应生成g
D.固体g溶于氢碘酸的离子方程式为
9.下列物质中,不能使水溶液中的 转化为 的是
A.钠块 B.铁粉 C.KI溶液 D.铜粉
试卷第2页,共3页10.中华文化源远流长、博大精深。下列有关说法错误的是。
A.《梦溪笔谈》记载“方家以磁石磨针锋,则能指南”,磁石的主要成分为
B.《中医药典》记载木耳具有“和血养营”(治疗贫血症)功效,黑木耳富含铁元素
C.《淮南万毕术》记载“曾青 得铁,则化为铜,外化而内不化”,说明铁的
还原性强于铜
D.《本草图经》“绿矾”项记载:“盖此矾色绿,味酸,烧之则赤……”,绿矾的
化学式为 , 属于混合物
11.下列说法错误的是
A. 为红棕色粉末 B.碳酸钠俗称纯碱
C. 为黄绿色气体 D. 为红棕色气体
12.铁放置时间长了就会生锈。铁容易生锈,除了由于它的化学性质活泼以外,同时
与外界条件也有很大关系。水分是使铁容易生锈的物质之一。然而,光有水也不会使
铁生锈,只有当空气中的氧气溶解在水里时,氧在有水的环境中与铁反应,才会生成
一种叫氧化铁的东西,这就是铁锈,铁生锈总的反应为
。铁锈是一种棕红色的物质,它不像铁那么坚硬,很
容易脱落,一块铁完全生锈后,体积可胀大8倍。如果铁锈不除去,这海绵状的铁锈
特别容易吸收水分,铁也就锈蚀的更快了。Fe O 属于
2 3
A.混合物 B.碱性氧化物 C.酸性氧化物 D.两性氧化物
13.下列有关铁及其化合物的说法中正确的是
A. 和 都可以通过化合反应制取
B.细铁丝在空气里剧烈燃烧,火星四射,生成黑色固体
C.向饱和 溶液中滴加过量氨水,可制取 胶体
D.若某铁的氧化物可表示为 ,则该氧化物中
14.将 铁和氧化铁的混合物加入 浓度为 盐酸中,恰好完全反应,
放出标准状况下的气体 。滴加 溶液,溶液不变色。则下列判断正确的是
A.原混合物中B.无法计算原混合物的质量
C.收集产生的气体刚好能与 完全反应
D.向溶液中通入 ,可以将 完全转化为
15.下列实验现象描述不正确的是
A.向久置的氯水中滴加石蕊溶液,先变红后褪色
B.向装有 的试管中加入水后,立即滴加酚酞试液,溶液先变红后褪色
C.加热坩埚中的钠块,钠先熔化,然后剧烈反应,发出黄色火焰,生成淡黄色固体
D.向 溶液中滴入 溶液,生成白色絮状沉淀变为灰绿色,一段时间后有红
褐色物质生成
二、填空题
16.现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡
萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有_______,属于非电解质的有_______。(填序号)
(2)除去③中少量②的化学方程式为_______。
(3)现有100 mL⑩溶液中含Fe3+ 5.6g,则溶液中SO 的物质的量浓度是_______。
(4)若在⑦中缓慢加入①的水溶液,产生的现象是_______。
17.
化
学 Fe(OH) Fe(OH)
2 3
式
颜
色
白色固体 红褐色固体
状
态
与
盐
酸 Fe(OH) +2H+=Fe2++2H O Fe(OH) +3H+=Fe3++3H O
2 2 3 2
反
应
受
热
- ___________
分
解
试卷第4页,共3页制 可溶性亚铁盐与碱溶液反应: 可溶性铁盐与碱溶液反应:
备 ___________ ___________
二
者 在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是白色絮状沉
2 3
的 淀迅速变成___________色,最后变成___________色,反应的化学方程式为
关 ___________
系
18.向FeCl 溶液中滴加少量NaOH溶液,观察到有沉淀生成,该反应的离子方程式为
3
_______,该沉淀的颜色是_______色,将该沉淀加热分解后得到一种红棕色物质,该
物质的化式为________。
19.将铁屑溶于过量的稀硫酸中,再加入适量硝酸,反应完全后加入过量的氨水,有
红褐色沉淀生成。过滤,灼烧沉淀物至质量不再发生变化,得到红棕色的残渣。上述
沉淀是_________,残渣是_________。
20.按要求完成下列问题
(1)用小苏打片(NaHCO )治疗胃酸过多的离子方程式为_______。
3
(2)请写出氢氧化铁胶体制备的原理 _______ (用化学方程式表示)
(3)区分Fe(OH) 胶体和FeCl 溶液的方法_______
3 3
(4)写出下列物质的电离方程式:
①NH NO _______
4 3
②H SO _______
2 4
三、实验题
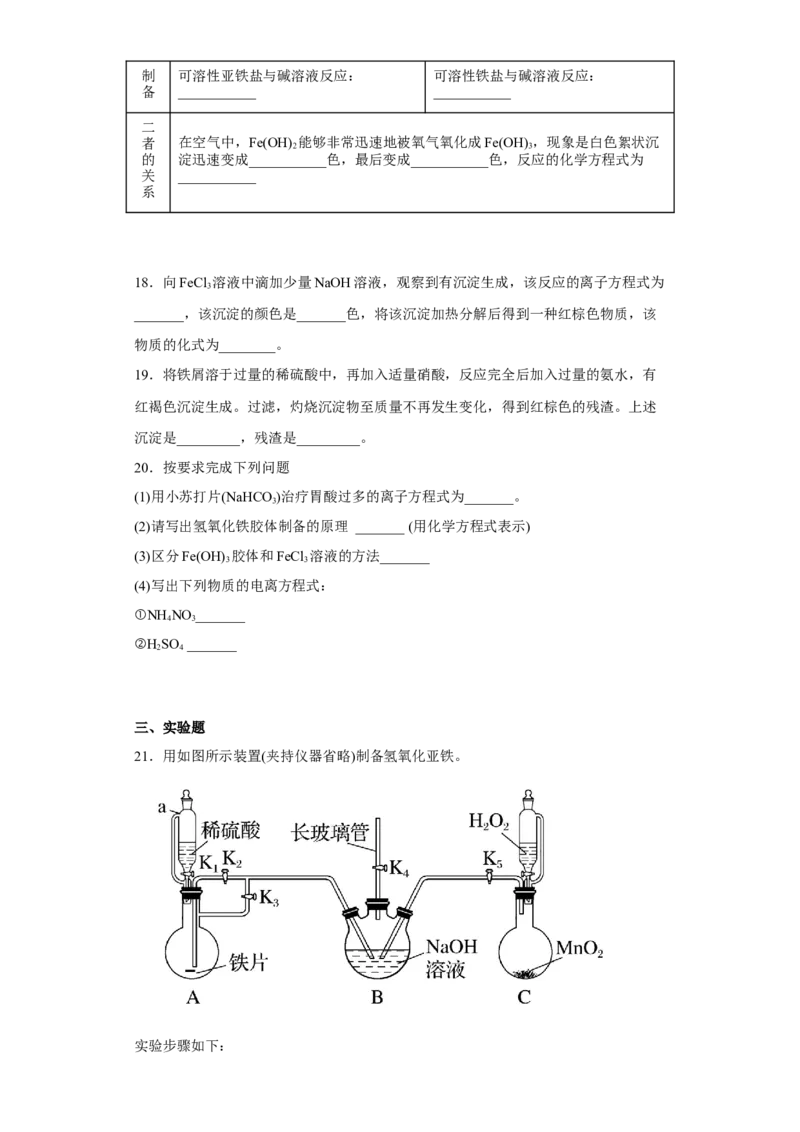
21.用如图所示装置(夹持仪器省略)制备氢氧化亚铁。
实验步骤如下:Ⅰ.检查装置气密性后,关闭K、K,打开K、K、K,使装置A中产生的气体进入装
2 5 1 3 4
置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K,打开K,将A中溶液压入B中并观察现象。
3 2
Ⅲ.关闭K、K,打开K,使C中气体通入B中并观察现象。
1 2 5
回答下列问题:
(1)仪器a的名称是_______,B中长玻璃管的作用是_______。
(2)装置A中金属离子的检验方法是_______。
(3)步骤 Ⅲ 装置B中的现象是_______,其发生反应的化学方程式为_______。
22.将少量饱和 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:饱和 溶液滴加到冷水中;
乙:饱和 溶液滴加到NaOH溶液中;
丙:饱和 溶液滴加到沸水中。
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为___________。
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论
___________。
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化,但最终得到和甲相同的
溶液,写出该过程发生反应的离子方程式:___________。
(4)在氯化铁溶液、氢氧化铁胶体、氢氧化铁悬浊液三种分散系中,分散质粒子直径最
小的是___________,最大的是___________,氢氧化铁胶体分散质粒子直径大小介于
___________之间。
试卷第6页,共3页参考答案:
1.C
【详解】A.向某溶液中滴入KSCN溶液不变红色,加氯水仍不变色,后说明不含Fe2+,
直接加KSCN溶液呈红色,说明含Fe3+,不能确定是否存在Fe2+,故A错误;
B.向某溶液中加入酸性KMnO 溶液,溶液褪色,说明原溶液可能含 ,不能检验
4
溶液中是否含有 ,故B错误;
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中一定含有Fe3+,故C正确;
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,白色氢氧化
亚铁被氧化为红褐色氢氧化铁,说明该溶液中含有Fe2+,可能含有Mg2+,故D正确;
故答案选选C。
【点睛】本题考查阳离子的检验,题目难度不大,注意常见阳离子二价铁离子和三价铁离
子的检验为高考的热点,注意归纳总结检验方法。
2.C
【详解】红热的铁与水蒸气反应 ,反应的产物为 和 ,
故选C。
3.B
【详解】A.维生素C有还原性,把铁离子还原成易吸收的亚铁离子,A错误;
B.氯化铁和铜生成氯化亚铁和氯化铜,氯化铁做氧化剂,说明 的氧化性比 强,
B正确;
C.FeO不稳定,在空气中加热迅速被氧化成 ,C错误;
D.铁粉与水蒸气在高温下反应,生成 和 ,D错误;
故选B。
4.C
【详解】A.金属性属于元素的性质,“纳米铁”和铁片都为铁元素,金属性相同,故A
错误;
B.纳米铁之所以具有较强的化学活性是由于纳米材料的颗粒较小,表面积较大,与氧气的接触面积较大而能在空气中的燃烧,失电子能力相同,故B错误;
C.纳米铁之所以具有较强的化学活性是由于纳米材料的颗粒较小,表面积较大,与氧气
的接触面积较大而能在空气中的燃烧,失电子能力相同,“纳米铁”的还原性与铁片相同,
故C正确;
D.金属Fe不具有氧化性,故D错误;
故选C。
5.B
【详解】A.1mol 中含有的原子数为3 ,A项错误;
B.1mol 中含有的共价键数为3 ,B项正确;
C.标况下,水不是气态不能进行计算,C项错误;
D.5.6g Fe与足量硫粉反应, 转移电子数为0.2 ,D项错误;
答案选B。
6.D
【详解】A.过量铁粉加入稀硝酸中生成 ,离子方程式为:
,故A错误;
B.向稀硝酸中滴加 溶液发生氧化还原反应生成硫酸根和一氧化氮,离子方程式为
,故B错误;
C.硫酸铜溶液中通入 气体转化成弱酸 ,方程式为: ;
D.碳酸氢钠溶液中加入足量石灰水生成碳酸钙,氢氧化钠和水,离子方程式为:
,故D正确;
故答案选D。
7.C
【详解】A.铁和稀硫酸生成硫酸亚铁和氢气,A正确;
B.镁和稀硫酸生成硫酸镁和氢气,B正确;
答案第2页,共2页C.铁和稀盐酸生成氯化亚铁,不是氯化铁,C错误;
D.锌和稀硫酸生成硫酸锌和氢气,D正确;
故选C。
8.A
【分析】部分含铁物质的分类与相应化合价关系如图所示,则abgde分别为铁、氧化亚铁、
氧化铁、氢氧化亚铁、氢氧化铁,ef分别为亚铁盐、铁盐;
【详解】A.氯化亚铁和氢氧化钠生成氢氧化亚铁,氢氧化亚铁和氧气生成氢氧化铁,氢
氧化铁和盐酸生成氯化铁,氯化铁和铁生成氯化亚铁,A正确;
B.氢氧化亚铁和氧气生成氢氧化铁,故可以通过化合反应得到氢氧化铁,B错误;
C.铁和水蒸气高温生成四氧化三铁,C错误;
D.三价铁和碘离子会生成亚铁离子和碘单质,D错误;
故选A。
9.A
【详解】A.钠加入水中先与水反应生成 , 与 反应生成 沉淀,故
A符合题意;
B.铁粉与 发生反应 ,故B不符合题意;
C.KI溶液中I-与 发生反应 ,故C不符合题意;
D.铜粉与 发生反应 ,故D不符合题意;
故答案选A。
10.D
【详解】A.四氧化三铁又名磁铁,磁石的主要成分为 ,A正确;
B.黑木耳富含铁元素,饮食铁元素可以防止贫血,B正确;
C.曾青 得铁,则化为铜,是铁和硫酸铜反应生成铜和硫酸亚铁,说明铁的还原性
强于铜,C正确;
D. 是一种物质,属于纯净物,D错误;
故选D。11.C
【详解】A.Fe O 俗称铁红,是一种红棕色粉末,故A正确;
2 3
B.碳酸钠溶液显碱性,俗称纯碱,故B正确;
C. 为无色透明气体,故C错误;
D.常温常压下,NO 是一种红棕色气体,叙述正确,故D正确;
2
故答案选C。
12.B
【详解】 能与酸反应生成铁盐和水,体现碱性, 为碱性氧化物。故选B。
13.A
【详解】A.Fe在 中燃烧生成 , 与 生成 , 与 , 生
成 均是化合反应,故A正确;
B.铁在空气中不能燃烧,故B错误;
C.饱和 溶液中滴加过量氨水,生成 沉淀,不能制取 胶体,故C错误;
D.设Fe O的物质的量为 , 为 , 为 ,则有 ,
0.96
解得:x=0.88,y=0.08, ,故D错误;
故答案选A。
14.D
【分析】由于反应生成H,则表明反应生成的Fe3+全部被Fe还原,所以反应方程式可表示
2
为:Fe O+Fe+6HCl=3FeCl +3H O,2Fe+2HCl==FeCl +H ,n(H )= ,则
2 3 2 2 2 2 2
反应②中,n(Fe)= n(FeCl )=n(H )=0.02mol,n(HCl)=2n(H )=0.04mol,反应①中,
2 2 2
n(HCl)=0.1mol-0.04mol=0.06mol,则n(Fe)=n(Fe O)=0.01mol,n(FeCl )=0.03mol。所以,反
2 3 2
应前,n(Fe)= 0.02mol+0.01mol=0.03mol,n(Fe O)=0.01mol,反应后的溶液中,n(FeCl )=
2 3 2
0.05mol。
【详解】A.由分析可知,原混合物中n (Fe)=0.03mol,n (Fe O) =0.01mol,,所以n (Fe O)
2 3 2 3
答案第4页,共2页: n (Fe) =1: 3,故A错误;
B.原混合物中n (Fe) =0.03mol,n(Fe O) =0.01mol,则可以计算原混合物的质量,故B错
2 3
误;
C.n (H ) =0.02mol,刚好能与0.02mol氯气反应,该选项未指明“标况”条件,所以无法
2
知道氯气的体积,故C错误;
D.反应后的溶液中,n (FeCl ) =0.05mol,由反应2FeCl +Cl=2FeCl 可知,向溶液中通入
2 2 2 3
0.025molCl ,可以将Fe2+完全转化为Fe3+,故D正确;
2
故选D。
15.A
【详解】A.久置的氯水,由于次氯酸见光分解为盐酸和氧气,最终溶液中只含盐酸,不
含HClO,有酸性无漂白性,所以久置的氯水中滴入紫色石蕊试液,溶液变红不褪色,故A
错误;
B.过氧化钠与水反应生成碱,且过氧化钠具有漂白性,则溶液先变红后褪色,故B正确;
C.钠燃烧生成过氧化钠,则钠受热后先熔化,然后剧烈燃烧,产生黄色火焰,生成淡黄
色的过氧化钠,故C正确;
D.氯化亚铁与氢氧化钠溶液反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成氢
氧化铁,可观察到生成白色沉淀,沉淀很快变为灰绿色,最后变为红褐色,故D正确;
故答案选A。
16.(1) ①②③⑥ ④⑤
(2)2NaHCO NaCO + H O + CO ↑
3 2 3 2 2
(3)1.5mol/L
(4)先产生红褐色沉淀后沉淀溶解,溶液变黄色
【详解】(1)①液态氯化氢在水溶液中能导电,是电解质;
②小苏打是NaHCO ,在水溶液中能够导电,是电解质;
3
③固体纯碱是碳酸钠,在水溶液或者熔融状态下能够导电,是电解质;
④二氧化碳在水溶液中与水反应生成碳酸,能够导电,但二氧化碳本身不能电离,属于非
电解质;
⑤葡萄糖是在熔融状态和水溶液中都不能导电的化合物,是非电解质;
⑥氢氧化钾在水溶液或者熔融状态下能够导电,是电解质;⑦氢氧化铁胶体属于混合物,既不是电解质也不是非电解质;
⑧氨水属于混合物,既不是电解质也不是非电解质;
⑨空气属于混合物,既不是电解质也不是非电解质;
⑩硫酸铁溶液属于混合物,既不是电解质也不是非电解质;
综上所述属于电解质的是:①②③⑥,非电解质的有:④⑤;
故答案为:①②③⑥;④⑤;
(2)碳酸钠加热不分解,碳酸氢钠加热分解得到碳酸钠、水、二氧化碳,所以除去固体纯
碱中少量小苏打的操作是加热,化学方程式为: ,故答
案为: ;
(3)Fe3+的物质的量为 ,溶液中2n( )=3n(Fe3+),则 的物质的
量为0.1mol× =0.15mol, 的物质的量浓度为 =1.5mol/L,故答案为:
1.5mol/L;
(4)若在氢氧化铁胶体中缓慢加入盐酸,胶体发生聚沉,产生红褐色沉淀,继续加入盐酸,
沉淀溶解得到黄色溶液,故答案为:先产生红褐色沉淀后沉淀溶解,溶液变黄色。
17. 2Fe(OH) Fe O+3H O Fe2++2OH-=Fe(OH) ↓ Fe3++3OH-=Fe(OH) ↓ 灰
3 2 3 2 2 3
绿 红褐 4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
【详解】氢氧化铁受热分解生成氧化铁和水,2Fe(OH) Fe O+3H O;
3 2 3 2
可溶性亚铁盐与碱溶液中氢氧根离子生成氢氧化亚铁沉淀,Fe2++2OH-=Fe(OH) ↓;
2
可溶性铁盐与碱溶液中氢氧根离子生成氢氧化铁沉淀,Fe3++3OH-=Fe(OH) ↓;
3
在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象是白色絮状沉淀迅速变成
2 3
灰绿色,最后变成红褐色,反应为氢氧化亚铁和氧气生成氢氧化铜,化学方程式为
4Fe(OH) +O +2H O=4Fe(OH) 。
2 2 2 3
18. Fe3++3OH-=Fe(OH) ↓ 红褐 Fe O
3 2 3
【详解】
答案第6页,共2页向FeCl 溶液中滴加少量NaOH溶液,反应生成NaCl和Fe(OH) 沉淀,该反应的离子方程
3 3
式为:Fe3++3OH-=Fe(OH) ↓;生成的沉淀是Fe(OH) ,颜色呈红褐色;将Fe(OH) 加热分解
3 3 3
生成氧化铁和水,氧化铁是红棕色固体,则该物质的化式为Fe O。
2 3
19.
【详解】将铁屑溶于过量的稀硫酸中,生成 , 再加入适量硝酸, 被氧化生成
,反应完全后加入过量的氨水,有红褐色沉淀 生成。过滤,灼烧
沉淀受热分解, 得到红棕色的残渣 。
20.(1)
(2)
(3)丁达尔效应
(4)
【详解】(1)小苏打为NaHCO ,胃酸的成分为盐酸,碳酸氢钠和盐酸反应的离子方程式
3
为: ,故答案为: ;
(2)在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,即制得
氢氧化铁胶体,其制备的原理为: ,故答案为:
;
(3)胶体能产生丁达尔效应,溶液不能产生丁达尔效应,因此区分Fe(OH) 胶体和FeCl
3 3
溶液的方法是丁达尔效应,故答案为:丁达尔效应;(4)①硝酸铵为强电解质,完全电离为铵根离子和硝酸根离子,其电离方程式为:
,故答案为: ;
②H SO 在水溶液中完全电离生成H+和 ,其电离方程式为 ,故答案为:
2 4
。
21.(1) 恒压滴液漏斗 平衡气压,辅助排出装置B中的空气
(2)取少量装置A烧瓶中的液体于洁净试管中,滴加几滴KSCN溶液,无红色出现,再滴加
HO,溶液变为红色,则证明存在Fe2+
2 2
(3) 白色沉淀逐渐变为灰绿色,最后变为红褐色 4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
【分析】仪器a为恒压滴液漏斗,目的是连通内外压强使液体能顺利流下,仪器B为三颈
烧瓶,B中的玻璃管为平衡装置气压,氢氧化亚铁溶液被空气中的氧气氧化变为氢氧化铁,
故排除装置B的空气防止氧化,稀硫酸与金属铁发生反应生成亚铁离子,加入硫氰化钾溶
液无红色出现,再加入过氧化氢溶液溶液变为红色,装置C会产生氧气,氢氧化亚铁与氧
气发生反应生成氢氧化铁的沉淀,现象为白色沉淀变为灰绿色最终变为红褐色,据此答题。
(1)
①仪器a的名称为恒压滴液漏斗,其作用为连通内外压强使液体能顺利流下;
②装置B为三颈烧瓶,氢氧化亚铁在空气中极易被氧化,因此打开K、K、K,关闭K
1 3 4 2
和K,装置A中产生H,装置B中的玻璃管是为了排除装置内的空气;
5 2
(2)
装置A为金属铁与稀硫酸反应生成亚铁离子,其化学方程式为:Fe+H SO =FeSO+H ↑,亚
2 4 4 2
铁离子的检验:取少量装置A烧瓶中的液体于洁净试管中,滴加几滴KSCN溶液,无红色
出现,再滴加HO,溶液变为红色,则证明存在Fe2+;
2 2
(3)
①步骤 Ⅲ装置B中,关闭K、K,打开K,使C中产生的氧气通入装置B,氢氧化亚铁
1 2 5
为白色沉淀,氢氧化铁为红褐色沉淀,观察到的现象为:白色沉淀逐渐变为灰绿色,最后
变为红褐色;
②发生的化学方程式为:4Fe(OH) +O +2H O=4Fe(OH) 。
2 2 2 3
答案第8页,共2页22. 将丙中的物质置于暗处,用
激光笔(或手电筒)照射,在与光束垂直的方向观察,若液体中有一条光亮的“通路”,则
说明 胶体已经制备成功 Fe(OH) +3H+=Fe3++3H O 氯化铁溶液
3 2
氢氧化铁悬浊液 1~100 nm
【详解】(1) 继续加热煮沸得到红褐色透明Fe(OH) 液体,化学反应方程式为:
3
,故答案为: ;
(2) 检验丙中是否成功制备胶体的方法是 将丙中的物质置于暗处,用激光笔(或手电筒)照
射,在与光束垂直的方向观察,若液体中有一条光亮的“通路”,则说明 胶体已
经制备成功,故答案为:将丙中的物质置于暗处,用激光笔(或手电筒)照射,在与光束垂
直的方向观察,若液体中有一条光亮的“通路”,则说明 胶体已经制备成功;
(3) 饱和 溶液滴加到沸水中生成 ,加入盐酸生成 ,发生反应的离子方
程式:Fe(OH) +3H+=Fe3++3H O,故答案为:Fe(OH) +3H+=Fe3++3H O;
3 2 3 2
(4) 溶液分散质粒子直径小于1 nm,浊液分散质粒子直径大于100 nm,胶体分散质粒子直
径在1~100 nm之间,分散质粒子直径最小的是氯化铁溶液,最大的是氢氧化铁悬浊液,氢
氧化铁胶体分散质粒子直径大小介于1~100 nm之间,故答案为:氯化铁溶液,氢氧化铁悬
浊液,1~100 nm。答案第10页,共2页