文档内容
第三章 第二节 第1课时 合金 铝和铝合金 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共60分)
1. 合金的应用极大地促进了人类社会的发展。下列不属于合金的是( )
B.柔性显示屏(基 D.潜水器外壳
A.狗头兽首铜像 C.流通硬币
础材料:石墨烯) (钛、铝等)
2. 人类的日常生活中离不开合金,下列物质中不属于合金的是( )
A.用于门窗框架上的硬铝 B.用于冶炼金属铁的赤铁矿
C.用于生产铁锅的生铁 D.用于制造手术刀的不锈钢
3. 青铜是我国使用最早的合金。下列关于青铜性质的说法,不正确的是( )
A.熔点比纯铜低 B.能够导电
C.能够导热 D.硬度比纯铜小
4. 有关合金的叙述正确的是( )
A.合金的导电性比成分金属强
B.合金的抗腐蚀性能都很好
C.合金的机械强度比各成分金属小
D.多数合金比成分金属熔点低,硬度大
5. 关于合金的叙述,不正确的是( )
A.合金的熔沸点一般比组成它们的各成分金属要高
B.合金的硬度可以比原金属更高,化学性质也可能和原成分金属不同
C.非金属和金属之间也可以形成合金
D.合金的用途比纯金属的用途更广
6. 下列有关金属的说法中,正确的是( )
①不锈钢抗腐蚀性较好
②钛合金可用于飞机、火箭的制造
③后(司)母戊鼎是铁合金
④缺钙会引起骨质疏松,缺铁会引起贫血
⑤青铜、不锈钢都是合金
⑥形成合金时金属与金属之间发生了化学反应
A.①②④⑤ B.②③④⑤⑥
C.①③④⑤ D.①②③④⑤⑥
7. 铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途。下列关于铝的说法正确的是(
1
学科网(北京)股份有限公司)
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.常温下不与任何酸、碱反应
C.铝元素在地壳中的含量高,储量丰富,仅次于铁
D.工业上通常用钠与铝盐溶液反应来制备铝
8. 下列说法正确的是( )
A.Al O 难溶于水,不跟水反应,所以它不是Al(OH) 对应的氧化物
2 3 3
B.因为Al O 是金属氧化物,所以它是碱性氧化物
2 3
C.Al O 能跟所有的酸、碱溶液反应
2 3
D.Al O 能跟强的酸、碱溶液反应
2 3
9. 铝制品具有较强的抗腐蚀性,主要是因为( )
A.铝的化学性质稳定
B.铝在常温时与氧气不反应
C.铝具有金属性,也具有非金属性
D.铝与氧气反应生成一层致密的氧化物薄膜
10.Na、Cu、Al、Fe四种金属的熔、沸点如下表所示:
金属 Na Cu Al Fe
熔点(℃) 97.8 1 083 660 1 535
沸点(℃) 883 2 595 2 200 3 000
其中不能形成合金的是( )
A.Cu与Al B.Fe与Cu
C.Fe与Na D.Al与Na
11.下列说法不正确的是( )
A.我国最早使用的合金是由铜锌合金制成的青铜器
B.储氢合金是一类能大量吸收H,并与H 结合成金属氢化物的材料
2 2
C.一般汽车的发动机使用的是密度小、强度大且耐腐蚀的铝合金材料
D.钛合金、形状记忆合金、耐热合金以及储氢合金都属于新型合金
12.钛和钛的合金被誉为“21世纪最有发展前景的金属材料”,它们具有很多优良的性能,如熔
点高、密度小、可塑性好、易于加工,尤其是钛合金与人体器官具有很好的”生物相容性”。
根据它们的主要性能,下列用途不切合实际的是( )
A.用来做保险丝
B.用于制造航天飞机
C.用来制造人造骨
D.用于家庭装修,做钛合金装饰门
13.2019年12月17日,我国第一艘国产航空母舰山东舰在海南三亚某军港交付海军,它宣告了中
2
学科网(北京)股份有限公司国海军的国产航母时代正式来临。据报道, 该舰艇的“超级甲板”采用了大量新型铝锂合金
和铝镁合金等航天材料,真正实现了“浴千度火仍无恙”。下列关于两种合金的说法正确的是
( )
A.铝锂合金是铝与锂形成的新型化合物
B.铝锂合金的硬度比铝小,熔、沸点比铝高
C.铝镁合金不能全部溶解于稀盐酸中
D.铝镁合金焊接前用NaOH溶液处理氧化铝膜
14.自然界里常见金属元素存在最多的是铝,其次是铁,铜的含量较少。然而人类冶炼金属最早获
得成功的反而是含量较少的铜,含量最多的铝最迟被冶炼出来。金属是当今社会不可缺少的材
料之一。下列有关金属的说法错误的是( )
A.铜比铝先获得成功冶炼的原因是铜矿较易被还原,铝矿很难被还原
B.目前已制得的纯金属只有几十种,但制得的合金已达几千种,大量使用的不是纯金属而是
它们的合金
C.生铁易生锈不耐腐蚀,但纯铁具有耐腐蚀性,所以不锈钢应是最纯的铁
D.废弃铝制包装既浪费金属材料又造成环境污染
15.铝是一种很重要的金属,可以发生一系列反应制备物质。下列说法错误的是( )
A.反应①又称铝热反应,常用于野外焊接铁轨
B.利用②③反应都能产生氢气,产生等量氢气消耗Al的质量相等且转移电子数也相等
C.常用反应⑥制备Al(OH) ,方法是向Al (SO ) 溶液中滴加NaOH溶液至恰好完全沉淀
3 2 4 3
D.工业上常用反应⑦制备金属铝,制备过程中常加入冰晶石以降低Al O 的熔点
2 3
二、填空题(本题包括3个小题,共40分)
16.(12分)历史上金、银、铜主要是作为货币金属或装饰品被应用。
(1)金、银、铜常被作为钱币流通,从化学角度来看,主要是利用它们的 (填字母)。
A.硬度适中
B.密度适中
C.在自然界里都可得到纯净的单质
D.不活泼性
(2)试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样,按下图所示进行实验:
请写出步骤③中所发生的全部反应的离子方程式: 。
若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中
氧化铜的质量为 (用m表示)。
3
学科网(北京)股份有限公司17.(14分)为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b
L。
反应的化学方程式是______________________________;样品中铝的质量为________g。
(2)另取a g样品将其点燃,恰好完全反应,该反应的化学方程式是2Al+Fe O 2Fe+Al O,
2 3 2 3
氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得
气体的体积比c∶b=________。
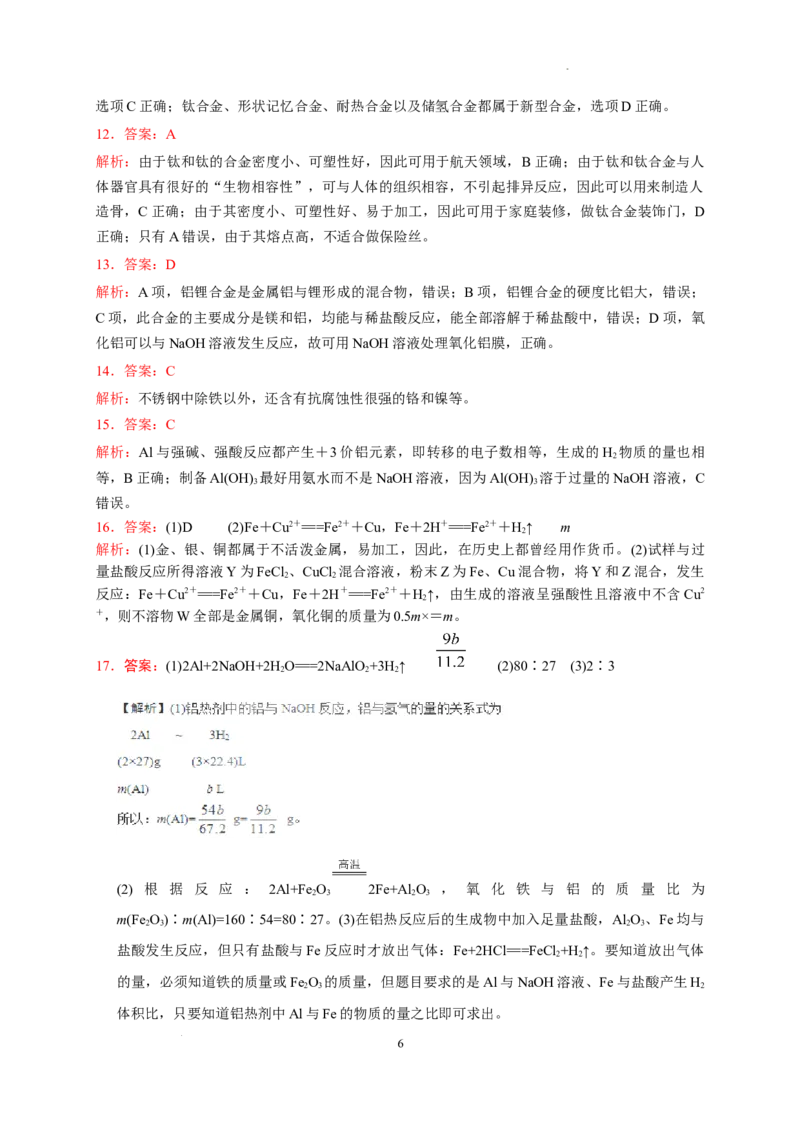
18.(14分)某学习小组用如图所示装置测定铝镁合金中的铝的质量分数和铝的相对原子质量。
(1)A中试剂为______________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是___________________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的
液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至
室温后,记录C的液面位置;④由A向B滴加足量试剂;⑤检查气密性。上述操作的顺序
是 ________( 填 序 号 ) ; 记 录 C 的 液 面 位 置 时 , 除 视 线 平 视 外 , 还 应
___________________________。
(4)B中发生反应的化学方程式为_____________________。
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体
的质量为c g,则铝的相对原子质量为_________________。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得的质量分数将________(填“偏大”“偏
小”或“不受影响”)。
1.答案:B
解析:合金是由两种或两种以上金属或金属与非金属熔合而成具有金属特性的物质,据此解答。
A.狗头兽首铜像属于合金,A错误;B.柔性显示屏(基础材料:石墨烯)不属于合金,B正确;
4
学科网(北京)股份有限公司C.流通硬币属于合金,C错误;D.潜水器外壳(钛、铝等)属于合金,D正确。答案选B。
2.答案:B
解析:硬铝是铝和铜、镁等熔合而成的合金;赤铁矿的主要成分是氧化铁,氧化铁属于氧化物;生
铁和不锈钢是铁和碳等物质形成的合金。
3.答案:D
解析:青铜是铜的合金,其熔点比纯铜低,具有金属导电、导热的性质,硬度比成分金属纯铜大。
4.答案:D
解析:A项,合金的导电性一般比成分金属弱,错误;B项,合金的抗腐蚀性不一定都很好,如生
铁的抗腐蚀性不如纯铁,错误;C项,合金的机械强度一般比各成分金属大,错误;D项,多数合
金比成分金属的熔点低,硬度大,正确。
5.答案:D
解析:合金的熔点比各成分金属的熔点低,所以纯铁的熔点高于1200℃,故选D。
6.答案:A
解析:不锈钢是由铁、铬、镍等制成的,具有强的抗腐蚀性能,①正确;钛是一种具有许多优良性
能的较为昂贵的金属,钛合金可用于飞机、火箭的制造,②正确;后(司)母戊鼎是世界上现存最大
的青铜器,③错误;钙是组成骨骼的重要元素,缺钙会引起骨质疏松,血红蛋白中含有铁元素,缺
铁会引起贫血,④正确;青铜为铜锡合金、不锈钢为铁合金,都是合金,⑤正确;形成合金的过程
为在金属中加热熔合某些金属或非金属,形成具有金属特性的物质,形成合金时金属与金属之间未
发生化学反应,⑥错误。
7.答案:A
解析:铝既能和强酸反应,又能和强碱反应,B项错误;铝元素在地壳中的含量高于铁,C项错误;
钠不能从铝盐溶液中置换出铝单质,D项错误。
8.答案:D
解析:Al O 虽然难溶于水,但是2Al(OH) =====Al O +3HO,Al O 和Al(OH) 中Al的化合价相
2 3 3 2 3 2 2 3 3
同,所以Al O 是Al(OH) 对应的氧化物;金属氧化物与碱性氧化物是两个不同的概念,二者没有
2 3 3
必然的联系;Al O 是两性氧化物,能与强酸、强碱反应,与弱酸、弱碱不反应。
2 3
9.答案:D
解析:铝是活泼金属,化学性质活泼,故A错误;铝被氧气氧化生成氧化铝,而不是不反应,故B
错误;铝具有金属性,不具有非金属性,故C错误;铝被氧气氧化生成致密的氧化物薄膜,能阻止
铝进一步被氧化,故D正确。
10.答案:C
解析:当一种金属的熔点高于另一种金属的沸点时,两者不能形成合金。
11.答案:A
解析:青铜是铜锡合金,是我国最早使用的合金,选项 A错误; 储氢合金能够大量吸收氢气,并
与氢气结合成金属氢化物,选项B正确;铝合金材料密度小、强度大且耐腐蚀,适合制造发动机,
5
学科网(北京)股份有限公司选项C正确;钛合金、形状记忆合金、耐热合金以及储氢合金都属于新型合金,选项D正确。
12.答案:A
解析:由于钛和钛的合金密度小、可塑性好,因此可用于航天领域,B正确;由于钛和钛合金与人
体器官具有很好的“生物相容性”,可与人体的组织相容,不引起排异反应,因此可以用来制造人
造骨,C正确;由于其密度小、可塑性好、易于加工,因此可用于家庭装修,做钛合金装饰门,D
正确;只有A错误,由于其熔点高,不适合做保险丝。
13.答案:D
解析:A项,铝锂合金是金属铝与锂形成的混合物,错误;B项,铝锂合金的硬度比铝大,错误;
C项,此合金的主要成分是镁和铝,均能与稀盐酸反应,能全部溶解于稀盐酸中,错误;D项,氧
化铝可以与NaOH溶液发生反应,故可用NaOH溶液处理氧化铝膜,正确。
14.答案:C
解析:不锈钢中除铁以外,还含有抗腐蚀性很强的铬和镍等。
15.答案:C
解析:Al与强碱、强酸反应都产生+3价铝元素,即转移的电子数相等,生成的H 物质的量也相
2
等,B正确;制备Al(OH) 最好用氨水而不是NaOH溶液,因为Al(OH) 溶于过量的NaOH溶液,C
3 3
错误。
16.答案:(1)D (2)Fe+Cu2+===Fe2++Cu,Fe+2H+===Fe2++H↑ m
2
解析:(1)金、银、铜都属于不活泼金属,易加工,因此,在历史上都曾经用作货币。(2)试样与过
量盐酸反应所得溶液Y为FeCl 、CuCl 混合溶液,粉末Z为Fe、Cu混合物,将Y和Z混合,发生
2 2
反应:Fe+Cu2+===Fe2++Cu,Fe+2H+===Fe2++H↑,由生成的溶液呈强酸性且溶液中不含Cu2
2
+,则不溶物W全部是金属铜,氧化铜的质量为0.5m×=m。
17.答案:(1)2Al+2NaOH+2H O===2NaAlO+3H ↑ (2)80∶27 (3)2∶3
2 2 2
(2) 根 据 反 应 : 2Al+Fe O 2Fe+Al O , 氧 化 铁 与 铝 的 质 量 比 为
2 3 2 3
m(Fe O)∶m(Al)=160∶54=80∶27。(3)在铝热反应后的生成物中加入足量盐酸,Al O 、Fe均与
2 3 2 3
盐酸发生反应,但只有盐酸与Fe反应时才放出气体:Fe+2HCl===FeCl +H ↑。要知道放出气体
2 2
的量,必须知道铁的质量或Fe O 的质量,但题目要求的是Al与NaOH溶液、Fe与盐酸产生H
2 3 2
体积比,只要知道铝热剂中Al与Fe的物质的量之比即可求出。
6
学科网(北京)股份有限公司2Al ~ Fe O ~ 2Fe
2 3
3H 2H
2 2
b c
故b∶c=3∶2。
18.答案:(1)NaOH溶液 (2)除去镁铝合金表面的氧化膜
(3)⑤①④③② 使D和C的液面相平
(4)2Al+2NaOH+2H O===2NaAlO+3H ↑
2 2 2
(5) (6)偏小
[来源:学.科.网Z.X.X.K]
解析:(1)观察实验装置图可知是用量气法完成实验目的,故A中应盛NaOH溶液,在B中发生
2Al+2NaOH+2H O===2NaAlO+3H ↑的反应。(2)目的是除去铝镁合金表面的氧化膜。(3)正确顺序应
2 2 2
为⑤①④③②;为使C中气体的压强相等,还应使D与C液面相平。(5)据2 mol Al~3 mol H 得
2
M(Al)= (6)据w(Al)= ×100%的计算公式可知未洗涤不溶物会造成Al的质量分
数偏小。
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司