文档内容
第 04 讲 氧化还原反应的基本概念
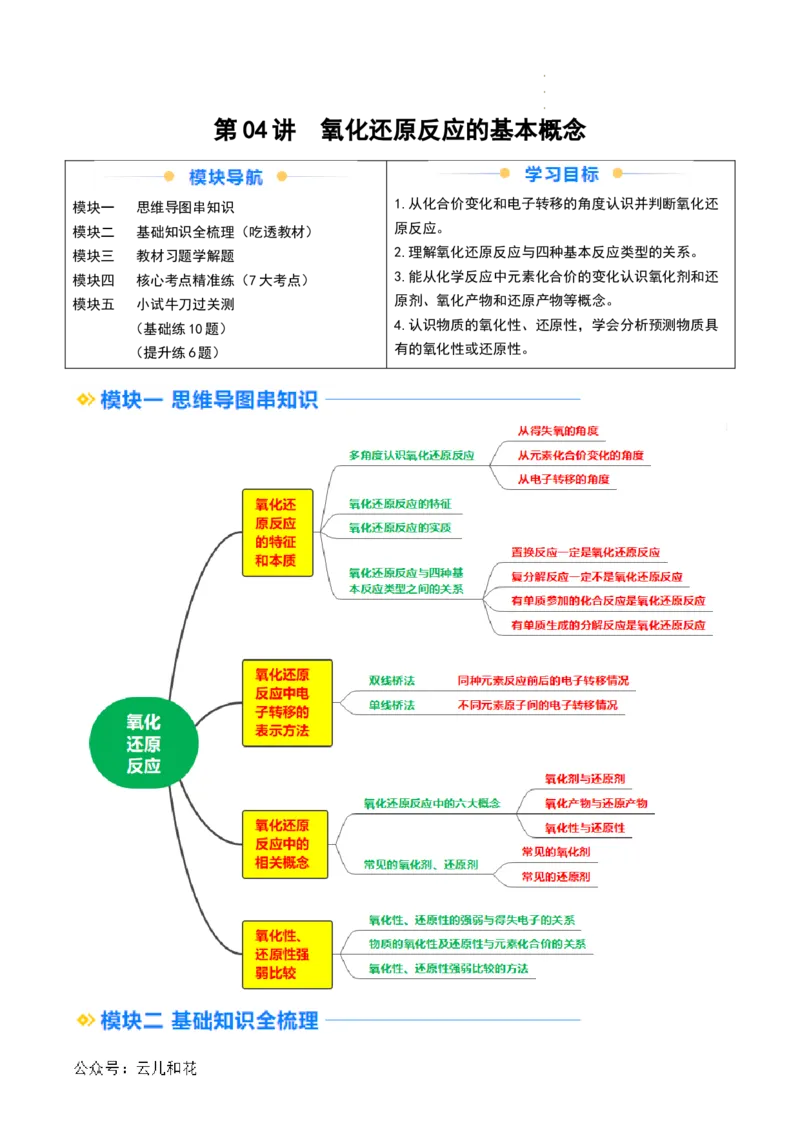
模块一 思维导图串知识 1.从化合价变化和电子转移的角度认识并判断氧化还
模块二 基础知识全梳理(吃透教材) 原反应。
模块三 教材习题学解题 2.理解氧化还原反应与四种基本反应类型的关系。
模块四 核心考点精准练(7大考点) 3.能从化学反应中元素化合价的变化认识氧化剂和还
模块五 小试牛刀过关测 原剂、氧化产物和还原产物等概念。
(基础练10题) 4.认识物质的氧化性、还原性,学会分析预测物质具
(提升练6题) 有的氧化性或还原性。
学科网(北京)股份有限公司一、氧化还原反应的特征和本质
1.多角度认识氧化还原反应
(1)从得失氧的角度
对于反应2CuO+C=====2Cu+CO↑
2
(1)氧化铜失去氧,发生还原反应,被碳还原。
(2)碳得到氧,发生氧化反应,被氧化铜氧化。
(3)结论:在化学反应中,一种物质得到氧发生氧化反应,必然有一种物质失去氧发生还原反应。氧化
反应和还原反应是在一个反应中同时发生的,这样的反应称为氧化还原反应。
(2)从元素化合价变化的角度
(1)对于有氧得失的反应2CuO+C=====2Cu+CO↑
2
①铜元素化合价降低,发生还原反应。
②碳元素化合价升高,发生氧化反应。
(2)对于无氧得失的反应Fe+CuSO ===FeSO+Cu
4 4
①铜元素化合价降低,发生还原反应。
②铁元素化合价升高,发生氧化反应。
(3)结论:①反应前后有元素化合价变化(升降)的反应称为氧化还原反应。
②物质所含元素化合价升高的反应是氧化反应,物质所含元素化合价降低的反应是还原反应。
③氧化还原反应的特征:反应前后有元素化合价的 变化 ( 升降 )。
(3)从电子转移的角度
(1)从电子得失的角度分析反应:2Na+Cl=====2NaCl
2
在有些氧化还原反应中,物质所含元素的原子失去电子,该物质发生氧化反应;得到电子,该物质发生还
原反应。
(2)从共用电子对偏移的角度分析反应:H+Cl=====2HCl
2 2
在有些氧化还原反应中,元素的原子间有共用电子对的偏移(偏离和偏向)。
共用电子对偏离的物质发生氧化反应,共用电子对偏向的物质发生还原反应。
(3)结论:①有电子转移(电子得失或共用电子对偏移)的反应是氧化还原反应。
②元素的原子失去电子(或电子对偏离),则元素的化合价升高,物质被氧化,发生氧化反应;元素的原子
得到电子(或电子对偏向),则元素的化合价降低,物质被还原,发生还原反应。
③氧化还原反应的本质是电子转移。
2.氧化还原反应的特征
一种或几种元素的化合价发生变化。
3.氧化还原反应的实质
氧化还原反应的实质是 电子转移 ( 得失或偏移 )。
4.氧化还原反应与四种基本反应类型之间的关系
学科网(北京)股份有限公司(1)置换反应一定是氧化还原反应。
(2)复分解反应一定不是氧化还原反应。
(3)有单质参加的化合反应是氧化还原反应。
(4)有单质生成的分解反应是氧化还原反应。
二、氧化还原反应中电子转移的表示方法
1.双线桥法
表明同一种元素反应前后的电子得失(或偏移)情况。
①双线桥法表示电子转移的基本步骤
【易错警示】
a.箭尾、箭头必须指向反应物、生成物中相应的同种元素。
b.采用a×be-形式表示得失电子数,a为得失电子的原子总数,b为每个原子得失电子数,a、b是“1”时
省略。得到与失去的电子总数相等。
2.单线桥法
表明反应中化合价变化的元素原子间的电子转移情况。
①单线桥法表示电子转移的基本步骤
学科网(北京)股份有限公司【易错警示】
a.单线桥法从反应物中失电子的元素指向反应物中得电子的元素,表示反应物中变价元素原子间电子的
转移情况;
b.箭头已标明电子转移的方向,因此不需再标明“得”或“失”,只标明电子转移数目。
三、氧化还原反应中的相关概念
1.氧化还原反应中的六大概念
(1)氧化剂与还原剂
氧化剂:在氧化还原反应中,所含元素的化合价降低,即得到电子(或电子对偏向)的物质。
还原剂:在氧化还原反应中,所含元素的化合价升高,即失去电子(或电子对偏离)的物质。
(2)氧化产物与还原产物
氧化产物:还原剂失去电子被氧化的产物。
还原产物:氧化剂得到电子被还原的产物。
(3)氧化性与还原性
氧化性:物质得电子的性质或能力。
还原性:物质失电子的性质或能力。
【归纳提升】氧化还原反应概念间的关系
记忆口诀:
升→失→氧→氧→氧
降→得→还→还→还
2.常见的氧化剂、还原剂
(1)常见的氧化剂
①活泼的非金属单质:如Cl、O 等。
2 2
②变价元素的高价态化合物
a.某些酸:如浓HSO 、HNO、HClO等;
2 4 3
b.某些氧化物、过氧化物:如MnO 、HO、NaO 等;
2 2 2 2 2
学科网(北京)股份有限公司c.某些盐:如KMnO 、FeCl 、NaClO等。
4 3
(2)常见的还原剂
①活泼的金属单质:如Al、Fe、Zn等。
②某些非金属单质:如H、S、C等。
2
③变价元素的低价态化合物
a.某些氧化物:如CO、SO 等;
2
b.某些氢化物:如HCl、HS等;
2
c.某些盐:如KI、NaS、FeCl 等。
2 2
【易错警示】
(1)在一个具体的化学反应中氧化剂和还原剂可能是同一物质,被氧化和被还原的也可能是同种元素,
氧化产物和还原产物也可能是同一物质。
(2)氧化还原反应中的反应物可能既不是氧化剂也不是还原剂,生成物也可能既不是氧化产物也不是还
原产物。
四、氧化性、还原性强弱比较
1.氧化性、还原性的强弱与得失电子的关系
(1)氧化性:物质越易得电子,氧化性越强。
(2)还原性:物质越易失电子,还原性越强。
【易错警示】
物质氧化性、还原性的强弱与得失电子的难易有关,与得失电子的多少无关。
2.物质的氧化性及还原性与元素化合价的关系
核心元素化合价 实例 性质
最高价 KMnO、浓HNO、浓HSO 只有氧化性
4 3 2 4
中间价 SO、NaSO、FeSO 、S 既有氧化性又有还原性
2 2 3 4
最低价 Fe、Na、KI 只有还原性
3.氧化性、还原性强弱比较的方法
(1)根据元素的活动性顺序比较
如:Fe+CuSO ===FeSO+Cu
4 4
金属还原性:Fe>Cu
在反应中Fe是还原剂,Cu是还原产物。
(2)根据氧化还原反应的化学方程式比较
学科网(北京)股份有限公司氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
(3)根据氧化产物的价态高低判断
同一物质在相同条件下,被不同氧化剂氧化的程度越大,氧化剂的氧化性越强。
例如:2Fe+3Cl=====2FeCl 、Fe+S=====FeS
2 3
Fe被Cl 氧化成+3价,而S只能把其氧化成+2价,故氧化性:Cl>S;判断还原剂还原性的原理类似。
2 2
(4)根据反应条件来判断
当不同的氧化剂(或还原剂)与同一还原剂(或氧化剂)反应时,反应越易进行,则对应的氧化剂(或还原剂)的
氧化性(或还原性)越强,反之越弱。如:
①MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
②2KMnO+16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
后者比前者更容易发生,故氧化性:KMnO >MnO。
4 2
教材习题01 解题思路
下列诗词中不涉及氧化还原反应的是( ) 爆竹声中一岁除,涉及元素化合价变化,属于氧化
A.爆竹声中一岁除 还原反应,A错误;吹尽狂沙始到金,为物理法淘
B.吹尽狂沙始到金 金,不涉及氧化还原反应,B正确;野火烧不尽,
蜡炬成灰泪始干,存在燃烧现象,燃烧属于氧化还
C.野火烧不尽
原反应,C、D错误。
D.蜡炬成灰泪始干
【答案】B
教材习题02 解题思路
二氧化氯(ClO )是一种在水处理等方面有广泛应用的 反应物中没有单质参加反应,则该反应不是置换反
2
高效安全消毒剂,它可以根据反应:2NaClO+ 应,A错误;HCl中Cl元素的化合价升高,则HCl
3
4HCl=2ClO 2 ↑+Cl 2 ↑+NaCl+2H 2 O制备,对于该 是还原剂,B错误;NaClO 3 中Cl元素的化合价降
反应,下列说法正确的是( ) 低,则NaClO 3 是氧化剂,C错误;NaClO 3 中Cl元
A.该反应属于置换反应 B.HCl是氧化剂 素的化合价由+5价降低为+4价,在反应中得电子
C.NaClO 3 是还原剂 D.ClO 2 是还原产物 D被还原生成ClO 2 ,ClO 2 是其还原产物,D正确。
是还原产物
【答案】D
学科网(北京)股份有限公司核心考点一:氧化还原反应的概念及判断
【例1】下列铜及其化合物的性质实验中,涉及到的反应不属于氧化还原反应的是( )
A.铜丝在空气中加热
B.用氢气还原氧化铜
C.将铁丝插入CuSO 溶液中
4
D.向CuSO 溶液中滴加NaOH溶液
4
【答案】D
【解析】铜丝在空气中加热与氧气反应生成氧化铜,反应前后有元素化合价的变化,属于氧化还原反应,
故A不符合题意;用氢气还原氧化铜为加热条件下氢气与氧化铜反应生成铜和水,反应前后有元素化合价
的变化,属于氧化还原反应,故B不符合题意;将铁丝插入硫酸铜溶液中,铁与硫酸铜溶液反应生成硫酸
亚铁和铜,反应前后有元素化合价的变化,属于氧化还原反应,故 C不符合题意;向硫酸铜溶液中滴加氢
氧化钠溶液,硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,反应前后没有元素化合价的变化,不属
于氧化还原反应,故D符合题意。
核心考点二:氧化还原反应与四种基本反应类型的关系
【例2】氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于阴影区域的是( )
A.2HClO=====2HCl+O↑
2
B.NH HCO =====NH ↑+HO+CO↑
4 3 3 2 2
C.4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
D.Fe O+3CO=====2Fe+3CO
2 3 2
【答案】D
【解析】阴影区域的反应必须属于氧化还原反应,且不属于化合、分解、置换反应。A项,该反应既属于
分解反应,又属于氧化还原反应;B项,该反应属于分解反应,不属于氧化还原反应;C项,该反应既属
于化合反应,又属于氧化还原反应;D项,该反应属于氧化还原反应,但不属于化合、分解、置换反应中
的任意一种,故属于阴影区域。
核心考点三:氧化还原反应中的电子转移
【例3】下列氧化还原反应中电子转移数目及方向都正确的是( )
学科网(北京)股份有限公司A.
B.
C.
D.
【答案】B
【解析】A项,Cl得到电子,O失去电子,该反应转移12e-,图中电子转移数目不正确,错误;B项,Fe
得到电子,I失去电子,该反应转移2e-,正确;C项,F得到电子,O失去电子,该反应转移4e-,图中
箭头的方向标反,错误;D项,Br得到电子,S失去电子,该反应转移2e-,图中箭头的方向标反,错误。
核心考点四:氧化剂和还原剂等概念的判断
【例4】下列反应中,属于氧化还原反应,但水既不做氧化剂又不做还原剂的是( )
A.SO +HO===HSO
3 2 2 4
B.3NO +HO===2HNO+NO
2 2 3
C.2F+2HO===4HF+O
2 2 2
D.2Na+2HO===2NaOH+H↑
2 2
【答案】B
【解析】各元素的化合价均没有发生变化,不属于氧化还原反应,A错误;NO 中N元素的化合价发生变
2
化,属于氧化还原反应,但水中H、O元素的化合价均不变,故水既不做氧化剂又不做还原剂,B正确;
水中O元素的化合价升高,水做还原剂,C错误;水中H元素的化合价降低,水做氧化剂,D错误。
核心考点五:物质氧化性、还原性的判断
【例5】硫代硫酸钠(Na SO)被称为“养鱼宝”,可降低水中的氯对鱼的危害。脱氯反应的化学方程式为
2 2 3
SO+4Cl+5HO===2SO+10H++8Cl-,下列说法正确的是( )
2 2 2
A.SO表现氧化性
2
B.HO既表现氧化性又表现还原性
2
学科网(北京)股份有限公司C.SO既表现氧化性又表现还原性
2
D.Cl 表现氧化性
2
【答案】D
【解析】该反应中S元素的化合价由+2价升高为+6价,SO是还原剂,表现还原性,HO中没有元素化
2 2
合价的变化,Cl元素的化合价由0价降低为-1价,氯气被还原,做氧化剂,Cl 表现氧化性,D项正确。
2
核心考点六:氧化还原反应的综合考查
【例6】为了防止钢铁零件生锈,常采用化学处理方法使钢铁零件表面生成 Fe O 的致密保护层——“发
3 4
蓝”。化学处理过程中其中一步的反应为 3Fe+NaNO +5NaOH===3NaFeO +HO+NH ↑。下列叙述不
2 2 2 2 3
正确的是( )
A.上述反应涉及的物质中,Fe的还原性最强
B.上述反应涉及的物质中,NaNO 的氧化性最强
2
C.上述反应中,铁是还原剂,NaNO 和NaOH是氧化剂
2
D.NO的氧化性大于FeO的氧化性
【答案】C
【解析】反应3Fe+NaNO +5NaOH===3Na FeO+HO+NH ↑中,Fe是还原剂,NaNO 是氧化剂,所以上
2 2 2 2 3 2
述反应涉及的物质中,铁的还原性最强,NaNO 的氧化性最强,故A、B正确;上述反应中,NaOH中元
2
素化合价不变,既不是氧化剂又不是还原剂,故C错误;NaNO 是氧化剂,NaFeO 是氧化产物,所以NO
2 2 2
的氧化性大于FeO的氧化性,故D正确。
【基础练】
1.下列技术应用中,其工作原理不涉及化学反应的是
A.火药使用 B.用 和 合成 C.转轮排字 D.用氧化铁冶炼铁
【答案】C
【解析】A.火药使用中发生氧化还原反应,涉及到化学反应,A不符合题意;
B.氮气与氢气在一定条件下发生化合反应合成 ,B不符合题意;
C.转轮排字属于物理变化,C符合题意;
D.用氧化铁冶炼铁发生氧化还原反应,涉及到化学反应,D不符合题意;
故选C。
2.下列化学反应基本类型中一定是氧化还原反应的是
学科网(北京)股份有限公司A.化合反应 B.分解反应 C.复分解反应 D.置换反应
【答案】D
【解析】凡有元素化合价升降或变化的化学反应就是氧化还原反应,在四大基本类型的反应中,只有置换
反应一定有化合价变化,所以置换反应一定是氧化还原反应,故选D。
3.下列关于氧化还原反应的说法中正确的是
A.得到电子的一定是还原剂
B.氧化还原反应前后可以没有元素化合价发生变化
C.元素化合价升高的反应是氧化反应
D.氧化剂和还原剂一定是不同的物质
【答案】C
【解析】A.氧化还原反应中,得到电子的为氧化剂,失去电子的为还原剂,A错误;
B.氧化还原反应的宏观特征为元素化合价发生变化,B错误;
C.氧化还原反应中,元素化合价升高的为氧化反应,化合价降低的为还原反应,C正确;
D.氧化剂和还原剂未必一定不同,如水的分解反应,氧化剂与还原剂均为 ,D错误;
故选C。
4.下列化学反应中,属于化合反应但不属于氧化还原反应的是
A. B.
C. D.
【答案】B
【解析】
A. 属于化合反应且有化合价的变化,属于氧化还原反应,A错误;
B. 属于化合反应但没有化合价的变化,不属于氧化还原反应,B正确;
C. 属于分解反应且属于氧化还原反应,C错误;
D. 不属于化合反应但属于氧化还原反应,D错误。
故选B。
5.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是
学科网(北京)股份有限公司A. B.
C. D.
【答案】D
【解析】A.Cl+2KBr=Br +2KCl是置换反应,属于氧化还原反应,属于区域4,A不符合题意;
2 2
B. 是复分解反应,不是氧化还原反应,B不符合题意;
C. 是化合反应,属于氧化还原反应,属于区域1,C不符合题意;
D. 不属于四大基本反应类型,属于氧化还原反应,属于区域3,D符合题
意;
故选D。
6.下列反应中, 只作为氧化剂的是
A. B.
C. D.
【答案】D
【解析】A.F元素的化合价降低,水中上元素的化合价升高,水为还原剂,A错误;
B.只有Cl元素的化合价变化,水既不是氧化剂也不是还原剂,B错误;
C.没有元素的化合价变化,不是氧化还原反应,C错误;
D.Na元素的化合价升高,水中H元素的化合价降低,水为氧化剂,D正确;
故选D。
7.下列氧化还原反应中,电子转移的方向和数目均正确的是
A. B.
C. D.
【答案】D
【解析】
A.该反应中Cl化合价从+5价降低为-1价,共得到2×6=12个电子,同理O共失去6×2=12个电子,
学科网(北京)股份有限公司,A错误;
B.C化合价从0价升高到+4价,共失去4个电子,则氧共得到4个电子, ,B错误;
C.该反应中Cu化合价从+2价降低为0价,共得到2×2=4个电子,则碳共失去4个电子,
,C错误;
D.该反应中Mg化合价从0价升高为+2价,共失去2×2=4个电子,同理O共得到2×2=4个电子,D正
确;
故选D。
8.自然界中的元素大多以化合态存在,而我们在生产和生活中需要许多单质如金属铁、硅单质等。如果
需要把某元素由化合态转变为游离态,则该元素
A.被氧化 B.被还原
C.有可能被氧化,也有可能被还原 D.由高价变为0价
【答案】C
【解析】这里的“某元素”可能是金属元素,也可能是非金属元素.金属元素在化合物里都显正价,非金
属元素在化合物里既可能显正价又可能显负价。因此,元素由化合态转变为游离态(元素的单质),既有可
能由正价变为零价,被还原,又有可能由负价变为零价,被氧化;
故答案选C。
9.下列物质中的硫元素不能表现出氧化性的是
A.S B. C. D.
【答案】B
【解析】A.在单质S中元素化合价为0价,可以得到电子变为-2价,也可以失去电子变为+4、+6价,因
此S既表现氧化性,又表现还原性,A不符合题意;
B.在KS中S为-2价,是S元素的最低化合价,只能失去电子变为较高价态,因此只有还原性,而没有
2
氧化性,B符合题意;
C.在SO 中S为+4价,介于S元素的最低-2价和最高+6价之间,既可以得到电子变为低价态,也可以失
2
去电子变为高价态,因此SO 既可表现氧化性,又可表现还原性,C不符合题意
2
D.在HSO 中S元素化合价为+6价,是S元素的最高化合价,只能得到电子变为低价态,因此只有氧化
2 4
性,而不具有还原性,D不符合题意;
故选B。
学科网(北京)股份有限公司10.反应 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。在该
反应中: 元素的化合价升高,该元素的原子 电子,被 ;在该反应
中,Fe O 发生了 反应, 是还原剂, 是氧化产物, 是还原
2 3
产物。
【答案】Al(铝) 失去 氧化 还原 Al Al O Fe
2 3
【解析】该反应是置换反应,在该反应中,铝元素的化合价由0价升到+3价,失去电子,被氧化,发生氧
化反应,铝为还原剂,对应的产物氧化铝为氧化产物;氧化铁中的铁元素化合价由+3价降到0价,得到电
子,被还原,发生还原反应,氧化铁为氧化剂,对应的产物氧化铁为还原产物。
【提升练】
11.浩瀚的海洋是一个巨大的宝库,从海水中除了可以提取食盐外,还可以从海水提取食盐后的母液(也称
苦卤水,含 、 等)中提取镁、钾、溴及其他化工产品。从海带灰浸取液提取碘单质发生的反应为
。下列有关该反应的说法正确的是
A. 发生还原反应 B. 是还原产物
C. 是氧化剂 D. 得到电子
【答案】D
【分析】反应中I元素化合价由-1价升高到0价,失去电子发生氧化反应,KI为还原剂,I 为氧化产物;
2
HO 中O元素化合价由-1价降低到-2价,得到电子发生还原反应,HO 为氧化剂,HO为还原产物,据此
2 2 2 2 2
判断:
【解析】A.KI发生氧化反应,A错误;
B.KSO 既不是氧化产物又不是还原产物,B错误;
2 4
C.HSO 既不是氧化剂又不是还原剂,C错误;
2 4
D.HO 中O元素化合价由-1价降低到-2价,得到电子发生还原反应,D正确;
2 2
故选D。
12.下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.Fe+CuSO=FeSO+Cu B.AgNO+NaCl=AgCl↓+NaNO
4 4 3 3
C.Fe O+3CO 2Fe+3CO D.2KMnO KMnO +МnO+O ↑
2 3 2 4 2 4 2 2
【答案】C
【解析】A.属于置换反应,属于氧化还原反应,A错误;
B.属于复分解反应,不属于氧化还原反应,B错误;
C.不属于四种基本反应类型,但Fe、C元素化合价发生变化,属于氧化还原反应,C正确;
D.属于有单质生成的分解反应,属于氧化还原反应,D错误;
故选C。
13.下列各组物质间的反应既属于氧化还原反应,又属于离子反应的是
学科网(北京)股份有限公司A. 与 B. 与
C. 与盐酸 D. 溶液与 溶液
【答案】B
【解析】A. 与 反应生成三氯化铁是氧化还原反应,但不是离子反应,A错误;
B. 与 是氧化还原反应,2Na+2HO═2Na+ +2OH- +H ↑,也是离子反应,B正确;
2 2
C. 与盐酸反应生成氯化铁与水,元素化合价没有发生改变,是非氧化还原反应,C错误;
D.NaCl溶液与AgNO 生成硝酸钠和氯化银沉淀,元素化合价没有发生改变,是非氧化还原反应,D错
3
误;
故选B。
14.ClO 是可代替Cl 进行自来水消毒的新一代消毒剂。我国成功研制出制取ClO 的新方法,其反应的微观
2 2 2
过程如图所示,下列有关该反应的叙述正确的是
A.该反应属于置换反应
B.该反应的化学方程式为Cl+2NaClO =2ClO +2NaCl
2 2 2
C.NaClO 转化为ClO 的过程是还原反应
2 2
D.Cl 既是氧化剂又是还原剂
2
【答案】B
【解析】A.置换反应是指单质与化合物反应生成另一种单质和另一种化合物,而此反应生成物中不含有
单质,故此反应不是置换反应,是氧化还原反应,A错误;
B.根据分析可知该反应的化学方程式为Cl+2NaClO =2ClO +2NaCl,B正确;
2 2 2
C.NaClO 转化为ClO 的反应中Cl的化合价由+3价升高为+4价,是氧化反应,C错误;
2 2
D.该反应中Cl 中Cl元素化合价由0价降低为-1价,故Cl 为氧化剂,发生得电子的还原反应,D错误;
2 2
故选B。
15.已知:① ;② 。则下列判断正确的是
A.在反应②中 只表现出还原性
B.氧化性强弱:
C. 只有氧化性, 只有还原性
学科网(北京)股份有限公司D.用双线桥法表示反应②电子得失情况:
【答案】B
【解析】A.反应 中有5个HCl的Cl由-1价升高为0价,作还原剂,
表现还原性,有1个HCl的Cl化合价不变,表现酸性,A错误;
B.氧化剂的氧化性大于氧化产物,反应 中Cl 作氧化剂,Fe3+作氧化产物,则氧化性
2
Cl> FeCl ,反应 中KClO 作氧化剂,Cl 作氧化产物,则氧化性
2 3 3 2
KClO>Cl,综上氧化性强弱: ,B正确;
3 2
C. 是Fe元素的最高价态,只有氧化性, 是Fe元素的中间价态,既有氧化性又有还原性,C错
误;
D.氧化还原反应中同种元素遵循只靠拢不交叉的原则,根据得失电子守恒,该反应用双线桥法表示电子
得失情况为 ,D错误;
答案选B。
16.氧化还原反应在物质的制备和转化中有重要的应用。
(1)碘酸钾(KIO )是一种重要的食品添加剂,可作为食盐中的补碘剂。一种制备KIO 的方法是将I 与
3 3 2
KOH溶液共热,生成KIO 、HO和另一种化合物。
3 2
写出该反应的化学方程式: 。
(2)一种有效成分为NaClO、NaHSO、NaHCO 的“二氧化氯泡腾片”能快速溶于水,放出大量CO,
2 4 3 2
得到ClO 溶液。生成ClO 的化学方程式为5NaClO+4NaHSO =4ClO +NaCl+4Na SO +2H O。
2 2 2 4 2 2 4 2
①该反应的离子方程式为 。
②该反应中氧化剂为 (填化学式,下同),还原剂为 。
③用双线桥法表示该反应中电子转移的方向和数目: 。
④产生CO 的离子方程式为 。
2
【答案】(1)
(2) NaClO NaClO
2 2
学科网(北京)股份有限公司【解析】(1)I 与KOH溶液共热生成KIO 、HO,根据得失电子守恒,另一种化合物为KI,反应方程式
2 3 2
为 ;
(2)①由化学方程式可知,5NaClO+4NaHSO =4ClO +NaCl+4Na SO +2H O反应的离子方程式为
2 4 2 2 4 2
。
②NaClO 中部分Cl元素化合价由+3升高为+4、部分Cl元素化合价由+3降低为-1,该反应中氧化剂为
2
NaClO,还原剂为NaClO。
2 2
③NaClO 中Cl元素化合价由+3升高为+4、Cl元素化合价由+3降低为-1,用双线桥法表示该反应中电子转
2
移的方向和数目为 。
④NaHSO 、NaHCO 反应生成硫酸钠、二氧化碳、水,反应的离子方程式为 。
4 3
学科网(北京)股份有限公司