文档内容
第五章 化工生产中的重要非金属元素
第一节 硫及其化合物
第2课时 硫酸 硫酸根离子的检验
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学实验中安全意识是重要的科学素养,下列实验操作中不正确的是
A.氯气有毒,需在实验室通风橱内制备氯气
B.切割金属钠时,左手捏住钠块,右手拿小刀切割
C.液溴应用少量的水液封并放在冷暗处保存
D.使用危险化学品应注意其分类标识,浓硫酸对应的标识是
2.下列生产活动中涉及的化学原理正确的是
选
生产活动 化学原理
项
A 使用碳纳米管、石墨烯制作新型电池 碳纳米管、石墨烯均可燃烧生成
B 侯氏制碱法得到 沉淀 溶解度较小
C 利用 溶液刻蚀印刷电路板 Fe的活动性比Cu强
D 常温下,可以利用钢瓶储存浓 常温下浓 与Fe不反应
A.A B.B C.C D.D
3.实验室中,下列行为不符合安全要求的是
A.氯气制备应在通风橱内进行
B.金属钠着火时,立即用干燥沙土覆盖
C.实验结束后,将废液倒入下水道中
D.稀释浓硫酸时,将浓硫酸沿器壁缓慢倒入水中并用玻璃棒不断搅拌
4.关于硫及其化合物的叙述错误的是
A.SO 能使酸性KMnO 溶液褪色,是由于SO 具有漂白作用
2 4 2
B.分离黑火药中的KNO、炭、硫要用到二硫化碳、水以及过滤操作
3C.浓硫酸与氯化钠固体反应可以制得HCl,且说明了浓硫酸的难挥发性
D.0.8g硫与3.2 g铜反应能得到4.0 g纯净硫化物
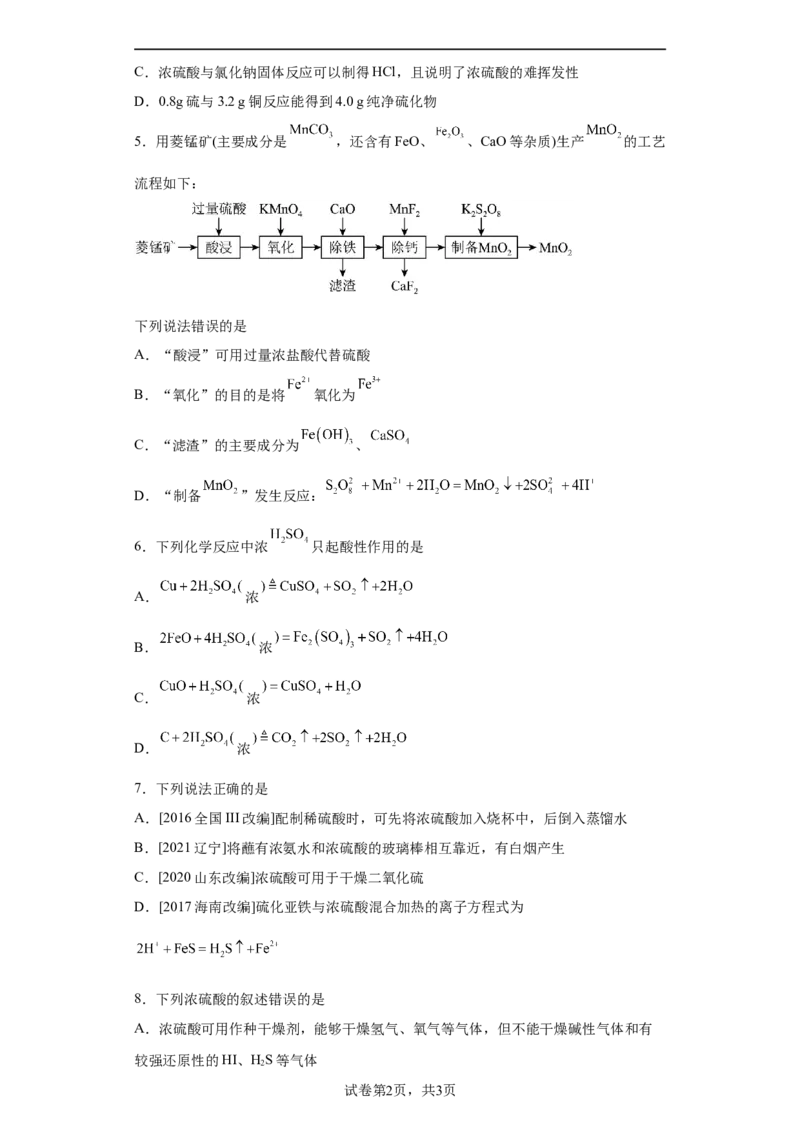
5.用菱锰矿(主要成分是 ,还含有FeO、 、CaO等杂质)生产 的工艺
流程如下:
下列说法错误的是
A.“酸浸”可用过量浓盐酸代替硫酸
B.“氧化”的目的是将 氧化为
C.“滤渣”的主要成分为 、
D.“制备 ”发生反应:
6.下列化学反应中浓 只起酸性作用的是
A. 浓
B. 浓
C. 浓
D. 浓
7.下列说法正确的是
A.[2016全国III改编]配制稀硫酸时,可先将浓硫酸加入烧杯中,后倒入蒸馏水
B.[2021辽宁]将蘸有浓氨水和浓硫酸的玻璃棒相互靠近,有白烟产生
C.[2020山东改编]浓硫酸可用于干燥二氧化硫
D.[2017海南改编]硫化亚铁与浓硫酸混合加热的离子方程式为
8.下列浓硫酸的叙述错误的是
A.浓硫酸可用作种干燥剂,能够干燥氢气、氧气等气体,但不能干燥碱性气体和有
较强还原性的HI、HS等气体
2
试卷第2页,共3页B.浓硫酸与木炭反应的化学方程式为C+2HSO (浓) CO↑+2SO ↑+2HO,在此
2 4 2 2 2
反应中,浓硫酸既表现了强氧化性又表现了酸性
C.1 mol铜粉投到足量浓硫酸中,加热得到气体体积标准状况下为22.4 L
D.常温下能够用铁、铝等容器盛放浓硫酸,是因为浓硫酸能使铁、铝钝化
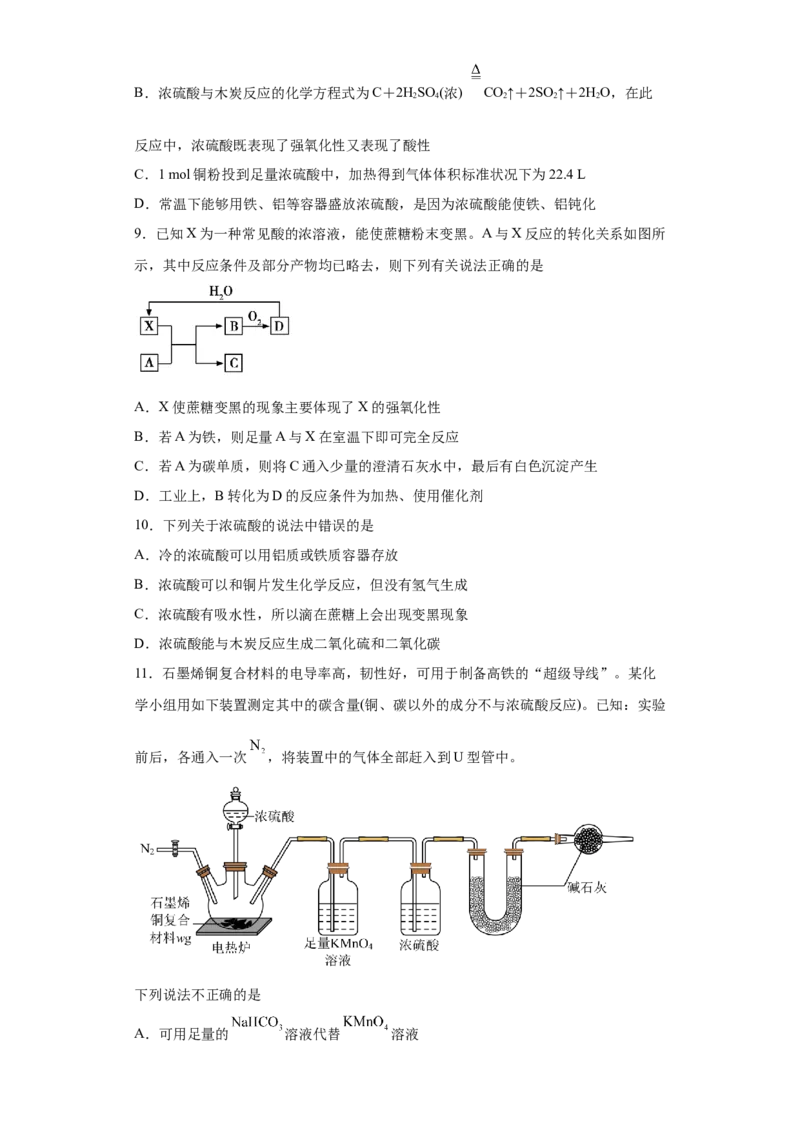
9.已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所
示,其中反应条件及部分产物均已略去,则下列有关说法正确的是
A.X使蔗糖变黑的现象主要体现了X的强氧化性
B.若A为铁,则足量A与X在室温下即可完全反应
C.若A为碳单质,则将C通入少量的澄清石灰水中,最后有白色沉淀产生
D.工业上,B转化为D的反应条件为加热、使用催化剂
10.下列关于浓硫酸的说法中错误的是
A.冷的浓硫酸可以用铝质或铁质容器存放
B.浓硫酸可以和铜片发生化学反应,但没有氢气生成
C.浓硫酸有吸水性,所以滴在蔗糖上会出现变黑现象
D.浓硫酸能与木炭反应生成二氧化硫和二氧化碳
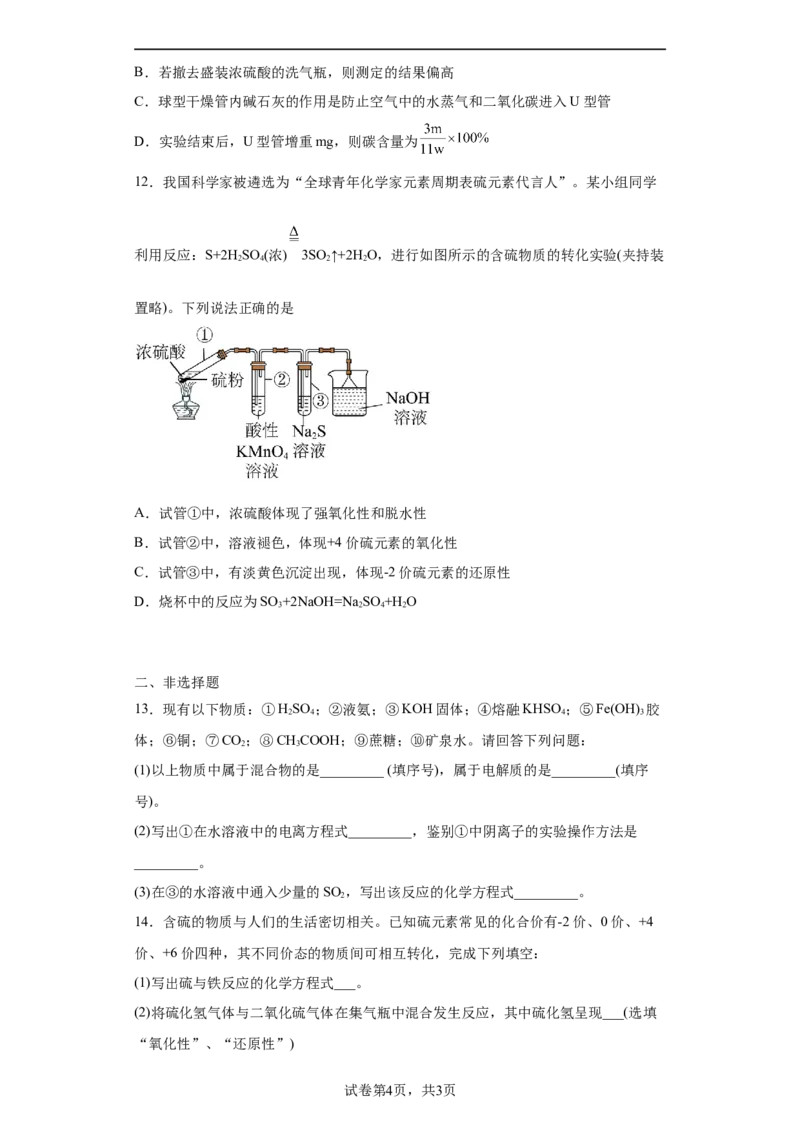
11.石墨烯铜复合材料的电导率高,韧性好,可用于制备高铁的“超级导线”。某化
学小组用如下装置测定其中的碳含量(铜、碳以外的成分不与浓硫酸反应)。已知:实验
前后,各通入一次 ,将装置中的气体全部赶入到U型管中。
下列说法不正确的是
A.可用足量的 溶液代替 溶液B.若撤去盛装浓硫酸的洗气瓶,则测定的结果偏高
C.球型干燥管内碱石灰的作用是防止空气中的水蒸气和二氧化碳进入U型管
D.实验结束后,U型管增重mg,则碳含量为
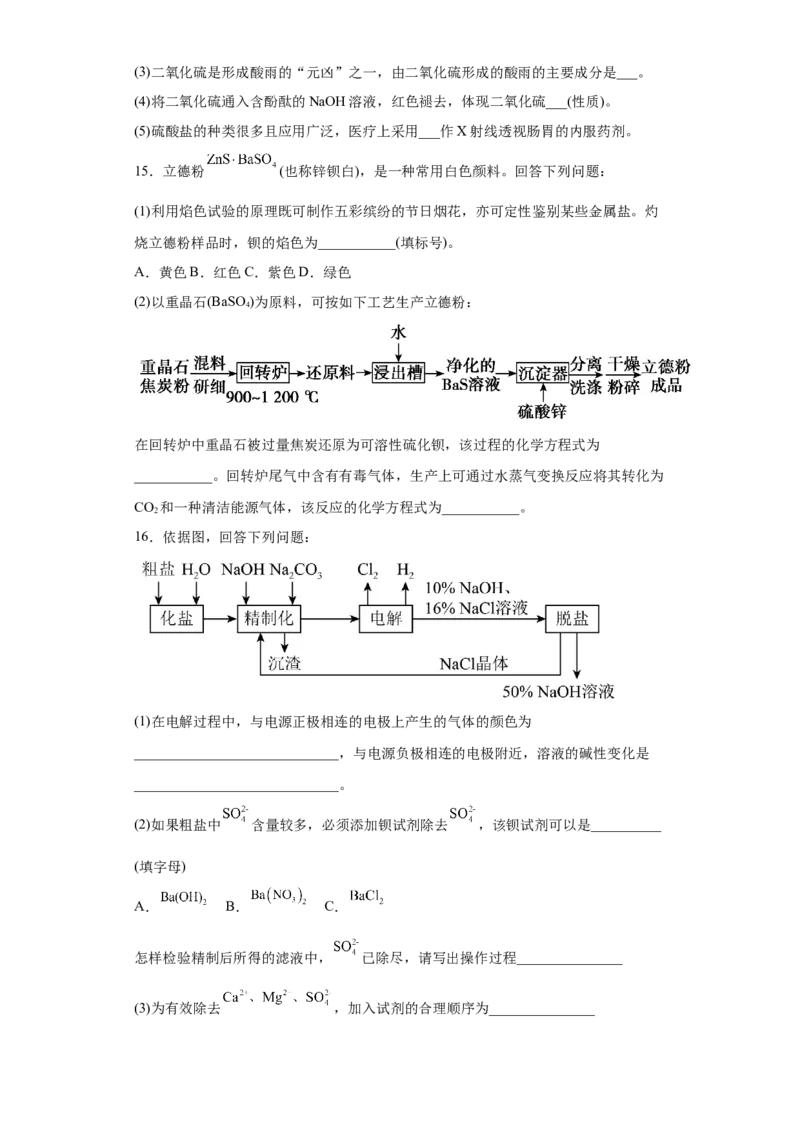
12.我国科学家被遴选为“全球青年化学家元素周期表硫元素代言人”。某小组同学
利用反应:S+2HSO (浓) 3SO ↑+2H O,进行如图所示的含硫物质的转化实验(夹持装
2 4 2 2
置略)。下列说法正确的是
A.试管①中,浓硫酸体现了强氧化性和脱水性
B.试管②中,溶液褪色,体现+4价硫元素的氧化性
C.试管③中,有淡黄色沉淀出现,体现-2价硫元素的还原性
D.烧杯中的反应为SO +2NaOH=Na SO +H O
3 2 4 2
二、非选择题
13.现有以下物质:①HSO ;②液氨;③KOH固体;④熔融KHSO;⑤Fe(OH) 胶
2 4 4 3
体;⑥铜;⑦CO;⑧CHCOOH;⑨蔗糖;⑩矿泉水。请回答下列问题:
2 3
(1)以上物质中属于混合物的是_________ (填序号),属于电解质的是_________(填序
号)。
(2)写出①在水溶液中的电离方程式_________,鉴别①中阴离子的实验操作方法是
_________。
(3)在③的水溶液中通入少量的SO ,写出该反应的化学方程式_________。
2
14.含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2价、0价、+4
价、+6价四种,其不同价态的物质间可相互转化,完成下列填空:
(1)写出硫与铁反应的化学方程式___。
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现___(选填
“氧化性”、“还原性”)
试卷第4页,共3页(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是___。
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫___(性质)。
(5)硫酸盐的种类很多且应用广泛,医疗上采用___作X射线透视肠胃的内服药剂。
15.立德粉 (也称锌钡白),是一种常用白色颜料。回答下列问题:
(1)利用焰色试验的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼
烧立德粉样品时,钡的焰色为___________(填标号)。
A.黄色B.红色C.紫色D.绿色
(2)以重晶石(BaSO)为原料,可按如下工艺生产立德粉:
4
在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为
___________。回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为
CO 和一种清洁能源气体,该反应的化学方程式为___________。
2
16.依据图,回答下列问题:
(1)在电解过程中,与电源正极相连的电极上产生的气体的颜色为
_____________________________,与电源负极相连的电极附近,溶液的碱性变化是
_____________________________。
(2)如果粗盐中 含量较多,必须添加钡试剂除去 ,该钡试剂可以是__________
(填字母)
A. B. C.
怎样检验精制后所得的滤液中, 已除尽,请写出操作过程_______________
(3)为有效除去 ,加入试剂的合理顺序为_______________A.先加 ,后加 ,再加钡试剂
B.先加 ,后加钡试剂,再加
C.先加钡试剂,后加 ,再加
(4)在上述工业流程中,循环使用的物质是_______________。
(5)某同学用惰性电极电解未精制的饱和食盐水,食盐水装在U形管内。结果很快在某
一电极附近出现食盐水浑浊现象。造成浑浊的难溶物主要是______________。
A.碳酸镁 B.硫酸钡 C.氢氧化镁 D.碳酸钡
试卷第6页,共3页参考答案:
1.B
【详解】A.氯气有毒,会污染环境,在实验室制备氯气时,应在通风橱内进行,A正确;
B.钠能与手上汗液中的水反应,生成具有腐蚀性的烧碱,并放出热量,所以切割金属钠
时,不能用手捏住钠块,B不正确;
C.液溴的密度比水大、易挥发,保存液溴时,应用少量的水液封,并放在冷暗处,C正确;
D.浓硫酸具有强烈的腐蚀性,会灼伤皮肤,属于危险化学品,其对应的标识是
,D正确;
故选B。
2.B
【详解】A.使用碳纳米管、石墨烯制作新型电池,利用的是其具有良好的导电能力,不
是利用其可燃烧生成CO 的性质,故A错误;
2
B.侯氏制碱法得到NaHCO 沉淀,利用NaHCO 溶解度较小,故B正确;
3 3
C.反应中Cu是还原剂,Fe2+是还原产物,还原剂的还原性强于还原产物的还原性,不能
说明Fe的活动性比Cu强,故C错误;
D.钢瓶的主要成分为铁,其中浓HSO 使铁钝化,钝化也是化学反应,故D错误;
2 4
故选B。
3.C
【详解】A.氯气是有毒气体,易对人体造成伤害,制备时应在通风橱内进行,防止使人
体中毒,A不符合题意;
B.金属钠的化学性质活泼,与氧气、水等物质反应,因此金属钠着火时,应立即用干燥
沙土覆盖,B不符合题意;
C.实验结束后不可将实验的废液倒入下水道,否则会腐蚀管道、造成污染,C符合题意;
D.稀释浓硫酸时,必须将浓硫酸缓缓地沿器壁注入水中,同时要搅动液体,以使热量及
时地扩散,D不符合题意;
故答案为:C。
4.A【详解】A.SO 能使酸性KMnO 溶液褪色,是因为SO 具有还原性,两者发生了氧化还
2 4 2
原反应,并不是由于SO 具有漂白作用,A错误;
2
B.炭、硫不溶于水,KNO 可以溶于水,用水可以分离KNO,硫易溶于二硫化碳,可用
3 3
二硫化碳分离炭和硫,分离三者要用到二硫化碳、水以及过滤操作,B正确;
C.浓硫酸与氯化钠固体反应制得HCl,是难挥发性的酸制备易挥发性的酸,说明了浓硫酸
的难挥发性,C正确;
D.0.8g硫的物质的量为 ,3.2 g铜的物质的量为
,根据反应2Cu+S Cu S可知两者能恰好反应生成0.025mol
2
的Cu S,即0.4 g纯净硫化物,D正确;
2
故答案为:A。
5.A
【分析】菱锰矿加硫酸溶解,加高锰酸钾将Fe2+氧化成Fe3+,加氧化钙提高pH,生成氢氧
化铁除铁,加入MnF 生成CaF 沉淀除去钙, 加入KSO 将Mn2+氧化成MnO 。
2 2 2 2 8 2
【详解】A.浓盐酸具有还原性,能在氧化阶段被加入的高锰酸钾氧化,不但消耗原料,
还会产生有毒气体氯气,则“酸浸”不可用过量浓盐酸代替硫酸,A错误;
B.“氧化”的目的是用高锰酸钾将Fe2+氧化为Fe3+,B正确;
C.提高pH生成氢氧化铁沉淀,并且钙离子变多,硫酸钙微溶于水,也会沉淀,“滤渣”
的主要成分为Fe(OH) 、CaSO,C正确;
3 4
D.KSO 将Mn2+氧化成MnO ,反应为 +Mn2++2H O=MnO ↓+2 +4H+,D正确;
2 2 8 2 2 2
故答案为:A。
6.C
【详解】A.Cu与浓HSO 反应生成CuSO 和SO ,浓HSO 的化合价部分降低,部分未
2 4 4 2 2 4
变,所以浓HSO 起到酸性和氧化性作用,A不符合题意;
2 4
B.FeO与浓HSO 反应生成Fe (SO ) 和SO ,浓HSO 的化合价部分降低,部分未变,所
2 4 2 4 3 2 2 4
以浓HSO 起到酸性和氧化性作用,B不符合题意;
2 4
C.CuO和浓HSO 反应生成CuSO ,化合价不变化,浓 只起酸性作用,C符合题意;
2 4 4
答案第2页,共2页D.C与浓HSO 反应生成CO 和SO ,浓HSO 化合价全部降低,所以浓HSO 只起到氧
2 4 2 2 2 4 2 4
化性作用,D不符合题意;
故答案为:C。
7.C
【详解】A.稀释浓 需要将浓 沿着玻璃棒缓慢注入盛有蒸馏水的烧杯中,并
不断搅拌,A错误;
B.浓硫酸不具有挥发性,蘸有浓氨水和浓硫酸的玻璃棒相互靠近,不会产生白烟,B错误;
C.浓硫酸具有吸水性,且不与 反应,可用于干燥 ,C正确;
D.浓硫酸具有强氧化性,能将 氧化,D错误;
故选C。
8.B
【详解】A.浓硫酸具有吸水性,可用作种干燥剂,能够干燥氢气、氧气等气体;浓硫酸
具有强氧化性和酸性,不能干燥碱性气体和有较强还原性的HI、HS等气,故A正确;
2
B.浓硫酸与木炭反应的化学方程式为C+2HSO (浓) CO↑+2SO ↑+2HO,在此反应
2 4 2 2 2
中,S元素化合价降低,浓硫酸既表现了强氧化性,故B错误;
C.Cu能和浓硫酸反应生成硫酸铜和二氧化硫,方程式为:Cu+2HSO (浓) CuSO +
2 4 4
SO ↑+2HO,1 mol铜粉投到足量浓硫酸中,加热得到1mol二氧化硫,标准状况下为22.4
2 2
L,故C正确;
D.浓硫酸能使铁、铝钝化,常温下能够用铁、铝等容器盛放浓硫酸,故D正确;
故选B。
9.D
【分析】X为一种常见酸的浓溶液,能使蔗糖粉末变黑,则X为硫酸,D和水反应生成硫
酸,则D是三氧化硫,B和氧气反应生成三氧化硫,则B是二氧化硫,据此解答。
【详解】由分析可知,X为硫酸、B为二氧化硫、D为三氧化硫;
A.浓硫酸使蔗糖变黑的现象主要体现了浓硫酸的脱水性,故A错误;
B.若A为铁,常温下,铁与浓硫酸反应生成致密的氧化物保护膜,发生钝化现象,所以铁不能完全溶解,故B错误;
C.若A为碳单质,浓硫酸和碳在加热条件下反应生成二氧化碳、二氧化硫和水,故C为
二氧化碳,二氧化碳与少量的澄清石灰水生成可溶性的碳酸氢钙,故C错误;
D.工业上,二氧化硫转化为三氧化硫的反应条件为400~500℃、常压、使用催化剂,故
D正确;
故选D。
10.C
【详解】A.常温下,浓硫酸能使铁、铝发生钝化,所以冷的浓硫酸可以用铝质或铁质容
器存放,A正确;
B.加热时,浓硫酸与铜片反应生成硫酸铜和二氧化硫,不产生氢气,B正确;
C.浓硫酸具有吸水性,能做干燥剂,滴在蔗糖上会出现变黑现象是由于浓硫酸的脱水性,
C错误;
D.浓硫酸具有强氧化性,与热的木炭发生氧化还原反应生成二氧化硫和二氧化碳,D正
确;
故选:C。
11.A
【分析】电热炉中C、Cu和浓硫酸反应生成CO、SO 气体,足量的高锰酸钾溶液吸收SO
2 2 2
气体,浓硫酸用于干燥CO 气体,U型管中碱石灰吸收CO 气体,干燥管中碱石灰防止空
2 2
气中成分对实验的干扰。
【详解】A.SO 和NaHCO 反应生成CO 气体,则不能有效测量电热炉中生成CO 的质量,
2 3 2 2
故不能用 溶液代替 溶液,A错误;
B.若撤去盛装浓硫酸的洗气瓶,水蒸气进入U型管,U型管增重质量偏高,则测定的结
果偏高,B正确;
C.球型干燥管内碱石灰的作用是防止空气中的水蒸气和二氧化碳进入U型管,减少实验
误差,C正确;
D.根据C+2H SO (浓) CO↑+2SO↑+2H O,根据C元素守恒,碳含量为 ,
2 4 2 2 2
D正确;
故选A。
12.C
答案第4页,共2页【详解】A.在试管①中发生反应S+2HSO (浓) 3SO ↑+2H O,浓硫酸得到电子被还原产
2 4 2 2
生SO ,故浓硫酸仅体现了强氧化性,A错误;
2
B.在试管②中看到酸性KMnO 溶液褪色,是由于SO 具有还原性,被酸性KMnO 溶液氧
4 2 4
化,故体现+4价硫元素的还原性,B错误;
C.在试管③中,SO 与NaS在溶液中发生氧化还原反应产生S,S是不溶于水的淡黄色固
2 2
体,因此看到有淡黄色沉淀出现,S元素化合价由NaS的-2价变为S单质的0价,这体
2
现-2价硫元素的还原性,C正确;
D.在烧杯中SO 与NaOH溶液反应产生+4价的NaSO ,反应的化学方程式应为
2 2 3
SO +2NaOH=Na SO +H O,D错误;
3 2 3 2
故合理选项是C。
13.(1) ⑤⑩; ①③④⑧;
(2) HSO = 2H++SO ; 取溶液少量,先加盐酸,无明显现象,再加BaCl 溶
2 4 2
液,产生白色沉淀;
(3)SO +2KOH=K SO +HO。
2 2 3 2
【详解】(1)①HSO 属于纯净物,溶于水能导电是电解质;②液氨是纯净物,不能电离
2 4
出离子,不导电,属于非电解质;③KOH固体是纯净物,熔融状态下能导电,属于电解质,
固体不导电,④熔融KHSO 能电离出阴阳离子而导电,属于电解质;⑤Fe(OH) 胶体属于
4 3
混合物,能导电,不是电解质,也不是非电解质;⑥铜是金属单质,能导电,不是电解质,
也不是非电解质;⑦CO 是纯净物,不能电离出离子,不导电,属于非电解质;
2
⑧CHCOOH是纯净物,溶于水能电离出离子而导电,属于电解质;⑨蔗糖是纯净物,不
3
能电离出离子,不导电,属于非电解质;⑩矿泉水属于混合物,能导电,不是电解质,也
不是非电解质;以上物质中属于混合物的是:⑤⑩,以上物质中属于电解质的是:
①③④⑧;
(2)HSO 在水溶液中电离出氢离子和硫酸根离子,电离方程式为:HSO = 2H++SO
2 4 2 4
;检验硫酸根的方法为:取溶液少量,先加盐酸,无明显现象,再加BaCl 溶液,产生白
2
色沉淀;故答案为:HSO = 2H++SO ;取溶液少量,先加盐酸,无明显现象,再加
2 4BaCl 溶液,产生白色沉淀;
2
(3)少量的SO 与氢氧化钾反应,会生成亚硫酸钾和水,故反应的化学方程式为:SO +
2 2
2KOH=K SO +HO;答案为:SO +2KOH=K SO +HO。
2 3 2 2 2 3 2
14. S+Fe FeS 还原性 硫酸 酸性氧化物 硫酸钡
【详解】(1)硫的氧化性比较弱,与铁在加热时反应产生FeS,该反应的化学方程式为:
S+Fe FeS;
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应:2HS+SO=3S+2H O,其中硫
2 2 2
化氢中的S反应前为-2价,反应后变为S单质的0价,化合价升高,失去电子被氧化,因
此HS呈现还原性;
2
(3)二氧化硫是形成酸雨的“元凶”之一,二氧化硫溶于水反应产生亚硫酸,亚硫酸不稳定,
容易被溶解在其中的氧气氧化为硫酸,故由二氧化硫形成的酸雨的主要成分是硫酸;
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,这是由于SO 是酸性氧化物,与碱
2
NaOH发生反应产生NaSO 和HO,使溶液的碱性减弱。酚酞遇碱变为红色,溶液碱性减
2 3 2
弱,溶液的红色逐渐变浅,甚至褪色,体现二氧化硫的酸性氧化物的性质;
(5)硫酸盐的种类很多且应用广泛,医疗上根据硫酸钡既不溶于水也不溶于酸,同时不能被
X光透过的性质,作X射线透视肠胃的内服药剂。
15. D
【分析】重晶石和过量的焦炭粉在回转炉中加热,生成硫化钡和一氧化碳,加入水得到硫
化钡溶液,加入硫酸锌反应生成立德粉,据此回答。
【详解】(1)钡元素的焰色为绿色,答案选D。
(2)已知反应物有BaSO、C,生成物有BaS,因焦炭过量则生成CO,根据得失电子守恒、
4
原子守恒写出化学方程式为 ;回转炉中有毒气体为一氧化碳,
和水蒸气反应生成二氧化碳和一种清洁能源气体,从元素守恒的角度分析,该气体应为氢
气,方程式为: 。
16.(1) 黄绿色 溶液碱性变强
(2) C 取精制后所得的滤液于试管中,加入足量盐酸酸化,再加 溶液没有明显现
答案第6页,共2页象,证明 已除尽;
(3)BC
(4) 和
(5)C
【详解】(1)在电解过程中,与电源正极相连的电极为阳极,Cl-放电生成氯气,故该极
上产生的气体的颜色为黄绿色;与电源负极相连的电极为阴极,电极反应为
,附近溶液的碱性变强;
(2)如果粗盐中 含量较多,必须添加钡试剂除去 , 、 会引入新
的杂质离子氢氧根、硝酸根。故该钡试剂可以是 ,避免引入新的杂质离子,故选C;
取精制后所得的滤液于试管中,加入足量盐酸酸化,再加 溶液没有明显现象,证明
已除尽;
(3)为有效除去 ,并保证所加试剂的离子易于除去,碳酸钠一定要在氯
化钡之后加入,可以除去过量的钡离子, 的加入顺序没有特别要求;
A.先加 ,后加 ,再加钡试剂,A不符合要求;
B.先加 ,后加钡试剂,再加 ,B符合要求;
C.先加钡试剂,后加 ,再加 ,C符合要求;
故选BC;
(4)由图可知在上述工业流程中,循环使用的物质是 和 ;
(5)未精制的饱和食盐水含有 ,阴极发生反应 ,
镁离子会与氢氧根生成氢氧化镁沉淀,故造成浑浊的难溶物主要是氢氧化镁;
故选C。答案第8页,共2页