文档内容
人教版(2019) 必修第二册第五章第三节 无机非金属材料
课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.近年来,我国在航天、通信、环保等领域取得了举世瞩目的成就。下列说法正确的
是
A.富勒烯、石墨烯和碳纳米管等碳纳米材料均属于新型无机非金属材料
B.“玉兔二号”月球车上的太阳能电池的材料是碳化硅
C.“神舟十四号”载人飞船返回舱外表面使用了高温结构陶瓷,其主要成分是硅酸盐
D.二氧化硅常被用于制造光缆,是由于其导电能力强
2.下列说法正确的是
A.二氧化硫溶于水能导电,二氧化硫是电解质
B. 的催化氧化制NO属于氮的固定
C.常温下硅的性质很稳定,自然界中存在游离态的硅
D.可用丁达尔效应区分溶液和胶体
3.下列说法不正确的是
A.工业上通常以氯气和烧碱为原料制造漂白粉
B.中国华为集团自主研发的“麒麟”芯片在生产时需要用到硅
C.氧化铁是俗称铁红,常用作油漆、涂料、油墨和橡胶的红色颜料
D.二氧化硫可作食品添加剂起到漂白、防腐和抗氧化等作用
4.下列说法正确的是
①合成纤维和光导纤维都是新型无机非金属材料
②硅酸可制备硅胶,硅胶可用作袋装食品、瓶装药品的干燥剂
③ 、 、 、 在水溶液中能大量共存
④向含 、 、 、 的溶液中通入 后仍能大量共存
⑤ 不与任何酸反应,可用石英制造耐酸容器
⑥硅酸钠可制备木材防火剂,也可用于制备硅酸胶体
⑦ 均能一步转化
A.①⑤⑥ B.①②⑥⑦ C.②⑥ D.③④⑥5.下列说法正确的是
A.氢氟酸具有强酸性,可用于雕刻玻璃
B.在粗硅的制取中发生反应2C+SiO 2CO+Si,硅被还原,所以碳的还原性大于
2
硅的还原性
C.高温时SiO 能跟NaCO 反应放出CO,所以硅酸的酸性比碳酸强
2 2 3 2
D.氨气不能用无水CaCl 干燥,SO 能用浓硫酸干燥
2 2
6.下列说法正确的是
A.常温下铁与浓硫酸不发生化学反应
B.铜粉与硫粉加热反应可生成硫化铜
C.石油裂解、煤的干馏和气化都是化学变化
D.石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体
7.设N 为阿伏加德罗常数,下列说法正确的是
A
A.用含0.01molFeCl 的饱和溶液制成的Fe(OH) 胶体中所含胶粒数等于0.01N
3 3 A
B.1mol Na O 固体中含有O 离子的个数为2×6.02×1023
2 2
C.1molSiO 晶体中Si—O键的个数为4N
2 A
D.0.5mol Na O 与HO反应时转移的电子数为N
2 2 2 A
8.化学与社会、环境密切相关,下列说法不正确的是
A.红宝石与蓝宝石主要成分都是α-氧化铝
B.水泥生产中,可用重晶石调节水泥的凝结时间
C.Ba2+浓度较高危害健康,但BaSO 可服于体内,作为造影剂用于X-射线检查肠胃道
4
疾病
D.金属切削加工废液中含有2 %~5 %的亚硝酸钠,为防止污染环境,可用氯化铵溶液
处理
9.下列有关试剂的保存方法正确的是
A.浓硫酸敞口放置
B.碳酸钠粉末保存在细口瓶中
C.漂白粉要密封存放于干燥阴凉处
D.氢氧化钠溶液保存在带磨口玻璃塞的玻璃试剂瓶中
10.广府文化是中华文明的重要组成,其代表有“广绣”、“广彩”、“镬耳屋”、
“粤菜”等。下列说法不正确的是
A.使用蚕丝制作“广绣”,蚕丝的主要成分是蛋白质
B.使用黏土烧制“广彩”,黏土中含有硅酸盐
试卷第2页,共3页C.使用青砖建造“镬耳屋”,青砖的青色来自
D.添加小苏打蒸制“粤菜”糕点,小苏打的化学式为
11.下列物质的性质与用途对应关系错误的是
A.NaN 分解产生大量气体,用于汽车安全气囊
3
B.Al(OH) 分解吸热且生成Al O 和水蒸气,可作阻燃剂
3 2 3
C.钠钾合金常温下呈液态、导电性好,可用于快中子反应堆的热交换剂
D.无水CoCl 呈蓝色,吸水后为粉红色(CoCl ∙6H O),可用于制造变色硅胶干燥剂
2 2 2
12.“生活无处不化学”。下列关于生活中的化学问题解释合理的是
A.硅胶常用作干燥剂,是因为硅胶多孔疏松
B.明矾可以净水,是因为Al3+具有强吸附性
C.以氨为原料可以制得铵盐或尿素等化肥,这是氮的人工固定
D.可用铁或铝制容器盛装浓硫酸,是因为常温下浓硫酸与铁或铝不反应
13.下列有关硅及其化合物的叙述错误的是
A.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
B.可用磨口玻璃瓶保存NaOH溶液
C.硅酸的酸性比碳酸的酸性弱,且硅酸不溶于水
D.NaSiO 的水溶液俗称“水玻璃”,可用作防火材料
2 3
14.某溶液可能含有Na+、NH 、Fe2+、Al3+、I-、AlO 、SiO 、SO 、CO 、SO
。现进行如下实验:
(1)向溶液中加入过量稀盐酸,产生沉淀X和气体Y,过滤;
(2)向滤液中加入过量氨水,产生白色沉淀;
(3)另取一定量原无色溶液,滴加少量溴水,溶液呈无色。
下列判断不正确的是
A.沉淀 是纯净物 B.气体 可以使澄清石灰水变浑浊
C.原溶液可能含NH 、I-、CO 、SO D.原溶液一定含Na+、AlO 、SO 和
SiO
二、多选题
15.可用来制取硅酸的反应是A.硅酸钙中加入稀硫酸
B.二氧化硅加入沸水中
C.水玻璃中通入足量二氧化碳
D.硅酸钠溶液中加入盐酸
三、填空题
16.硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)保存NaOH溶液的试剂瓶不能用玻璃磨口塞,用离子方程式表示其原因___________,
工艺师常用___________(填物质名称)来雕刻玻璃。
(2)绿柱石(绿宝石矿藏的主要化学成分为Be Al Si O ,可用氧化物形式表示为
n 2 6 18
nBeO•Al O•6SiO ,其n值为___________。
2 3 2
(3)用NaSiO 水溶液浸泡过的棉花不易燃烧,说明NaSiO 可用作___________。
2 3 2 3
NaSiO 可通过SiO 与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的
2 3 2
是___________(填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.铁坩
埚
17.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)SiO 是玻璃的主要成分之一,SiO 与氢氧化钠溶液反应的化学方程为______,工艺
2 2
师常用______(填物质名称)来雕刻玻璃,其所对应的方程式为______。
(2)Na SiO 溶液俗称______。
2 3
(3)工业上常用2C+SiO Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物
2
质是_____(填化学式),氧化剂是______。
18.A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制
造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)写出元素A在周期表中的位置_______,与A同族但相对原子质量比A小的元素B
的原子结构示意图为_______。
(2)A的单质与烧碱反应的离子方程式_______,工业上制取含有杂质的A单质的化学
反应方程式_______。
(3)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物
E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物
F。分别写出生成D和F的化学方程式:_______,_______。
试卷第4页,共3页19.硅胶和石英的主要成分都是SiO,前者是结构疏松的SiO,后者是结构致密的
2 2
SiO,二者成分相同,结构不同,化学性质相同,物理性质上表现出差别,具有不同
2
的用途。由石英制取硅胶,经历以下三步,试写出每步反应的化学方程式(是离子反应
的,写出离子方程式)。
(1)用NaOH(aq)溶解石英:___________。
(2)过滤,向滤液中加入盐酸,至沉淀不再产生:___________。
(3)微热,浓缩硅酸溶液,加热蒸干溶液,并使固体完全分解:___________。写出硅胶
的一种用途:___________。
20.中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是__________________。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是________________;乘务
员使用的无线通话机的芯片材料是________________。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与比例中的
二氧化硅反应的化学方程式______________________________。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是
纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子
方程式_________。
四、实验题
21.某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次
加入大小相近的钠(Na)、镁(Mg)、铝(Al)、钾(K)金属块,观察现象。
(1)反应最剧烈的烧杯中金属是_______(填字母序号);
A.钠 B.镁 C.铝 D.钾
(2)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮助选择
下列合适的方法_______(填字母序号)。
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
实验结论:随原子序数增大,同周期元素失电子能力依次_______(填“增强”或“减
弱”,下同),得电子能力依次_______。同主族元素失电子能力依次_______(填“增
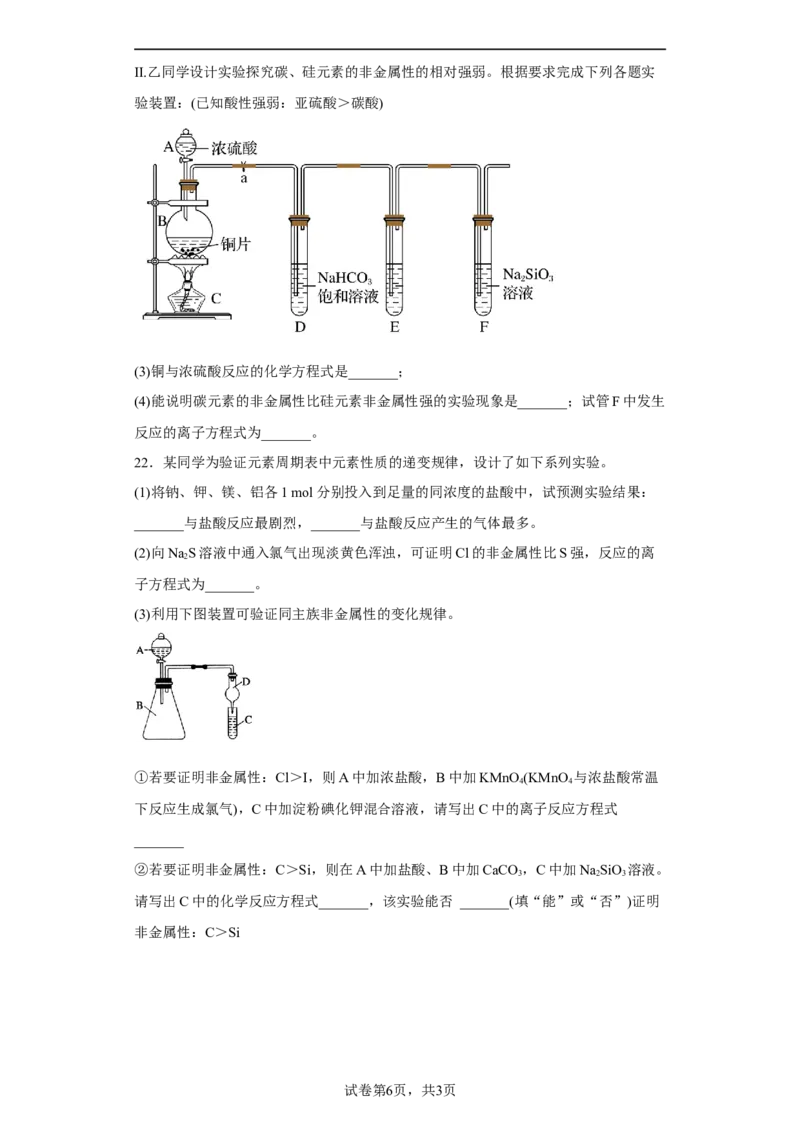
强”或“减弱”,下同),得电子能力依次_______;Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱。根据要求完成下列各题实
验装置:(已知酸性强弱:亚硫酸>碳酸)
(3)铜与浓硫酸反应的化学方程式是_______;
(4)能说明碳元素的非金属性比硅元素非金属性强的实验现象是_______;试管F中发生
反应的离子方程式为_______。
22.某同学为验证元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
_______与盐酸反应最剧烈,_______与盐酸反应产生的气体最多。
(2)向NaS溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离
2
子方程式为_______。
(3)利用下图装置可验证同主族非金属性的变化规律。
①若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO (KMnO 与浓盐酸常温
4 4
下反应生成氯气),C中加淀粉碘化钾混合溶液,请写出C中的离子反应方程式
_______
②若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO ,C中加NaSiO 溶液。
3 2 3
请写出C中的化学反应方程式_______,该实验能否 _______(填“能”或“否”)证明
非金属性:C>Si
试卷第6页,共3页参考答案:
1.A
【详解】A.富勒烯、石墨烯和碳纳米管都是由碳元素组成的单质,均属于新型无机非金
属材料,A正确;
B.“玉兔二号”月球车上的太阳能电池的材料是硅单质,B错误;
C.高温结构陶瓷的主要成分是氮化硅,属于新型无机非金属材料,C错误;
D.二氧化硅不导电,用于制造光缆是由于能够传导光信号,D错误;
故答案选A。
2.D
【详解】A.二氧化硫本身不能电离出自由移动的离子,属于非电解质,故A错误;
B.氮的固定是游离态氮元素转化为化合态氮元素的过程,则氨气的催化氧化制一氧化氮
不属于氮的固定,故B错误;
C.硅元素是亲氧元素,在自然界中不存在游离态的硅元素,故C错误;
D.胶体能发生丁达尔效应,溶液不能发生丁达尔效应,则可用丁达尔效应区分溶液和胶
体,故D正确;
故选D。
3.A
【详解】A.工业上通常以氯气和石灰乳为原料制造漂白粉,故A错误;
B.芯片的主要成分是硅,所以“麒麟”芯片在生产时需要用到硅,故B正确;
C.氧化铁为红棕色粉末,俗称铁红,常用作油漆、涂料、、油墨和橡胶的红色颜料,故C
正确;
D.二氧化硫有毒,但食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用,
不会对人体产生伤害,故D正确;
故选A。
4.C
【详解】①光导纤维是新型无机非金属材料,而合成纤维属于有机高分子材料,错误;②
硅胶就是硅酸干凝胶,硅酸可制备硅胶,硅胶可用作袋装食品、瓶装药品的干燥剂,正确;
③ Mg2+ 、 H+ 都能和 生成沉淀,在水溶液中不能大量共存,错误;④碳酸酸性比
硅酸强,向含 的溶液中通入 CO 会生成硅酸沉淀,不能大量共存,错误;⑤ SiO 能
2 2与氢氟酸反应,错误;⑥硅酸钠的水溶液俗称水玻璃,可制备木材防火剂,也可和酸反应
制备硅酸胶体,正确;⑦ Si和氧气可以生成SiO,但SiO 不和水反应,不能一步转化为
2 2
HSiO,错误;
2 3
综上所述,选C。
5.D
【详解】A.氢氟酸是弱酸,氢氟酸能与二氧化硅反应,所以氢氟酸用于雕刻玻璃,故A
错误;
B.由 可知,为非自发进行的氧化还原反应,不能比较碳、硅的还原
性,故B错误;
C.常温下,硅酸钠与二氧化碳反应生成硅酸,所以硅酸的酸性比碳酸弱,故C错误;
D.氨气和氯化钙结合生成络合物,不能用无水CaCl 干燥,SO 能用酸性干燥剂浓硫酸干
2 2
燥,故D正确;
故选:D。
6.C
【详解】A.常温下铁遇到浓硫酸会钝化,钝化属于化学反应,A错误;
B.硫粉的氧化性较弱,铜粉与硫粉加热反应生成硫化亚铜,B错误;
C.石油裂解是将相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低
的烃的过程,有新物质生成,属于化学变化;煤的干馏是煤在隔绝空气条件下加热、分解,
生成焦炭、煤焦油、粗苯、煤气等产物的过程,有新物质生成,属于化学变化;煤的气化
是以煤或煤焦为原料,以氧气、水蒸气或氢气等作气化剂,在高温条件下通过化学反应把
煤或煤焦中的可燃部分转化为气体的过程,有新物质生成,属于化学变化,C正确;
D.石英坩埚主要化学成分是SiO,烧碱、纯碱高温下与SiO 反应,因此石英坩埚不能用
2 2
来加热熔化烧碱、纯碱等固体,D错误;
故答案为:C。
7.C
【详解】A.胶体粒子是多个微粒的聚合体,充分作用后所得胶体中胶粒数小于0.01N ,A
A
错误;
B.1个NaO 当中,含有1个O ,则1mol Na O 固体中含有O 离子的个数为
2 2 2 2
1×6.02×1023,B错误;
答案第2页,共2页C.在SiO 晶体中,1个Si原子形成4个Si—O键,故1molSiO 晶体中Si—O键的个数为
2 2
4N ,C正确;
A
D.反应中NaO 中的氧原子一个得1个电子,一个失1个电子,所以0.5mol Na O 与水完
2 2 2 2
全反应转移的电子数为0.5N ,D错误;
A
故选C。
8.B
【详解】A.红宝石、蓝宝石的化学成分是Al O,主要成分都是α-氧化铝,故A正确;
2 3
B.水泥生产中,可用石膏CaSO 调节水泥的凝结时间,重晶石是硫酸钡的俗名,化学式
4
为BaSO,故B错误;
4
C.硫酸钡难溶于盐酸,BaSO 可作为钡餐服入体内,作为造影剂用于X射线检查肠胃道疾
4
病,故C正确;
D.利用NH Cl处理NaNO 发生反应NaNO +NHCl=NaCl+NH NO 、NH NO =N +2H O,
4 2 2 4 4 2 4 2 2 2
最终转化为NaCl、N 和HO无毒物质,故D正确;
2 2
故选:B。
9.C
【详解】A.浓硫酸易吸水,应密封保存,A错误;
B.碳酸钠粉末为固体,应保存在广口瓶中,B错误;
C.漂白粉易与空气中二氧化碳,水等发生反应,产生HClO,HClO见光易分解,故漂白
粉应密封保存在干燥阴凉处,C正确;
D.氢氧化钠能和玻璃中SiO 反应生成硅酸钠,硅酸钠具有胶黏性,应用橡胶塞,D错误;
2
故选C。
10.C
【详解】A.蚕丝为动物蛋白,主要成分是蛋白质,A正确;
B.黏土属于无机非金属材料,含有硅酸盐,B正确;
C. 是红色的,C错误;
D.小苏打为碳酸氢钠,化学式为 ,D正确;
故选C。
11.C
【详解】A.NaN 在受到猛烈撞击时分解产生大量气体N,因此用于汽车安全气囊,A正
3 2
确;B.Al(OH) 受热分解生成Al O 和水蒸气,分解时吸收大量热量,使环境温度降低,因此
3 2 3
可作阻燃剂,B正确;
C.钠钾合金在常温下呈液态,其导热性好,因此可用于快中子反应堆的热交换剂,C错误;
D.无水CoCl 可以制造变色硅胶是由于其能吸水且吸水后变色,与无水CoCl 呈蓝色、
2 2
吸水后为粉红色(CoCl ∙6H O)有关,D正确;
2 2
故合理选项是C。
12.A
【详解】A.硅胶多孔疏松,具有吸水性,可以用作干燥剂,故A正确;
B.明矾可以净水,铝离子水解生成具有吸附性的氢氧化铝胶体,故B错误;
C.以氨为原料可以制得铵盐或尿素等化肥,是不同氮的化合物之间的转化,不是氮的固
定,故C错误;
D.浓硫酸具有强的氧化性,常温下使铁、铝钝化,生成致密的氧化膜,所以可用铁或铝
制容器盛装浓硫酸,钝化属于化学变化,故D错误;
故选:A。
13.B
【详解】A.硅单质的导电能力比金属单质弱,但比绝缘体强,所以硅单质是良好的半导
体材料, A正确;
B.NaOH能与SiO 反应,生成黏性物质硅酸钠,将瓶塞与瓶口黏在一起,所以不可用磨
2
口玻璃瓶保存NaOH溶液,B错误;
C.Si的非金属性弱于C的,故硅酸的酸性比碳酸的酸性弱,且硅酸不溶于水,C正确;
D.NaSiO 的水溶液俗称“水玻璃”,木材和织物用水玻璃浸泡后既可防腐又不易着火,
2 3
所以可用作防火材料,D正确;
故选B。
14.C
【分析】(1)向溶液中加入过量的稀盐酸,产生沉淀X和气体Y,则气体Y为SO 或CO,
2 2
沉淀X为HSiO,即原溶液中含有SiO 和SO 或CO 中的至少一种,则溶液中不含有
2 3
Fe2+、Al3+;
(2)向滤液中加入过量氨水,又有白色沉淀产生,则沉淀为Al(OH) ,原溶液中含有AlO ,
3
答案第4页,共2页AlO 与NH 不能共存,故一定不含NH ;
(3) 另取一定量原无色溶液,滴加少量溴水,溶液呈无色,原溶液中含有SO ,根据溶
液电中性可知,原溶液中一定含有Na+;故原溶液一定含有Na+、AlO 、SO 和SiO ,
一定不含有Fe2+、Al3+、NH ,可能含有 、CO 、SO ,据此分析。
【详解】A.沉淀X为HSiO,A正确;
2 3
B.气体Y为SO 或CO,均可以使澄清石灰水变浑浊,B正确;
2 2
C.由上述分析可知,不可能含 ,C错误;
D.结合三个实验可知,原溶液一定含 、 、 和 ,D正确;
故本题选C。
15.CD
【详解】A.硅酸钙中加入稀硫酸反应生成微溶物硫酸钙和硅酸沉淀,反应难以持续且生
成物无法分离,A不符合题意;
B.二氧化硅与水不反应,B不符合题意;
C.碳酸酸性强于硅酸,反应NaSiO+CO+HO=Na CO+HSiO↓可制取硅酸,C符合题
2 3 2 2 2 3 2 3
意;
D.盐酸酸性强于硅酸,可由反应NaSiO+2HCl=2NaCl+HSiO↓制取硅酸,D符合题意;
2 3 2 3
故选CD。
16.(1) SiO+2OH-=SiO +H O 氢氟酸
2 2
(2)3
(3) 防火剂 C
【解析】(1)
玻璃中的主要成分是二氧化硅,二氧化硅是酸性氧化物,能和碱反应,也能和氢氟酸反应
生成四氟化硅和水。保存NaOH溶液的试剂瓶不能用玻璃磨口塞,其原因是SiO+2OH-
2=SiO +H O;氢氟酸常用来雕刻玻璃;
2
(2)
根据氧元素守恒可知n=18-3-6 2=3;
(3)
普通玻璃坩埚和石英玻璃坩埚的主要成分有二氧化硅,SiO 与纯碱混合高温熔融反应,故
2
高温熔融纯碱时可选用铁坩埚。
17.(1) 氢氟酸
(2)水玻璃
(3) C SiO
2
【详解】(1)SiO 是酸性氧化物,可以与碱发生反应: ;
2
SiO 化学性质较稳定,但可以与氢氟酸反应: ,因此可以用氢氟酸
2
来雕刻玻璃。
(2)NaSiO 溶液俗称水玻璃。
2 3
(3)根据化学方程式可知,该反应中,化合价升高的是C,氧化剂(所含元素化合价降低
的物质)是SiO。
2
18.(1) 第三周期ⅣA族
(2) Si +2OH-+H O=SiO +2H ↑ SiO+2C Si+2CO
2 2 2
(3) SiO+Na CO NaSiO+CO ↑ Na SiO+CO +H O=Na CO+H SiO↓
2 2 3 2 3 2 2 3 2 2 2 3 2 3
【分析】含A元素的一种单质是一种重要的半导体材料,则A为Si,含A元素的一种化合
物C可用于制造高性能的现代通讯材料--光导纤维,则C为SiO,C与烧碱反应生成含A
2
元素的化合物D为NaSiO;
2 3
(1)
答案第6页,共2页含A元素的一种单质是一种重要的半导体材料,A为Si,,位于第三周期ⅣA族,与A同
族但相对原子质量比A小的元素B为C,其原子结构示意图为 ;
(2)
A的单质Si与烧碱反应生成硅酸钠和氢气,反应的离子方程式Si +2OH-+H O=SiO
2
+2H ↑;工业上用CO和二氧化硅在高温下还原制取硅单质,反应方程式为SiO+2C
2 2
Si+2CO;
(3)
将SiO 与纯碱混合高温熔融时反应生成NaSiO,同时还生成B的最高价氧化物E,则E为
2 2 3
CO,反应为方程式为:SiO+Na CO NaSiO+CO ↑;将全部的CO 与全部的NaSiO
2 2 2 3 2 3 2 2 2 3
在足量的水中混合后,生成了含A的化合物F为HSiO,反应方程式为:
2 3
NaSiO+CO +H O=Na CO+H SiO↓。
2 3 2 2 2 3 2 3
19. 2OH-+SiO = +H O +2H+=H SiO↓ HSiO HO+SiO 干
2 2 2 3 2 3 2 2
燥剂或作催化剂的载体
【详解】(1)石英的主要成分是酸性氧化物SiO,与碱反应生成盐和水,离子方程式为2OH-
2
+SiO = +H O;
2 2
(2)过滤,除去石英中的杂质,得到的滤液为NaSiO 溶液,硅酸是弱酸,NaSiO 与盐酸发
2 3 2 3
生复分解反应生成白色沉淀硅酸,反应的离子方程式为 +2H+=H SiO↓。
2 3
(3)微热,HSiO(aq)浓缩,HSiO 聚合为胶体,加热硅酸溶胶脱水,生成多孔硅胶,反
2 3 2 3应的化学方程式为HSiO HO+SiO;硅胶的主要用途有作干燥剂或作催化剂的载体。
2 3 2 2
20. 黏土 石灰石 SiO Si 4HF+SiO ==SiF↑+2H O 2H++SiO 2-
2 2 4 2 3
==H SiO(胶体)
2 3
【详解】(1)水泥属于三大硅酸盐产品之一,主要原材料是黏土和石灰石,故答案为:黏
土、石灰石;
(2)纯净的二氧化硅具有良好的导光性,可以用于制备光导纤维;硅单质是良好的半导体
材料,可以用作芯片材料,故答案为:SiO;Si;
2
(3)氢氟酸与二氧化硅反应生成四氯化硅气体和水,反应方程式为:
4HF+SiO ==SiF↑+2H O,故答案为:4HF+SiO =SiF ↑+2H O;
2 4 2 2 4 2
(4)硅酸钠与盐酸发生复分解反应生成难溶的硅酸和氯化钠,离子方程式为:2H++SiO 2-
3
=H SiO(胶体),故答案为:2H++SiO 2-=H SiO(胶体)。
2 3 3 2 3
21.(1)D
(2) AB 减弱 增强 增强 减弱
(3)Cu+2H SO (浓) CuSO +SO↑+2H O
2 4 4 2 2
(4) E试管中的溶液褪色不完全,F试管中出现白色沉淀 CO+HO+
2 2
=H SiO↓+
2 3
【分析】乙同学设计实验探究碳、硅元素的非金属性的相对强弱。气体发生装置用于制取
SO ,用D装置制取CO 气体,用E装置除去CO 中混有的SO 并检验SO 已经除尽,所以
2 2 2 2 2
E中应加入酸性高锰酸钾溶液;E装置中生成的CO 通入硅酸钠溶液中,生成硅酸沉淀,
2
从而证明碳酸的酸性大于硅酸的酸性。
【详解】(1)在钠、镁、铝、钾中,钾的金属性最强,则反应最剧烈的烧杯中金属是钾,
故选D。答案为:D;
(2)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,可以进行的操
作是:A.把烧杯中的冷水换成热水,镁与热水反应,铝与热水不反应;B.把烧杯中的冷
水换成盐酸,镁、铝与盐酸都能发生反应,但镁与盐酸反应比铝与盐酸反应剧烈,故选
AB。
答案第8页,共2页实验结论:随原子序数增大,同周期元素失电子能力依次减弱,得电子能力依次增强。同
主族元素失电子能力依次增强,得电子能力依次减弱。答案为:AB;减弱;增强;增强;
减弱;
(3)铜与浓硫酸反应,生成硫酸铜、二氧化硫等,化学方程式是Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O。答案为:Cu+2H SO (浓) CuSO +SO↑+2H O;
4 2 2 2 4 4 2 2
(4)由分析可知,要想说明碳元素的非金属性比硅元素非金属性强,则需保证通入F试管
内的CO 中不混有SO ,所以E试管内KMnO 溶液应过量,则实验现象是:E试管中的溶
2 2 4
液褪色不完全,F试管中出现白色沉淀;试管F中,碳酸与硅酸钠发生复分解反应,生成
硅酸沉淀等,发生反应的离子方程式为:CO+HO+ =H SiO↓+ 。答案为:E
2 2 2 3
试管中的溶液褪色不完全,F试管中出现白色沉淀;CO+HO+ =H SiO↓+ 。
2 2 2 3
【点睛】比较两种酸的酸性强弱时,常利用强酸制弱酸的原理。
22.(1) 钾 铝
(2)S2-+Cl=S↓+2Cl-
2
(3) Cl +2Br-=2Cl-+Br Na SiO+CO +2H O=HSiO↓+Na CO 否
2 2 2 3 2 2 2 3 2 3
【分析】分液漏斗内的盐酸滴入锥形瓶内,与CaCO 发生复分解反应生成二氧化碳气体。
3
二氧化碳气体通入NaSiO 溶液中,发生复分解反应生成硅酸等。两个反应的原理都是强
2 3
酸制弱酸,由后一反应,若不考虑其它因素的干扰,可得出酸性HCO>HSiO,从而得
2 3 2 3
出非金属性:C>Si。
【详解】(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,由于钾的金
属性最强,所以与盐酸反应最剧烈,1mol钠、钾、镁、铝与盐酸反应,放出氢气的物质的
量分别为0.5mol、0.5mol、1mol、1.5mol,则实验结果:钾与盐酸反应最剧烈,铝与盐酸
反应产生的气体最多。答案为:钾;铝;
(2)向NaS溶液中通入氯气,发生反应NaS+Cl =2NaCl+S↓,从而出现淡黄色浑浊,可
2 2 2
证明Cl的非金属性比S强,离子方程式为S2-+Cl=S↓+2Cl-。答案为:S2-+Cl=S↓+2Cl-;
2 2
(3)①若要证明非金属性:Cl>I,则发生反应
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O、2KI+Cl =2KCl+I ,I 使淀粉变蓝,则C中
4 2 2 2 2 2 2的离子反应方程式:Cl+2Br-=2Cl-+Br 。
2 2
②若要证明非金属性:C>Si,则C中的化学反应方程式:
NaSiO+CO +2H O=HSiO↓+Na CO,由于盐酸挥发出的氯化氢气体溶解在C中也能与
2 3 2 2 2 3 2 3
NaSiO 发生反应,所以该实验不能证明非金属性:C>Si。答案为:Cl+2Br-=2Cl-+Br ;
2 3 2 2
NaSiO+CO +2H O=HSiO↓+Na CO;否。
2 3 2 2 2 3 2 3
【点睛】若想由实验证明非金属性:C>Si,则应在CO 气体进入装置C前,用饱和
2
NaHCO 溶液除去CO 中混有的HCl气体。
3 2
答案第10页,共2页