文档内容
课时作业
A篇·知识对点训练
1.下列物质中,不含有硅酸盐的是( )
A.水玻璃 B.硅芯片
C.黏土 D.普通水泥
答案 B
解析 水玻璃是Na SiO 的水溶液,黏土和普通水泥的主要成分都是硅酸盐,
2 3
硅芯片的主要成分是硅单质。
2.下列说法错误的是( )
A.二氧化硅是光导纤维的主要原料
B.硅是信息技术的关键材料
C.陶瓷餐具所用材料为硅酸盐
D.水晶镜片所用原料为硅酸盐
答案 D
解析 水晶、光导纤维主要成分为SiO 。Si用于信息产业及太阳能电池。传
2
统硅酸盐材料是陶瓷、水泥、玻璃。
3.下列叙述正确的是( )
A.Na SiO 是硅酸盐,所以不溶于水
2 3
B.电影银幕用水玻璃浸泡,主要是为了防腐
C.建筑工业常用水玻璃作黏合剂
D.用水玻璃浸泡铁道的木制枕木,主要是为了防火
答案 C
解析 Na SiO 既是硅酸盐,又是钠盐,硅酸盐大多难溶于水,而钠盐均易
2 3
溶于水,Na SiO 能溶于水;浸泡银幕主要是为了防火,而浸泡枕木主要是为了
2 3
防腐;水玻璃有黏合作用,常作黏合剂。
4.下列物质是纯净物的是( )
A.玻璃 B.水泥 C.纯碱 D.水玻璃答案 C
解析 玻璃、水泥均是多种硅酸盐的混合物,水玻璃是 Na SiO 的水溶液,
2 3
也是混合物;纯碱Na CO 是纯净物。
2 3
5.制取下列物质不需要用石灰石作原料的是( )
A.硅酸 B.水泥 C.玻璃 D.生石灰
答案 A
解析 硅酸由可溶性硅酸盐与酸反应制得。
6.镁橄榄石(2MgO·SiO )中阴离子是( )
2
A.SiO B.SiO C.SiO D.SiO
答案 A
解析 将镁橄榄石写成硅酸盐的形式,其化学式为 Mg SiO ,故阴离子为
2 4
SiO。
7.下列关于SiO 和CO 的说法中不正确的是( )
2 2
A.CO 和SiO 都能与碱及碱性氧化物反应
2 2
B.CO 和SiO 都能与水反应生成相应的酸
2 2
C.CO 和SiO 都能与焦炭反应生成CO
2 2
D.SiO 可用于制光导纤维,干冰可用于人工降雨
2
答案 B
解析 CO 能与水反应生成碳酸,但SiO 不能与水反应生成相应的酸,B错
2 2
误。
8.不能与SiO 发生反应的物质是( )
2
A.烧碱溶液 B.氧化钙
C.浓硝酸 D.焦炭
答案 C
解析 除HF外SiO 不与其他酸反应。
2
9.二氧化硅气凝胶是一种世界上最轻的固体,可以经受住 1 kg炸药的爆炸
威力。下列有关说法正确的是 ( )
A.利用二氧化硅气凝胶能够开发导电材料B.激光照射二氧化硅气凝胶可产生丁达尔效应
C.计算机芯片的主要成分是二氧化硅
D.二氧化硅气凝胶能溶于水
答案 B
解析 二氧化硅不导电,A错误;二氧化硅气凝胶属于胶体,能产生丁达尔
效应,B正确;计算机芯片的主要成分是单晶硅,C错误;二氧化硅不溶于水,
D错误。
10.在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅
的常用方法为Si(粗)+2Cl =====SiCl SiCl +2H =====Si(纯)+4HCl。“从沙
2 4 4 2
滩到用户”涉及多个反应,其中制取粗硅的反应方程式为__________________。
纯 净 的 石 英 与 烧 碱 反 应 可 以 制 得 水 玻 璃 , 反 应 的 离 子 方 程 式 为
____________________________________。
答案 SiO +2C=====Si+2CO↑
2
SiO +2OH-===SiO+H O
2 2
B篇·综合提升训练
11.化学在生产生活和科学研究中具有重要的作用。下列说法正确的是(
)
①石英的主要成分是二氧化硅
②三峡大坝使用了大量水泥,水泥是硅酸盐材料
③太阳能电池的主要成分是硅,太阳能电池在生活中的应用有利于环保、节
能
④二氧化硅的熔点高,硬度大,所以可用来制造电子部件和光学器件
⑤水晶项链和餐桌上的瓷盘都是硅酸盐制品
A.①②③ B.②④⑤
C.③④⑤ D.①②③④
答案 A
解析 石英的主要成分是二氧化硅;水泥属于传统硅酸盐产品;太阳能电池
的主要成分是硅;水晶项链的主要成分是 SiO ,餐桌上的瓷盘是硅酸盐制品;
2
硅是半导体材料,可制造电子部件,二氧化硅光学性能优良,可制光学器件。综上所述,选A。
12.已知滑石粉的化学式为Mg Si O (OH) ,色白、滑爽、柔软、耐火。下
3 4 10 2
列有关说法不正确的是( )
A.滑石粉属于无机硅酸盐类物质
B.滑石粉组成可表示为3MgO·4SiO ·H O
2 2
C.爽身粉中添加滑石粉是利用它的滑爽、柔软、耐火性
D.滑石粉可能会与氢氟酸、NaOH溶液发生反应
答案 C
解析 硅酸盐是由硅、氧元素与其他元素组成的一类无机物的总称,故滑石
粉属于无机硅酸盐类物质,A正确;可以将硅酸盐改写成氧化物的形式,B正确;
爽身粉中添加滑石粉,主要是利用它的滑爽、柔软、干燥的特点,与耐火性无关,
C错误;滑石粉中可能含有SiO ,可以与氢氟酸、NaOH溶液发生反应,D正确。
2
13.《青花瓷》中所描绘的“瓶身描绘的牡丹一如你初妆”“色白花青的锦
鲤跃然于碗底”等图案让人赏心悦目,但古瓷中所用颜料成分一直是个谜。近年
来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi O ,铜为+2价),
2 x
下列关于硅酸铜钡的说法不正确的是( )
A.可用氧化物形式表示为BaO·CuO·2SiO
2
B.性质稳定,不易脱色
C.易溶解于强酸和强碱
D.x等于6
答案 C
解析 “硅酸铜钡”能稳定存在说明其性质稳定,不易脱色,不易与酸、碱
反应;硅酸铜钡中Ba为+2价,Cu为+2价,Si为+4价,则x=6。因此,A、
B、D均正确。
14.证明生石灰中既混有石英,又混有石灰石的正确方法是( )
A.加入过量盐酸,观察是否有气泡冒出
B.加入过量烧碱溶液,观察是否有固体溶解C.加热至高温,观察是否有气体冒出,是否有硅酸钙生成
D.先加入过量盐酸搅拌,观察是否有不溶物剩余及气泡出现
答案 D
解析 SiO 不溶于除氢氟酸以外的任何酸,CaO、CaCO 均可溶于盐酸,且
2 3
CaCO 溶于盐酸有气泡生成。
3
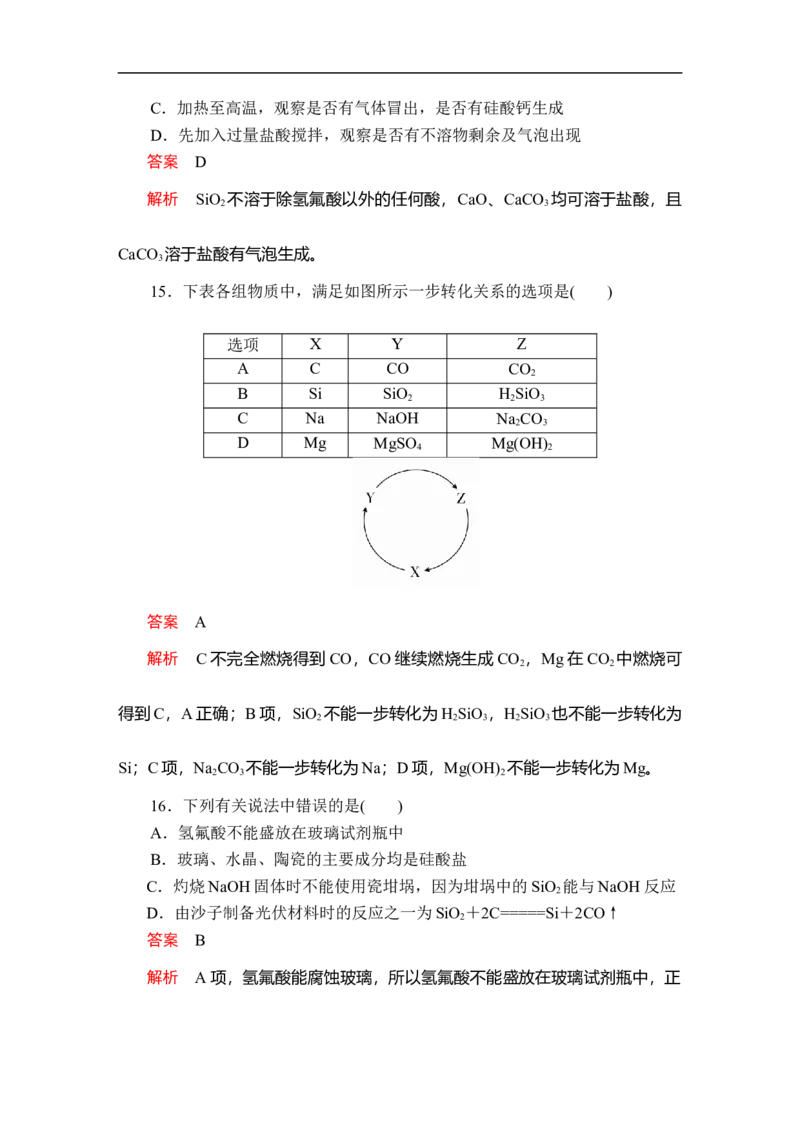
15.下表各组物质中,满足如图所示一步转化关系的选项是( )
选项 X Y Z
A C CO CO
2
B Si SiO H SiO
2 2 3
C Na NaOH Na CO
2 3
D Mg MgSO Mg(OH)
4 2
答案 A
解析 C不完全燃烧得到CO,CO继续燃烧生成CO ,Mg在CO 中燃烧可
2 2
得到C,A正确;B项,SiO 不能一步转化为H SiO ,H SiO 也不能一步转化为
2 2 3 2 3
Si;C项,Na CO 不能一步转化为Na;D项,Mg(OH) 不能一步转化为Mg。
2 3 2
16.下列有关说法中错误的是( )
A.氢氟酸不能盛放在玻璃试剂瓶中
B.玻璃、水晶、陶瓷的主要成分均是硅酸盐
C.灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO 能与NaOH反应
2
D.由沙子制备光伏材料时的反应之一为SiO +2C=====Si+2CO↑
2
答案 B
解析 A项,氢氟酸能腐蚀玻璃,所以氢氟酸不能盛放在玻璃试剂瓶中,正确;B项,水晶的主要成分是SiO ,不是硅酸盐,错误;C项,瓷坩埚是硅酸盐
2
产品,坩埚中的SiO 能与NaOH反应,正确;D项,沙子的主要成分是SiO ,
2 2
光伏材料的成分是晶体硅,由沙子制备光伏材料时的反应之一为 SiO +
2
2C=====Si+2CO↑,正确。
17.铝硅合金具有熔点低、凝固时收缩率小等优点,适合铸造。现取试样
10.0 g,放在纯净氧气中完全燃烧,燃烧后的固体经称量发现比原来试样增重
9.23 g,由此计算硅铝合金中硅的质量分数约为( )
A.12.3% B.15.4% C.13.4% D.17.0%
答案 C
解析 铝、硅燃烧反应的化学方程式分别为 4Al+3O =====2Al O ,Si+
2 2 3
O =====SiO 。固体增重质量就是参加反应的氧气的质量。设 Si的质量为x g,
2 2
则Al的质量为(10-x) g,根据化学反应方程式知,铝消耗的氧气的质量为 96(10
-x)÷108,硅消耗的氧气的质量为32x÷28,96(10-x)÷108+32x÷28=9.23 g,解得
x≈1.34 g,硅铝合金中硅的质量分数为1.34 g÷10.0 g×100%=13.4%。
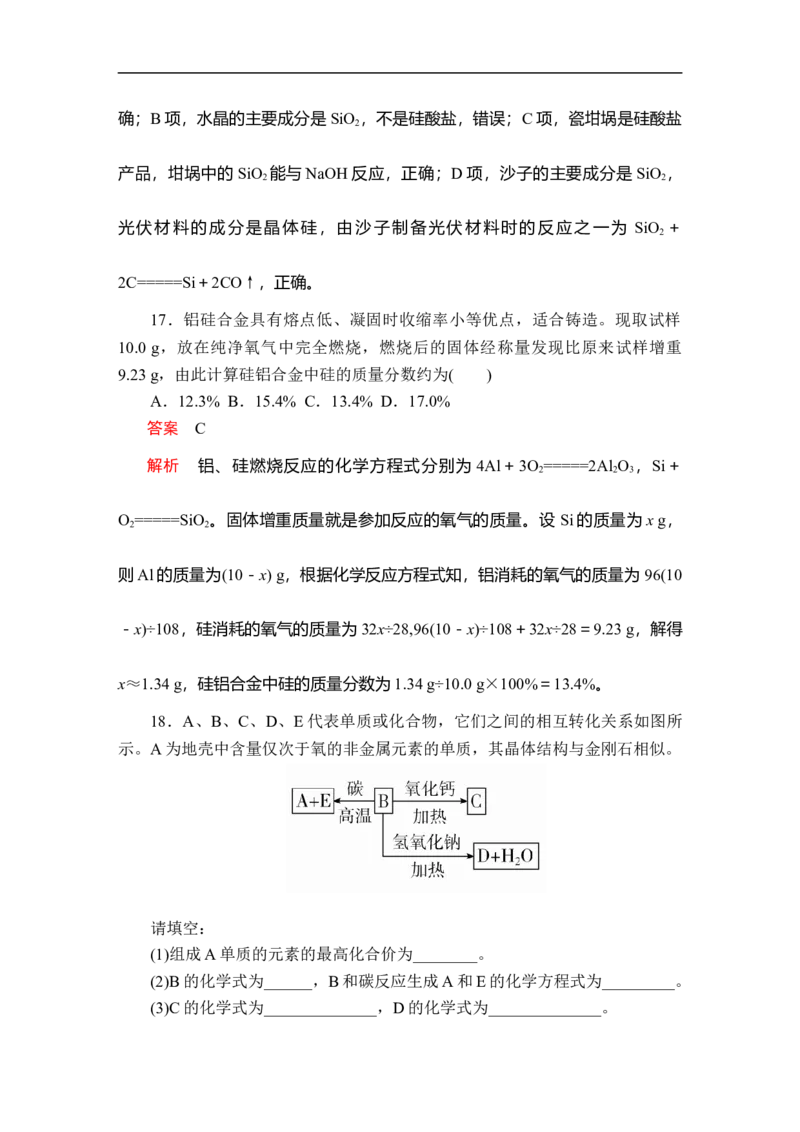
18.A、B、C、D、E代表单质或化合物,它们之间的相互转化关系如图所
示。A为地壳中含量仅次于氧的非金属元素的单质,其晶体结构与金刚石相似。
请填空:
(1)组成A单质的元素的最高化合价为________。
(2)B的化学式为______,B和碳反应生成A和E的化学方程式为_________。
(3)C的化学式为______________,D的化学式为______________。答案 (1)+4价
(2)SiO SiO +2C=====Si+2CO↑
2 2
(3)CaSiO Na SiO
3 2 3
解析 由本题题眼“A为地壳中含量仅次于氧的非金属元素的单质,其晶体
结构与金刚石相似”,推知A为硅;根据框图B+碳―→Si+E,B既能与氧化
钙反应又能与氢氧化钠反应,推知 B为二氧化硅,进一步推知C为硅酸钙,D
为硅酸钠,E为一氧化碳。
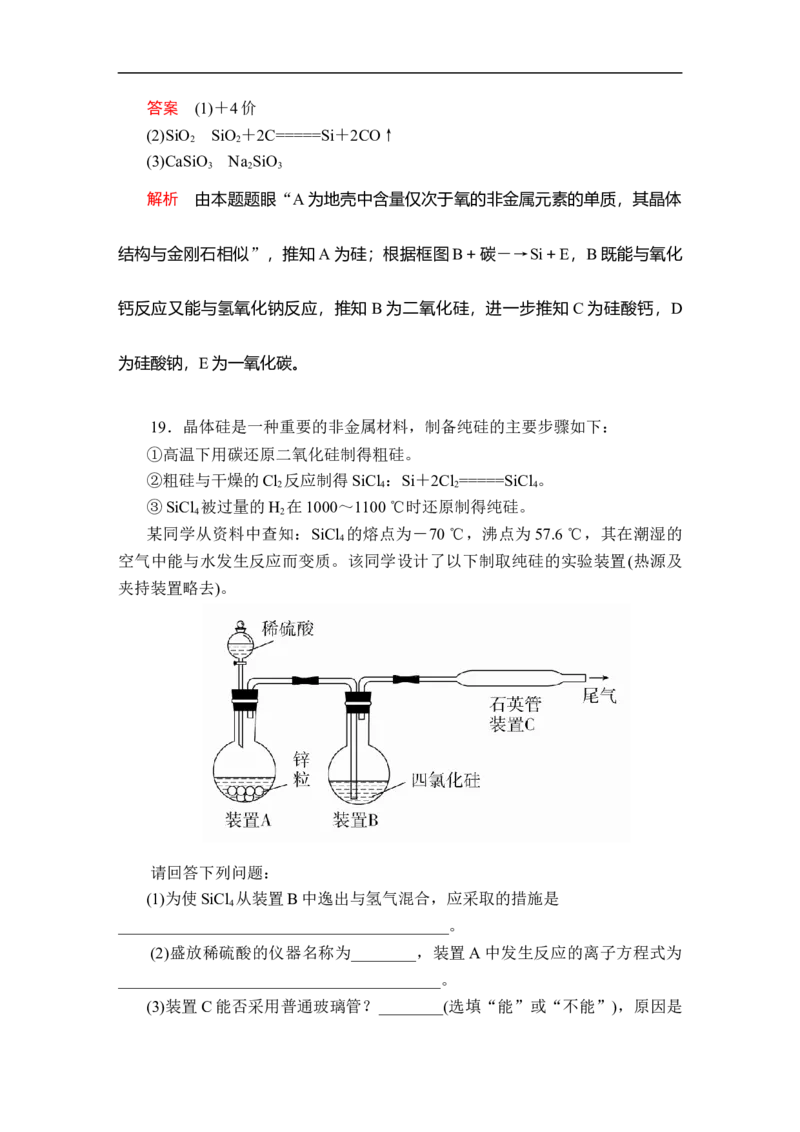
19.晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅。
②粗硅与干燥的Cl 反应制得SiCl :Si+2Cl =====SiCl 。
2 4 2 4
③SiCl 被过量的H 在1000~1100 ℃时还原制得纯硅。
4 2
某同学从资料中查知:SiCl 的熔点为-70 ℃,沸点为57.6 ℃,其在潮湿的
4
空气中能与水发生反应而变质。该同学设计了以下制取纯硅的实验装置(热源及
夹持装置略去)。
请回答下列问题:
(1)为使SiCl 从装置B中逸出与氢气混合,应采取的措施是
4
_________________________________________。
(2)盛放稀硫酸的仪器名称为________,装置A中发生反应的离子方程式为
________________________________________。
(3)装置C能否采用普通玻璃管?________(选填“能”或“不能”),原因是____________________________。
(4)已知SiCl 在潮湿的空气中能与水发生反应生成氯化氢,为防止空气污染,
4
含有SiCl 的尾气要通入盛有________溶液的烧杯中。
4
(5)为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控
制好反应温度,还应对该装置进行的改进是___________________________。
答案 (1)对装置B进行水浴加热
(2)分液漏斗 Zn+2H+===Zn2++H ↑
2
(3)不能 在1000~1100 ℃时普通玻璃管会软化
(4)NaOH
(5)在装置A与装置B之间连接一盛有浓硫酸的洗气瓶(或盛有碱石灰的干燥
管)
解析 (1)SiCl 的沸点较低(57.6 ℃),欲使其逸出烧瓶与装置C中的H 反应,
4 2
需对装置B进行水浴加热。
(3)由于H 与SiCl 在1000~1100 ℃时反应制得纯硅,反应温度高,普通玻
2 4
璃管在此温度下会软化,因此需要用石英管。
(5)为了防止装置A中的水蒸气进入装置 B中,应在装置A、B之间加一干
燥装置。