文档内容
2024年重庆市普通高中学业水平选择性考试
高考模拟调研卷化学(一) 参考答案
1~5 CBAAC 6~10 DDBBC 11~14 CCDD
1.C
A. 纳米碳酸钙是纯净物,不是分散系, 不属于胶体,A 错误;
B. 胃舒平的主要成分是 Al(OH)₃, FeSO₄和Al(OH)₃混合食用不能增强效果, B错误;
C. 碳化硅是新型无机非金属材料,C 正确;
D.光纤的主要成分是 SiO₂, D 错误。
2.B
A. Al3+水解的离子方程应是可逆符号,A 错误;
C. 向NaOH 溶液中通入少量CO 的离子方程式为 CO+2OH-=CO2− +H O,C 错误;
2 2 3 2
D. I⁻的还原性比Fe²⁺强,少量HO 先氧化I⁻, D错误。
2 2
3.A
A. 镁是活泼金属,不能用热还原法制取, A 错误;
B.制造玻璃的主要原料是纯碱、石灰石、SiO,B正确;
2
C. 浓硫酸具有吸水性, 且不氧化SO ,故可以干燥,C正确;
2
D.K CaCO <K CaSO , 水垢中的CaSO 可以与饱和Na₂CO 溶液反应生成CaCO , D 正确。
sp 3 sp 4 4 3 3
4. A
A.1个NH 分子中含有18个电子,6.4gN₂H₄为0.2mol,其电子数为3.6 N , A 正确;
2 4 A
B. 未告知溶液体积,不能计算,B错误;
C. 未标明温度和压强,无法计算,C 错误;
D. 水在标准状况下为液体, 33.6L H₂O 不是 1.5mol, D错误。
5. C
A. 该装置验证铁粉发生吸氧腐蚀, A 错误;
B. 铜与浓硫酸反应需要加热,B错误;
C.该装置是密闭体系,可以用此方法检查气密性,C 正确;D.乙醇与水互溶,不能用乙醇萃取碘水中的碘,D 错误
6. D
A. 中子数为8的 N原子为¹⁵N, A 错误;
B. 基态原子第一电离能由大到小:N>O>B,B错误;
C. B原子反应前是 sp³杂化, 反应后是 sp²杂化, C错误;
D. 氨硼烷中与N原子相连的H原子呈正电性,与B原子相连的 H 原子呈负电性,它们之间有相互吸引作
用,D正确。
7. D
A. M中只有1个手性碳原子, A 错误;
B.1mol G最多可消耗2mol NaOH, B错误;
O
C. 中含有酚羟基,N中没有酚羟基,它们不是同系物 ,C错误;
HO C Cl
D. 显碱性,能消耗反应生成的HCl,有利于反应正向进行,提高转化率,D 正确。
8. B
【解析】W、X、Y、Z原子序数依次增大且不相邻,W形成1个共价键,W为H,X形成4个共价键,X
为C,Y 形成2 个共价键, Y 为O, Z 形成1个共价键, 则Z在第三周期, 为 Cl。
A. Cl的原子结构示意图为 ,A错误。
B.X、Y、Z的简单氢化物分别为CH、HO、HCl,其中NO分子之间有氢键,沸点最高, B正确;
4 2 2
C. X是碳,碳的基态原子有 4种空间运动状态的电子,C错误;
D. 该化合物与在酸性条件下水解生成的气体是 CO₂,CO₂是非极性分子,D错误。
9. B
A. Ag⁺过量, 不能证明Ksp(AgCl)>Ksp(AgI), A错误;
B. 发生的反应是 Cu₂O+2H⁺ =Cu+Cu²⁺ +H₂O,Cu₂O既作氧化剂又作还原剂,B 正确;
C. 若产生的气体只有SO₂,通过饱和 NaHCO₃溶液也可以产生CO₂,澄清石灰水变浑浊不能说明浓硫酸和木
炭反应产生了 CO₂, C 错误;
D. Cu2+与氨水反应生成Cu(OH)₂,氨水过量会生成[ [Cu(NH₃)₄]²⁺,沉淀溶解, 不能说明Cu(OH)₂有两性, D错
误。
10. C
【解析】在压力梯度的驱动下,储氢材料极生成的质子(H+)通过交换膜移向Pd 极,外电路电子流
动方向为:Pt极→负载→Pd极, 故Pd 极为正极, Pt极为负极。
A. Pd极发生还原反应, A 错误;
B. 电流方向为 Pd极→负载→Pt极→交换膜→Pd极, B错误;
C. 电池负极反应为 PdHₓ−e⁻ =PdHₓ₋₁+H⁺,, C 正确;
D. Pt极的电势低于 Pd 极的电势; D错误。11. C
【解析】从该反应历程图可以看出反应物为乙二醇,催化剂为MoO₃,生成物为水、 乙烯、 甲醛,
为反应的中间体。
A. 催化剂不能提高反应物的平衡转化率,A错误;
B. 该过程中没有C—H键断裂,B错误;
C. HOCH₂CH₂OH 滴入过量酸性高锰酸钾溶液,生成的乙二酸会被过量酸性高锰酸钾氧化成CO₂, C正确;
D. 由图中反应③可知, 连接两个醇羟基的碳原子之间C-C键断裂分别生成甲醛, 由反应①②④可知
相邻的两个醇羟基生成水分子的同时还生成碳碳双键,如果原料为HOOH(CH )CH(OH)CH , 则生成
3 3
的有机物为乙醛和2一丁烯,D错误。
12. C
【解析】N 点导电能力最强, 说明此时 CH₃COOH 与】 NH₃⋅H₂O恰好完全反应,Kₐ=Kb, CH₃COONH₄呈中
性,
A. N 点pH=7, A 正确;
B. 根据质子守恒, B 正确;
C. 由电荷守恒可得 c(NH⁺)+c(H⁺)=c(CH₃COO⁻)+c(OH⁻), C 错误;
D. M、N、O三点中, M点溶质是 NH₃·H₂O, N 点溶质是 CH₃COONH₄,Q点溶质是 CH₃COONH₄和
CH₃COOH,Q点都是抑制水的电离,N 点是促进水的电离,D 正确.
13. D
A.晶体中In和P的配位数相同, 与P 最近且等距离的 In有4个, 故In的配位数为 4, A 正确;
B. 图2中, 1、2、3、4为晶体内的P原子, 1、2原子间间距与2、4 相等, B 正确;
(115+31)
×4
C. 1个晶胞中有4个 InP, 晶体密度为 N A = 584 ×102lg⋅cm−3, C 正确;
(a×10−7) 3 N ×a3
A
1 √3a
D. P原子与 In原子之间的最近距离为晶胞体对角线的 , 即 , D错误。
4 4
14. D
A. 反应②的平均相对分子质量始终不变, 而反应①正方向平均相对分子质量增大,由图可知,温度升高,
容器中混合气体的平均相对分子质量减小,反应①逆向移动,所以反应①为放热反应,A 正确;
B. 由图可知,当温度高于 250℃ ,CO 的转化率随温度的升高而增大,则250℃以后以反应②为主,反应
2
①的选择性减小,B 正确;
C. T℃, CO₂转化率为 50%, 则转化的CO₂为0.5mol, 平均相分子质量为20. 混合气体总物质的量为:
44+2×2
= 2.4mol,设 甲 醇 为 xmol , CO 为 ymol , 根 据 方 程 式 x+
20
y=0.5,n(H₂)=2−(3x+ y),n(H₂O)=x+ y,n(H₂O) +n(H₂)+n(CO)+n(CHOH)+n(CO )=2.4mol,
3 2
0.2
计算n(CHOH)有0.3mol, n(CO)=0.2mol, 反应②的选择性为 ×100%=40%,C正确;
3 0.5
D.n(H₂O)=0.5mol,H₂O的压强是CO的2.5倍,D错误。15. (14分)
( 1 ) (2分), +6(1分)
(2)[Zn(NH₃)₄]²⁺(1分),搅拌、适当升温、将锌焙炒粉碎、延长浸出时间等(2分)
(3)2ASO3−+2Fe2++3S O2−+2H O=2FeAsO ↓+6SO2−+4H− ⁺(2分)
3 2 8 2 4 4
(4)1.25×10⁻²mol⋅L⁻¹(2分)
(5)Zn(N H₃)₂SO₄+CO₂+H₂O=ZnCO₃↓+(NH₄)₂SO₄(2分)
(6) NH₃·H₂O(1分)、CO₂(1分)
(1) Zn 的 价 层 电 子 排 布 式 为 3d¹⁰4s² , 其 轨 道 表 达 式 为
(NH )SO 法化学中有两个-1价的氧原子,其余氧原子都是-2价,S原子为+6价
4 2 2 8
K (CuS) K (PbS)
(4) 溶液中
c(S2−)= so =6.4×10−26mol⋅L−1,c(Pb2+)= so =1.25×10−2mol⋅L−1;
c(Cu2) c(S2)
(6) 溶液 1 的溶质为 1 NH₃⋅H₂O,,气体 1 为 CO₂, 流程中可循环利用的物质除(NH₄)₂SO₄,还有
NH₃·H₂O、CO₂。
16. (15分)
(1) 直型冷凝管(1分)
(2)防止E中的水蒸气进入反应装置;(2分) 吸收COCl₂(2分)
(3)排除装置中的空气,防CrCl 氧化 (2分)
3
(4)Cr O +3CCl 2CrGl +3COCl (2分)
2 3 4 3 2
(5) pH 传感器读数保持不变(2分)
(6)2Cr³⁺ +3H₂O₂+10OH⁻ =2CrO2
4
− +8H
2
O(2分)
(7) 79.25%(2分)
【 解 析 】 (7) 根 据 元 素 守 恒 和 氧 化 还 原 反 应 中 得 失 电 子 守 恒 得 2CrCl - 2
3
CrO2−→Cr O2−→ 6(N H ) Fe(SO ) ,
4 2 7 4 2 4 2
1 25
n(CrCl )= ×25×n[(NH ) Fe(SO ) ]= ×0.12×25×10−3=2.5×10−2mol, CrCl₃
3 3 4 2 4 2 3
2.5×10−2×158.5
的纯度为 ×100%=79.25%
5
17. (14分)(1) -197.8 (2分)
(2) 放热(1分); 1(1分); 50% (2分); 10(2分)
(3)不一定处于平衡状态,转化率不一定为平衡转化率,因温度升高可能影响催化剂的活性而影响反应速
率,从而影响转化率(2分)
(4)①2HSO−+2e−+2H+=S O2−+2H O (2分) ②8.96 (2分)
3 2 4 2
【解析 】(1)由盖斯定律可知,反应Ⅱ-2×Ⅰ得Ⅲ:2NO(g)+2CO(g)⇌N
2
(g)+2CO
2
(g)
ΔS₃=ΔS₂−2ΔS₁=−197.8J⋅K⁻¹⋅mol⁻¹
(2) 由图可知,随着温度升高,K 减小,平衡逆向移动,则反应Ⅰ 为放热反应; 温度为t K下,
p
1gK =0,则 Kₚ =1
p
NO
2
(g)+CO(g)⇌NO(g)+CO
2
(g)
起(mol) 2 2
转(mol) a a a a
平(mol) 2-a 2-a a a
a×a
K p = (2−a) 2 =1,a=1mol,则达到平衡时, NO₂的转化率为 1/2=50%,测得起始压强为 40kPa, NO 的
1
平衡分压为 40× =10kPa。
4
1
(4) 0.8mol H⁺通过质子交换膜,说明装置中转移电子的物质的量为0.8mol, NO→ N ,转移 2mole- 标准
2 2
状况下处理 NO 的体积为0.8×0.5×22.4 =8.96L。
18. (15 分)
(1)取代反应(1分)
(2)一氯乙酸(或2-氯乙酸)(1分);羟基、羧基(2分)
O
(3) (2分)
OC H
2 5
OC H
2 5
OC H
2 5
∆NH
(4)OHCCOOH+2Ag(NH
3
)
2
OH 4OOCCOONH
4
+2Ag↓+2NH
3
+H
2
O(2分)
→
(5)保护醛基(1分) (6)4(2分)
(7) (2分)、 (2分)
【解析】已知A溶于水,结合A的分子式和B的结构可知A为CH₃COOH, 由 F 逆推得 E为 ;由B 和
H2N
O
CHC
N
O N H
COOCH3H2N
O
CHC
N
O N H
COOCH3
E的结构可推得C为HOCH₂COOH, D为OHCCOOH。X是D的同系物,且相对分子质量大 14, 则X为
OHCCH₂COOH,符合条件的 X 的同分异构体有:CH COCOOH、OHCCOOCH₃、HCOOCH₂CHO、
3
HCOOCOCH₃,
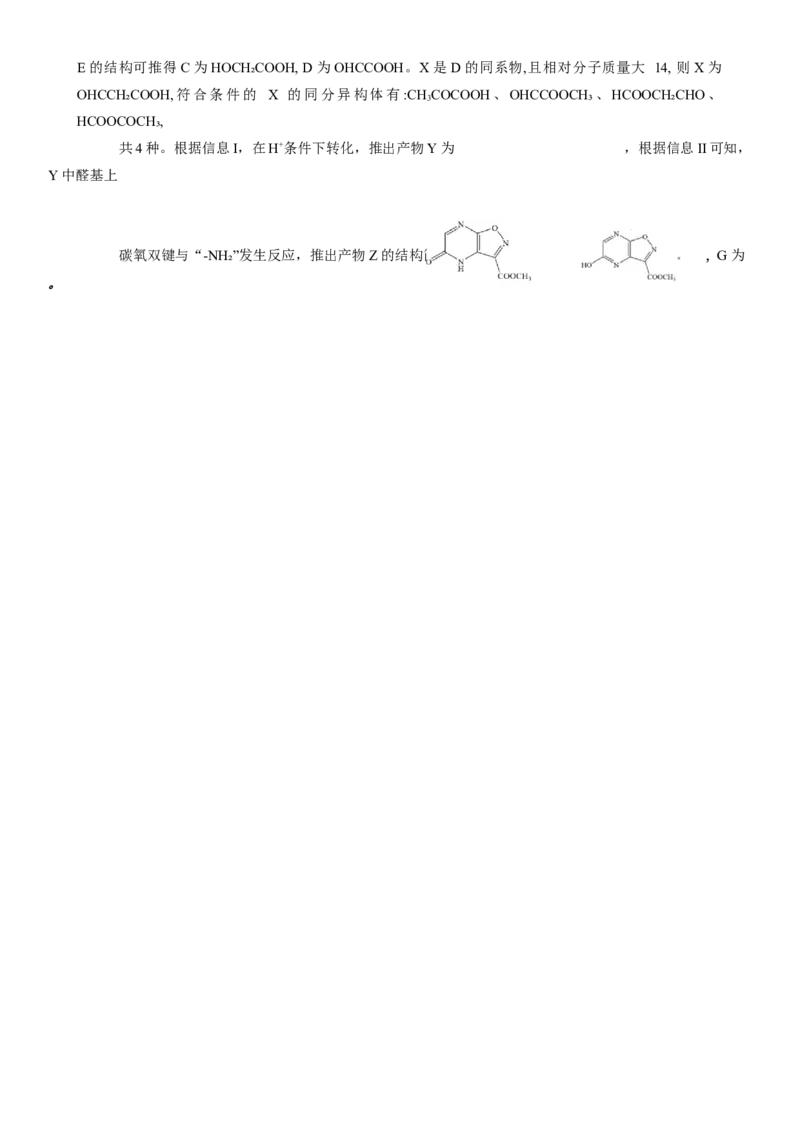
共4种。根据信息I,在H+条件下转化,推出产物Y为 ,根据信息II可知,
Y中醛基上
碳氧双键与“-NH₂”发生反应,推出产物Z 的结构简式为 , G 为
。