文档内容
天津市耀华中学第一学期期末考试
高一年级化学学科试卷
Ⅰ卷
可能用到的相对原子质量: -1 -12 -14 -16 -23 -32 -35.5 -64 -65 -137
一、选择题(每小题只有一个选项符合题意)
1. 下列叙述中正确的是( )
A. HO+和OH-中具有相同的质子数和电子数
3
B. BaSO 不溶于水,因此是弱电解质
4
C. 和 互为同位素,化学性质几乎相同,物理性质不同
D. 和 是中子数不同质子数相同的同种核素
【答案】C
【解析】
【分析】
【详解】A.HO+中质子数是11,电子数是10,而OH-中质子数是9,电子数是10,可见二者具有相同的
3
电子数,但质子数不同,A错误;
B.虽然BaSO 不溶于水,但其溶于水的部分完全电离变为离子,因此是强电解质,B错误;
4
C. 和 互为同位素,质子数相同,原子核外电子数相同,核外电子排布也相同,因此化学性质
几乎相同,但由于质量数不同,因此二者的物理性质不同,C正确;
D. 和 质子数相同但中子数不同,因此二者是同一元素的不同种核素,D错误;
故合理选项是C。
2. 下列说法正确的是( )
A. 第二周期元素从左到右,最高正价从+1递增到+7
B. 同主族元素从上到下,单质的熔点逐渐降低
C. 不同元素的原子构成的分子只含极性共价键
D. 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构
【答案】D【解析】
【分析】
【详解】A.第二周期元素从左到右,元素的非金属性逐渐增强。由于O、F原子半径小,得到电子能力强,
不能失去电子,与其它非金属元素的原子形成共用电子对时,电子对偏小 O或F元素,因此没有与族序数
相当的最高价态+6或+7价,A错误;
B.同主族金属元素从上到下,金属单质的熔点逐渐降低;而非金属元素的单质若都是分子晶体,则熔沸
点逐渐升高;若同一主族元素形成的单质晶体类型不同,则没有规律性, B错误;
C.不同元素的原子构成的分子可能只含极性共价键,也可能含有非极性共价键和极性共价键,如HO、
2 2
CH-CH 等中都含有非极性共价键和极性共价键,C错误;
3 3
D.短周期第ⅣA元素的原子最外层有4个电子,第ⅦA族元素的原子最外层有7个电子,二者按1:4原
子个数比形成共价键而构成的分子,均满足原子最外层8电子结构,D正确;
故合理选项是D。
3. 下列叙述正确的是( )
A. 第三周期非金属元素含氧酸的酸性从左到右依次增强
B. 锂在氧气中加热,产物是LiO
2
C. 元素周期表位于金属和非金属交界线的元素属于过渡元素
D. Li、Na、K的金属性和密度均随原子序数的增加而增大
【答案】B
【解析】
【分析】
【详解】A.第三周期非金属元素的最高价含氧酸的酸性从左到右依次增强,A错误;
B.Li原子最外层只有1个电子,与O 在加热条件下反应产生LiO,B正确;
2 2
C.元素周期表位于金属和非金属交界线的元素既具有金属的性质,又具有非金属元素的性质,导电性介
于导体和绝缘体之间;过渡元素包括副族元素与第VIII族元素,C错误;
D.Li、Na、K都是第IA的元素,从上到下,原子核外电子层数逐渐增多,元素的金属性逐渐增强;金属
密度呈增大趋势,其中K的密度比Na要小些,D错误;
故合理选项是B。
4. 若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,一定能大量共存的是( )
A. NH 、SO 、CO 、K+ B. Na+、Ba2+、Ca2+、HCO
C. Mg2+、SO 、K+、Cl- D. K+、Cl-、Na+、SO
【答案】D【解析】
【分析】
加入铝粉能放出氢气 的溶液中,可能含有OH-;可能含有H+,但不含有 。
【详解】A.NH 在碱性溶液中不能大量存在,CO 在酸性溶液中不能大量存在,A不合题意;
B.HCO 在酸性、碱性溶液中都不能大量存在,B不合题意;
C.Mg2+在碱性溶液中不能大量存在,C不合题意;
D.K+、Cl-、Na+、SO 在酸性和碱性溶液中都能大量存在,D符合题意;
故选D。
5. 设N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A. NaO 与足量的HO反应,共生成0.2 mol O,转移电子数目为0.4N
2 2 2 2 A
B. 常温常压下,7.8 g过氧化钠中含有阴离子的数目为0.1N
A
C. 1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1N
A
D. 标准状况下,22.4 LCl 与足量的铁充分反应,转移的电子数为3N
2 A
【答案】D
【解析】
【分析】
【详解】A.在NaO 与足量的HO反应中,NaO 既是氧化剂又是还原剂,每生成0.2 mol O ,转移0.4
2 2 2 2 2 2
mol电子,则转移的电子数目为0.4N ,A正确;
A
B.NaO 的式量是78,7.8 g过氧化钠的物质的量是0.1 mol,在1个NaO 中含有2个Na+和1个 ,因
2 2 2 2
此在0.1 mol Na O 中含有阴离子的数目为0.1N ,B正确;
2 2 A
C.O、O 都是由O原子构成,1.6 g由O、O 组成的混合物中含有氧原子的物质的量是n(O)=
2 3 2 3
=0.1 mol,故其中含有的O原子数目为0.1N ,C正确;
A
D.标准状况下,22.4 LCl 的物质的量是1 mol,其与足量的铁充分反应,转移2 mol电子,则转移的电子
2
数为2N ,D错误;
A
故合理选项是D。
6. 根据元素周期表和元素周期律,判断下列叙述不正确的是
A. 气态氢化物的稳定性:HO>NH >SiH
2 3 4B. 氢元素与其他元素可形成共价化合物或离子化合物
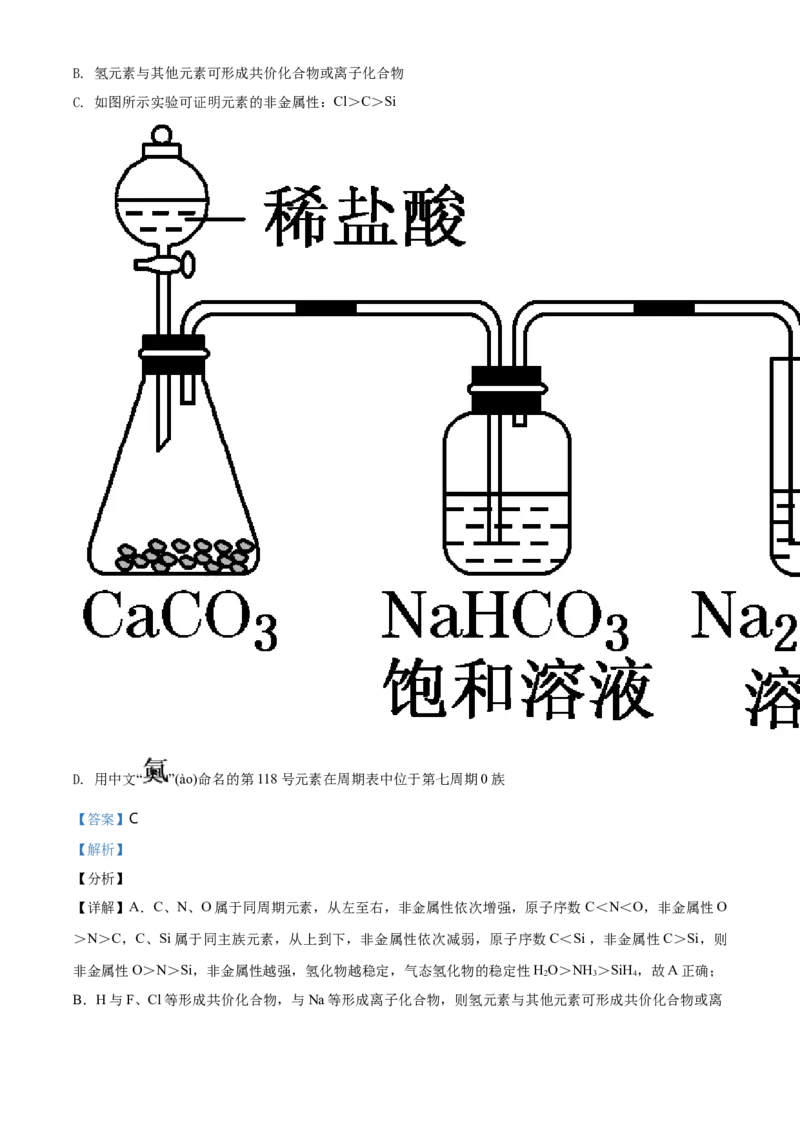
C. 如图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
【答案】C
【解析】
【分析】
【详解】A.C、N、O属于同周期元素,从左至右,非金属性依次增强,原子序数 C<N<O,非金属性O
>N>C,C、Si属于同主族元素,从上到下,非金属性依次减弱,原子序数C<Si ,非金属性C>Si,则
非金属性O>N>Si,非金属性越强,氢化物越稳定,气态氢化物的稳定性HO>NH >SiH,故A正确;
2 3 4
B.H与F、Cl等形成共价化合物,与Na等形成离子化合物,则氢元素与其他元素可形成共价化合物或离子化合物,故B正确;
C.利用最高价含氧酸的酸性比较非金属性强弱,HCl不是最高价含氧酸,则不能比较Cl、C的非金属性,
故C错误;
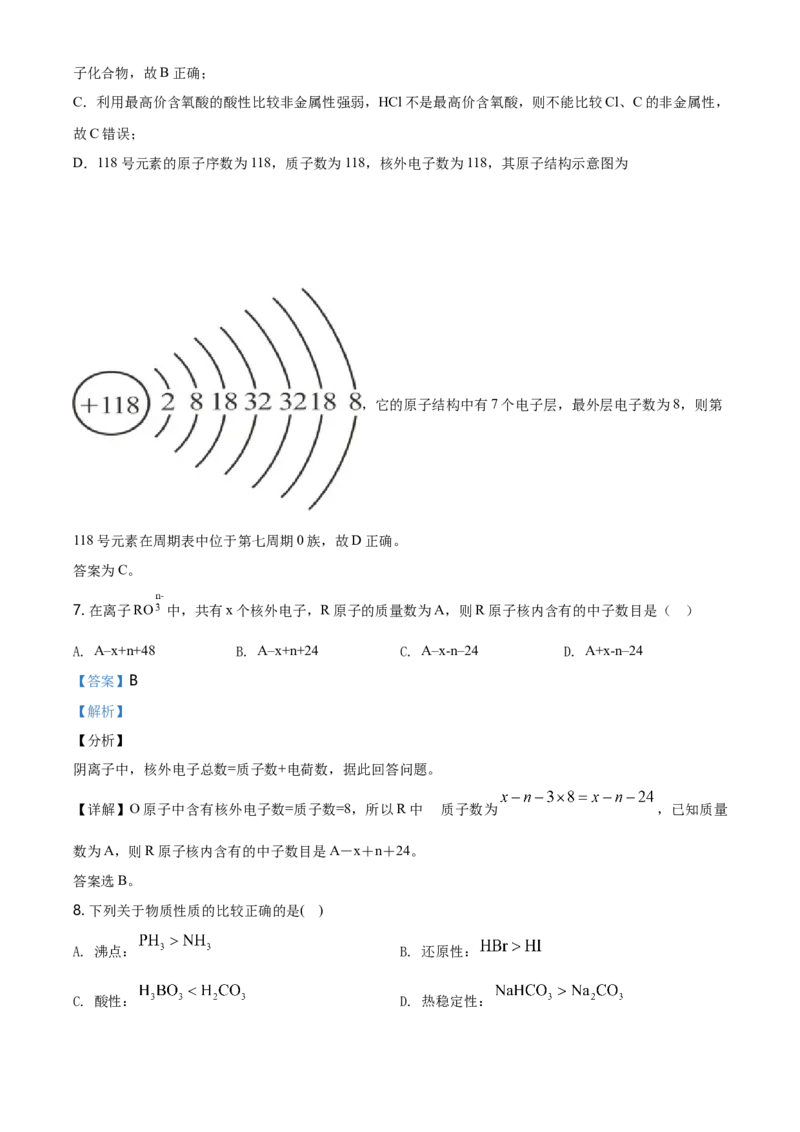
D.118号元素的原子序数为118,质子数为118,核外电子数为118,其原子结构示意图为
,它的原子结构中有7个电子层,最外层电子数为8,则第
118号元素在周期表中位于第七周期0族,故D正确。
答案为C。
7. 在离子RO 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是( )
A. A–x+n+48 B. A–x+n+24 C. A–x-n–24 D. A+x-n–24
【答案】B
【解析】
【分析】
阴离子中,核外电子总数=质子数+电荷数,据此回答问题。
【详解】O原子中含有核外电子数=质子数=8,所以R中 的质子数为 ,已知质量
数为A,则R原子核内含有的中子数目是A-x+n+24。
答案选B。
8. 下列关于物质性质的比较正确的是( )
A. 沸点: B. 还原性:
C. 酸性: D. 热稳定性:【答案】C
【解析】
【分析】
【详解】A.NH 分子间存在氢键,PH 分子间没有氢键,故沸点:NH >PH ,A错误;
3 3 3 3
B.通过反应Br +2HI=I +2HBr可知,还原性:HI>HBr,B错误;
2 2
C.非金属性:B<C,则它们最高价氧化物对应的水化物的酸性:HBO<HCO,C正确;
3 3 2 3
D.NaHCO 受热易分解,NaCO 的热稳定性良好,故热稳定性:NaCO>NaHCO ,D错误;
3 2 3 2 3 3
故选C。
9. 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲
教授曾主持测定了铟( In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷( Rb)同周
49 37
期。下列说法不正确的是
A. In是第五周期第ⅢA族元素
B. 115 In的中子数与电子数的差值为17
49
C. 原子半径:In>Al
D. 碱性:In(OH) >RbOH
3
【答案】D
【解析】
【分析】
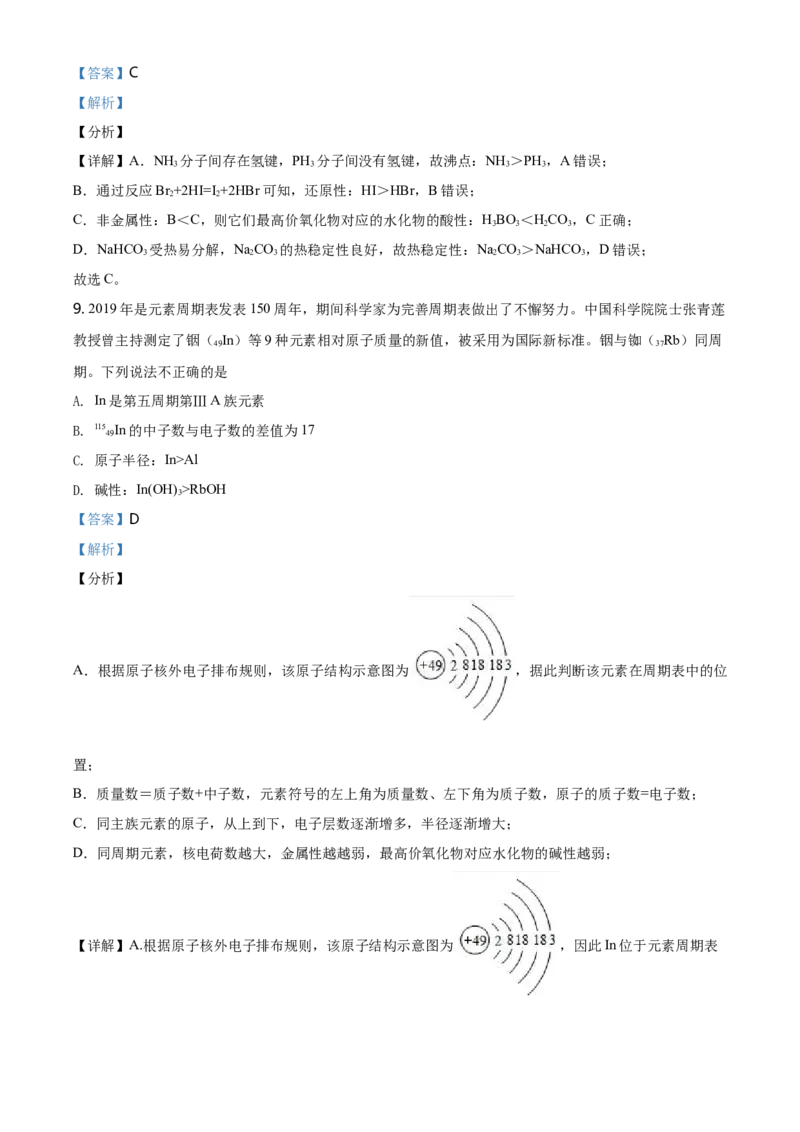
A.根据原子核外电子排布规则,该原子结构示意图为 ,据此判断该元素在周期表中的位
置;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数,原子的质子数=电子数;
C.同主族元素的原子,从上到下,电子层数逐渐增多,半径逐渐增大;
D.同周期元素,核电荷数越大,金属性越越弱,最高价氧化物对应水化物的碱性越弱;
【详解】A.根据原子核外电子排布规则,该原子结构示意图为 ,因此In位于元素周期表第五周期第IIIA族,故A不符合题意;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数,因此该原子的质子数=电子数
=49,中子数为115-49=66,所以中子数与电子数之差为66-49=17,故B不符合题意;
C.Al位于元素周期表的三周期IIIA族,In位于元素周期表第五周期IIIA族,同主族元素的原子,从上到下,
电子层数逐渐增多,半径逐渐增大,因此原子半径In>Al,故C不符合题意;
D.In位于元素周期表第五周期,铷(Rb)位于元素周期表第五周期第IA族,同周期元素,核电荷数越大,
金属性越越弱,最高价氧化物对应水化物的碱性越弱,因此碱性:In(OH) <RbOH,故D符合题意;
3
综上所述,本题应选D。
【点睛】本题考查原子结构与元素性质,题目难度不大,明确原子结构与元素周期律的关系为解答关键,
注意掌握原子构成及表示方法,试题培养了学生的分析能力及灵活应用能力。
10. 具有相同质子数和相同核外电子数的两种微粒,它们不可能是( )
A. 两种不同的离子 B. 两种不同的分子
C. 一种分子和一种离子 D. 一种分子和一种原子
【答案】C
【解析】
【分析】
【详解】A.具有相同质子数和相同核外电子数的两种微粒,可以是两种不同的离子,如 Na+与 质子
数是11,电子数是10个,A不符合题意;
B.具有相同质子数和相同核外电子数的两种微粒可以是两种不同的分子,如HO、HF的质子数和电子数
2
都是10个,B不符合题意;
C.分子是中性微粒,核外电子数与核内质子数相等,而离子是带有电荷的原子或原子团,核外电子数与
核内质子数不相等。若离子与分子的质子数相等,则核外电子数一定不相等,因此具有相同质子数和相同
核外电子数的两种微粒不可能一种分子和一种离子,C符合题意;
D.具有相同质子数和相同核外电子数的两种微粒,它们一种分子和一种原子,如HF与Ne的质子数与电
子数都是10个,D不符合题意;
故合理选项是C。
11. 反应①②分别是从海藻灰和某种矿石中提取碘的主要反应:①
;② 。下列说法正确的
是( )
A. 两个反应中硫元素均被氧化B. 碘元素在反应①中被还原,在反应②中被氧化
C. 氧化性:
D. 反应①②中生成等量的 时,转移电子数之比为1:5
【答案】D
【解析】
【分析】
【详解】A.反应①中硫元素化合价未发生变化,反应②中硫元素化合价升高,被氧化,故A项错误;
B.反应①中碘元素化合价升高,被氧化,反应②中碘元素化合价降低,被还原,故B项错误;
C.由反应①可知氧化性: ,由反应②可知氧化性: ,故C项错误;
D.由反应①得,生成1mol 转移2 mol ,由反应②得,生成1mol 转移10 mol ,所以当生成等量
的 时,转移电子数之比为1:5,故D项正确。
故选D。
12. 配制一定物质的量浓度的 溶液,产生误差会偏低的是( )
A. 配制 的 溶液,用托盘天平称取固体
B. 将称量好的 固体溶解后,未经冷却直接转移到容量瓶
C. 容量瓶中有少量蒸馏水
D. 定容时俯视刻度线
【答案】A
【解析】
【分析】
【详解】A.配制 的 溶液,需用500mL的容量瓶,用托盘天平称取氢氧化钠固
体 ,若称取固体 ,浓度偏小,故选A;
B.将称量好的 固体溶解,未经冷却直接转移到容量瓶,溶液体积偏小,浓度偏大,故不选B;
C.定容时,需要加入蒸馏水,容量瓶中有少量蒸馏水,对溶液浓度无影响,故不选C;
D.若俯视刻度线,溶液体积偏小,浓度偏大,故不选D;选A 。
13. 下列说法正确的是( )
A. FeCl 不能通过单质之间的化合反应制得
2
B. Fe(OH) 只能由可溶性铁盐和碱通过复分解反应制得,不能通过化合反应制得
3
C. 向溶液中加入NaOH溶液,生成红褐色沉淀,则溶液中一定含有Fe3+,一定不存在Fe2+
D. 除去FeCl 溶液中少量的CuCl 杂质,可向溶液中加入过量铁粉,然后过滤
3 2
【答案】A
【解析】
【分析】
【详解】A.Fe与Cl 反应产生FeCl ,不能制取得到FeCl ,A正确;
2 3 2
B.Fe(OH) 、O、HO反应产生Fe(OH) ,反应方程式为:4Fe(OH) +O +2H O=4Fe(OH) ,该反应属于化合
2 2 2 3 2 2 2 3
反应,B错误;
C.向溶液中加入NaOH溶液,生成红褐色沉淀,则溶液中一定含有Fe3+,可能存在Fe2+,C错误;
D.Fe与FeCl 、CuCl 都会发生反应,因此不能达到除杂、净化的目的,D错误;
3 2
故合理选项是A。
14. 向四支试管中分别加入少量不同的无色溶液进行如下操作,其中结论正确的是( )
选项 操作 现象 结论
A 滴加BaCl 溶液 生成白色沉淀 原溶液中有
2
B 滴加氯水和淀粉溶液 溶液显蓝色 原溶液中有I-
C 用洁净的铂丝蘸取溶液进行焰色试验 火焰呈黄色 原溶液中有Na+、无K+
D 滴加适量稀盐酸,再滴加AgNO 溶液 产生白色沉淀 原溶液中有Cl-
3
A. A B. B C. C D. D
【答案】B
【解析】
【分析】
【详解】A.滴加BaCl 溶液生成白色沉淀,该沉淀可能是BaCO 、AgCl,也可能是BaSO 沉淀,因此不
2 3 4
能确定原溶液中是否含有 ,A错误;
B.滴加氯水和淀粉溶液,溶液显蓝色,证明反应产生了I,I 遇淀粉溶液变为蓝色,可说明原溶液中有
2 2I-,B正确;
C.用洁净的铂丝蘸取溶液进行焰色试验,火焰呈黄色,原溶液中一定有Na+,可能含有K+,C错误;
D.滴加适量稀盐酸时引入了Cl-,再滴加AgNO 溶液,产生白色沉淀,该沉淀为AgCl,不能确定原溶液
3
中是否含有Cl-,D错误;
故合理选项是B。
15. 如图是硫酸试剂瓶标签上的部分内容。据此下列说法中正确的是( )
硫酸 化学纯(CP)(500 mL)
品名:硫酸 化学式:HSO
2 4
相对分子质量:98
密度:1.84 g/cm3
质量分数:98%
A. 该硫酸的溶剂和溶质的物质的量之比为9:1
B. 该硫酸的物质的量浓度为9.2 mol/L
C. 配制480 mL0.3 mol/L的稀硫酸需取该硫酸8.2 mL
D. 若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗
【答案】C
【解析】
【分析】
【详解】A.质量分数是98%的硫酸表示100 g溶液中含有溶质HSO 的质量是98 g,溶剂HO是2 g,则
2 4 2
该硫酸的溶剂和溶质的物质的量之比为 : =1:9,A错误;
B.该硫酸的物质的量浓度c= mol/L=18.4 mol/L,B错误;
C.在实验室没有规格是480 mL的容量瓶,根据选择仪器的标准是大而近,应该配制500 mL的该溶液,
由于溶液在稀释前后溶质的物质的量不变,则需量取该硫酸的体积V= =8.2 mL,C正确;
D.若不小心将该硫酸溅到皮肤上,应立即用干抹布擦拭,然后用大量水冲洗,最后涂抹稀NaHCO 溶液,
3
D错误;
故合理选项是C。Ⅱ卷
二、非选择题
16. 按要求写出下列方程式。
(1)过量碳酸氢钠溶液与石灰水反应的离子方程式:_______。
(2)氢氧化铁胶体制备的离子方程式:_______。
(3)氯化铁溶液与硫氰化钾反应的离子方程式:_______。
(4)铝与氢氧化钠溶液反应离子方程式:_______。
(5)硫酸亚铁与酸性高锰酸钾溶液的离子方程式:_______。
(6)足量 的氯气与溴化亚铁溶液反应的离子方程式:_______。
(7)氯酸钾与浓盐酸混合可生成氯气、氯化钾和水,写出化学方程式:_______。其中,氧化产物和还原产
物的质量之比为_______。
【答案】 (1). Ca2++2OH-+2 =CaCO ↓+ +2H O (2). Fe3++3H O Fe(OH) (胶体)+3H+ (3).
3 2 2 3
Fe3++3SCN-=Fe(SCN) (4). 2Al+2OH-+2H O=2 +3H ↑ (5). 5Fe2++8H++ =5Fe3++Mn2++4H O
3 2 2 2
(6). 2Fe2++4Br-+3Cl=2Fe3++2Br +6Cl- (7). KClO+6HCl(浓)=KCl+3Cl ↑+3H O (8). 5:1
2 2 3 2 2
【解析】
【分析】
【详解】(1)过量碳酸氢钠溶液与石灰水反应,要以不足量的 Ca(OH) 为标准书写反应方程式,假设
2
Ca(OH) 的物质的量是1 mol,反应消耗2 mol NaHCO,反应产生CaCO 沉淀、NaCO、HO,反应的离子
2 3 3 2 3 2
方程式为:Ca2++2OH-+2 =CaCO ↓+ +2H O;
3 2
(2)将几滴饱和FeCl 溶液滴入沸水中继续加热至液体呈红褐色,停止加热,就制取得到氢氧化铁胶体制备,
3
反应的离子方程式为:Fe3++3H O Fe(OH) (胶体)+3H+;
2 3
(3)氯化铁溶液与硫氰化钾反应产生Fe(SCN) 和KCl,反应的离子方程式:Fe3++3SCN-=Fe(SCN) ;
3 3
(4)铝与氢氧化钠溶液反应产生NaAlO 和H,反应的离子方程式为:2Al+2OH-+2H O=2 +3H ↑;
2 2 2 2
(5)硫酸亚铁与酸性高锰酸钾溶液反应,产生Fe (SO )、KSO 、MnSO 、HO,反应的离子方程式为:
2 4 3 2 4 4 2
5Fe2++8H++ =5Fe3++Mn2++4H O;
2(6)足量的氯气与溴化亚铁溶液反应产生FeCl 、Br ,反应的离子方程式为:2Fe2++4Br-+3Cl=2Fe3+
3 2 2
+2Br +6Cl-;
2
(7)氯酸钾与浓盐酸混合可生成氯气、氯化钾和水,该反应的化学方程式为:
KClO+6HCl(浓)=KCl+3Cl ↑+3H O,在该反应中KClO 是氧化剂,HCl为还原剂,反应产生的Cl 既是氧化
3 2 2 3 2
产物,又是还原产物。在反应产生的3个Cl 的6个Cl原子中,有5个是HCl氧化产生,1个是KClO 还原
2 3
产生,故氧化产物和还原产物的质量之比为5:1。
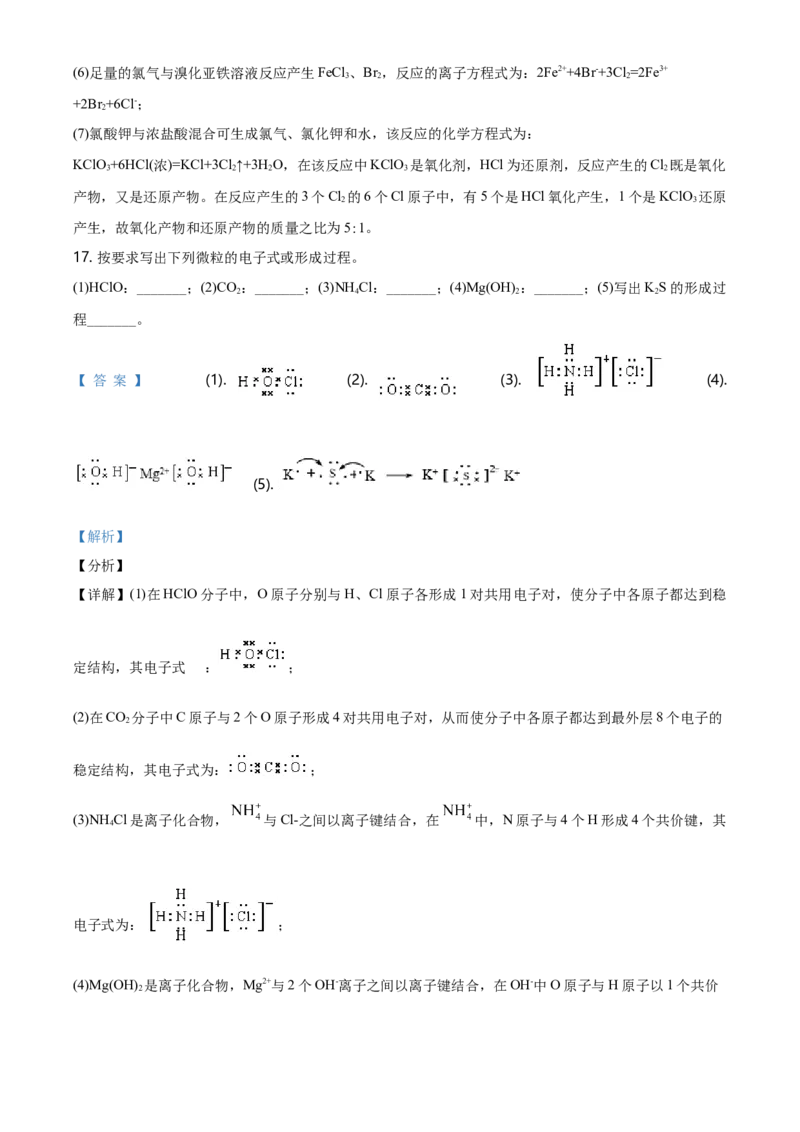
17. 按要求写出下列微粒的电子式或形成过程。
(1)HClO:_______;(2)CO :_______;(3)NH Cl:_______;(4)Mg(OH) :_______;(5)写出KS的形成过
2 4 2 2
程_______。
【 答 案 】 (1). (2). (3). (4).
(5).
【解析】
【分析】
【详解】(1)在HClO分子中,O原子分别与H、Cl原子各形成1对共用电子对,使分子中各原子都达到稳
定结构,其电子式 为: ;
(2)在CO 分子中C原子与2个O原子形成4对共用电子对,从而使分子中各原子都达到最外层8个电子的
2
稳定结构,其电子式为: ;
(3)NH Cl是离子化合物, 与Cl-之间以离子键结合,在 中,N原子与4个H形成4个共价键,其
4
电子式为: ;
(4)Mg(OH) 是离子化合物,Mg2+与2个OH-离子之间以离子键结合,在OH-中O原子与H原子以1个共价
2键结合,其电子式为: ;
(5)在K原子最外层只有1个电子容易失去形成K+,而S原子最外层有6个电子,容易得到2个电子形成
S2-,2个K+与S2-之间以离子键结合形成KS,其形成过程用电子式表示为:
2
。
18. (1)在一定条件下,将NH HCO 受热分解生成NH 、CO、HO(g),得到的混合气体的平均摩尔质量为
4 3 3 2 2
_______g/mol(保留小数点后一位)。
(2)在10.0 mL0.1 mol/LNa CO 溶液中逐滴加入0.1 mol/L的稀盐酸,边加边振荡,若使反应不产生CO 气体,
2 3 2
加入的稀盐酸的体积最多不超过_______mL。
(3)将不纯的NaOH样品1 g (样品含少量NaCO 和水),放入50 mL 2 mol/L的盐酸中,充分反应后,溶液呈
2 3
酸性,中和多余的酸又用去40 mL1 mol/L的NaOH溶液,蒸发中和后的溶液,最终得到_______ 的固体。
【答案】 (1). 26.3 (2). 10 (3). 5.85
【解析】
【分析】
【详解】(1)在一定条件下,将NH HCO 加热分解生成NH 、CO 、HO(g),反应方程式为:NH HCO
4 3 3 2 2 4 3
NH ↑+CO ↑+H O(g),可见1 mol NH HCO 受热分解得到3 mol气体,由于反应前后气体质量不变,则得到
3 2 2 4 3
的混合气体的平均摩尔质量M= =26.3 g/mol;
(2)Na CO 与盐酸在溶液中反应分步进行,首先发生反应:NaCO+HCl=NaCl+NaHCO ,然后发生反应:
2 3 2 3 3
NaHCO +HCl=NaCl+CO ↑+H O。若不产生气体,则只发生第一步反应,加入盐酸中HCl的物质的量最大
3 2 2
值与NaCO 的物质的量相等,n(HCl)=n(Na CO)=0.1 mol/L×0.01 L=0.001 mol,故需要0.1 mol/L的盐酸体
2 3 2 3
积V(HCl)= L=10 mL;
(3)根据元素守恒可知最后得到NaCl 的物质的量与盐酸中HCl的物质的量相等,n(NaCl)=n(HCl)=2
mol/L×0.05 L=0.1 mol,则NaCl的质量m(NaCl)=0.1 mol×58.5 g/mol=5.85 g。
19. X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为
0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)Y在周期表中的位置为_______。(2)Z、Q、R的简单离子半径由小到大的顺序为_______(用化学用语表示,下同);写出Q、R最高价氧化物
的水化物相互反应的离子方程式:_______;Q、R简单离子中氧化性比较小的是_______。
(3)上述五种元素的某些元素可形成既含离子键又含非极性共价键的化合物,写出其中一种化合物的电子式:
_______。
(4)Z、X两元素按原子数目比1:1和1:2构成分子A和B,A的结构式为_______,B是_______(填“极性
分子”或“非极性分子”)。
(5)QX的电子式为_______。
(6)下列事实能说明 元素的非金属性比S元素的非金属性强的是_______;
a.Z单质与HS溶液反应,溶液变浑浊
2
b.在氧化还原反应中,1 mol Z单质比1 mol S得电子多
c.Z和S两元素的简单氢化物受热分解,前者的分解温度高
(7)制备单质R时,电解熔点很高的R的氧化物而不电解熔点相对低的R的氯化物的原因是_______。
【答案】 (1). 第二周期ⅣA族 (2). r(Al3+)<r(Na+)<r(O2-) (3). Al(OH) +OH-= +2H O (4).
3 2
Na+ (5). (6). H-O-O-H (7). 极性分子 (8). (9). ac (10). 氯化铝
为共价化合物,熔融状态下不导电
【解析】
【分析】
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0,
则X是H元素,Y是C元素;Q与X同主族,则Q是Na元素;Z、R分别是地壳中含量最高的非金属元
素和金属元素,则Z是O元素,R是Al元素,然后根据元素周期律及物质的性质分析解答。
【详解】根据上述分析可知:X是H,Y是C,Z是O,Q是Na,R是Al元素。
(1)Y是C元素,原子核外电子排布是2、4,根据元素的原子结构与其在周期表的位置关系可知,C元素位
于元素周期表第二周期第IVA族;
(2)对于电子层结构相同的离子来说,核电荷数越大离子半径越小。Z是O,Q是Na,R是Al,它们形成的
简单离子核外电子排布是2、8,具有相同的电子层结构,则它们形成的简单离子半径由小到大的顺序为:
r(Al3+)<r(Na+)<r(O2-);
Q、R最高价氧化物的水化物分别是NaOH、Al(OH) ,Al(OH) 是两性氢氧化物,能够与强碱NaOH反应产
3 3
生可溶性NaAlO 、HO,相互反应的离子方程式为:Al(OH) +OH-= +2H O;对于电子层结构相同的
2 2 3 2离子来说,离子半径越小,离子电荷数越多,则离子的氧化性就越强,所以Na+、Al3+中氧化性比较小的是
Na+;
(3)在上述五种元素的某些元素中,可形成既含离子键又含非极性共价键的化合物,该化合物可以是
NaO,其电子式为: ;
2 2
(4)X是H,Z是O,二者形成的原子个数比为1:1、1:2的化合物A、B分别是HO、HO,其中A结构
2 2 2
式是H-O-O-H,B分子式是HO,分子中含有2个H-O极性共价键,由于空间排列不对称,因此HO为极
2 2
性分子;
(5)X是H,Q是Na,二者形成的化合物NaH属于离子化合物,其电子式为: ;
(6)a.Z是O,O 与HS在溶液中发生置换反应产生HO和S单质,产生的S单质难溶于水,使溶液变浑
2 2 2
浊,二者能够发生置换反应,可以证明元素的非金属性:O>S,a正确;
b.不能根据在氧化还原反应中1 mol的单质得到电子的多少判断物质氧化性的强弱,b错误;
c.元素的非金属性越强,其相应的氢化物的稳定性就越强,越不容易分解,由HO比HS难分解,可以
2 2
说明元素的非金属性:O>S,c正确;
故合理选项是ac;
(7)Al元素在自然界中以化合物形式存在,制备单质Al通常是采用电解熔点高的Al O 的方法,这是由于
2 3
AlCl 为共价化合物,在液体时仍然是由分子构成,熔融状态下不导电。
3
20. 为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
4
Ⅰ. 甲方案
实验原理:CuSO +BaCl =BaSO ↓+CuCl
4 2 4 2
实验步骤:
(1)步骤③灼烧时盛装样品的仪器名称为_______。
(2)固体质量为w g,则c(CuSO )=_______mol/L。
4
(3)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO )_______(填“偏高”、“偏低”或“无影响”)。
4
Ⅱ. 乙方案
实验原理:Zn+ CuSO=ZnSO +Cu,Zn+CuSO =ZnSO +H ↑
4 4 4 4 2
实验步骤:
①按如图安装装置(夹持仪器略去);②……
③在仪器A、B、C、D、E中加入图示的试剂;
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录;
⑤将CuSO 溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
4
⑥待体系恢复到室温,__________,读数并记录;
⑦处理数据。
(4)步骤②为_______。
(5)Zn粉质量为a g,若测得H 体积为b mL,已知实验条件下 ,则
2
c(CuSO )=_______mol/L(列出计算表达式)。
4
(6)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO )_______(填“偏高”、“偏低”或“无影响”)。
4
(7)补全步骤⑥的空白处:_______。
(8)是否能用同样的装置和方法测定MgSO 溶液的浓度:_______(填“是”或“否”)。
4
【答案】 (1). 坩埚 (2). (3). 偏低 (4). 检查装置气密性 (5). (6).
偏高 (7). 移动E管,保持D、E中两液面相平 (8). 否
【解析】
【分析】
甲方案:利用CuSO 与BaCl 反应生成BaSO ,称重BaSO ,来求出CuSO 的质量;乙方案:一定量的Zn
4 2 4 4 4
与CuSO 反应后,剩余的Zn粉再与硫酸反应生成氢气,测定生成氢气的体积,再结合 Zn的质量计算硫酸
4
铜的量,进而计算其浓度。
【详解】(1)步骤③灼烧时盛装样品的仪器名称为坩埚;(2)根据S元素守恒可得:n(CuSO )=n(BaSO)= mol,则c(CuSO )= mol/L;
4 4 4
(3)步骤①从烧杯中转移沉淀时未洗涤烧杯,有沉淀附着在烧杯内壁,造成生成的n(BaSO)减小,则
4
n(CuSO )减小,则测得c(CuSO )偏低;
4 4
(4)实验需要测定氢气的体积,组装仪器后需要检验装置气密性,步骤②为:检验装置气密性;
(5)由方程式:Zn+CuSO =ZnSO +Cu,Zn+H SO =ZnSO +H ↑,可知n(Zn)=n(CuSO )+n(H ),故
4 4 2 4 4 2 4 2
n(CuSO )=n(Zn)-n(H ),m(H )=b×10-3 L×d g/L=bd×10-3 g,则n(H )= =5bd×10-4 mol,n(Zn)=
4 2 2 2
mol,故n(CuSO )=n(Zn)-n(H )= ,则c(CuSO )=
4 2 4
mol/L;
(6)若步骤⑥E管液面高于D管,未调液面即读数,气体体积被压缩,测得H 体积偏小,结合c(CuSO ) =
2 4
可知:硫酸铜的浓度偏高;
(7)为保持气体的压强与外界大气压强相同,则待体系恢复到室温,需要移动E管,保持D、E中两液面相
平,读数并记录故步骤⑥的空白处应该是移动E管,保持D、E中两液面相平;
(8)Mg比Zn活泼,在MgSO 溶液中加入Zn无Mg析出,因此无法用同样的装置和方法测定MgSO 溶液的
4 4
浓度。