文档内容
萍乡实验学校2025届高三月考试卷(四)
大联考
暨长郡十八校联考考前演练
化 学
命题人:汤德清 审题人:黄柳
注意事项:
1.答卷前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2 . 回答选择题,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号 。回答非选择题,将答案写在答题卡上。试卷上无效。
3. 考试结束后,将本试卷和答题卡一并交回。
第 卷选择题 (共 42分)
Ⅰ
一、选择题(本大题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1
.下列选项中,未涉及到化学反应的是
A B C D
.冰雪融化 .湿法炼铜 .铝热反应 .酒精燃烧
2
.下列有关物质用途的说法错误的是
A SO B Al(OH)
. 2用于熏蒸粉丝 . 3用作制胃酸的中和剂
C AgI D Fe O
. 用于人工降雨 . 2 3用于制造红色油漆和涂料
3 萍乡市新开的“玉湖美食节”是萍城市民们闲暇时间品味美食与人间烟火气的理想打卡地。人间烟火气,最抚凡人心。
.
在一个个摊位的美食交织下点亮了萍乡夜市经济发展。下列有关玉湖美食城常见的几款美食说法正确的是
A 塔斯汀的炸鸡薯条类食品用的植物油主要成分是天然有机高分子
.
B 萍乡炒粉所用的米粉的主要成分(淀粉)的分子式为 C H O
. 6 10 5 n
C 可瑞朵烘焙的蛋糕甜品中含有的蔗糖是还原糖
.
D 腊肉熏制过程中腊肉中的蛋白质发生了盐析
.
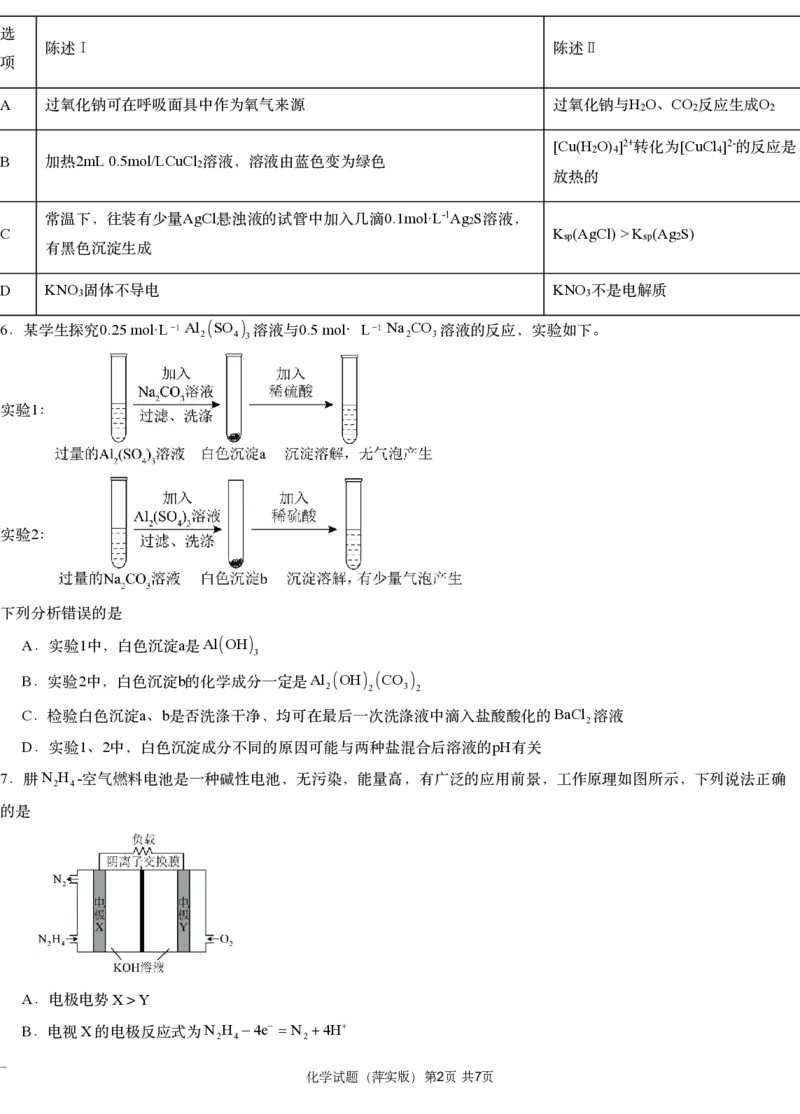
4 2L 2mol X 1mol Y 2X(g)+Y(g)3Z(g) ΔH<0
.在 恒容密闭容器中充入 和 发生反应: ,反应过程持续升高温度,测得混
X
合体系中 的体积分数与温度的关系如图所示,下列推断正确的是
A
.升高温度,平衡常数增大
B W X M X
. 点 的正反应速率等于 点 的正反应速率
C Q Y
. 点时, 的转化率最大
D Z Z
.恒温下,平衡时充入 ,达到新平衡时 的体积分数比原平衡时大
5
.下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
思思想政治
化学试题(萍实版)第1页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}选
陈述Ⅰ 陈述Ⅱ
项
A 过氧化钠可在呼吸面具中作为氧气来源 过氧化钠与 H 2 O 、 CO 2反应生成 O 2
[Cu(H O) ]2+ [CuCl ]2-
2 4 转化为 4 的反应是
B 加热 2mL0.5mol/LCuCl 2溶液,溶液由蓝色变为绿色
放热的
AgCl 0.1mol·L-1Ag S
常温下,往装有少量 悬浊液的试管中加入几滴 2 溶液,
C K (AgCl)>K (Ag S)
sp sp 2
有黑色沉淀生成
D KNO 3固体不导电 KNO 3不是电解质
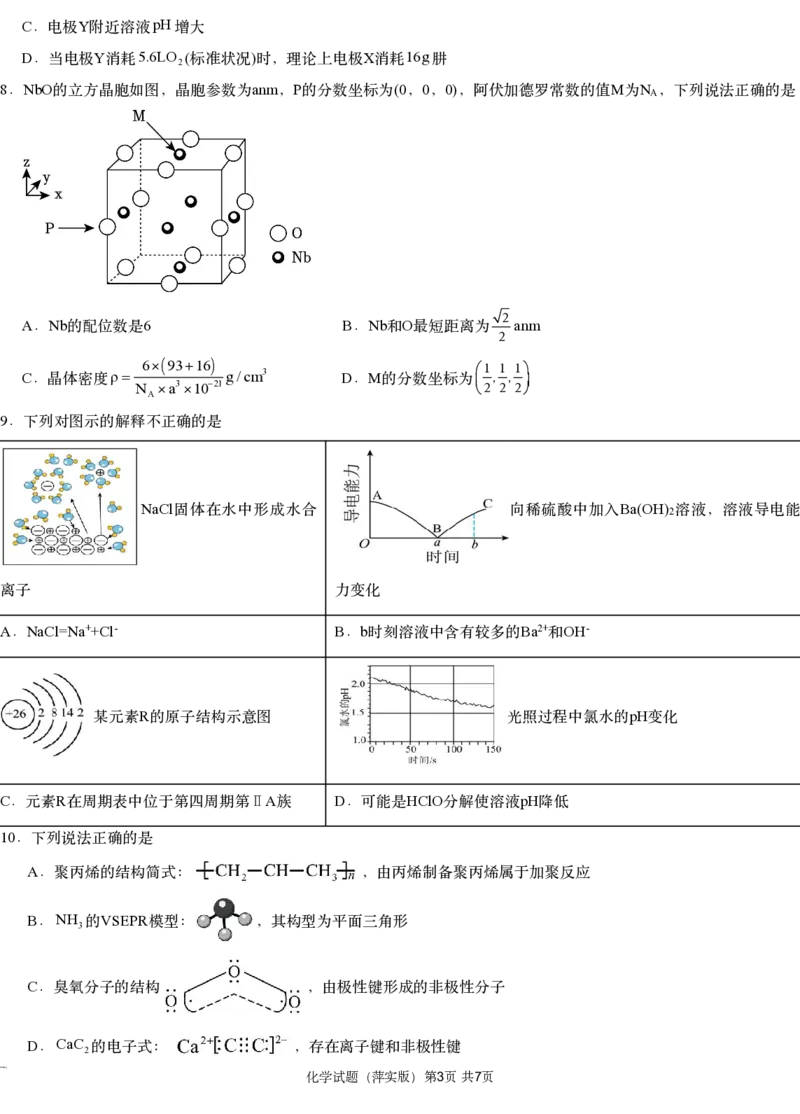
6 0.25mol·L1 Al SO 0.5mol L1 Na CO
.某学生探究 2 4 3溶液与 ⋅ 2 3溶液的反应,实验如下。
1
实验 :
2
实验 :
下列分析错误的是
A 1 a
AlOH
.实验 中,白色沉淀 是 3
B 2 b Al OH CO
.实验 中,白色沉淀 的化学成分一定是 2 2 3 2
C a b BaCl
.检验白色沉淀 、 是否洗涤干净,均可在最后一次洗涤液中滴入盐酸酸化的 2溶液
D 1 2 pH
.实验 、 中,白色沉淀成分不同的原因可能与两种盐混合后溶液的 有关
7 N H -
.肼 2 4 空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,工作原理如图所示,下列说法正确
的是
A XY
.电极电势
B X N H 4e N 4H
.电视 的电极反应式为 2 4 2
思思想政治
化学试题(萍实版)第2页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}C Y pH
.电极 附近溶液 增大
D Y 5.6LO ( ) X 16g
.当电极 消耗 2 标准状况 时,理论上电极 消耗 肼
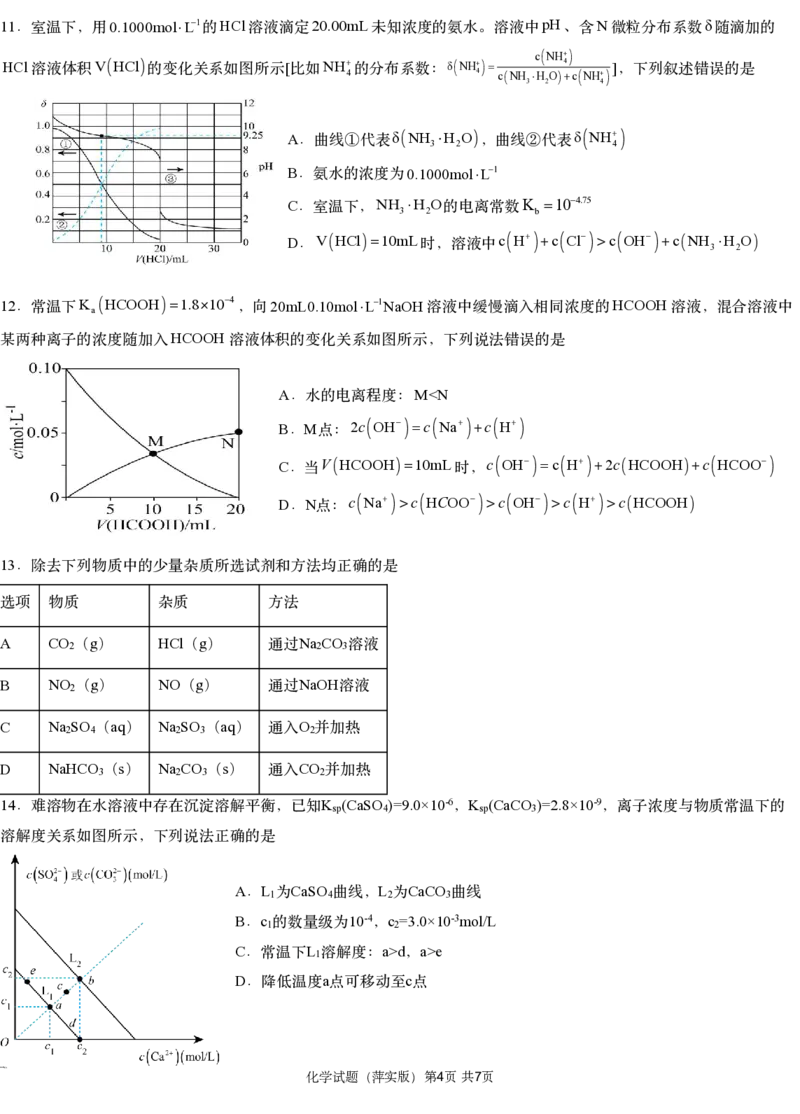
8 NbO anm P (0 0 0) M N
. 的立方晶胞如图,晶胞参数为 , 的分数坐标为 , , ,阿伏加德罗常数的值 为 A,下列说法正确的是
2
A Nb 6 B Nb O anm
. 的配位数是 . 和 最短距离为 2
69316
1 1 1
C ρ g/cm3 D M ,,
.晶体密度 N a31021 . 的分数坐标为2 2 2
A
9
.下列对图示的解释不正确的是
NaCl Ba(OH)
固体在水中形成水合 向稀硫酸中加入 2溶液,溶液导电能
离子 力变化
A NaCl=Na++Cl- B b Ba2+ OH-
. . 时刻溶液中含有较多的 和
R pH
某元素 的原子结构示意图 光照过程中氯水的 变化
C R A D HClO pH
.元素 在周期表中位于第四周期第Ⅱ 族 .可能是 分解使溶液 降低
10
.下列说法正确的是
A
.聚丙烯的结构简式: ,由丙烯制备聚丙烯属于加聚反应
B NH VSEPR
. 3的 模型: ,其构型为平面三角形
C
.臭氧分子的结构 ,由极性键形成的非极性分子
D CaC
. 2的电子式: ,存在离子键和非极性键
思思想政治
化学试题(萍实版)第3页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}11 0.1000molL1 HCl 20.00mL pH N δ
.室温下,用 的 溶液滴定 未知浓度的氨水。溶液中 、含 微粒分布系数 随滴加的
HCl VHCl [ NH δ NH c
NH 4
]
溶液体积 的变化关系如图所示 比如 4的分布系数: 4 cNH HOc NH ,下列叙述错误的是
3 2 4
A δNH H O δ NH
.曲线①代表 3 2 ,曲线②代表 4
B 0.1000molL1
.氨水的浓度为
C NH H O K 104.75
.室温下, 3 2 的电离常数 b
D VHCl10mL c H c Cl c OH cNH H O
. 时,溶液中 3 2
12 K HCOOH1.8104 20mL0.10molL1NaOH HCOOH
.常温下 a ,向 溶液中缓慢滴入相同浓度的 溶液,混合溶液中
HCOOH
某两种离子的浓度随加入 溶液体积的变化关系如图所示,下列说法错误的是
A Md a>e
.常温下 1溶解度: ,
D a c
.降低温度 点可移动至 点
思思想政治
化学试题(萍实版)第4页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}第 卷非选择题 (共 58分)
Ⅱ
二、非选择题(本大题共 4小题,共 58分)
15 14分 (MnCO ) (
.( )高纯碳酸锰 3 广泛应用于电子工业,是制造高性能磁性材料的主要原料。工业上以软锰矿 主要成分
MnO Fe O Al O SiO )
是 2、含有少量的 3 4、 2 3、 2 为主要原料制备高纯碳酸锰的工艺流程如图所示:
Ksp(MnCO )=2.2×10-11
已知:① 3 。
100
②碳酸锰难溶于水和乙醇,潮湿时易被空气氧化, ℃开始分解。
(1) ( ) MnO
为了加快浸取速率,可以采取的措施是 写两条即可 ,浸取过程中 2发生反应的离子方程式为 。
(2)
滤渣Ⅱ的主要成分是 。
(3) A NH HCO (NH ) CO
沉锰过程中, 溶液可以选用 4 3溶液或 4 2 3溶液。
NH HCO
①若是选用 4 3溶液,则反应的离子方程式为: 。
(NH ) CO 100mL c(Mn2+)=2.0mol/L (NH ) CO “
②若是选用 4 2 3溶液。取过滤Ⅱ的滤液 ,其中 ,加入等体积的 4 2 3溶液。如果使 沉
” c(Mn2+)=1.0×10-10mol/L c((NH ) CO )= mol/L
锰 后的溶液中 ,则加入的 4 2 3 。
(4)
为了得到高纯碳酸锰,在过滤Ⅲ操作后,最好选择用乙醇洗去表面的杂质。选择用乙醇洗涤的原因是 。
(5) MnCO ( ) B (
在空气中加热所得 3固体 不含其他杂质 ,随着温度的升高,残留固体的质量如图所示。则 点的成分为 填
)
化学式 。
16 14分 (DME)
.( )二氧化碳催化加氢制取二甲醚 有利于减少温室气体二氧化碳,制取过程发生如下反应:
CO g3H gCH OHgH OgΔH
反应Ⅰ. 2 2 3 2 1
2CH OHgCH OCH gH OgΔH 23.4kJmol1
反应Ⅱ. 3 3 3 2 2
CO gH gCOgH OgΔH 41.2kJmol1
反应Ⅲ. 2 2 2 3
回答下列问题:
(1)T 0.2molCO (g) 0.6molH (g) 4kJ
1℃时,向恒压容器中充入 2 和 2 ,若在该条件下只发生反应Ⅰ,达平衡时,放出 能量;
0.4molCH OH(g) 0.4molH O(g) 11.8kJ H= kJ/mol
若向相同容器中充入 3 和 2 ,吸收 能量,则反应Ⅰ的△ 1 。
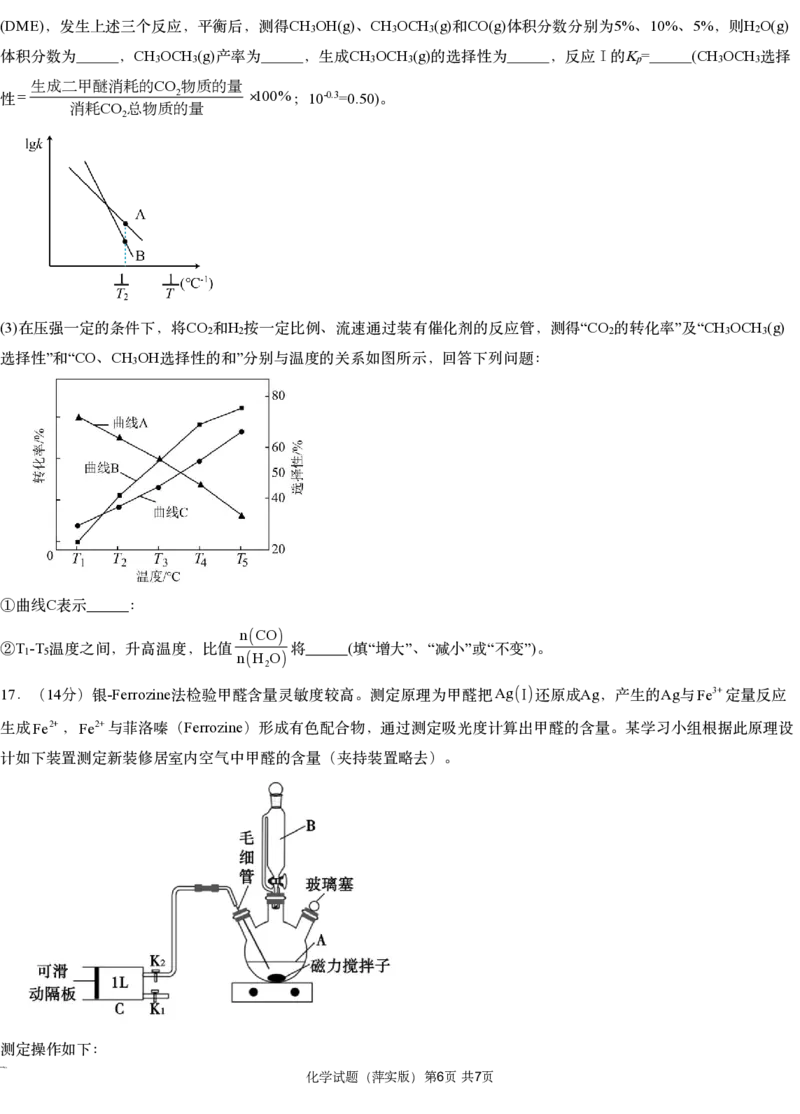
(2) v =k pCO pH v =k pCOpH O lgk T
已知反应Ⅲ的速率方程可表示为 正 正 2 2 , 逆 逆 2 , 与温度的关系如图所示, 2℃
A B a-0.7 a-1 T 200MPa CO (g) H (g)
下,图中 、 点的纵坐标分别为 、 。 2℃、 时,向恒压容器中充入 2 和 2 混合气体制取二甲醚
思思想政治
化学试题(萍实版)第5页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}(DME) CH OH(g) CH OCH (g) CO(g) 5% 10% 5% H O(g)
,发生上述三个反应,平衡后,测得 3 、 3 3 和 体积分数分别为 、 、 ,则 2
CH OCH (g) CH OCH (g) K= (CH OCH
体积分数为 , 3 3 产率为 ,生成 3 3 的选择性为 ,反应Ⅰ的 p 3 3选择
生成二甲醚消耗的CO 物质的量
2 100% 10-0.3=0.50)
性 消耗CO 总物质的量 ; 。
2
(3) CO H “CO ” “CH OCH (g)
在压强一定的条件下,将 2和 2按一定比例、流速通过装有催化剂的反应管,测得 2的转化率 及 3 3
” “CO CH OH ”
选择性 和 、 3 选择性的和 分别与温度的关系如图所示,回答下列问题:
C
①曲线 表示 :
nCO
T -T ( “ ” “ ” “ ”)
② 1 5温度之间,升高温度,比值nH O将 填 增大 、 减小 或 不变 。
2
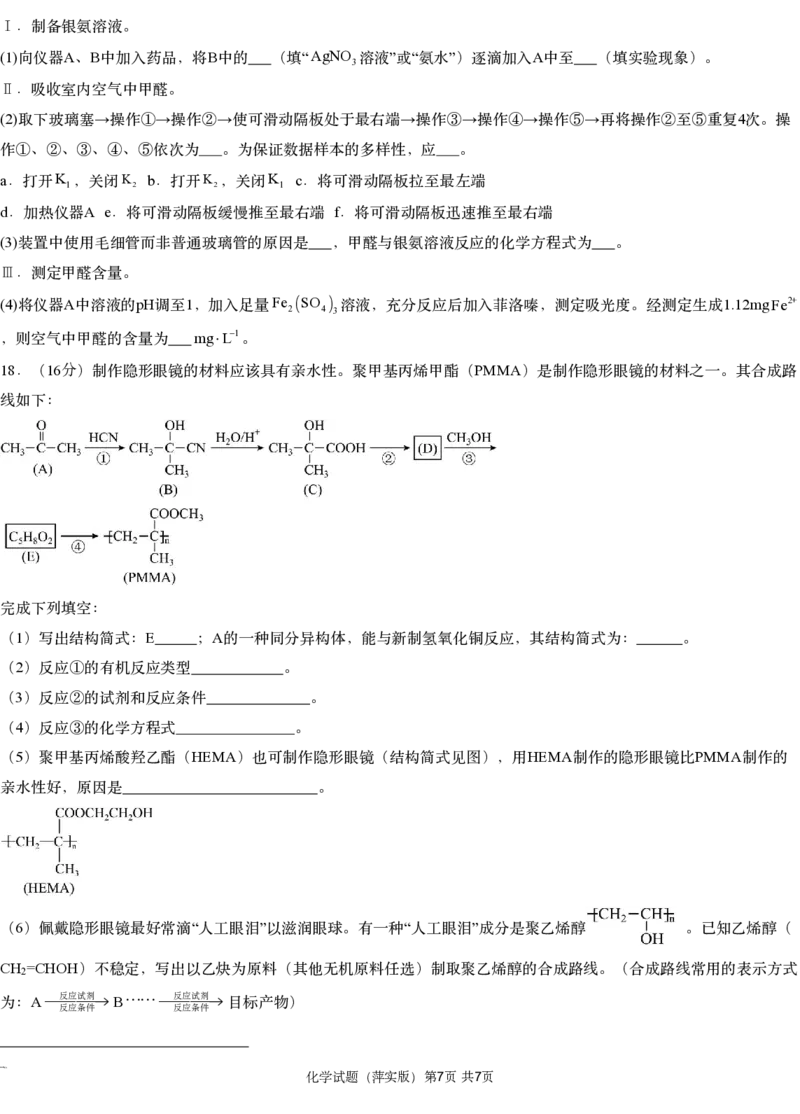
17 14分 -Ferrozine Ag Ⅰ Ag Ag Fe3+
.( )银 法检验甲醛含量灵敏度较高。测定原理为甲醛把 还原成 ,产生的 与 定量反应
Fe2+ Fe2+ Ferrozine
生成 , 与菲洛嗪( )形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组根据此原理设
计如下装置测定新装修居室内空气中甲醛的含量(夹持装置略去)。
测定操作如下:
思思想政治
化学试题(萍实版)第6页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}Ⅰ.制备银氨溶液。
(1) A B B “AgNO ” “ ” A
向仪器 、 中加入药品,将 中的 (填 3溶液 或 氨水 )逐滴加入 中至 (填实验现象)。
Ⅱ.吸收室内空气中甲醛。
(2) → → → → → → → 4
取下玻璃塞 操作① 操作② 使可滑动隔板处于最右端 操作③ 操作④ 操作⑤ 再将操作②至⑤重复 次。操
作①、②、③、④、⑤依次为 。为保证数据样本的多样性,应 。
a K K b K K c
.打开 1,关闭 2 .打开 2,关闭 1 .将可滑动隔板拉至最左端
d A e f
.加热仪器 .将可滑动隔板缓慢推至最右端 .将可滑动隔板迅速推至最右端
(3)
装置中使用毛细管而非普通玻璃管的原因是 ,甲醛与银氨溶液反应的化学方程式为 。
Ⅲ.测定甲醛含量。
(4) A pH 1 Fe SO 1.12mgFe2+
将仪器 中溶液的 调至 ,加入足量 2 4 3溶液,充分反应后加入菲洛嗪,测定吸光度。经测定生成
mgL1
,则空气中甲醛的含量为 。
18 16分 PMMA
.( )制作隐形眼镜的材料应该具有亲水性。聚甲基丙烯甲酯( )是制作隐形眼镜的材料之一。其合成路
线如下:
完成下列填空:
1 E A
( )写出结构简式: ; 的一种同分异构体,能与新制氢氧化铜反应,其结构简式为: 。
2
( )反应①的有机反应类型 。
3
( )反应②的试剂和反应条件 。
4
( )反应③的化学方程式 。
5 HEMA HEMA PMMA
( )聚甲基丙烯酸羟乙酯( )也可制作隐形眼镜(结构简式见图),用 制作的隐形眼镜比 制作的
亲水性好,原因是 。
6 “ ” “ ”
( )佩戴隐形眼镜最好常滴 人工眼泪 以滋润眼球。有一种 人工眼泪 成分是聚乙烯醇 。已知乙烯醇(
CH =CHOH
2 )不稳定,写出以乙炔为原料(其他无机原料任选)制取聚乙烯醇的合成路线。(合成路线常用的表示方式
A反应试剂B反应试剂
为: 反应条件 反应条件 目标产物)
思思想政治
化学试题(萍实版)第7页共7页
{#{QQABYYKAgggAQBIAAAgCAQVSCgMQkgECAagOwAAEIAAAyBFABCA=}#}