文档内容
名校联盟·2025 年上学期高二开学质量检测
化学
本试卷共 6 页。全卷满分 100 分,考试时间 75 分钟。
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在本试卷和答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应的答案标号涂黑,如有改动,用
橡皮擦干净后,再选涂其他答案;回答非选择题时,将答案写在答题卡上,写在本试卷上无
效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Fe 56 Ni 59
Cu 64
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学的实用性表现在它与人们的生产、生活紧密相连,在生活的各个方面体现出来。下列说法正确的是
A. 生活中常利用 与 两种溶液制作泡沫灭火剂
B. 生活中使用碳酸钠溶液处理锅炉水垢不能用勒夏特列原理解释原因
C. 工业上用石墨电极电解熔融 冶炼金属铝时,阳极因被氧气氧化须定期更换
D. 工业上用 处理含 、 的废水,是因为 具有强还原性
2. 下列化学用语或表述正确的是
A. 基态 的价层电子排布式:
B. 基态氮原子核外能量最高电子的电子云的形状:
C. 原子的结构示意图为
D. 镁原子最外层电子的电子云轮廓图为
3. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 25℃, 的 溶液中, 数目为
第 1页/共 11页B. 电解精炼铜时,若阳极质量减少 3.2g,转移的电子数目一定为
C. 的 溶液中 和 的离子数之和为
D. 和 在密闭容器中充分反应,生成 分子的数目为
4. 下列说法正确的是
A. 钠原子由 时,原子释放能量,由基态转化成激发态
B. 电子云轮廓图中稠密部分代表此处电子数多,电子出现的概率大
C. 在第三能层中自旋状态相同的电子最多有 10 个
D. 同一原子中, 、 、 能级的轨道数依次增多
5. 下列关于能层与能级的说法中,正确的是
A. 同一原子中,符号相同的能级,其上电子能量一定相同
B. 多电子原子中,每个能层上电子的能量一定不同
C. 同是 s 能级,在不同的能层中所能容纳的最多电子数是不相同的
D. 任一能层的能级总是从 s 能级开始,而且能级数一定等于该能层序数
6. 下列装置的有关说法正确的是
A. 装置Ⅰ中 电极的电极反应式:
B. 装置Ⅱ中将镁块换成锌块也能起到保护作用
C. 装置Ⅲ中可根据右面试管中现象验证铁的析氢腐蚀
D. 装置Ⅳ可用于蒸发 溶液制取 固体
7. 逆水煤气变换体系中存在以下两个反应:
反应Ⅰ: ;
反应Ⅱ: 。
在恒压条件下,按 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所
第 2页/共 11页示。下列说法错误的是
A. 反应Ⅰ的 ,反应Ⅱ的
B. 加入合适的催化剂可使 N 点移动到 P 点
C. 恒温恒压条件下,向体系中充入氩气, 的产率降低
D. M 点反应Ⅰ的平衡常数 等于 1
8. 制作紫砂壸所用的紫砂泥主要含有 、 、 和 ,还含有少量的 、 、 和 P 等元素。下
列说法正确的是
A. 若将基态 原子的核外电子排布式写为 ,则未违背能量最低原理
B. 若将基态 原子的核外电子排布图写为 ,则违反了泡利原理
C. 若将基态 原子的核外电子排布式写为 ,则违反了构造原理
D. 若将基态 O 原子的价层电子的轨道表示式写为 ,则违背了洪特规则
9. 如图所示的新型电池可以处理含 的碱性废水,同时还能淡化海水。下列说法正确的是
A. a 极电势高于 b 极电势
第 3页/共 11页B. 电池工作一段时间后,右室溶液的稀硫酸变为浓硫酸
C. 交换膜Ⅰ为阳离子交换膜,交换膜Ⅱ为阴离子交换膜
D. 若除去海水中 58.5g 的 ,可将含 5.2g 的碱性废水处理完全
10. 已知 A、B、G、D、E、L 是原子序数依次增大的前四周期元素。其中 A 是宇宙中含量最多的元素;基
态 B 原子核外有 7 种不同运动状态的电子;G 元素原子的价层电子排布式是 ;D 元素在短周期主族
元素中金属性最强;E 与 D 的最高能层数相同,但其最外层电子数等于其能层数。L 元素位于元素周期表
的第四周期第ⅠB 族。下列说法错误的是
A. 六种元素中有两种元素位于元素周期表的 p 区
B. A、B、G 三种元素的电负性:G>B>A
C. B、G、D 三种元素的第一电离能:B>G>D
D. 基态 L 原子的价层电子排布式:
11. 下列实验操作与现象及结论均正确的是
选
实验操作与现象 结
论 项
室温下,将一元酸 溶液和
A 一定为弱酸、 一定为强碱
溶液等体积混合(忽略体积变化),
反应后溶液显碱性
向 的 溶液中滴加酚酞溶液,溶液
变 B
为浅红色
用注射器吸入 20mL 和 的混合气体,将细管
减小压强时该平衡向着生成
的 C
端用橡胶塞封闭。迅速向外拉活塞,观察到气体颜色先
方向移动
变浅后变深(最终颜色比拉动活塞前要深)
向 2mL 溶液中加入 1mL
相同温度下,
D 溶液,产生白色沉淀;再加入 1mL
溶液,产生红褐色沉淀
第 4页/共 11页A. A B. B C. C D. D
12. 在石墨烯负载型 单原子催化剂( )上还原 生成 和 的路径机理及活化能
( )如图所示:
下列说法正确的是
A. 还原 生成 过程中,决速步 反应
B. 升温能加快反应速率,并提高 的平衡转化率
C. 上 还原 ,更容易生成
D. 由图示可知,所有化学反应都存在多个基元反应
13. 近日,某团队设计出了一种双极膜(将 H
2
O 解离成 H+ 和 OH-)电解合成 NH
3
反应器,简化模型如下图
所示。下列说法错误的是
A. a 极为阴极,与电源的负极相连
B. 通电时双极膜将水解离为 H+ 和 OH-,OH-向 b 极方向移动
C. 阳极的电极反应式为
第 5页/共 11页D. 若电路中转移 1.5mole-,理论上共产生标准状况下 8.4L 气体(不考虑气体的溶解)
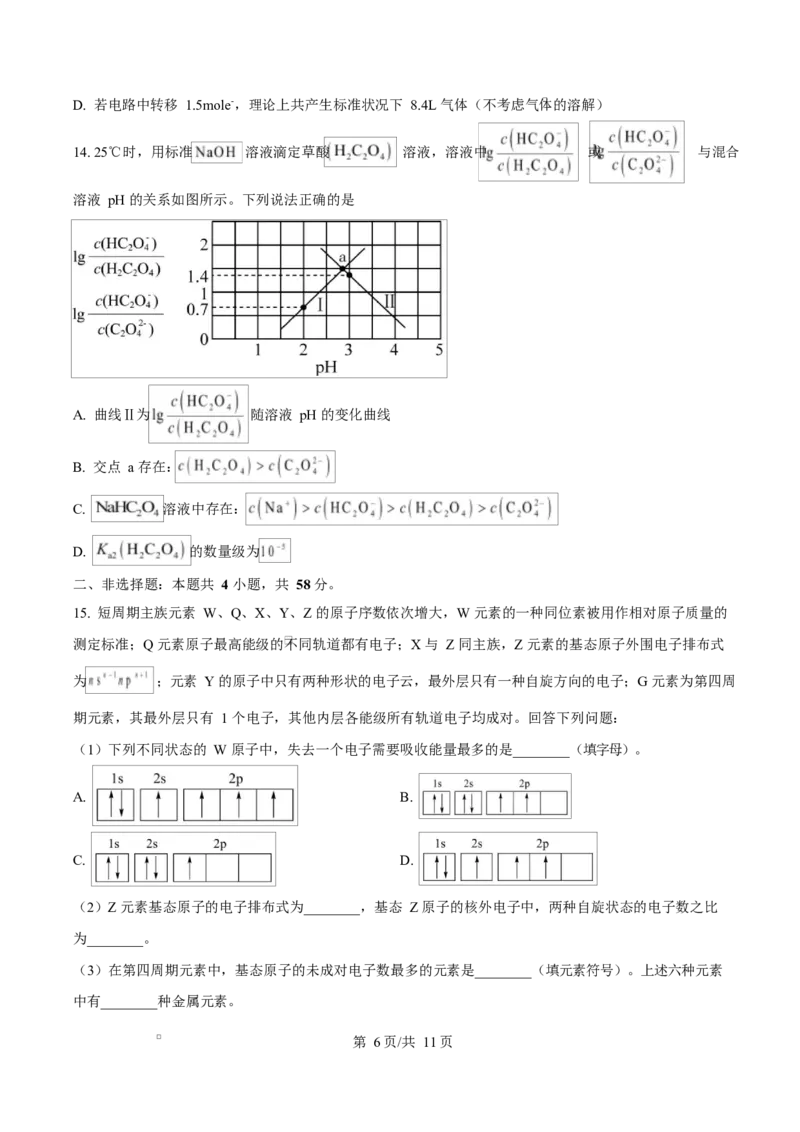
14. 25℃时,用标准 溶液滴定草酸 溶液,溶液中 或 与混合
溶液 pH 的关系如图所示。下列说法正确的是
A. 曲线Ⅱ为 随溶液 pH 的变化曲线
B. 交点 a 存在:
C. 溶液中存在:
D. 的数量级为
二、非选择题:本题共 4 小题,共 58 分。
15. 短周期主族元素 W、Q、X、Y、Z 的原子序数依次增大,W 元素的一种同位素被用作相对原子质量的
测定标准;Q 元素原子最高能级的不同轨道都有电子;X 与 Z 同主族,Z 元素的基态原子外围电子排布式
为 ;元素 Y 的原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;G 元素为第四周
期元素,其最外层只有 1 个电子,其他内层各能级所有轨道电子均成对。回答下列问题:
(1)下列不同状态的 W 原子中,失去一个电子需要吸收能量最多的是________(填字母)。
A. B.
C. D.
(2)Z 元素基态原子的电子排布式为________,基态 Z 原子的核外电子中,两种自旋状态的电子数之比
为________。
(3)在第四周期元素中,基态原子的未成对电子数最多的元素是________(填元素符号)。上述六种元素
中有________种金属元素。
第 6页/共 11页(4)元素 W、Q、X 的第二电离能最大的是________(填元素符号),判断的依据是________。
(5)G 元素的元素符号为________;含有 Y 元素的盐的焰色试验为黄色,许多金属盐都可以发生焰色试验,
其原因是________。
16. 依据是否具有在熔融状态或水溶液中导电 能力,可以将化合物分为电解质和非电解质。水作为一种分
布极为广泛的化合物,它实际上也是一种极弱的电解质。不同的物质对于水的电离存在不同程度的影响。
学习小组在实验室中通过某酸 和氨水对其进行探究。
步骤一:在常温下,量取 50mL 去离子水,利用 pH 计测定其 pH,记为 ;
步骤二:在常温下,量取 的 溶液,利用 pH 计测定其 pH,记为 ;
步骤三:在常温下,利用 氨水滴定步骤二中的 溶液,并记录 pH 计的数值变化。
回答下列问题:
(1)配制 的 溶液时必需的玻璃仪器除烧杯,玻璃棒,量筒外,还有________(填
仪器名称)。
(2)小组同学在实验过程中将 pH 计插到另一杯温度较低的去离子水中,发现其测量值比 大,由此认
为温度变化对电离存在影响。升高温度对去离子水的电离起________(填“无影响”“促进”或“抑制”)
作用,从化学键的角度解释该作用:________。
(3)步骤二中测得 ,则水电离出的 ________ 。
(4)步骤三滴定过程中通过计算得到水电离的 变化如图所示。
由此提出以下相关假设:
假设一:碱电离出的阳离子会促进水的电离;
假设二:酸 稀溶液浓度与水的电离程度成正比。
①设计实验,验证假设。室温下,取两份产品,依次进行表中实验。请完成下表:
第 7页/共 11页序号 操作 现象或结论
各取一份 的 溶液、 pH________7(填“>”“<”或“=”),假设
一不 1
成立
溶液以体积比 1:2 的比例混合,测定 pH
取一份 20mL 的 溶液稀释
,则假设二________(填“成立”
“不 2
至 40mL,测定其 pH,记录为 成立”或“无法判断”)
②有同学发现根据变化图可得假设一成立,而实验 1 中假设一却不成立,问题的关键在于________。
③根据实验以及图像可知,________会促进水的电离。
17. 镍废料中主要含有 ,还含有 、 、 、 等的化合物及少量难溶性杂质,以镍废料为原料
回收 及制备硫酸镍晶体( )的工艺流程如图所示:
已知:①酸浸液中镍元素以 的形式存在;
②常温下,部分物质溶度积如下:
物质
回答下列问题:
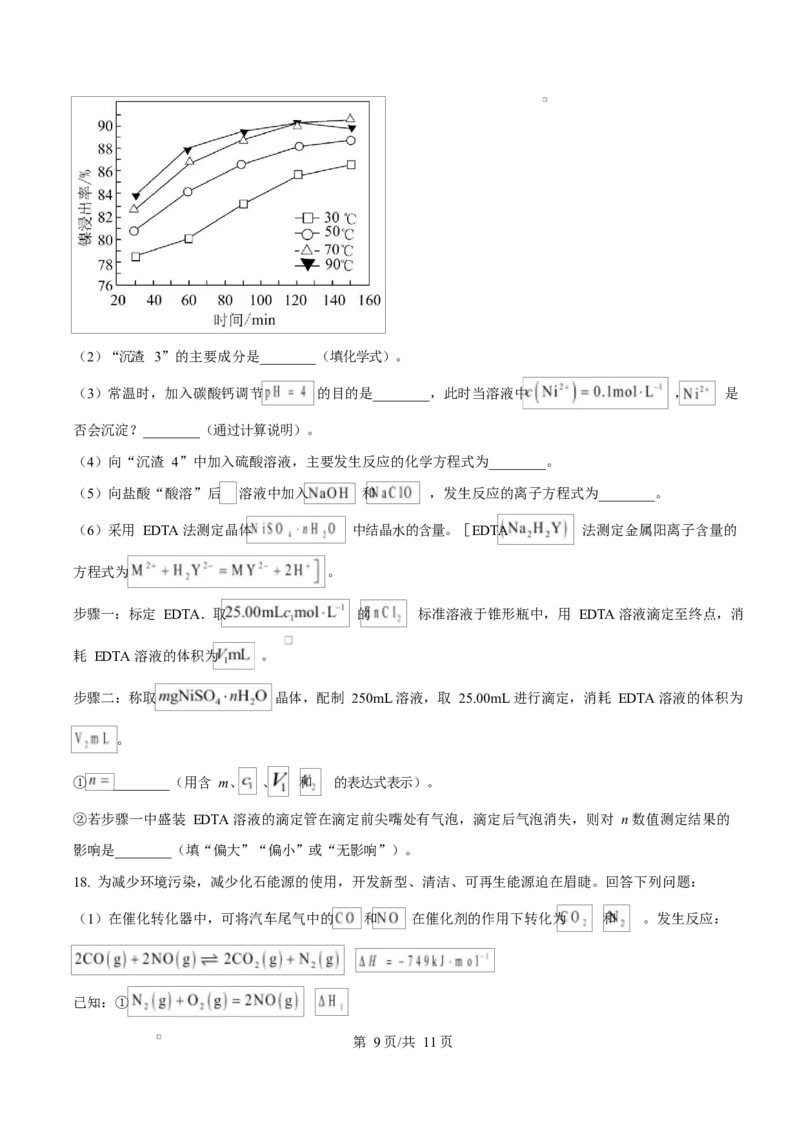
(1)基态镍原子的价层电子轨道表示式为________;“酸浸”过程中镍的浸出率与温度和时间的关系如图
所示,酸浸的最佳温度和时间是________。
第 8页/共 11页(2)“沉渣 3”的主要成分是________(填化学式)。
(3)常温时,加入碳酸钙调节 的目的是________,此时当溶液中 , 是
否会沉淀?________(通过计算说明)。
(4)向“沉渣 4”中加入硫酸溶液,主要发生反应的化学方程式为________。
(5)向盐酸“酸溶”后 溶液中加入 和 ,发生反应的离子方程式为________。
(6)采用 EDTA 法测定晶体 中结晶水的含量。[EDTA 法测定金属阳离子含量的
方程式为 。
步骤一:标定 EDTA.取 的 标准溶液于锥形瓶中,用 EDTA 溶液滴定至终点,消
耗 EDTA 溶液的体积为 。
步骤二:称取 晶体,配制 250mL 溶液,取 25.00mL 进行滴定,消耗 EDTA 溶液的体积为
。
① ________(用含 m、 、 和 的表达式表示)。
②若步骤一中盛装 EDTA 溶液的滴定管在滴定前尖嘴处有气泡,滴定后气泡消失,则对 n 数值测定结果的
影响是________(填“偏大”“偏小”或“无影响”)。
18. 为减少环境污染,减少化石能源的使用,开发新型、清洁、可再生能源迫在眉睫。回答下列问题:
(1)在催化转化器中,可将汽车尾气中的 和 在催化剂的作用下转化为 和 。发生反应:
已知:①
第 9页/共 11页②
则 ________ 。
(2)用钌的配合物作催化剂,一定条件下可直接催化分解 ,发生反应:
,该反应的 ________(填“>”或“<”)0,该反应在________(填“高
温”“低温”或“任何温度”)下能自发进行。
(3)以 为原料制备甲醇和 是实现“碳中和”目标的有效途径。涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
①若 T℃时将 和 充入容积为 1L 的恒容密闭容器中只发生反应Ⅰ,下列说法正确的是
________(填字母)。
A.混合气体的平均相对分子质量保持不变时,说明反应Ⅰ已达到平衡
B.平衡时向容器中充入 气,容器压强增大,反应速率加快
C.达到平衡时,若 ,则该温度下反应Ⅰ的平衡常数为 0.5
D.加入适当催化剂,能降低反应Ⅰ的反应热,进而可加快反应速率
②反应 的速率表达式为 (k 为速率常数,
受温度影响),T℃时测得有关实验数据如下:
序号
① 0.01 0.01
② 0.02 0.01
③ 0.01 0.02
该温度下向 1L 恒容密闭容器中,充入 和 ,则起始化学反应速率:
________
③一定温度和催化剂条件下,在总压强为 3.0MPa 的恒压密闭容器中充入 , 和
第 10页/共 11页(已知 不参与反应)进行反应Ⅰ和反应Ⅱ,平衡时测得容器中 的体积分数为 12.5%
, ,计算该温度下反应Ⅱ的平衡常数 ________(计算结果保留分数形式,已知:分
压=总压 物质的量分数)。
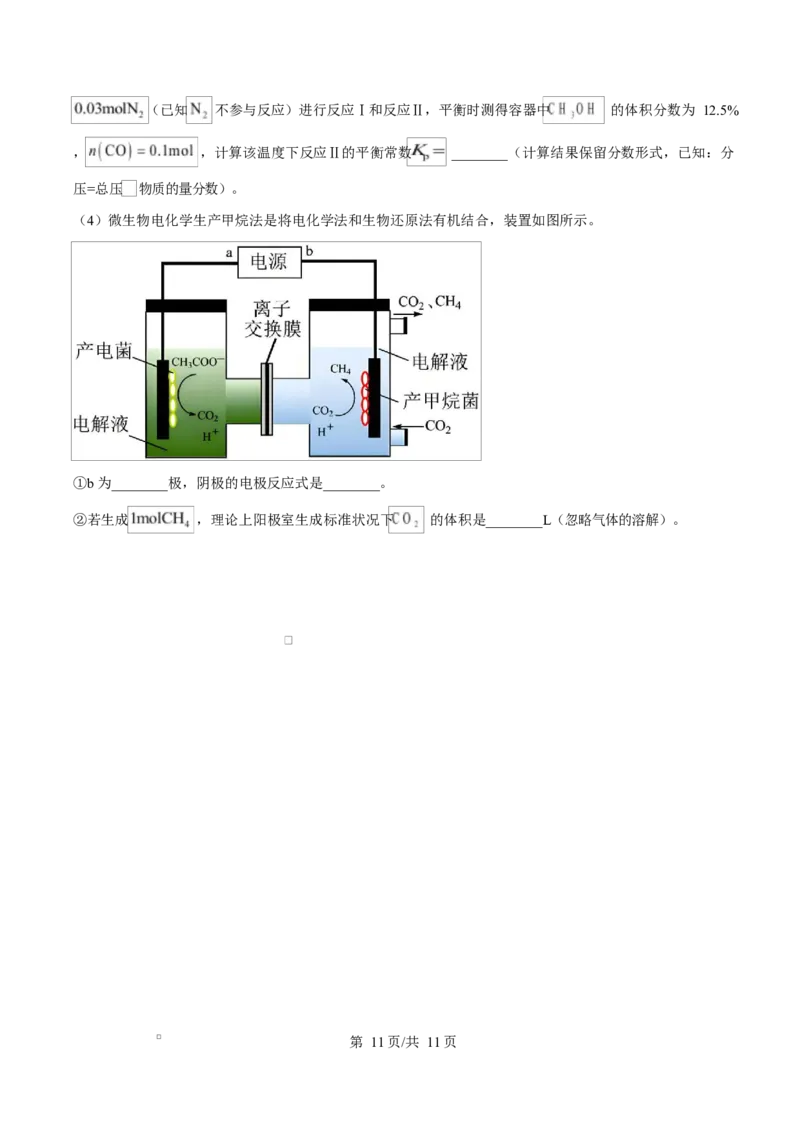
(4)微生物电化学生产甲烷法是将电化学法和生物还原法有机结合,装置如图所示。
①b 为________极,阴极的电极反应式是________。
②若生成 ,理论上阳极室生成标准状况下 的体积是________L(忽略气体的溶解)。
第 11页/共 11页