文档内容
(共100分)
相对原子质量(原子量):H-1 C-12 N-14 O-16 Na-23 S-32
一、选择题(本大题共7小题,每小题6分,共42分。在每小题给出的四个备选项中,只有一项符合题目
要求)
1.下列物质的使用不涉及化学变化的是
A.明矾用作净水剂 B.液氨用作制冷剂学科网
C.氢氟酸刻蚀玻璃 D.生石灰作干燥剂
【答案】B
2.下列实验可实现鉴别目的的是
[来源:学#科#网Z#X#X#K]
A.用KOH溶液鉴别SO (g)和SO
3 2
B.用湿润碘化钾淀粉试纸鉴别Br (g)和NO
2 2
C.用CO 鉴别NaAlO 溶液和CH COONa溶液
2 2 3
D.用BCl 溶液鉴别AgNO 溶液和K SO 溶液
2 3 2 4
【答案】C
第1页 | 共11页3.下列叙述正确的是
A.浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 胶体
3 3
B.CH COONa溶液中滴加少量浓盐酸后c(CH COO-)增大学科网
3 3
C.Ca(HCO ) 溶液与过量NaOH溶液反应可得到Ca(OH)
3 2 2
D.25℃时Cu(OH) 在水中的溶解度大于其在Cu(NO ) 溶液中的溶解度
2 3 2
【答案】D
[来源:学科网]
4.茶叶中铁元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是
A.将茶叶灼烧灰化,选用①、②和⑨
B.用浓硝酸溶解茶叶并加蒸馏水稀释,选用④、⑥和⑦
第2页 | 共11页C.过滤得到滤液,选用④、⑤和⑦
[来源:学§科§网]
D.检验中滤液中的Fe3+,选用③、⑧和⑩学科网
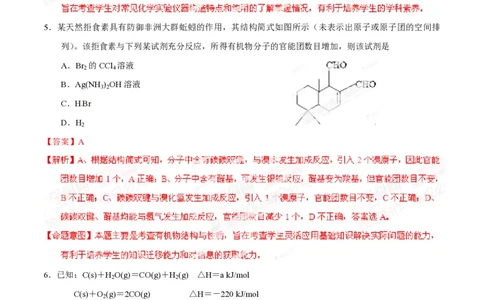
5.某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图所示(未表示出原子或原子团的空间排
列)。该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是
[来源:Zxxk.Com]
A.Br 的CCl 溶液
2 4
B.Ag(NH ) OH溶液
3 2
C.HBr
[来源:Zxxk.Com]
D.H
2
【答案】A
6.已知:C(s)+H O(g)=CO(g)+H (g) △H=a kJ/mol学科网
2 2
C(s)+O (g)=2CO(g) △H=-220 kJ/mol
2
H-H、O=O和O-H键的键能分别为436、496和462 kJ/mol,则a为
A.-332 B.-118 C.+350 D.+130
第3页 | 共11页运用所学化学知识解决相关化学问题的能力。
7.在恒容密闭容器中通入X并发生反应:2X(g) Y(g),温度T 、T 下X的物质的量浓度c(x)随时间t
1 2
变化的曲线如图所示,下列叙述正确的是
A.该反应进行到M点放出的热量大于进行到W点放出的热量
a-b
B.T 下,在0~t 时间内,υ(Y)= mol/(L·min)
2 1 t1 [来源:学科网]
C.M点的正反应速率υ 大于N点的逆反应速率υ
正 逆
D.M点时再加入一定量的X,平衡后X的转化率减小
【答案】C
二、非选择题(本大题共4小题,共58分
8.(15分)月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为_____________。学科网
(2)Na的原子结构示意图为______,Na在氧气中完全燃烧所得产物的电子式为_______。
第4页 | 共11页(3)MgCl 在工业上应用广泛,可由MgO制备。
2
①MgO的熔点比BeO的熔点________(填“高”或“低”)
②月球上某矿石经处理得到的MgO中含有少量SiO ,除去SiO 的离子方程式为______;SiO 的
2 2 2
晶体类型为________。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl 。若尾气可用足量NaOH溶液完全吸收,则
2
生成的盐为______(写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH 和700kgN ,若以所得H 和
2 2 2
N 为原料经一系列反应最多可制得碳酸氢铵___kg。
2 [来源:学。科。网Z。X。X。K]
+11 2 8 1
【答案】(1)1 (2) ;
(3)①高 ②2OH-+SiO =SiO 2-+H O;原子晶体 ③NaCl、NaClO、Na CO (4)3950
2 3 2 2 3
【解析】(1)在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。因为质子数和中子数
第5页 | 共11页(4)根据反应的方程式可知
3H + N = 2NH
2 2 3
9.(15分)中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO 最大使用量为0.25g/L。某兴趣小
2
组用题9图1装置(夹持装置略)收集某葡萄酒中SO ,并对含量碱性测定。
2
第6页 | 共11页(1)仪器A的名称是_______,水通入A的进口为_________。
(2)B中加入300.00ml葡萄酒和适量盐酸,加热使SO 全部逸出并与C中H O 完全反应,其化学方
2 2 2
程式为______________。
(3)除去C中过量的H O ,然后用0.0900mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择
2 2
题9中图2中的_____;若滴定终点时溶液的pH=8.8,则选择的指示剂为__________;若用50ml
滴定管进行实验,当滴定管中的液面在“10”处,则管内液体的体积(填序号)____(①=
10ml,②=40ml,③<10ml,④>40ml)
(4)滴定至终点时,消耗NaOH溶液25.00ml,该葡萄酒中SO 含量为:__g/L。
2
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施_______。
【答案】(1)冷凝管或冷凝器;b (2)SO +H O =H SO (3)③;酚酞;④ (4)0.24
2 2 2 2 4
(5)原因:盐酸的挥发;改进措施:用不挥发的强酸例如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行
对比实验,扣除盐酸挥发的影响。
[来源:学.科.网Z.X.X.K]
【解析】(1)根据仪器的构造特点可知,仪器A是冷凝管或冷凝器。冷凝时冷却水的流向应该是下口进,
上口出,即水通入A的进口是b。学科网
第7页 | 共11页【命题意图】本题主要是考查化学实验方案设计与评价、涉及仪器识别、氧化还原反应方程式书写、滴定
管和指示剂选择、物质含量计算以及误差分析与实验改进等,题目综合性强,考查了学生对化学实验
基本操作的掌握,对常见仪器或试剂的主要用途和使用方法的掌握情况。考察了应用所学知识进行必
要的分析、类推或计算一些具体的化学问题的能力。高考化学试题中对考生设计简单实验能力的考查
赋予较多的关注,它要求学生能够通过题给实验情境中适当迁移,准确把化学实验基础知识和基本操
作技能运用到某些类似的实验中去,解决一些原理和操作较简单的问题。
10.结晶玫瑰是具有强烈玫瑰香气的香料,可由下列反应路线合成(部分反应条件略去):
(1)A的类别是________,能与Cl 反应生成A的烷烃是__________。B中的官能团是__________。
2
(2)反应③的化学方程式为______________。
KOH
(3)已知:B————→苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副
产物是_____________。
第8页 | 共11页(4)已知: ,则经反应路线②得到的一种副产
物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为___________。
(5)G的同分异构体L遇FeCl 溶液显色,与足量饱和溴水反应未见白色沉淀产生,则L与NaOH的
3
乙醇溶液共热,所得有机物的结构简式为____________。(任写一种)学科网
【解析】(1)A是三氯甲烷,属于卤代烃,甲烷与氯气在光照条件下即可产生三氯甲烷。B是苯甲醛,官能
团是醛基。
第9页 | 共11页程式书写等,属于中等难度试题的考查,难度不是很大,侧重考查学生对信息的获取能力以及灵活应用已
知信息解决实际问题的能力和知识的迁移能力。该题设计命题背景新颖,设问角度合理、巧妙,符合考纲
要求。突出了对学生基本知识和基本技能的考查,能较准确的反映出学生的知识掌握水平和化学思维能力。
11.(14分)氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)氢气是清洁能源,其燃烧产物为__________。
(2)NaBH 是一种重要的储氢载体,能与水反应达到NaBO ,且反应前后B的化合价不变,该反应的
4 2
化学方程式为___________,反应消耗1mol NaBH 时转移的电子数目为__________。
4
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
。某温度下,向恒容密闭容器中加入环己烷,
起始浓度为a mol/L,平衡时苯的浓度为bmol/L,该反应的平衡常数K=_____。
(4)一定条件下,题11图示装置可实现有机物的电化学储氢(忽略其它有机物)。
[来源:Z+xx+k.Com]
①导线中电子移动方向为____________。
②生成目标产物的电极反应式为_________。
生成目标产物消耗的电子数
③该储氢装置的电流效率 =_____( = ×100%,计算结果保留
转移的电子总数
小数点后1位)
第10页 | 共11页【答案】(1)水或H O (2)NaBH +2H O=NaBO +4H ↑;4N 或2.408×1024
2 4 2 2 2 A
27b4
(3) mol3/L3 (4)①A→D ②C H +6H++6e-=C H ③64.3%
a-b 6 6 6 12
第11页 | 共11页