文档内容
厦泉五校 2024-2025 学年高二年级第一学期期中联考
化学试题
(考试时间:75分钟 满分:100分 命题人:郑志彬 审核人:黄锦东 )
可能用到的相对原子质量:H:1 C:12 P:31
第Ⅰ卷
一、选择题:(本题共14小题,每小题只有一个正确答案,每小题3分,共42分)
1.铁制文物在潮湿环境中,会受到严重的腐蚀。明代的三宝公铁矛出土时的外观如图。下列说法正确的
是( )
A.铁矛主要发生化学腐蚀
B.铁矛被腐蚀时会吸收能量
C.铁矛被腐蚀时,发生反应 Fe3e Fe3
D.将铁制文物放在干燥处,可延缓腐蚀
2.下列叙述中正确的是( )
A.冰在室温下自动熔化成水,这是熵增的过程
B.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀
C.在铜的精炼过程中,若转移1 mol电子,则阳极一定溶解32 g Cu
D.反应2AgBsCgDs在一定条件下可自发进行,则H
0
3.家用液化气的成分之一是丁烷(CH )。当10kg丁烷完全燃烧生成二氧化碳和液态水时,放出5×105kJ
4 10
的热量。下列有关丁烷燃烧的热化学方程式,正确的是( )
13
A.CH (g)+ O(g)=4CO(g)+5HO(g) ∆H= -2900kJ/mol
4 10 2 2 2
2
13
B.CH (g)+ O(g)=4CO(g)+5HO(l) ∆H=-50 kJ/mol
4 10 2 2 2
2
C.2CH (g)+13O(g)=8CO(g)+10HO(g) ∆H=-2000kJ/mol
4 10 2 2 2
D.2CH (g)+13O(g)=8CO(g)+10HO(l) ∆H=-5800kJ/mol
4 10 2 2 2
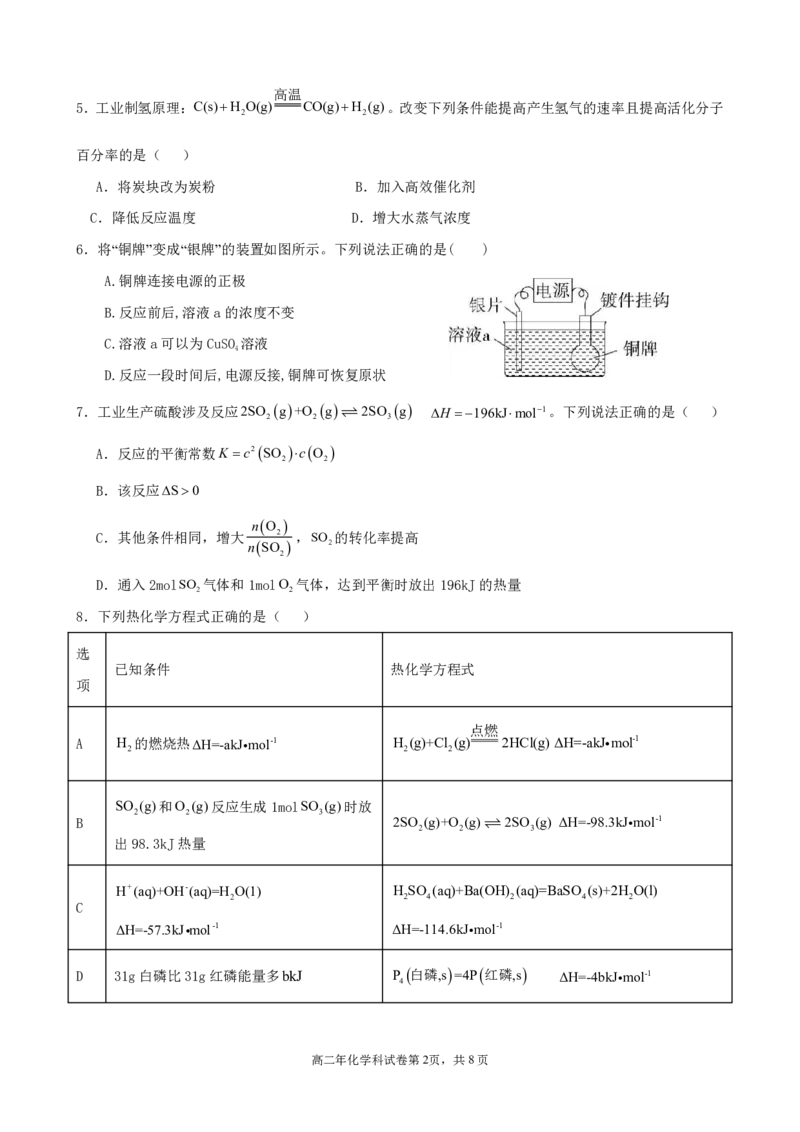
4.HIg分解的能量变化曲线如图所示。下列有关判断不正确的是( )
A.该反应为吸热反应
B.过程Ⅰ使用了催化剂,加快了反应速率
C.过程Ⅱ逆反应的活化能E 185kJmol1
2
D.催化剂通过参与反应改变反应历程、改变反应的活化能来改变化
学反应速率
高二年化学科试卷第1页,共8页
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}高温
5.工业制氢原理:C(s)H O(g) CO(g)H (g)。改变下列条件能提高产生氢气的速率且提高活化分子
2 2
百分率的是( )
A.将炭块改为炭粉 B.加入高效催化剂
C.降低反应温度 D.增大水蒸气浓度
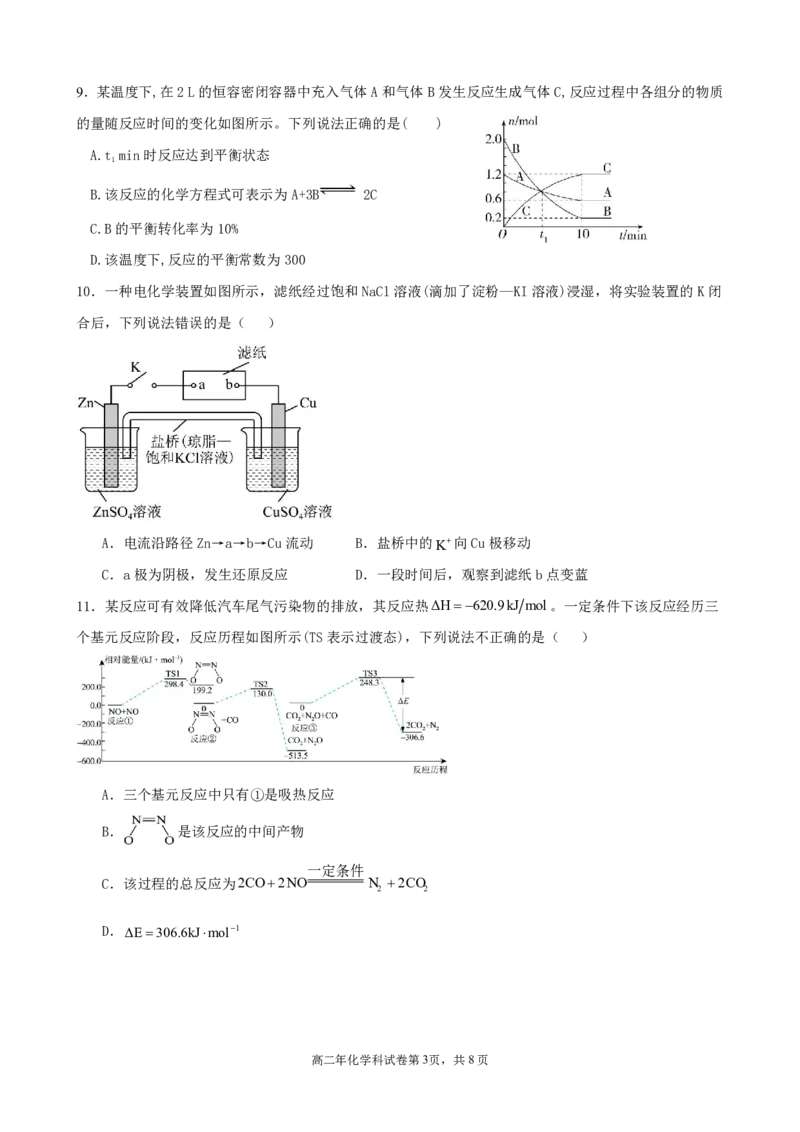
6.将“铜牌”变成“银牌”的装置如图所示。下列说法正确的是( )
A.铜牌连接电源的正极
B.反应前后,溶液a的浓度不变
C.溶液a可以为CuSO 溶液
4
D.反应一段时间后,电源反接,铜牌可恢复原状
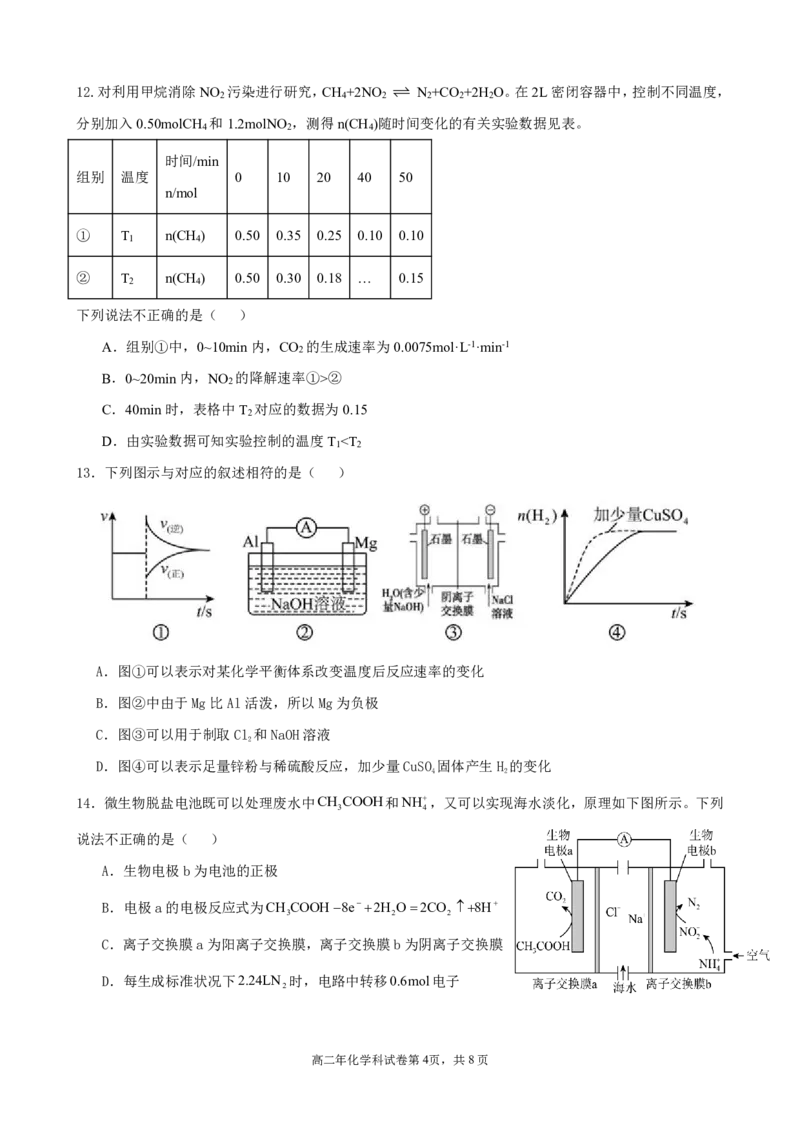
7.工业生产硫酸涉及反应2SO g+O g 2SO g H 196kJmol1。下列说法正确的是( )
2 2 3
A.反应的平衡常数K c2SO cO
2 2
B.该反应S0
nO
C.其他条件相同,增大 2 ,SO 的转化率提高
nSO 2
2
D.通入2molSO 气体和1molO 气体,达到平衡时放出196kJ的热量
2 2
8.下列热化学方程式正确的是( )
选
已知条件 热化学方程式
项
点燃
A H 的燃烧热ΔH=-akJmol-1 H (g)+Cl (g) 2HCl(g) ΔH=-akJmol-1
2 2 2
SO (g)和O (g)反应生成1molSO (g)时放
2 2 3
B 2SO (g)+O (g)2SO (g) ΔH=-98.3kJmol-1
2 2 3
出98.3kJ热量
H+(aq)+OH-(aq)=H O(1) H SO (aq)+Ba(OH) (aq)=BaSO (s)+2H O(l)
2 2 4 2 4 2
C
ΔH=-57.3kJmol-1 ΔH=-114.6kJmol-1
D 31g白磷比31g红磷能量多bkJ P 白磷,s =4P 红磷,s ΔH=-4bkJmol-1
4
高二年化学科试卷第2页,共8页
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}9.某温度下,在2L的恒容密闭容器中充入气体A和气体B发生反应生成气体C,反应过程中各组分的物质
的量随反应时间的变化如图所示。下列说法正确的是( )
A.t min时反应达到平衡状态
1
B.该反应的化学方程式可表示为A+3B 2C
C.B的平衡转化率为10%
D.该温度下,反应的平衡常数为300
10.一种电化学装置如图所示,滤纸经过饱和NaCl溶液(滴加了淀粉—KI溶液)浸湿,将实验装置的K闭
合后,下列说法错误的是( )
A.电流沿路径Zn→a→b→Cu流动 B.盐桥中的K向Cu极移动
C.a极为阴极,发生还原反应 D.一段时间后,观察到滤纸b点变蓝
11.某反应可有效降低汽车尾气污染物的排放,其反应热ΔH620.9kJ mol。一定条件下该反应经历三
个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法不正确的是( )
A.三个基元反应中只有①是吸热反应
B. 是该反应的中间产物
一定条件
C.该过程的总反应为2CO2NO N 2CO
2 2
D.ΔE306.6kJmol1
高二年化学科试卷第3页,共8页
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}12.对利用甲烷消除NO 污染进行研究,CH +2NO N +CO +2H O。在2L密闭容器中,控制不同温度,
2 4 2 2 2 2
分别加入0.50molCH 和1.2molNO ,测得n(CH )随时间变化的有关实验数据见表。
4 2 4
时间/min
组别 温度 0 10 20 40 50
n/mol
① T n(CH ) 0.50 0.35 0.25 0.10 0.10
1 4
② T n(CH ) 0.50 0.30 0.18 … 0.15
2 4
下列说法不正确的是( )
A.组别①中,0~10min内,CO 的生成速率为0.0075mol·L-1·min-1
2
B.0~20min内,NO 的降解速率①>②
2
C.40min时,表格中T 对应的数据为0.15
2
D.由实验数据可知实验控制的温度T ”或“=”)。
③反应Ⅱ的热化学方程式为 。
(3)二氧化碳回收利用是环保科学研究的热点课题。已知CO 经催化加氢可合成低碳烯烃:
2
2CO g6H g CH =CH g4H Og H
2 2 2 2 2
几种物质的相对能量(kJ∙mol-1)如表所示(规定单质的能量为0):
物质 CO g H g CH =CH g H Og
2 2 2 2 2
能量/kJ∙mol-1 -394 0 52 -242
△H= kJ∙mol-1
(4)工业上常用磷精矿[Ca (PO ) F]和硫酸反应制备磷酸。
5 4 3
已知25℃,101kPa时:
CaOsH SO lCaSO sH Ol H 271kJmol1
2 4 4 2
5CaOs3H PO lHFgCa PO Fs5H Ol H 937kJmol1
3 4 5 4 3 2
则Ca (PO ) F和硫酸反应生成磷酸的热化学方程式是 。
5 4 3
高二年化学科试卷第5页,共8页
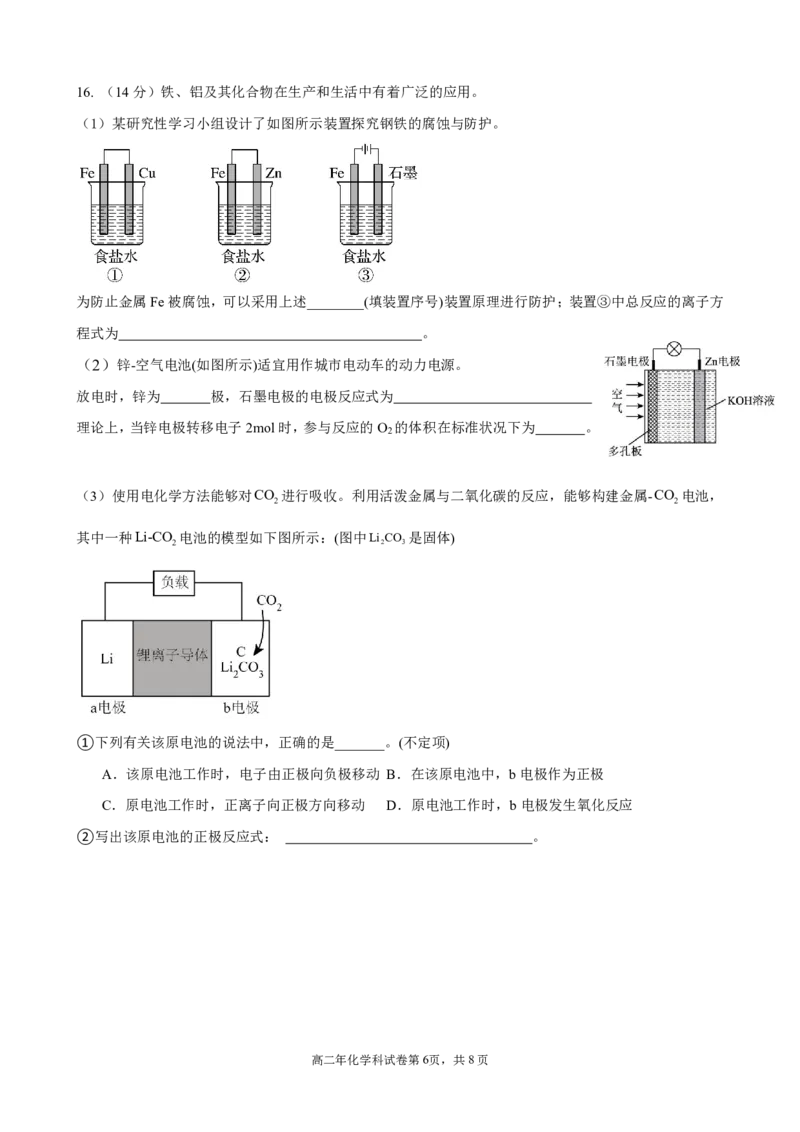
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}16. (14分)铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
为防止金属Fe被腐蚀,可以采用上述________(填装置序号)装置原理进行防护;装置③中总反应的离子方
程式为 。
(2)锌-空气电池(如图所示)适宜用作城市电动车的动力电源。
放电时,锌为 极,石墨电极的电极反应式为
理论上,当锌电极转移电子2mol时,参与反应的O 的体积在标准状况下为 。
2
(3)使用电化学方法能够对CO 进行吸收。利用活泼金属与二氧化碳的反应,能够构建金属-CO 电池,
2 2
其中一种Li-CO 电池的模型如下图所示:(图中Li CO 是固体)
2 2 3
①下列有关该原电池的说法中,正确的是_______。(不定项)
A.该原电池工作时,电子由正极向负极移动 B.在该原电池中,b电极作为正极
C.原电池工作时,正离子向正极方向移动 D.原电池工作时,b电极发生氧化反应
②写出该原电池的正极反应式: 。
高二年化学科试卷第6页,共8页
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}17.(14分)(1)单质碘可与氢气反应生成碘化氢。将物质的量比为2:1的氢气和碘蒸气放入密闭容器中进
行反应:H (g)I (g)2HI(g),反应经过5分钟测得碘化氢的浓度为0.1molL1,碘蒸气的浓度为
2 2
0.05molL1。前5分钟平均反应速率vH ,H 的初始浓度是 。
2 2
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为0.01molL1的H O 、H SO 、KI、Na S O 溶液
2 2 2 4 2 2 3
及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为H O 2S O22H S O22H O
2 2 2 3 4 6 2
反应分两步进行:
反应A:……
反应B:I 2S O2 2IS O2
2 2 3 4 6
①反应A的离子方程式是 。对于总反应,I的作用是 。
②探究溶液变蓝快慢的影响因素,实验I、II.(溶液浓度均为0.01molL1)
用量试剂 H O 溶液 H SO 溶液 Na S O 溶液 KI溶液(含淀粉) H O
2 2 2 4 2 2 3 2
实验I 5 4 8 3 0
实验II 5 2 x y z
i.溶液从混合时的无色变为蓝色的时间:实验I是30min、实验II是40min。实验II中,x、z所对成的数
值分别是 、 ;
ii.对比实验I、II,可得出的实验结论是 。
高二年化学科试卷第7页,共8页
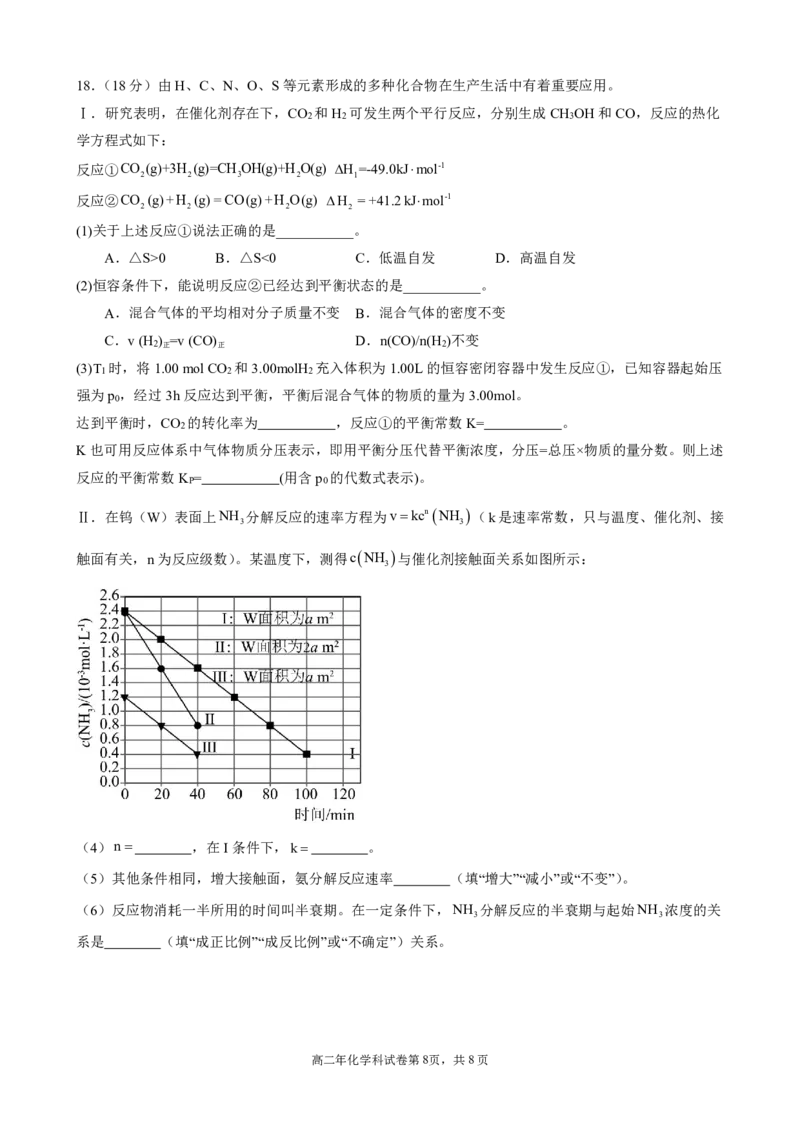
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}18.(18分)由H、C、N、O、S等元素形成的多种化合物在生产生活中有着重要应用。
Ⅰ.研究表明,在催化剂存在下,CO 和H 可发生两个平行反应,分别生成CH OH和CO,反应的热化
2 2 3
学方程式如下:
反应①CO (g)+3H (g)=CH OH(g)+H O(g) H =-49.0kJmol-1
2 2 3 2 1
反应②CO (g)+H (g)=CO(g)+H O(g) H =+41.2 kJmol-1
2 2 2 2
(1)关于上述反应①说法正确的是___________。
A.△S>0 B.△S<0 C.低温自发 D.高温自发
(2)恒容条件下,能说明反应②已经达到平衡状态的是___________。
A.混合气体的平均相对分子质量不变 B.混合气体的密度不变
C.v(H ) =v(CO) D.n(CO)/n(H )不变
2 正 正 2
(3)T 时,将1.00molCO 和3.00molH 充入体积为1.00L的恒容密闭容器中发生反应①,已知容器起始压
1 2 2
强为p ,经过3h反应达到平衡,平衡后混合气体的物质的量为3.00mol。
0
达到平衡时,CO 的转化率为 ,反应①的平衡常数K= 。
2
K也可用反应体系中气体物质分压表示,即用平衡分压代替平衡浓度,分压=总压×物质的量分数。则上述
反应的平衡常数K = (用含p 的代数式表示)。
P 0
Ⅱ.在钨(W)表面上NH 分解反应的速率方程为vkcnNH (k是速率常数,只与温度、催化剂、接
3 3
触面有关,n为反应级数)。某温度下,测得cNH 与催化剂接触面关系如图所示:
3
(4)n ,在I条件下,k 。
(5)其他条件相同,增大接触面,氨分解反应速率 (填“增大”“减小”或“不变”)。
(6)反应物消耗一半所用的时间叫半衰期。在一定条件下,NH 分解反应的半衰期与起始NH 浓度的关
3 3
系是 (填“成正比例”“成反比例”或“不确定”)关系。
高二年化学科试卷第8页,共8页
{#{QQABKY6UgggIAAJAAAhCQQGCCgKQkgGAAQgOxBAAMAABCAFABAA=}#}厦泉五校 2024-2025 学年高二年级第一学期期中联考
化学科参考答案及评分标准
一、选择题:(每小题只有一个正确答案,每小题3分,共42分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14
D A D C B B C D B A D B D C
二、非选择题:(每空2分,共58分)
15.(12分)(每空2分)
(1)D
COg+H Og=CO g+H g ΔH=-b kJ mol-1
(2)①a ② < ③ 2 2 2
(3)-128
(4)Ca (PO ) F(s)+5H SO (l)=5CaSO (s)+3H PO (l)+HF(g) △H= - 418kJ∙mol-1
5 4 3 2 4 4 3 4
16.(14分)(每空2分)
(1)②③ (漏选扣1分,选错不得分)
(2)负; O + 2H O +4e- = 4OH- ; 11.2L
2 2
(3)①BC (漏选扣1分,选错不得分)
②3CO +4e-+4Li+=C+2Li CO
2 2 3
17. (14分)(每空2分)
(1) 0.01mol•L-1•min-1 ; 0.2mol•L-1
(2) ① H O + 2I- + 2H+ = I + 2H O ; 催化剂
2 2 2 2
② i. 8 ; 2
ii. 其它条件不变,增大氢离子(或硫酸)浓度可以加快反应速率
18. (18分)(每空2分)
(1)BC (漏选扣1分,选错不得分)
(2)D
64
(3)50% ; 或 ;
27p 2
0
(4) 0 ; 2×10-5 mol•L-1•min-1(单位可以不写)
(5) 增大
(6) 成正比例