文档内容
天水一中高三下学期开学考试试卷
化 学
本试卷满分100分,考试时间75分钟
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号框涂黑。如需改动,
用橡皮擦干净后,再选涂其它答案标号框。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4. 可能用到的相对原子质量:H 1 C 12 N 14 O16 Cl 35.5 K 39 Fe 56
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。)
1. 化学与生活密切相关,下列不涉及化学变化的是( )
A.加入明矾后泥水变澄清 B.炖排骨汤时加点醋味道更鲜
C.北京冬奥会用水快速制冰 D.切开的茄子放置后切面变色
2.下列化学用语表述不正确的是( )
A.丙醛的结构简式:
B.顺—2—丁烯的球棍模型:
C.基态Si原子的价层电子排布图:
D. 的电子式:
3.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol乙醇中含有C-H键的数目为6N
A
B.0.78gNa O 与足量的水反应,转移的电子数为0.01N
2 2 A
C.1L0.01mol•L-1NaCO 溶液中含有CO 的数目为0.01N
2 3 A
D.标准状况下,22.4LHF中含有的分子数为N
A
4.下列反应的离子方程式正确的是( )
A.盐酸中滴加NaSiO 溶液:NaSiO+2H+= H SiO↓+2Na+
2 3 2 3 2 3
B.NaCO 溶液中通入少量SO :CO +2SO+H O=2HSO + CO
2 3 2 2 2 2
C.乙醇与KCr O 酸性溶液反应:3CHCHOH+2Cr O +16H+=3CH COOH+4Cr3++11H O
2 2 7 3 2 2 3 2
学科网(北京)股份有限公司 试卷 第 1 页D.溴与冷的NaOH溶液反应:Br +OH-= Br-+ BrO-+H+
2
5.对于下列实验,能正确描述其反应的离子方程式是( )
A.等物质的量浓度、等体积的Ca(HCO ) 溶液与NaOH溶液混合:Ca2++ +OH—=CaCO ↓+H O
3 2 3 2
B.向饱和NaCO 溶液中通入CO: +CO +H O=2
2 3 2 2 2
C.AlCl 溶液中加入过量的浓氨水:Al3++4NH·H O= +4 +2H O
3 3 2 2
D.向明矾溶液中滴加Ba(OH) 溶液,恰好使 沉淀完全:2Al3++3 +3Ba2++6OH—=Al(OH) ↓+
2 3
3BaSO↓
4
6.向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,
线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是( )
A.线段Ⅰ表示Fe2+的变化情况
B.根据图象可计算a=5
C.线段Ⅳ发生反应的离子方程式为I+5Cl+12OH-=2 +10Cl-+6H O
2 2 2
D.原溶液中c(Fe2+):c(I-):c(Br-)=2:1:3
7.下列方案设计、现象和结论有不正确的是( )
目的 方案设计 现象和结论
氯化铬化学式的 产生 沉淀,则此氯化铬化
氯化铬 在水溶液中
A
测定
用过量硝酸银溶液处理,观察现象 学式的
探究B、C、S
分别向饱和酸 溶液和稀硫酸溶 前者无气泡冒出,后者有气泡冒出,非
B 三种元素的非金
金属性:
液中加入少量 粉末
属性
检验碳酸与苯酚 向碳酸钠溶液中加入稀硫酸,反应产生
C 溶液变浑浊,说明酸性:碳酸>苯酚
的酸性强弱 的气体通入苯酚钠溶液中,观察现象
检验 与 的 向含 的 溶液中通入 溶液变蓝色,不能说明还原性:
D
还原性强弱 ,再滴加淀粉溶液,观察现象
A.A B.B C.C D.D
8.五种短周期主族元素甲、乙、丙、丁、戊的原子序数依次增大,甲和丙同族。乙和丁同族。乙和丁的
原子序数之和是甲和丙的2倍。下列判断错误的是( )
A.上述元素中原子半径最大的是丙
学科网(北京)股份有限公司 试卷 第 2 页B.元素的电负性大小为戊>丁>甲
C.甲和乙、丁、戊均只能形成一种共价型化合物
D.乙和戊形成的某种化合物是常用的消毒剂
9.航天飞机用铝粉与高氯酸铵( )的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵分解,
化学方程式为 。下列有关该反应的叙述正确的是( )
A. 分解需要加热,故该反应的
B. 分解是化学能转变为热能和动能
C. 分解生成液态水时放出的能量比生成气态水时的少
D.热化学方程式为
10.将 催化还原为 ,是促进碳中和的措施之一,已知 催化加氢的主要反应有:
①
②
其他条件不变时,在相同时间内温度对 催化加氢的影响如图。下列说法正确的是( )
[注] 的选择性 %
A.
B.其他条件不变,增大压强,有利于反应向生成 的方向进行
C.使用催化剂,能加快反应速率,但活化分子的百分数没有改变
D.220~240℃,升高温度,反应②的速率加快,反应①的速率减慢
11.在恒温恒压的密闭容器中,发生反应 。
下列说法正确的是( )
学科网(北京)股份有限公司 试卷 第 3 页A.
B.每充入 和 ,充分反应后转移电子数目小于
C.使用优质催化剂,体系中 的值增大
D.若升高温度,则反应速率加快,二氧化硫的平衡转化率增大
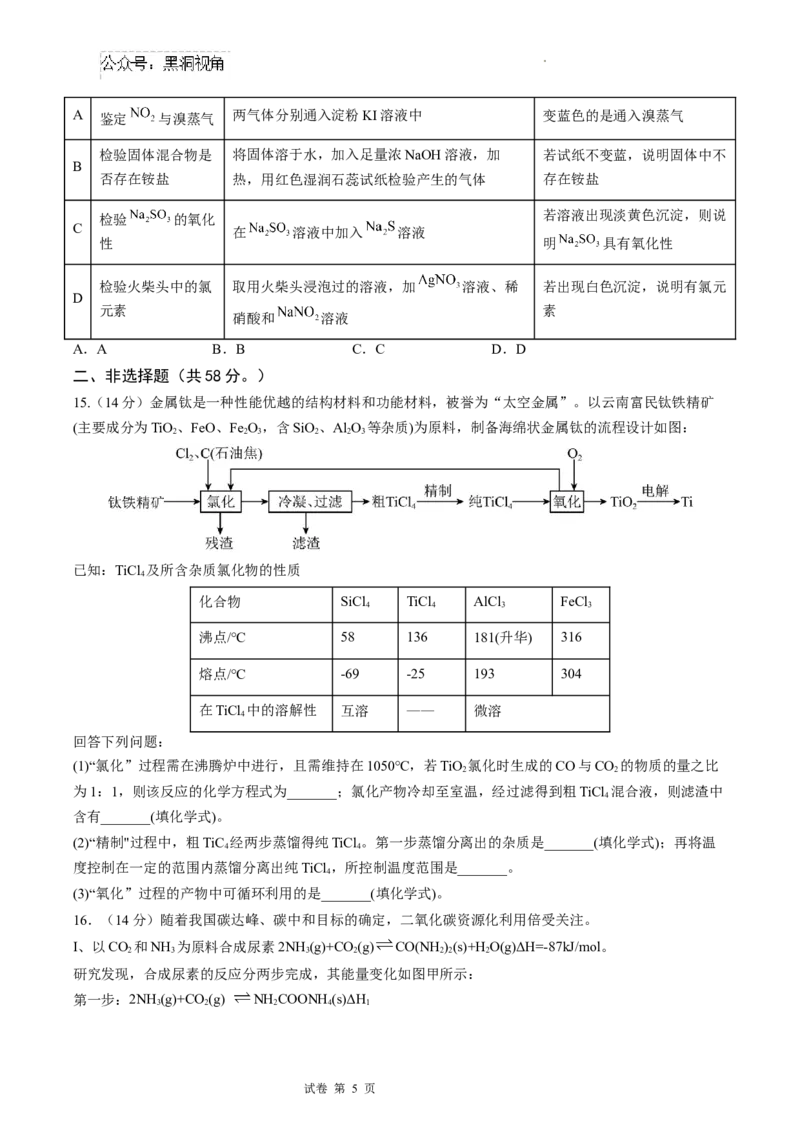
12. 可充电水系Zn-CO 电池用锌和催化剂材料作两极,电池工作示意图如图所示,其中双极膜是由阳膜
2
和阴膜制成的复合膜,在直流电场的作用下,双极膜复合层间的HO电离出的H+和OH-可以分别通过膜移
2
向两极。下列说法错误的是( )
A.放电时,右侧电极的电极反应式为CO+2H++2e-=HCOOH
2
B.放电时,金属锌为负极,发生氧化反应
C.充电时,双极膜产生的H+向阳极室移动
D.充电时,每生成22.4L(标准状况)O ,阴极增重130g
2
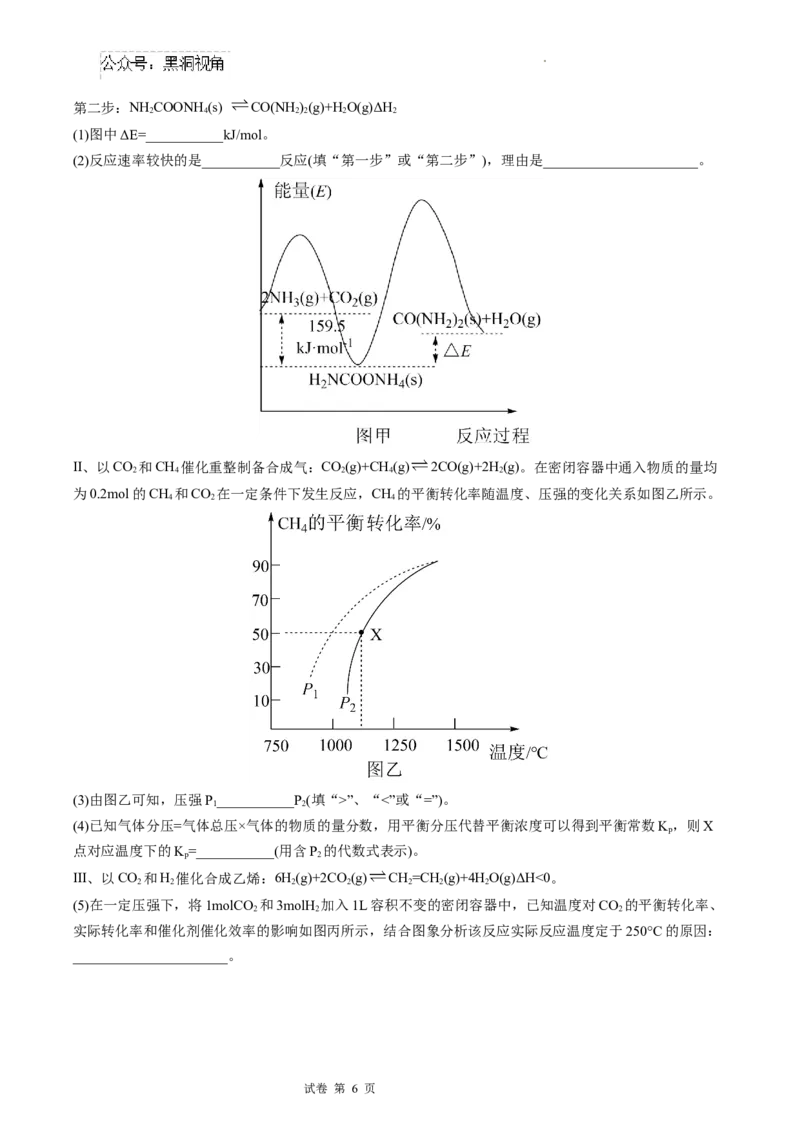
13. 次磷酸(H PO )是一元中强酸,次磷酸钠(NaH PO )广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如
3 2 2 2
图所示。下列有关说法正确的是( )
A.Ni2+价电子的轨道表示式为
B.“碱溶”时氧化剂与还原剂的物质的量之比为3:1
C.PH 、PO 中P的杂化方式相同,键角PO >PH
3 3
D.次磷酸铵与足量氢氧化钠共热,发生反应NH +H PO +3OH- NH ↑+3H O+PO
2 3 2
14. 下列方案设计、现象和结论有正确的是( )
目的 方案设计 现象和结论
学科网(北京)股份有限公司 试卷 第 4 页A 鉴定 与溴蒸气 两气体分别通入淀粉KI溶液中 变蓝色的是通入溴蒸气
检验固体混合物是 将固体溶于水,加入足量浓NaOH溶液,加 若试纸不变蓝,说明固体中不
B
否存在铵盐 热,用红色湿润石蕊试纸检验产生的气体 存在铵盐
若溶液出现淡黄色沉淀,则说
检验 的氧化
C 在 溶液中加入 溶液
性 明 具有氧化性
检验火柴头中的氯 取用火柴头浸泡过的溶液,加 溶液、稀 若出现白色沉淀,说明有氯元
D
元素 素
硝酸和 溶液
A.A B.B C.C D.D
二、非选择题(共58分。)
15.(14分)金属钛是一种性能优越的结构材料和功能材料,被誉为“太空金属”。以云南富民钛铁精矿
(主要成分为TiO、FeO、Fe O,含SiO、Al O 等杂质)为原料,制备海绵状金属钛的流程设计如图:
2 2 3 2 2 3
已知:TiCl 及所含杂质氯化物的性质
4
化合物 SiCl TiCl AlCl FeCl
4 4 3 3
沸点/℃ 58 136 181(升华) 316
熔点/℃ -69 -25 193 304
在TiCl 中的溶解性 互溶 —— 微溶
4
回答下列问题:
(1)“氯化”过程需在沸腾炉中进行,且需维持在1050℃,若TiO 氯化时生成的CO与CO 的物质的量之比
2 2
为1:1,则该反应的化学方程式为_______;氯化产物冷却至室温,经过滤得到粗TiCl 混合液,则滤渣中
4
含有_______(填化学式)。
(2)“精制"过程中,粗TiC 经两步蒸馏得纯TiCl 。第一步蒸馏分离出的杂质是_______(填化学式);再将温
4 4
度控制在一定的范围内蒸馏分离出纯TiCl ,所控制温度范围是_______。
4
(3)“氧化”过程的产物中可循环利用的是_______(填化学式)。
16.(14分)随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I、以CO 和NH 为原料合成尿素2NH (g)+CO (g) CO(NH)(s)+HO(g)ΔH=-87kJ/mol。
2 3 3 2 2 2 2
研究发现,合成尿素的反应分两步完成,其能量变化如图甲所示:
第一步:2NH (g)+CO (g) NH COONH(s)ΔH
3 2 2 4 1
学科网(北京)股份有限公司 试卷 第 5 页第二步:NH COONH(s) CO(NH)(g)+HO(g)ΔH
2 4 2 2 2 2
(1)图中ΔE=___________kJ/mol。
(2)反应速率较快的是___________反应(填“第一步”或“第二步”),理由是______________________。
II、以CO 和CH 催化重整制备合成气:CO(g)+CH (g) 2CO(g)+2H(g)。在密闭容器中通入物质的量均
2 4 2 4 2
为0.2mol的CH 和CO 在一定条件下发生反应,CH 的平衡转化率随温度、压强的变化关系如图乙所示。
4 2 4
(3)由图乙可知,压强P___________P(填“>”、“<”或“=”)。
1 2
(4)已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数K,则X
p
点对应温度下的K=___________(用含P 的代数式表示)。
p 2
III、以CO 和H 催化合成乙烯:6H(g)+2CO (g) CH=CH (g)+4HO(g)ΔH<0。
2 2 2 2 2 2 2
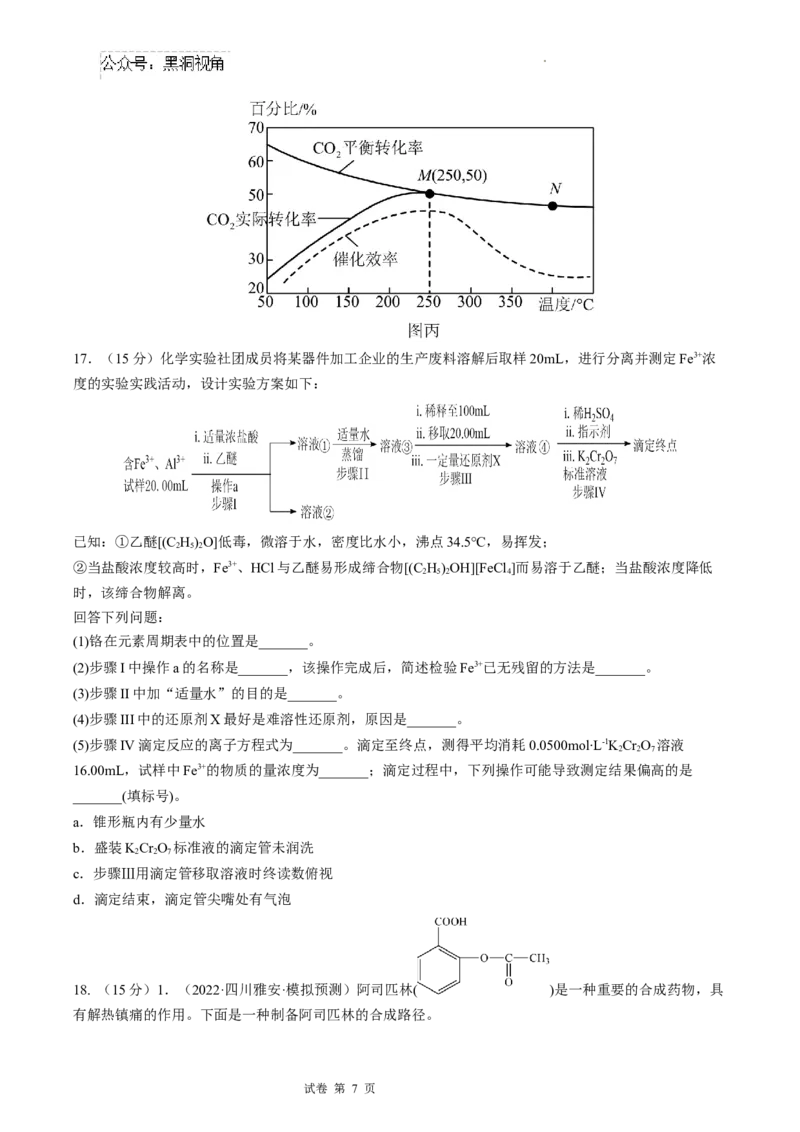
(5)在一定压强下,将1molCO 和3molH 加入1L容积不变的密闭容器中,已知温度对CO 的平衡转化率、
2 2 2
实际转化率和催化剂催化效率的影响如图丙所示,结合图象分析该反应实际反应温度定于250°C的原因:
______________________。
学科网(北京)股份有限公司 试卷 第 6 页17.(15分)化学实验社团成员将某器件加工企业的生产废料溶解后取样20mL,进行分离并测定Fe3+浓
度的实验实践活动,设计实验方案如下:
已知:①乙醚[(C H)O]低毒,微溶于水,密度比水小,沸点34.5℃,易挥发;
2 5 2
②当盐酸浓度较高时,Fe3+、HCl与乙醚易形成缔合物[(C H)OH][FeCl ]而易溶于乙醚;当盐酸浓度降低
2 5 2 4
时,该缔合物解离。
回答下列问题:
(1)铬在元素周期表中的位置是_______。
(2)步骤I中操作a的名称是_______,该操作完成后,简述检验Fe3+已无残留的方法是_______。
(3)步骤II中加“适量水”的目的是_______。
(4)步骤III中的还原剂X最好是难溶性还原剂,原因是_______。
(5)步骤IV滴定反应的离子方程式为_______。滴定至终点,测得平均消耗0.0500mol∙L-1KCr O 溶液
2 2 7
16.00mL,试样中Fe3+的物质的量浓度为_______;滴定过程中,下列操作可能导致测定结果偏高的是
_______(填标号)。
a.锥形瓶内有少量水
b.盛装KCr O 标准液的滴定管未润洗
2 2 7
c.步骤Ⅲ用滴定管移取溶液时终读数俯视
d.滴定结束,滴定管尖嘴处有气泡
18. (15分)1.(2022·四川雅安·模拟预测)阿司匹林( )是一种重要的合成药物,具
有解热镇痛的作用。下面是一种制备阿司匹林的合成路径。
学科网(北京)股份有限公司 试卷 第 7 页(1)A生成B的反应方程式为_______。
(2)C的官能团名称为_______;D的结构简式为_______。
(3)反应⑥的反应类型为_______。
(4)写出符合下列条件的E的同分异构体的结构简式_______。
①苯环上只有2种等效氢;②含有酯基。
学科网(北京)股份有限公司 试卷 第 8 页化学参考答案
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。)
1.【答案】C
【详解】A.明矾净水的原理为: , 胶体具有吸附性,可以使泥水变
澄清,涉及化学变化,A错误;
B.炖排骨汤时放点醋,可使骨头中的钙、磷、铁等矿物质溶解出来,营养值更价高。此外,醋还可以防
止食物中的维生素被破坏,涉及化学变化,B错误;C.水和冰的分子式都是HO,水快速制冰为物理变
2
化,C正确;D.茄子中存在一类叫“酚氧化酶”的物质,它见到氧气之后,发生化学反应产生一些有色
的物质。反应时间越长,颜色越深,D错误;故选B。
【答案】C
【详解】A.丙醛的分子式为C HO,官能团为醛基,结构简式为CHCHCHO,故A正确;
3 6 3 2
B.顺—2—丁烯的结构简式为 ,球棍模型为 ,故B正确;
C.硅元素的原子序数为14,价电子排布式为3s23p2,价层电子排布图为 ,故C错
误;
D.碳化钙为离子化合物,电子式为 ,故D正确;
故选C。
3.【答案】B
【详解】A.1mol乙醇中含有C-H键的数目为5N ,A错误;
A
B.0.78gNa O 与足量的水反应,转移的电子数为 ,B正确;
2 2
C.CO 在溶液中会水解,C错误;
D.标准状况下HF是液态,D错误;
4.【答案】C
【详解】A.NaSiO 是可溶性盐,能拆,应为 ,A错误;
2 3
B.SO 少量,应生成 ,应为 ,B错误;
2
C.CHCHOH为非电解质不能拆,CHCOOH为弱电解质不能拆,原子守恒、电荷守恒,C正确;
3 2 3
D.碱性条件下不能生成H+,应为 ,D错误;
故答案选C。
学科网(北京)股份有限公司 答案 第 1 页5.【答案】A
【详解】A.等物质的量浓度、等体积的碳酸氢钙溶液与氢氧化钠溶液反应生成碳酸钙沉淀、碳酸氢钠和
水,反应的离子方程式为Ca2++ +OH—=CaCO ↓+H O,故A正确;
3 2
B.饱和碳酸氢钠溶液与二氧化碳反应生成碳酸氢钠沉淀,反应的离子方程式为2Na++
+CO +H O=2NaHCO ↓,故B错误;
2 2 3
C.氯化铝溶液与过量的浓氨水反应生成氢氧化铝沉淀和氯化铵,反应的离子方程式为Al3++3NH·H O=
3 2
Al(OH) ↓+3 ,故C错误;
3
D.明矾溶液与氢氧化钡溶液恰好使硫酸根离子沉淀完全的反应为明矾溶液与氢氧化钡溶液反应生成偏铝
酸根、硫酸钡沉淀,反应的离子方程式为Al3++2 +2Ba2++4OH—=AlO +2BaSO↓+2H O,故D错误;
4 2
故选A。
6.【答案】D
【详解】A.由于还原性I->Fe2+>Br-,所以线段Ⅰ表示I-的变化情况,A错误;
B.线段Ⅰ表示I-的变化,根据反应2I-+Cl=I +2Cl-,反应消耗Cl 的物质的量是1 mol,则n(I-)=2 mol,线
2 2 2
段II发生反应:2Fe2++Cl=2Fe3++2Cl-,其其反应消耗Cl 的物质的量是2 mol,可知n(Fe2+)=4 mol;根据电
2 2
荷守恒可知:n(I-)+n(Br-)=2n(Fe2+),所以n(Br-)=2n(Fe2+)- n(I-)=2×4 mol-1×2 mol=6 mol,所以发生反应2Br-
+Cl=Br +2Cl-时,n(Cl )= n(Br-)=3 mol,故a=3+3=6,B错误;
2 2 2
C.线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素,该元素为I元素,2I-+Cl=I +2Cl-反
2 2
应消耗1 mol氯气,所以碘原子的物质的量为2 mol,已知:b-a=5,反应Ⅳ消耗氯气的物质的量为5 mol,
根据电子守恒,设该含氧酸中碘元素的化合价为x,(x-0) ×2 mol=5 mol×2,解得x=+5,则该含氧酸为
HIO ,反应的离子方程是I+5Cl+6H O=2 +10Cl-+12H+,C错误;
3 2 2 2
D.根据选项B分析可知:n(Fe2+)=4 mol,n(I-)=2 mol,n(Br-)=6 mol,所以n(Fe2+):n(I-):n(Br-)=4 mol:2
mol:6 mol=2:1:3,离子处于同一溶液,溶液的体积相同,故离子浓度比等于离子的物质的量的比,则
c(Fe2+):c(I-):c(Br-)=n(Fe2+):n(I-):n(Br-)=2:1:3,D 正确;
故合理选项是D。
7.【答案】A
【详解】A. 氯化铬 在水溶液中用过量硝酸银溶液处理,产生0.02molAgCl沉淀,说
明形成的配合物外界有两个Cl-即 ,符合题意,A正确;B.分别向饱和酸
溶液和稀硫酸溶液中加入少量 粉末,前者无气泡冒出,后者有气泡冒出,强酸能和弱酸盐反应生
成弱酸,证明非金属性: ,不符合题意,B错误;C.强酸能和弱酸盐反应生成弱酸,稀硫酸和碳
酸钠反应生成二氧化碳,二氧化碳和苯酚钠溶液反应生成苯酚沉淀,根据现象可以说明酸性:碳酸>苯
酚,不符合题意,C错误;D.氯气能氧化亚铁离子生成铁离子、能氧化碘离子生成碘,向含0.1mol的
FeI 溶液中通入0.1molCl ,再滴加淀粉溶液,溶液变蓝色,说明有碘生成,但不能说明亚铁离子是否被氧
2 2
化,所以不能得出结论,不符合题意,D错误;故答案为:A。
学科网(北京)股份有限公司 答案 第 2 页8.【答案】C
【详解】A.上述元素中,H的原子半径最小,Na、S、Cl为同周期元素,Na的原子序数最小,原子半径
最大,A正确;B.甲、丁、戊分别为H、S、Cl元素,非金属性Cl>S>H,则电负性大小为Cl>S>H,
B正确;C.甲、乙、丁、戊分别为H、O、S、Cl元素,H和S、Cl只能形成一种共价型化合物,但H和
O可形成HO、HO 两种共价型化合物,C错误;D.乙和戊分别为O和Cl,二者形成的化合物ClO 是常
2 2 2 2
用的消毒剂,D正确;故选C。
9.【答案】B
【详解】A. 为固体燃料,故该反应为放热反应,故A错误;B. 分解是放热反应,
化学能转化为热能,产生大量的高温气体,推动航天飞机飞行,热能转化为动能,故 分解是化学
能转变为热能和动能,故B正确;C. 气态水转化为液态水放出热量,故 分解生成液态水时放
出的能量比生成气态水时的多,故C错误;D. 热化学方程式中物质要标明状态,故D错误;故选B。
10.【答案】B
【详解】A.按盖斯定律:①-②得到
,A错误;B.反应①是气体体积减小的反应,其他条件不变,增大压强,平衡向正反应方向移动,有利
于 的生成,B正确;C.使用催化剂,能降低反应的活化能,增大活化分子的百分数,使反应速率
加快,C错误;D.220~240℃,升高温度,反应①、②的速率均加快,但加快的倍数不一样,D错误;
答案选B。
11.【答案】B
【详解】A.该反应是熵减反应,ΔS<0,A错误;B.该反应是可逆反应,2mol SO 和1mol O,不能完
2 2
全转化为2mol SO ,故充分反应后,转移电子数目小于4×6.02×1023,B正确;C.使用优质催化剂后,该
3
反应的化学平衡常数K= 不变,C错误;D.升高温度,反应速率加快,但该反应是放热反
应,升高温度,平衡逆向移动,二氧化硫的平衡转化率减小,D错误;故选B。
12.【答案】C
【详解】A.放电时,右侧电极为正极,发生还原反应,电极反应为CO+2H++2e−=HCOOH,故A正
2
确;B.放电时,左侧Zn电极为负极,Zn失电子发生氧化反应,故B正确;C.充电时,右侧为阳极,阳
离子向阴极移动,所以双极膜复合层间的HO电离出的H+通过膜移向左侧移动,故C错误;D.充电时,
2
电池总反应为 ;每生成22.4L(标准状况)即1molO ,生成
2
2molZn,阴极增重130g,故D正确;故答案选C。
13.【答案】C
【详解】A.基态Ni原子的价层电子排布式为3d84s2,Ni原子失去2个4s电子变为Ni2+,则Ni2+的价层电
子排布式为3d8,故其价电子的轨道表示式为 ,故A错误;B.“碱溶”时,发生的反应
为P+3NaOH+3HO=3NaH PO +PH↑,氧化剂与还原剂均为P,根据化合价变化,二者物质的量之比为
4 2 2 2 3 4
学科网(北京)股份有限公司 答案 第 3 页1:3,故B错误;C.PH 中P原子价层电子对数为:3+ =4,采取sp3杂化,有1对孤电子对,空间
3
构型为三角锥形;PO 中P原子价层电子对数为:4+ =4,采取sp3杂化,无孤电子对,空间构
型为正四面体形,所以PO 中P的杂化方式相同,键角PO >PH,故C正确;D.HPO 是一元酸,则
3 3 2
NH HPO 为正盐,HPO 不电离,次磷酸铵与足量氢氧化钠共热,发生反应NH +OH- NH ↑+H O,故D
4 2 2 2 3 2
错误;
答案选C。
14.【答案】D
【详解】A. 与溴蒸气均能把碘离子氧化为碘单质,故分别通入淀粉KI溶液中,均能变蓝,A错误;
B.铵根与亚硝酸根离子能在水溶液中发生归中反应产生氮气。则:将固体混合物溶于水,加入足量浓
NaOH溶液,加热,用红色湿润石蕊试纸检验产生的气体,若试纸不变蓝,不能说明固体中不存在铵盐,
B错误;
C.在 溶液中加入 溶液不发生反应,在酸性条件下,氢离子、亚硫酸根离子和硫离子发生反应
生成硫和水,溶液出现淡黄色沉淀, C错误;D.氯酸钾、硝酸银和亚硝酸钠反应生成氯化银白色沉淀,
则:取用火柴头浸泡过的溶液,加 溶液、稀硝酸和 溶液,若出现白色沉淀,说明有氯元
素, D正确;答案选D。
二、非选择题(共58分。)
15.【答案】(1) FeCl 、AlCl
3 3
(2) SiCl 高于136℃而低于181℃
4
(3)Cl
2
16.【答案】(1)72.5
(2) 第一步 第一步反应的活化能小于第二步的活化能,反应速率快
(3)<
(4)
(5)当温度低于250°C时,随着温度升高,催化剂活性增强,催化效率升高,反应速率加快,二氧化碳的实
际转化率变大;当温度高于250°C时,随着温度升高,催化剂活性降低,催化效率降低,反应速率变慢,
实际转化率变小(或温度为250°C时催化剂效率和二氧化碳的实际转化率均较高)
17.【答案】(1)第四周期ⅥB族
(2) 分液 取溶液②少许于试管中,滴加KSCN溶液,溶液不变为红色,说明溶液中不含有
Fe3+,已无残留
(3)使缔合物[(C H)OH][FeCl ] 解离为Fe3+
2 5 2 4
(4)若X为可溶性还原剂,溶液④中含有的X会使步骤IV滴定消耗KCr O 溶液体积偏大,所测结果偏高
2 2 7
学科网(北京)股份有限公司 答案 第 4 页(5) 6Fe2++ CrO +14H+=6Fe3++2Cr3++7H O 1.2mol/L bd
2 2
18.【答案】(1)
(2) 羧基
(3)取代反应
(4)
学科网(北京)股份有限公司 答案 第 5 页