文档内容
高二上学期第一次月考试卷
化学
命题人:曹广波
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用 2B铅笔把答题卡上对应题目的答
案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区
域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版选择性必修1第二章~第三章。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、选择题(本题共 15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的)
1.下列物质属于强电解质的是( )
A. B. C. D.
2.下列离子方程式中,属于水解反应的是( )
A. B.
C. D.
3.工业上用 和 合成氨的反应是放热反应,在合成氨的实际生产中,温度通常控制在500℃左右。这
是因为( )
A.高温有利于提高反应物的平衡转化率 B.高温能使逆反应速率减慢
C.在该温度范围内催化剂活性最强 D.在该温度下反应的平衡常数最大
4.下列物质的应用与水解有关的是( )
A.明矾净水 B. 蚀刻铜制电路板
C. 除去水溶液中的 、 D.食盐腌制食品
5.在10L密闭容器中,1mol A和3mol B在一定条件下反应: ,2min后反应
达到平衡时,测得混合气体共4mol且生成了0.4mol C,则下列说法错误的是( )
A.x等于1 B.平衡时,
C.A的转化率为20% D.B的平均反应速率为6.下列事实不能用勒夏特列原理解释的是( )
A. 溶液中加入固体KSCN后颜色变深
B.缩小容器体积,使 的平衡体系颜色变深
C.加压有利于合成氨反应
D.黄绿色的氯水光照后颜色变浅
7.下列说法中正确的是( )
A.若 ,该化学反应在任何温度下都不能自发进行
B.知道了某过程有自发性之后,就能确定该过程是否一定会发生
C.一定温度下,反应 的
D.某反应在低温条件下能自发进行,那么该反应在高温条件下也一定能自发进行
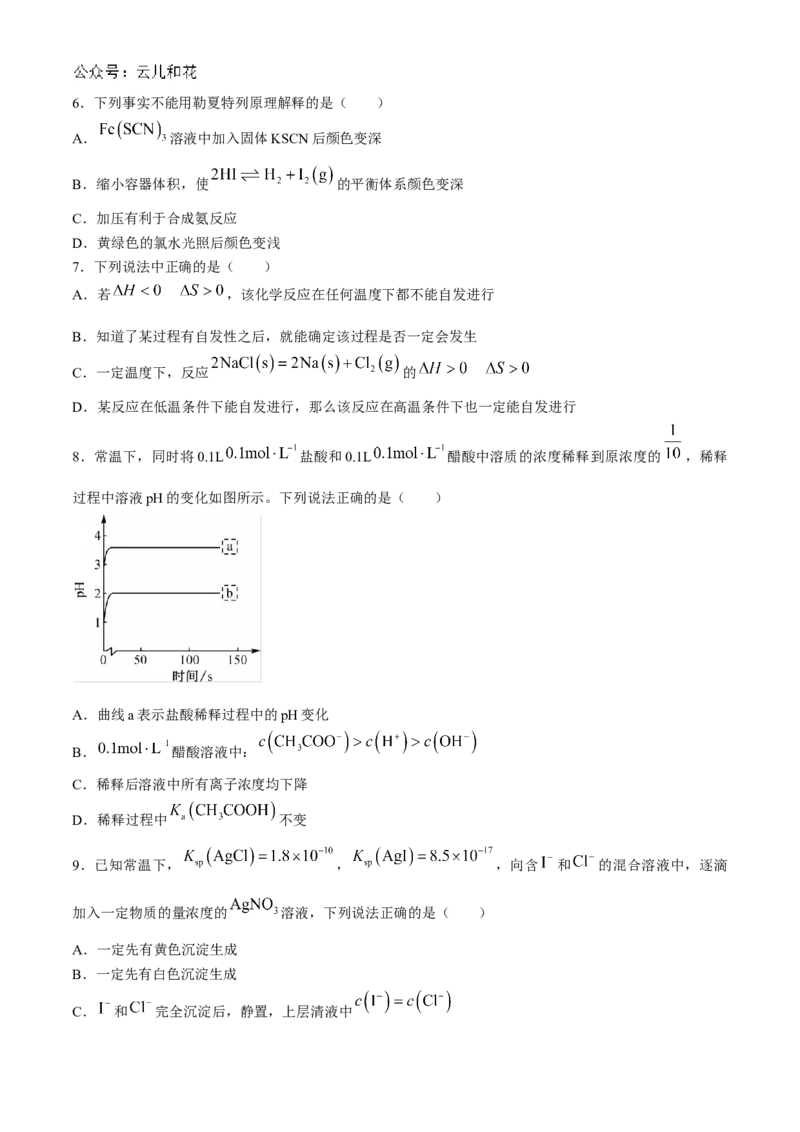
8.常温下,同时将0.1L 盐酸和0.1L 醋酸中溶质的浓度稀释到原浓度的 ,稀释
过程中溶液pH的变化如图所示。下列说法正确的是( )
A.曲线a表示盐酸稀释过程中的pH变化
B. 醋酸溶液中:
C.稀释后溶液中所有离子浓度均下降
D.稀释过程中 不变
9.已知常温下, , ,向含 和 的混合溶液中,逐滴
加入一定物质的量浓度的 溶液,下列说法正确的是( )
A.一定先有黄色沉淀生成
B.一定先有白色沉淀生成
C. 和 完全沉淀后,静置,上层清液中D.将AgI和AgCl加入浓NaCl溶液中,存在平衡:
10.为使 溶液中 减小,下列措施可行的是( )
A.加热 溶液 B.加适量的稀盐酸
C.加入适量蒸馏水 D.加入适量 固体
11.亚磷酸( )是一种二元弱酸,常温下电离常数 , 。下列说法
正确的是( )
A. 与足量的NaOH溶液反应生成
B.向亚磷酸溶液中加入少量NaOH固体, 增大
C.对亚磷酸溶液升温,溶液的pH增大
D. 的 溶液呈碱性
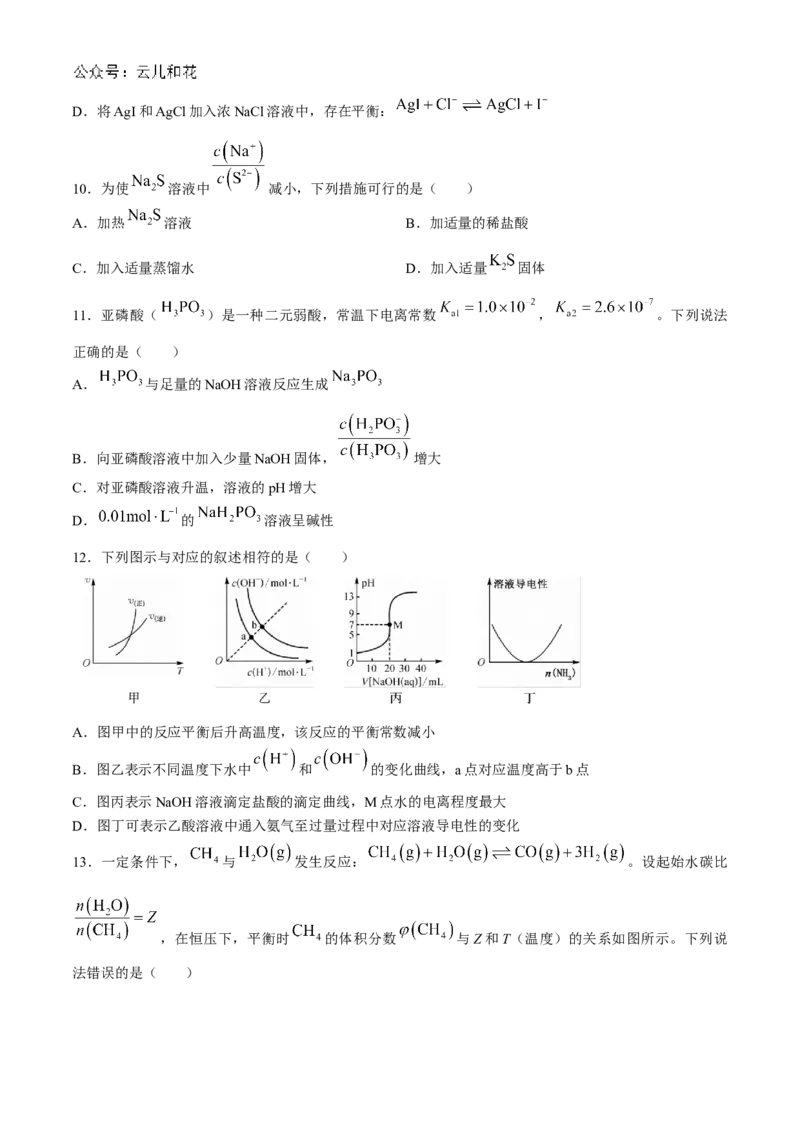
12.下列图示与对应的叙述相符的是( )
A.图甲中的反应平衡后升高温度,该反应的平衡常数减小
B.图乙表示不同温度下水中 和 的变化曲线,a点对应温度高于b点
C.图丙表示NaOH溶液滴定盐酸的滴定曲线,M点水的电离程度最大
D.图丁可表示乙酸溶液中通入氨气至过量过程中对应溶液导电性的变化
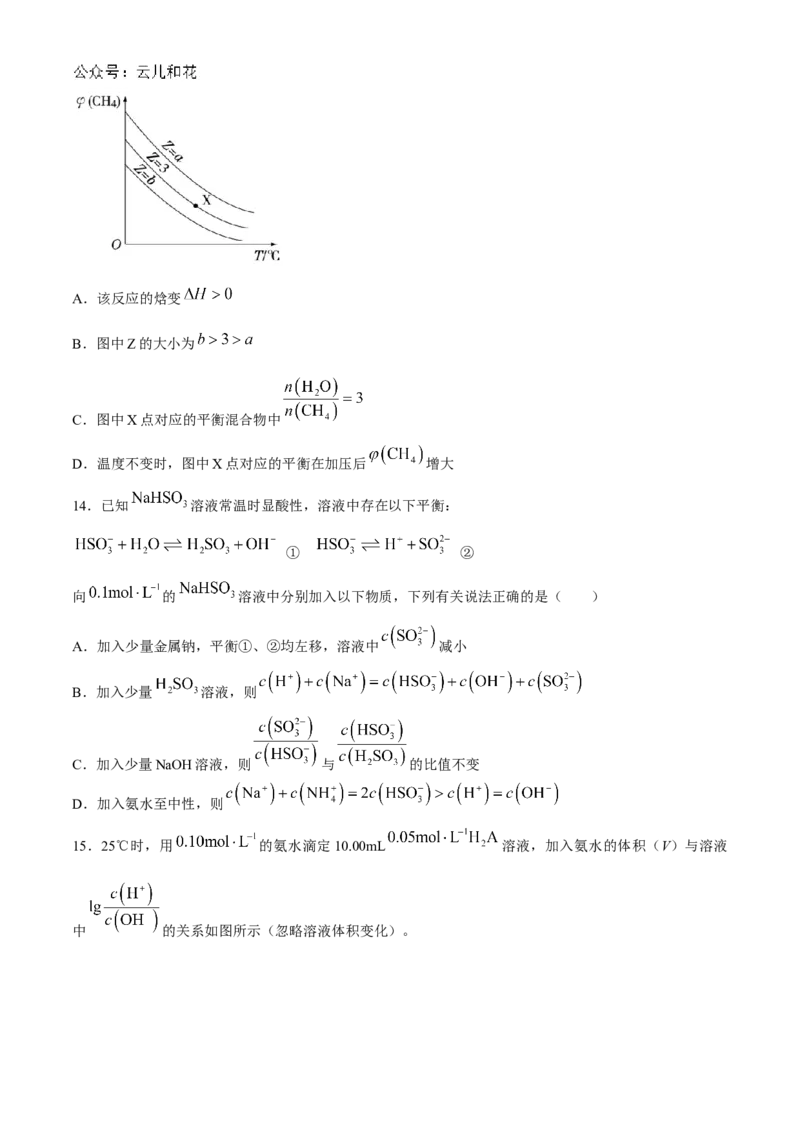
13.一定条件下, 与 发生反应: 。设起始水碳比
,在恒压下,平衡时 的体积分数 与Z和T(温度)的关系如图所示。下列说
法错误的是( )A.该反应的焓变
B.图中Z的大小为
C.图中X点对应的平衡混合物中
D.温度不变时,图中X点对应的平衡在加压后 增大
14.已知 溶液常温时显酸性,溶液中存在以下平衡:
① ②
向 的 溶液中分别加入以下物质,下列有关说法正确的是( )
A.加入少量金属钠,平衡①、②均左移,溶液中 减小
B.加入少量 溶液,则
C.加入少量NaOH溶液,则 与 的比值不变
D.加入氨水至中性,则
15.25℃时,用 的氨水滴定10.00mL 溶液,加入氨水的体积(V)与溶液
中 的关系如图所示(忽略溶液体积变化)。下列说法正确的是( )
A.a点溶液的pH等于2 B.由图中数据可知, 为弱酸
C.b点由水电离出的 浓度为 D.水的电离程度为:b>c>a
二、非选择题(本题共4小题,共55分)
16.(14分)常温下,几种酸或碱的电离常数如表所示。
酸或碱 HCN HF
(次磷酸) (甲胺)
或
回答下列问题:
(1)下列酸的酸性最强的是______(填字母)。
A.HCN B. C. D.HF
(2)甲胺是一元弱碱,在水中电离方程式为 ,乙胺(
)的第二步电离方程式为______。
(3)已知: 。
①对 的HF溶液适当加热,HF的电离程度______(填“增大”“减小”或“不变”)。向HF
溶液中滴加烧碱溶液,当 时 ______ 。
②如果用HF溶液替代盐酸测定中和反应热,测得 会______(填字母)。
A.偏高 B.偏低 C.无影响
(4)在KCN溶液中通入少量 ,离子方程式为______。
(5)次磷酸是一元酸。30mL NaOH溶液和______mL 溶液恰好完全反应。
(6) 的 大于 ,其原因是______(从平衡移动角度分析)。17.(14分)“水是生命之源”,科学家连续在木星、卫星和月球上都找到水的痕迹。回答下列问题:
(1)下列与水相关的说法正确的是______(填字母)。
A.100℃时,纯水的pH=7
B.温度升高,纯水中的 增大, 减小
C.水的电离程度很小,纯水中主要存在形态是水分子
D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小
(2)已知水中存在如下平衡: ,现欲使平衡向左移动,且所得
溶液呈酸性,可采取的方法是______。
(3)25℃时, 的NaOH溶液中由水电离出的 ______,向其中加入
的盐酸溶液直至过量,水的电离程度变化情况为______。
(4)若在木卫六上某地,水的离子积常数 ,利用我们的地球经验,木卫六上该地的温度
______(填“大于”“小于”或“等于”)25℃,其理由是______,若用pH试纸测定该温度下纯水的
pH,则试纸显______色,溶液呈______(填“酸性”“碱性”或“中性”)。
18.(13分)GB2719-2018《食品安全国家标准食醋》中规定食醋总酸指标≥3.5g/100mL(以乙酸计),
某同学在实验室用中和滴定法检测某品牌食醋是否合格。回答下列问题:
Ⅰ.实验步骤:
(1)用______(填仪器名称,下同)量取10.00mL食用白醋,在烧杯中用水稀释后转移到 100mL______
中定容,摇匀即得待测白醋溶液。
(2)量取20.00mL待测白醋溶液于锥形瓶中,向其中滴加2滴______作指示剂。
(3)读取盛装 NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,此时的读
数为______mL。
(4)滴定。滴定终点的现象是______。
Ⅱ.数据记录:
滴定次数
1 2 3 4
实验数据/mL
V(样品) 20.00 20.00 20.00 20.00
V(NaOH)(消耗) 15.95 15.00 15.05 14.95
Ⅲ.数据处理:
(5)该白醋的总酸度为______g/100mL,该品牌白醋______(填“合格”或“不合格”)。Ⅳ.反思与总结:
(6)实验过程中该同学出现了以下操作,其中可能导致结果偏大的是______(填字母)。
A.酸式滴定管没有进行润洗 B.锥形瓶用待测白醋润洗
C.滴定开始时滴定管中有气泡,结束时无气泡 D.指示剂变色立即停止滴定
E.滴定开始时俯视读数,结束时仰视读数
(7)老师指出,氢氧化钠溶液一般很难配制出准确浓度,标准氢氧化钠溶液是用基准物质进行标定得到
准确浓度的。氢氧化钠溶液难以配制出准确浓度的原因可能是______。
19.(14分)以镁铝复合氧化物(MgO- )为载体的负载型镍铜双金属催化剂(Ni-Cu/MgO-
)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下, , 。
回答下列问题:
(1)实验室配制 溶液时,需用硫酸酸化的目的是______。
(2)在加热条件下,尿素 在水中发生水解反应,放出______(写化学式,下同)和______
两种气体。
(3)下列说法错误的是______(填字母)。
A.“调pH”过程中,目的是把金属阳离子转化为氢氧化物
B.“晶化”过程中,需保持恒温60℃,可采用水浴加热
C.“焙烧”过程中,应使用蒸发皿
D.“还原”过程中,以M代表Ni或Cu,所发生的反应为
(4)“一系列操作”中,包含洗涤和110℃下干燥,则洗涤过程中检验滤饼是否洗净的方法是______。
(5)常温下,若“悬浊液”中 ,则该悬浊液的 ______。
(6)① 易溶于水,其水溶液显酸性。 溶液中各离子浓度的大小顺序为______。
② 溶液可在强碱溶液中被NaClO氧化,得到用作镍镉电池正极材料的NiOOH。该反应的离子方程
式为______。高二上学期第一次月考试卷·化学
参考答案、提示及评分细则
1.A 属于强电解质,A项正确; 属于非电解质,B项错误; 属于非电解质,C项
错误; 属于弱电解质,D项错误。
2.D 醋酸与水作用生成 和 ,属于醋酸的电离方程式,不属于水解反应方程式,A项错误;
,属于二氧化硫和水反应,并电离出氢离子的过程,不属于水解反应方程式,
B项错误; 是 与 之间发生化学反应的离子方程式,不属于水
解反应方程式,C项错误; 是 水解生成弱电解质 和
的水解反应方程式,D项正确。
3.C 对于放热反应而言,低温有利于提高反应物的转化率,A项错误;升高温度,正、逆反应速率均增
大,B项错误;在500℃左右时,铁和钼等催化剂的活性最高,可以加快反应速率,C项正确;升高温度,
合成氨反应的平衡常数减小,D项错误。
4.A 明矾净水利用 (胶体) ,A项正确; 蚀刻铜制电路板利用
的是 的氧化性,B项错误; 除去水溶液中的 、 、食盐腌制食品均未涉及水解,C、D
项均错误。
5.B
混合气体共 ,解得 ,A 项正确;根据方程式知,生成
0.4mol C 需要 0.2mol A、0.2mol B,平衡时,A、B、C 的物质的量分别为 、
、0.4mol,A、B、C的物质的量之比 ,B项
错误;A的转化率为20%,C项正确;用B表示的平均反应速率为 ,D项正确。6.B 溶液中加入固体KSCN, 增大, 平衡正向移动,
颜色加深,能用勒夏特列原理解释,A项不符合题意;平衡没有发生移动,只是浓度大了颜色加深,B项
符合题意;加压使得合成氨的反应右移,C项不符合题意;氯水中的次氯酸在光照下会分解,次氯酸浓度
减小,使得化学平衡 向右移动,D项不符合题意。
7.C 若 ,该化学反应在任何温度下都能自发进行,A项错误;知道了某过程有自发性
之后,不能确定该过程是否一定会发生,B项错误;反应 是熔融氯化钠的
电解过程,是吸热反应,则 ,反应后气体分子数增多,是熵增加的过程,则 ,C项正确;
根据吉布斯自由能判据可知,某反应在低温条件下能自发进行,则该反应在高温条件下不一定能自发进行,
D项错误。
8.D 常温下 盐酸的pH为1,稀释10倍后pH增大一个单位,所以曲线b表示盐酸稀释过程
中的pH变化,A项错误;溶液中电荷不守恒,B项错误;稀释后氢离子和醋酸根、氯离子浓度下降,酸对
于水的电离的抑制作用减弱,水的电离程度增大, 浓度增大,C 项错误;温度不变,
不变,D项正确。
9.D 由于 、 、 浓度未知,无法判断一定先生成AgCl或AgI,A、B项均错误;上层清液
中 相等,根据 可知 不等于 ,C项错误;将AgCl和AgI加入NaCl浓溶液中,由
于 较大,可使AgI转化为AgCl,D项正确。
10.D 加热促进 水解, 增大,A项错误;加入稀盐酸, 减小, 增大,B项
错误;加入适量蒸馏水, 、 均减小,由于 的水解平衡正向移动, 下降的更多,
增大,C项错误;加入 , 增大, 减小,D项正确。
11.B 已知亚磷酸( )是一种二元弱酸,故 与足量的NaOH溶液反应生成 ,不能生成 ,A项错误;向亚磷酸溶液中加入少量NaOH固体,电离平衡正向移动,溶液中 减
小,则 增大,B项正确;弱酸的电离过程是一个吸热过程,升高温度促进弱酸的电
离平衡正向移动,故对亚磷酸溶液升温,溶液中 增大,溶液的pH减小,C项错误; 溶
液的水解平衡常数 ,因此 的 溶液呈酸性,
D项错误。
12.C 图甲中,反应平衡后升高温度,正反应增大的速率大于逆反应增大的速率,说明平衡正向移动,
该反应是吸热反应,升高温度,该反应平衡常数增大,A项错误;图乙表示不同温度下水溶液中 和
的浓度变化曲线,a点的 小于b点的 ,则图中a点对应温度低于b点,B项错误;图丙
表示NaOH溶液滴定盐酸的滴定曲线,M点恰好完全反应,溶质为NaCl,因此M点水的电离程度最大,C
项正确;图丁乙酸溶液中通入氨气生成乙酸铵,由弱电解质变为强电解质,溶液的导电能力增强,到最大
值后,导电能力几乎不变,D项错误。
13.C 由图像分析,随着温度升高甲烷的体积分数逐渐减小,说明升温平衡正向移动,则正反应为吸热
反应,A项正确; 的比值越大,则甲烷的体积分数越小,故 ,B项正确;起始加入量的
比值为3,但随着反应的进行,甲烷和水是按等物质的量反应,所以到平衡时比值不是 3,C项错误;温度
不变时,加压,平衡逆向移动,甲烷的体积分数增大,D项正确。
14.C 加入少量金属钠,Na消耗 ,此时 浓度减小,平衡②右移,平衡①左移,溶液中
增大,A项错误;加入少量 溶液,根据电荷守恒得到
,B项错误;由于 ,且 、 均只与温度有关,所以其比值不变,C项
正确;加入氨水,根据电荷守恒 ,溶液呈中性,则 ,D项错误。
15 . D a 点 、 , 则 ,
,A项错误;通过A项分析可知,a点 ,则
在水溶液中能完全电离,所以 为二元强酸,B项错误;b点碱的体积与酸的体积相同,但碱的浓度是
酸浓度的 2倍,酸碱恰好完全反应生成 ,b点 、 ,
,b点 ,C项错误;a点是 的 溶液,
a点 ,抑制水的电离,b点反应产生 , 水解促进水的电离,c点为
、 按物质的量浓度之比为 2∶1 混合得到的混合溶液, 即
, ,此时 ,其对水的电离的抑制作用
小于a点的 的抑制作用,故水的电离程度为:b>c>a,D项正确。
16.(1)C(1分)
(2) (2分)
(3)①减小(1分); (2分)②B(2分)
(4) (2分)
(5)30(2分)
(6)第一步电离出的 使溶液中 增大,使第二步电离向逆反应方向移动,抑制第二步电离(2
分)
17.(1)C(2分)
(2)向水中通入氯化氢气体(加入 、 等,合理即可)(2分)(3) ;先增大后减小(直至几乎不变)(各2分)
(4)大于(2分); 随温度升高而增大(2分);黄(1分);中性(1分)
18.(1)酸式滴定管;容量瓶(各1分)
(2)酚酞(1分)
(3)0.70(2分)
(4)加入半滴氢氧化钠溶液后,溶液由无色恰好变为浅红色,且在半分钟内不变色(2分)
(5)4.5(2分);合格(1分)
(6)BCE(2分,不完整得1分,有错不得分)
(7)氢氧化钠易潮解、变质等(1分)
19.(1)抑制 水解(2分)
(2) ; (各1分)
(3)C(2分)
(4)取最后一次洗涤液少量于试管中,向其中加入稀盐酸,再加入 溶液,若有白色沉淀生成则未
洗净,若无沉淀生成则已洗净(2分)
(5)10(2分)
(6)① (2分)
② (2分)